Контрольные вопросы к коллоквиуму Онтогенез. Гомеостаз
 Скачать 2.67 Mb. Скачать 2.67 Mb.
|
|
Типы развития организмов в постэмбриональном периоде. Тип постнатального развития человека. Периоды постнатального онтогенеза человека. Особенности каждого периода, динамика адаптационных возможностей организма в разные периоды, риск развития различных заболеваний. Окончательное формирование органов человека в постнатальном периоде. Особенности роста в постнатальном периоде человека, его клеточные механизмы. Понятия ауксентичный, пролиферативный, мультипликативный и аккреционный типы клеточного роста. Свойства роста: аллометрия, эквифинальность, ограниченность, дифференциальность. Скачки роста в постнатальном развитии человека. Факторы, регулирующие рост. Рост — это увеличение общей массы в процессе развития, приводящее к постоянному увеличению размеров организма. Механизмы: 1) увеличением размера клеток, 2) увеличением числа клеток 3) увеличением неклеточного вещества, продуктов жизнедеятельности клеток. Ауксентичный — рост, идущий путем увеличения размеров клеток. Это редкий тип роста, наблюдающийся у животных с постоянным количеством клеток, таких, как коловратки, круглые черви, личинки насекомых. Пролиферационный — рост, протекающий путем размножения клеток. Он известен в двух формах: мультипликативный и аккреционный. Мультипликативный рост характеризуется тем, что обе клетки, возникшие от деления родоначальной клетки, снова вступают в деление. только в эмбриогенезе. Аккреционный рост заключается в том, что после каждого последующего деления лишь одна из клеток снова делится, тогда как другая прекращает деление . При этом число клеток растет линейно. Такой рост характерен для органов, где происходит обновление клеточного состава. Свойства роста Аллометрический роста. Его биологический смысл состоит в том, что организму в ходе роста надо сохранить не геометрическое, а физическое подобие, т.е. не превышать определенных отношений между массой тела и размерами опорных и двигательных органов. Дифференциальность - Это означает, что скорость роста неодинакова, во-первых, в различных участках организма и, во - вторых, на разных стадиях развития. Эквифинальность - особь стремится достичь типичного видового размера. Как дифференциальность, так и эквифинальность роста указывают на проявление целостности развивающегося организма. Скорость роста организма в постнатальном онтогенезе постепенно снижается к четырехлетнему возрасту, затем некоторое время остается постоянной, а в определенном возрасте опять делает скачок, называемый пубертатным скачком роста. Это связано с периодом полового созревания. Факторы: 1. Генетическая информация заключена в определенных генах, детерминирующих длину тела, а также в других генах, взаимодействующих между собой. 2. Реализация всей информации в значительной мере обусловлена посредством действия гормонов. Соматотропин, выделяемый гипофизом с момента рождения до подросткового периода. Гормон щитовидной железы — тироксин.С подросткового возраста рост контролируется стероидными гормонами надпочечников и гонад. Из факторов среды наибольшее значение имеют питание, время года, психологические воздействия.
Практикум стр 149 В постнатальном онтогенезе в критических периодов развития принадлежит период новорожденности (первый год жизни ребенка), период полового созревания (11-16 лет),период второй зрелости (55-60) Повреждающее действие на организм, особенно в критические периоды его развития, могут осуществлять химические вещества (в том числе лекарственные средства), ионизирующее излучение (в том числе рентгеновское с диагностической целью), гипоксия, голодание, наркотические средства (в том числе никотин и алкоголь) , вирусы, бактерии.
Старость представляет собой стадию индивидуального развития, по достижении которой в организме наблюдаются закономерные изменения в физическом состоянии, внешнем виде, эмоциональной сфере. 1. Теория соматических мутаций. Согласно этой теории, старение является следствием накопления в генах соматических клеток мутаций, возникающих под влиянием повреждающих агентов (например, различные виды радиации). 2. Генетическая мутационная теория является вариантом предыдущей теории и рассматривает старение как следствие ухудшения функционирования генетического аппарата клеток из-за нарушения репарации (восстановления) ДНК. 3. Теория накопления ошибок предполагает накопление ошибок в ходе процессов транскрипции и трансляции генетической информации, приводящих к образованию дефектных, функционально несостоятельных белков в организме, в том числе регуляторных. 4. Теория свободных радикалов. Свободные радикалы – это химические вещества, образующиеся в процессе метаболизма, которые содержат один непарный электрон во внешней орбите.Радикалы могут «атаковать» ДНК или белки, но одним из главных эффектов являются перекисное окисление липидов мембран, сильно влияющее на клеточные процессы. Предполагается, что свободные радикалы за счёт нарушения целостности мембран лизосом увеличивают проницаемость мембран для нуклеаз (ферментов, расщепляющих нуклеиновые кислоты). Последние же, выходя в цитоплазму, могут повреждать геном клетки. 5. Теория «сшивки» макромолекул исходит из свойств веществ, обладающих ионизированной группой, образовывать мостики между молекулами ДНК, коллагена и другими, вызывая тем самым нарушение их структуры. 1. Теория избыточного накопления. Эта теория рассматривает в качестве одной из причин старения накопление различных веществ в жизненно важных тканях. 3. Иммунологические и аутоиммунологические теории старения. Они связывают старение с нарушениями в иммунной системе, ответственной за различение «своего» и «чужого». Это приводит к поражению локусов ДНК, отвечающих за синтез антител. В результате начинают синтезироваться аномальные антитела, повреждающие собственные ткани организма. Современные представления о механизмах старения: старение является результатом природного процесса накопления повреждений, с которыми организм старается бороться, а различия старения у разных организмов являются результатом разной эффективности этой борьбы.
Организменный уровень: Как правило, после 40—50 лет у человека возникают стойкие внешние проявления старения, в частности кожных покровов. Появляются морщины, образующиеся из-за потери подкожной жировой ткани, пигментные пятна, бородавки. Признаки старения сердечно-сосудистой системы становятся заметными обычно в возрасте после 40 лет. Закономерные изменения наблюдаются в стенках сосудов: в них откладываются липиды, прежде всего холестерин. Разрастание в стенках сосудов и сердца соединительной ткани, замещающей рабочую мышечную ткань. В результате снижается эффективность работы сердца. В основе функциональных расстройств дыхательной системы лежит разрушение межальвеолярных перегородок, что сокращает дыхательную поверхность, разрастание в легких соединительной ткани, снижает эффективность аэрогематического обмена кислорода. В итоге с возрастом падает жизненная емкость легких. Легко заметным изменением в системе пищеварения является потеря зубов. Падает эффективность функционирования пищеварительных желез, нарушения двигательной (моторной) функции кишечника нередко приводят к привычным запорам. В процессе старения страдает функция мочевыделительной системы, снижается интенсивность фильтрации в почечных клубочках (на 31% в 75-летнем возрасте по сравнению с 30-летним), так же как и обратное всасывание веществ из фильтрата в почечных канальцах. Со стороны мышечной системы и скелета. Снижается сила сокращений поперечно-полосатой мускулатуры, быстрее развивается утомление, наблюдается атрофия мышц. Характерная для стареющих людей перестройка костей заключается в разрежении их вещества (старческий остеопороз), что приводит к снижению прочности. Репродуктивня система При этом они затрагивают обе основные функции главных органов названной системы — половых желез: выработку гамет и образование половых гормонов. У женщин овогенез прекращается по достижении ими менопаузы. Образование функционально полноценных сперматозоидов в мужском организме возможно, по-видимому, даже в преклонном возрасте. Изменения в процессе старения функций эндокринной системы носят объективно сложный характер. Изменения в стареющем организме функции щитовидной железы. Обнаружено, что к старости падает содержание в крови трииодтиронина и тироксина, в связи с изменением белков плазмы крови ухудшается перенос гормонов к тканям, в клетках уменьшается количество рецепторов, узнающих гормоны, а чувствительность рецепторов повышается. Молекулярные и клеточные проявления старения многообразны. Они заключаются в изменении показателей потоков информации и энергии, состояния ультраструктур дифференцированных клеток, снижении интенсивности клеточной пролиферации. В дифференцированных клетках млекопитающих животных старение сопровождается в целом снижением транскрипционной активности. Наиболее заметна возрастная перестройка постмитотических высокоспециализированных клеток—нейронов, кардиомиоцитов. Для стареющих нервных клеток, например, типично обеднение цитоплазмы мембранами, сокращение объема шероховатой эндоплазматической сети, увеличение содержания в клеточных телах микрофибрилл, что, возможно, связано с нарушением транспорта веществ по отросткам. 1) гетерохронность – разное время появления признаков старения в различных тканях, органах и системах; 2) гетерокинетичность – разная скорость развития в тканях различных возрастных изменений; 3) гетеротопность – неодинаковая выраженность процессов старения в разных органах и тканях. Различают хронологический и биологический (физиологический) возраст. Людей, хронологический возраст которых достиг 60—74 лет, называют пожилыми, 75—89 лет —старыми, свыше 90 лет —долгожителями. Точное определение биологического возраста затруднено тем, что отдельные признаки старости проявляются в разном хронологическом возрасте и характеризуются различной скоростью нарастания. Кроме того, возрастные изменения даже одного признака подвержены значительным половым и индивидуальным колебаниям.
Детерминацией (от лат. determinatio — ограничение, определение) называют возникновение качественных различий между частями развивающегося организма, которые предопределяют дальнейшую судьбу этих частей прежде, чем возникают морфологические различия между ними. Детерминация предшествует дифференцировке и морфогенезу. Главным содержанием проблемы детерминации является раскрытие факторов развития, за исключением генетических. Исследователей обычно интересует, когда наступает детерминация и чем она обусловлена. Исторически явление детерминации было обнаружено и активно обсуждалось в конце XIX в. В. Ру в 1887 г. укалывал горячей иглой один из первых двух бластомеров зародыша лягушки. Убитый бластомер оставался в контакте с живым. Из живого бластомера развивался зародыш, но не до конца и только в виде одной половины. Из результатов опыта Ру сделал вывод о зародыше как мозаике бластомеров, судьба которых предопределена. В дальнейшем стало ясно, что в описанном опыте Ру убитый бластомер, оставаясь в контакте с живым, служил препятствием для развития последнего в целый нормальный зародыш. В 90-х гг. прошлого столетия О. Гертвиг и другие исследователи показали, что при полном разделении двух бластомеров амфибий из каждого развивается целый нормальный зародыш. У многих беспозвоночных, например у гребневиков, круглых червей, спирально дробящихся кольчатых червей и моллюсков, а также у ящериц, изолированные бластомеры дают такие же зачатки, какие получаются из них при нормальном развитии. Они как бы обладают способностью к самодифференцировке. Яйца таких животных назвали мозаичными. Очень четко это показано у гребневиков, обладающих в норме восемью рядами гребных пластинок. При развитии зародыша из 1/2 яйца получается четыре ряда гребных пластинок, из 1/4, - только два, из 1/8 — один ряд. На этом основании предположили, что у подобных форм в период овоплазматической сегрегации достигается жесткая, необратимая расстановка структур. У многих других видов, например у гидромедуз, морского ежа и всех позвоночных, включая человека, отдельные изолированные бластомеры на стадии '/в и даже меньшей части зародыша могут развиваться в нормальную по строению особь. Яйцеклетки этих животных были названы регуляционными. Развитие из мозаичных и регуляционных яиц отличается также и в случаях удаления одного или группы бластомеров из развивающегося зародыша. У первых удаление одного из 24 бластомеров приводит к дефектному развитию, а у вторых — к совершенно нормальному строению зародыша. Детерминация предшествует дифференцировке и морфогенезу, которые обычно начинаются после дробления, а именно в периоде гаструляции и органогенеза. Детерминация имеет место и на этих, более продвинутых фазах эмбрионального развития, но уже в значении более узкого предопределения конкретного зачатка органа или его части. Если в фазе яйца, зиготы или бластулы важнейшим фактором детерминации выступает овоплазматическая сегрегация, то начиная с периода гаструляции и дальше главное место занимают межклеточные и межзачатковые взаимодействия. Надо помнить тем не менее, что взаимодействие клеток начинается со стадии двух бластомеров. В основе взаимодействий лежат химические, физические и биологические процессы и явления (изменение в среде концентрации ионов, обмен молекулами, выделение в среду продуктов жизнедеятельности, электрические и механические взаимодействия, излучения, действия поля, контакты клеточных мембран). Главным в понятии детерминации, по сути, есть проблема соотношения целостности организма и автономности, или способность к самодифференцировке, его частей в онтогенезе. Сохранение нормального хода развития целого зародыша после его нарушения, естественного или искусственного, получило название эмбриональной регуляции, а достижение нормального конечного результата развития разными путями — эквифинальности. Наличие периода развития, когда потенции элементов зародыша шире, чем реализующиеся при обычном развитии, т.е. когда детерминация не носит окончательного, необратимого характера, лежит в основе эмбриональных регуляций. Эмбриональные регуляции были открыты немецким эмбриологом Г.Дришем (1908). Таким образом, детерминация и эмбриональная регуляция являются противоположными свойствами и теснейшим образом взаимосвязаны в системе целостного развивающегося зародыша. Детерминация, как правило, идет от целого к частям: сначала детерминируется целый зачаток зародыша, но судьба отдельных его элементов (клеток) еще не определена, затем постепенно или скачкообразно детерминируются отдельные элементы. Обычно детерминация сменяется дифференциацией и специализацией частей организма, усиливается взаимная зависимость их друг от друга, возрастают интегрированность, целостность организма. Исключение составляют виды, у которых взрослые формы устроены проще личинок. Способность к эмбриональной регуляции в ходе онтогенеза соответственно падает, но не абсолютно, так как и у взрослого организма существует, например, способность к регенерации, т.е. к восстановлению утраченных или поврежденных частей. Вероятно гибкий регуляторный характер развития имеет существенные адаптивные преимущества: если какое-либо одно звено будет подавлено или полностью выпадает, сохраняются шансы на достижение нормального конечного результата. С другой стороны, в экстремальных условиях резерв изменчивости может стать источником эволюционных преобразований. Эти предположения вполне согласуются с фактом регуляционного типа яиц у позвоночных и с тем, что вообще способность к эмбриональной регуляции у них выражена сильнее, чем у многих беспозвоночных
Дифференцировка — это процесс, в результате которого клетка становится специализированной, т.е. приобретает химические, морфологические и функциональные особенности.Согласно различным гипотезам, дифференцировку обусловливают следующие факторы: 1) какое-то расщепление генетического материала при митозе; 2) возникновение в развивающемся зародыше химических градиентов; 3) соматические мутации; 4) действие химических организаторов или, наконец, 5) индукция специфических ферментов. Однако в настоящее время общепризнанной является точка зрения, ведущая начало от Т. Моргана, который, опираясь на хромосомную теорию наследственности, предположил, что дифференцировка клеток в процессе онтогенеза является результатом последовательных реципрокных (взаимных) влияний цитоплазмы и меняющихся продуктов активности ядерных генов. Таким образом, впервые прозвучала идея о дифферециальной экспрессии генов как основном механизме цитодифференцировки. В настоящее время собрано много доказательств того, что в большинстве случаев соматические клетки организмов несут полный диплоидный набор хромосом, а генетические потенции ядер соматических клеток могут сохраняться, т.е. гены не утрачивают потенциальной функциональной активности. Сохранение полного хромосомного набора развивающегося организма обеспечивается прежде всего механизмом митоза (возможные случаи соматических мутаций, возникающих, как исключение, во внимание не принимаем). Цитофотометрическим способом установлено, что количество ДНК в них не уменьшается, а методом молекулярной гибридизации показано, что клетки разных тканей идентичны по нуклеотидным последовательностям. На этом основании цитогенетический метод применяют для диагностики хромосомных и геномных болезней человека (хотя ошибки методов достигают 5— 10%), а метод гибридизации ДНК —для идентификации личности и установления степени родства. 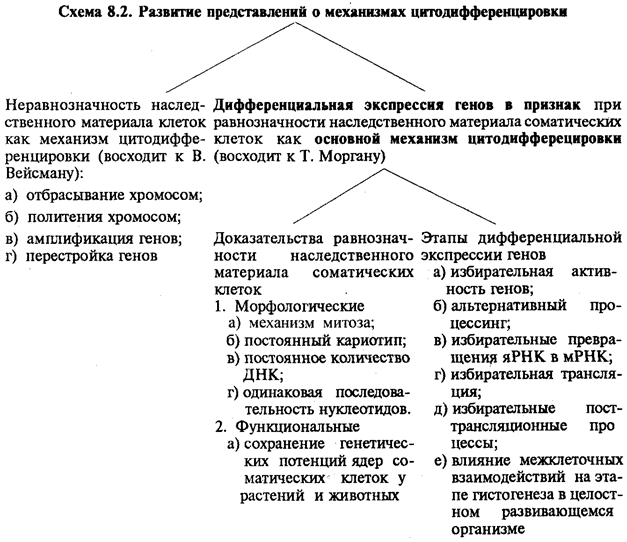 В эту тему также входит клонирование, подробнее о котором написано в практикуме стр 133-134 |
