Коллоквиум по БиоХимии. Краткая история развития биохимии
 Скачать 250.38 Kb. Скачать 250.38 Kb.
|
|
Rf для каждого соединения в стандартных условиях величина постоянная. Вопрос№11 Ионообменная хроматография – основана на притяжении противоположно заряженных частиц. Для этого используют различные ионообменные смолы: катионообменные – содержат отрицательно заряженные группы – сульфированные стиролы Анионообменные смолы, или основные ионообменники, содержат положительно заряженные группы, притягивающие отрицательно заряженные молекулы белков 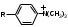 Триметиламиностирол, это производное стиролов и целлюлозы. Триметиламиностирол, это производное стиролов и целлюлозы.В зависимости от q разделяемых белков используют соответствующие ионообменники, с которыми взаимодействуют определенные белки, а другие беспрепятственно выходят из колонки. «Осажденные» на колонке белки снимают, используя более концентрированные солевые растворы или изменяя рН элюента Аффинная хроматография (или хроматография по сродству) основана на принципе избирательного взаимодействия белков или других макромолекул с иммобилизованными на носителях специфическими веществами – лигандами (это может быть кофермент, если выделяют фермент, антитело антиген и др. Благодаря высокой специфичности белков к иммобилизованным лигандам к нему присоединяется только один белок из смеси. Смывается буферными смесями с измененным рН или измененной ионной силой. Достоинство – возможность одноэтапно выделить заданное вещество высокой степени чистоты. Вопрос№12 Метод гель - фильтрации или метод молекулярных «сит» - это разновидность проникающей хроматографии. Разделение молекул по размерам и форме основано на свойствах молекулярного сита, которые обладают многие пористые материалы, например органические полимеры с трехмерной сетчатой структурой, придающей им свойства гелей. Гель фильтрация – это разделение веществ с помощью гелей, основанное на различиях в размере молекул (сефароза, сефадекс, сефакрил, биогели и т.д.). Под действием эпихлоргидрина полисахаридные цепочки декстрана (синтезируется микроорганизмами) сшиваются в сетчатую структуру, становятся нерастворимыми в воде, но сохраняют к ней большое сродство. Благодаря этой гидрофильности полученные зерна (называемые сефадексом) сильно набухают с образованием геля, которым заполняют колонку. Метод основан на том, что крупные молекулы не проникают во внутреннюю водную фазу, а более мелкие молекулы сперва проникают в поры «сита», как бы застревают в них, а поэтому движутся с меньшей скоростью. Соответственно белки с большей Mr первыми поступают в приемник. В последнее время в проникающей хроматографии все чаще используют в качестве молекулярного сита пористые стеклянные гранулы. Вопрос№13 Электрофоретический метод в биохимии – основан на различии скорости передвижения молекул в электрическом поле (аминокислоты, пептиды, белки, нуклеиновые кислоты). Различие скорости движения зависит: 1. от q молекулы: подвижность молекул тем больше, чем больше суммарный q. Величина q зависит от рН; 2. от размеров молекул: чем крупнее молекулы, тем меньше их подвижность. Это связано с возрастанием сил трения и электростатических взаимодействий крупных молекул с окружающей средой; 3. от формы молекул: молекулы одинакового размера, но различной формы, например, фибрилл и глобул белка обладают различной скоростью. Это связано с различиями в силах трения и электростатического взаимодействия. Виды электрофореза а) Изоэлектрическое фокусирование. Разделение происходит на вертикальной колонке в град. как рН, так и напряжения. С помощью специальных носителей амфолитов в колонке устанавливается град. рН от 0 до 14. В колонку помещают смесь веществ, подключаю электроток. Каждый из компонентов движется к той части колонки, где значение рН соответствует его изоэлектрической точке и там останавливается, то есть фокусируется. Достоинство: происходит разделение, очистка и идентификация белков в один прием. У метода высокая разрешительная способность (0,02 pI). б) Изотахофорез – это электрофорез на поддерживающих средах. После включения электротока ионы с самой высокой подвижностью движутся к соответствующему электроду первыми, с самой низкой – последними, обладающие промежуточной подвижностью – располагаются посередине. в) Диск-электрофорез – прибор состоит из двух сосудов с буфером – верхнего и нижнего, соединенных вертикальными трубками, содержащими разнопористый гель. По мере движения ионизированных частиц под действием электротока. Более высокая пористость – в верхней части геля. г) Иммуноэлектрофорез – метод сочетающий электрофорез с иммунодиффузией (для обнаружения антигенов в сложных физиологических смесях). На специальный носитель перпендикулярно друг другу помещают смесь антигенов и смесь антител. При включении электротока они разделяются на индивидуальные вещества и диффундируют на гелевом носителе. В месте встречи антигена с соответствующим антителом происходит специфическая реакция преципитации в форме дуги. Количеств образовавшихся дуг соответствует количеству антигенов. Вопрос№14-15 Методы определения Mr белков. У большого числа белков химический состав и последовательность аминокислот не установлена (1010–1012 белков), поэтому у таких белков определяют Mr. При этом используются различные методы. а) Седиментационный метод – определение Mr проводят в специальных центрифугах (первая центрифуга была предложена шведским биохимиком Сведбергом), в которых удается создать центробежное ускорение, которое больше в 200 тыс. и более раз ускорения земного притяжения. Mr определяют по V седиментации молекул. По мере перемещения молекул от центра к периферии образуется резкая граница белок-растворитель. Скорость седиментации выражают через константу седиментации (S): 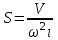 где V – скорость перемещения границы белок-растворитель (см/с); где V – скорость перемещения границы белок-растворитель (см/с); – угловая скорость ротора (рад/с); – расстояние от центра ротора до середины ячейки с раствором белков (см). Величина константы седиментации S, которая равна 110–13 С условно принята за 1 и называется 1 Сведбергом (S). S для белков лежит в пределах 1-50 S, иногда до 100 S. Mr белков определяется по уравнению Сведберга: 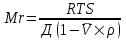 где R – универсальная газовая постоянная; где R – универсальная газовая постоянная;Т – абсолютная температура по Кельвину; S – константа седиментации; Д – коэффициент диффузии; – плотность растворителя; V – парциальный удельный объем газа. Этот метод дорогостоящий из-за применения аппаратуры. Более просты и дешевы: б) Гель-фильтрация в тонком слое сефадекса.
в) Диск-электрофорез в полиакриламидном слое – также существует зависимость между логарифмом Mr калибровочных белков и длиной их пробега. 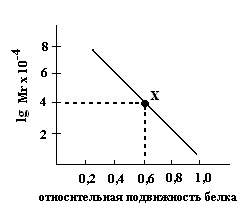 Методы определения гомогенности белков Степень чистоты выделенного белка определяется: ультрацентрифугированием; методом диск - электрофореза; различными иммунохимическими методами; определением растворимости белка (метод Нортропа) основан на правиле фаз, согласно которому растворимость чистого вещества при данных условиях опыта зависит только от температуры, но не зависит от концентрации вещества в твердой фазе.
Вопрос№16 Гемопротеиды – это Hb и его производное миоглобин (белок мышечной ткани), хлорофиллсодержащие белки и ферменты (цитохромы b, С, С1, каталаза, пероксидаза). Все они в качестве простетических групп содержат Fe (или Mg)–порфирины, а отличаются белковой частью.  Структуру гема впервые раскрыл Ненцкий, а его синтез провел Фишер. HbA1 – основной представитель Hb крови взрослого человека; Фетальный HbF – в крови новорожденного содержится до 80%, к концу 1-го года жизни он почти полностью заменяется на HbA1. HbA состоит из 4 ППЦ: 2α–субъединиц и 2–субъединиц. Четыре субъединицы или протомера ППЦ гемоглобина связаны друг с другом гидрофобными взаимодействиями. Молекула гемоглобина диссоциирует на два димера - ab и a1b1. Каждый протомер содержит гем, находящийся в гидрофобной «нише», защищающей его от окисления в ферри-форму. Mr ППЦ гемоглобина равна 64458 (64500) Да.   В основе простетической группы Нb лежит протопорфирин, у которогоимеются: в положении 1,3,5,8-СН3– метильный R; в положении 2,4 СН2=СН– винильнный R; в положении 6,7 СООН–СН2–СН2 – остатки пропионовой кислоты. Железо, входящее в состав гемоглобина, имеет 2 ковалентные и 4 координационные связи; четыре связи образуют связи с атомами азота, пятая координационная связь присоединяет кислород к гему, шестая – связывает гем и ППЦ.  Вопрос№17 Биологическая активность белков находится в прямой зависимости от сохранности ПСБ. При замене хотя бы одной аминокислоты могут возникнуть различные патологии. Например, при даже незначительных изменениях в ППЦ Hb возникают аномальные гемоглобинозы. Их около 200. Гемоглобинозы делятся на две основные группы: 1) гемоглобинопатии; 2) талассемии. Гемоглобинопатии – в их основе наследственное изменение структуры какой-либо цепи Hb. Например, серповидно-клеточная анемия (в основном в странах Южной Америки, Африки, Юго-Восточной Азии). Эритроциты в условиях низкого парциального давления принимают форму серпа. HbS после отдачи О2 (Полинг и авт.) превращается в плохо растворимую и выпадает в осадок в виде веретенообразных кристаллов, которые деформируют клетку и приводят к массивному гемолизу. Болезнь протекает остро и дети погибают в раннем возрасте. Причиной данной патологии является мутация в молекуле ДНК, кодирующей синтез -цепи Hb, где происходит замена только 1-ой аминокислоты – глу на вал в 6-м положении. Ежегодно погибает около 1 млн. человек. Талассемии – в основе – генетическое нарушение синтеза какой либо ППЦ Hb. При нарушении синтеза b-цепи возникают b-талассемии. Наряду с HbА1 обр. до 15% HbА2 и до 60% HbF – происходит гиперплазия и разрушение костного мозга, поражение печени, селезенки, деформация черепа, тяжелая гемолитическая анемия. Эритроциты приобретают форму мишени. Вопрос№18 В зависимости от химического состава белки делятся на 3 группы: 1) простые (протеины); 2) пептиды; 3) сложные (протеиды). 1. Простые белки построены из аминокислот и при гидролизе распадаются только на аминокислоты. Протамины и гистоны – содержат до 85% аргинина, поэтому имеют выраженные основные свойства. Белок сальмин, полученный из молок семги; клупеин – из молок сельди, скорее относятся к пептидам, т.к. имеют Mr не более 5000 Да. Протамины в основном являются белковой частью нуклеотидов (ДНК). Гистоны сосредоточены главным образом в ядре и представляют белковую часть РНК. Проламины и глютелины – белки растительного происхождения: зеин получают из кукурузы, глютенин - из пшеницы. Содержат до 25% глу, 10-15% про. Альбумины и глобулины – содержатся в сыворотке крови, молоке, яичном белке, мышцах и т.д. Это глобулярные белки, отличающиеся различной растворимостью (альбумины растворяются лучше), по Mr (альбумины имеют молекулярную массу, равную 69000 Да, глобулины - 150000Да). 2. Пептиды – это низкомолекулярные азотсодержащие соединения, состоящие из остатков аминокислот и имеющие молекулярную массу менее 5000 Да. а) с гормональной активностью (АКТГ, окситоцин, вазопрессин и др.); б) участвующие в процессах пищеварения (секретин, гастрин); в) содержащиеся в α2-глобулярной фракции сыворотки крови (брадикинин, ангиотензин); г) нейропептиды (рилизинг-факторы гормонов, например нейрофизины I и II гипоталамуса, способствуют выделению гормонов окситоцина и вазопрессина). 3. Сложные белки или протеиды – состоят из двух частей: белковой и небелковой. Небелковую часть называют простетической группой, а белковую часть, утратившую простетическую группу, называют апобелком.
|