Физиология-крови.. Кровь, как важнейшая часть внутренней среды организма. Роль системы крови в поддержании гомеостаза. Функции крови
 Скачать 3.08 Mb. Скачать 3.08 Mb.
|
|
Осмотическая резистентность эритроцитов. Виды гемолиза. Скорость оседания эритроцитов. Анемия. Под осмотической резистентностью (стойкостью) эритроцитов понимают их способность противостоять понижению осмотического давления (то есть, если закинуть эритроциты в гипотонический раствор, то вода из них стремится в эритроцит. Они начинают набухать и могут лопнуть). Осмотическая резистентность является показателем прочности мембран эритроцитов. Мерой осмотической стойкости эритроцитов является концентрация NaCl, при которой начинается гемолиз (осмотический). У человека это происходит в 0,4%-м растворе NaCl (минимальная осмотическая резистентность), а в 0,34%-м растворе разрушаются все эритроциты, наступает полный гемолиз крови (максимальная осмотическая резистентность). Виды гемолиза: (гемолиз-банальное разрушение эритроцитов, характеризующееся выходом гемоглобина в кровь) Физиологический гемолиз. Разрушение старых и дефектных эритроцитов в красной пульпе селезенки; Осмотический гемолиз. Был описан выше; Химический гемолиз.Возникает под действием химических веществ, разрушающих белково-липидную оболочку эритроцитов; Биологический гемолиз. Возникает при действии ядов змей, насекомых, микроорганизмов; Температурный гемолиз. Возникает при замораживании и размораживании крови в результате разрушения оболочки эритроцитов кристалликами льда; Механический гемолиз. Возникает при сильных механических воздействиях на кровь, например встряхивании ампулы с кровью; Иммунный гемолиз. Возникает либо при гемотрансфузиях, когда переливается несовместимая кровь, либо резус-конфликт между кровью матери и плода. Анемия-состояние, характеризующееся уменьшением содержания гемоглобина в единице объема крови. Виды анемии: Анемия, связанная с недостатком железа. При дефиците железа образуются мелкие эритроциты с пониженной массой гемоглобина (гипохромная микроцитарная анемия). Недостаток железа может быть вызван: 1) недостаточным содержанием элемента в пище (особенно часто у грудных детей); 2) снижением поглощения железа из пищеварительного тракта ; 3) хронической кровопотерей (например, при интенсивных менструальных кровотечениях, а также при язвах или злокачественных опухолях желудочно-кишечного тракта); Мегалобластические анемии. Причина аномалии-недостаток витамина В12 (пернициозная анемия) или фолиевой кислоты в пище или нарушение их усвоения, необходимые для синтеза ДНК. В результате чего возникают аномально крупных эритроцитов (мегалоцитов, или макроцитов) и их незрелых предшественников (мегалобластов) в крови или в костном мозге; Почечная анемия. Недостаток эритропоэтина при хронической почечной недостаточности приводит при отсутствии лечения к нормохромной нормоцитарной анемии; Апластическая анемия. Апластические анемии и панцитопении характеризуются тем, что, несмотря на наличие всех веществ, необходимых для кроветворения, гемопоэз в костном мозге снижен. Причинами панцитопений могут быть повреждения костного мозга ионизирующими излучениями (при радиотерапии), клеточные яды (цитостатики, бензол и т. д.) или замещение здоровых тканей опухолевыми; Гемолитические анемии. Скорость оседания эритроцитов (СОЭ). Эритроциты способны оседать в несвертывающемся неподвижном образце крови. Это обусловлено двумя причинами: 1) Их удельный вес (1,096) больше, чем у плазмы (1,027); 2) Электростатического взаимодействия между клетками (из-за отрицательного заряда на своей мембране эритроциты взаимно отталкиваются). . Скорость оседания эритроцитов (СОЭ) составляет у здоровой женщины 6–11 мм/ч, у здорового мужчины — 3–9 мм/ч. Величина СОЭ зависит от числа эритроцитов(гематокрита), их размеров, формы и, особенно, коллоидного состояния плазмы, обусловленной ее белковым составом. Определение СОЭ. При использовании стандартного метода Вестергрена из локтевой вены берут 1,6 мл крови 2-миллилитровым шприцом, содержащим 0,4 мл антикоагулянта цитрата натрия. Кровь переносят в градуированную пробирку объемом 200 мл и диаметром 2,5 мм, которую фиксируют в вертикальном положении. Высота супернатанта, свободного от эритроцитов, измеряется через 1 ч (= СОЭ). Гемоглобин. Количество, строение и функции гемоглобина. Типы гемоглобинов. Физиологические и нефизиологичсские соединения гемоглобина. Образование, разрушение и выведение продуктов обмена гемоглобина. Защитная функция крови. Неспецифический клеточный и гуморальный иммунитет. Механизмы специфического клеточного и гуморального иммунитета. Внедряющиеся в организм инородные тела и возбудители болезней обезвреживаются за счет растворимых белков, а также белых кровяных телец, или лейкоцитов, обладающих фагоцитарной активностью и образующих антитела (то бишь, иммунитет). Защитная функция достигается следующими механизмами: Реагированием на разнообразные антигены, выделяя и отделяя от них собственные молекулы организма; Запуском и усилением реакции на антиген в ограниченный период времени, чтобы победить инфекцию до момента гибели человека от заболевания; Запечатлением в иммунологической памяти антигены, однажды попавшие в организм, для повышения скорости и эффективности реагирования на них при повторном их появлении; Иммунная система утилизирует также погибшие, постаревшие, мутировавшие и перерождённые (онкологические) клетки собственного организма. Иммунитет делится на два типа: Неспецифический иммунитет (он же-врожденный, он же-естественный)-более древние тип, обуславливающий защиту на любые чужеродные антигены. Кроме того, неспецифический иммунитет вида генетически фиксирован (то есть, для одного вида животных возбудитель является патогенным, а у другого не может вызывать иммунные реакции). В свою очередь, неспецифический иммунитет делится на: Гуморальный иммунитет, Составляющие гуморального иммунитета: Лизоцим(мурамидаза)-фермент, расщепляющий обломки бактериальной стенки (действует на пептидогликан) Грам+ бактерий, а совместно с системой комплемента также Грам- бактерий. Он встречается в тканях и практически во всех жидкостях организма (особенно много его в слюне и слезе). С-реактивный белок. Связываясь с поверхностными структурами, которые находятся на многих грибах и бактериях, он метит их для дальнейшего связывания с системой комплемента и фагоцитами. Такое маркирование антитела антигеном (тут не только С-реактивный белок может быть антигеном, но еще куча других веществ, которые называются опсонинами) называется опсонизацией. Опсонизация значительно ускоряет процесс фагоцитоза фагоцитами ( в 5000 раз). Интерфероны-видоспецифичные гликопротеины, которые продуцируются клетками, зараженными вирусами. Они обладают антивирусной активность, влияют на размножение вирусов, тормозя процесс их дальнейшего распространения. Различают интерфероны α (ИФ лейкоцитов) и β (ИФ фибробластов) (с практически идентичным действием) и γ (иммунный ИФ). В то время как интерферон γ продуцируется только определенными иммунными клетками (NK-клетками, Т-клетками), интерфероны α и β высвобождаются практически любыми клетками в организме (например, клетками печени). Продуцируемые ИФ-α и ИФ-β связываются с интерфероновыми рецепторами окружающих клеток, за счет чего подавляется синтез белка и, таким образом, репликация вируса. Интерфероны стимулируют: - фагоцитоз - цитотоксическую активность макрофагов; - активность T-киллеров - активность NK - продукцию антител. Система комплемента-семья(система) из +- 20 белков-протеаз, которые находятся в норме в плазме крови, но могут быть также среди белков, просочившихся из капилляров в тканевые пространства. Основная функция белков системы комплемента состоит в том, что они, образуют атакующий мембрану комплекс, который обладает литической активностью, разрушая клеточную мембрану патогенных микроорганизмов (СК делает дыры в мембране, мб это приводит к осмотическому шоку и микробчики подыхают). многие белки системы комплемента являются предшественниками ферментов (проферментами). Проферменты в норме не активны, но они могут активироваться двумя различными способами: 1) классический путь активации: Контакт иммунной системы с патогеном (например, с бактерией) приводит к образованию антител против соответствующих структур (антигенов) возбудителя. Образуются комплексы антиген–антитело, активирующие фактор С1 системы комплемента. Таким образом запускается каскад ферментативный реакций (суть его,как я понял, состоит в том, что активированный фактор С1, являющийся протеазой, активирует следующий компонент и так далее до тех пор, пока не произойдет расщепления фактора С5 до C5b. C5b индуцирует в свою очередь сборку комплекса из факторов С6, С7, С8 и С9 в комплекс С5–9 (мембраноатакующий комплекс\атакующий мембрану комплекс), который встраивается в клеточную мембрану возбудителя и вызывает лизис. Этот путь и называют классическим путем каскада системы комплемента. 2) альтернативный путь: его отличие состоит в том, что каскад реакций запускает либо полисахаридами бактериальной клетки, либо посредством С-реактивного белка, либо фрагментами комплемента. В дальнейшем механизм схож с классическим путем ̶(̶н̶е̶ ̶п̶у̶т̶е̶м̶)̶. Как все это выглядит: 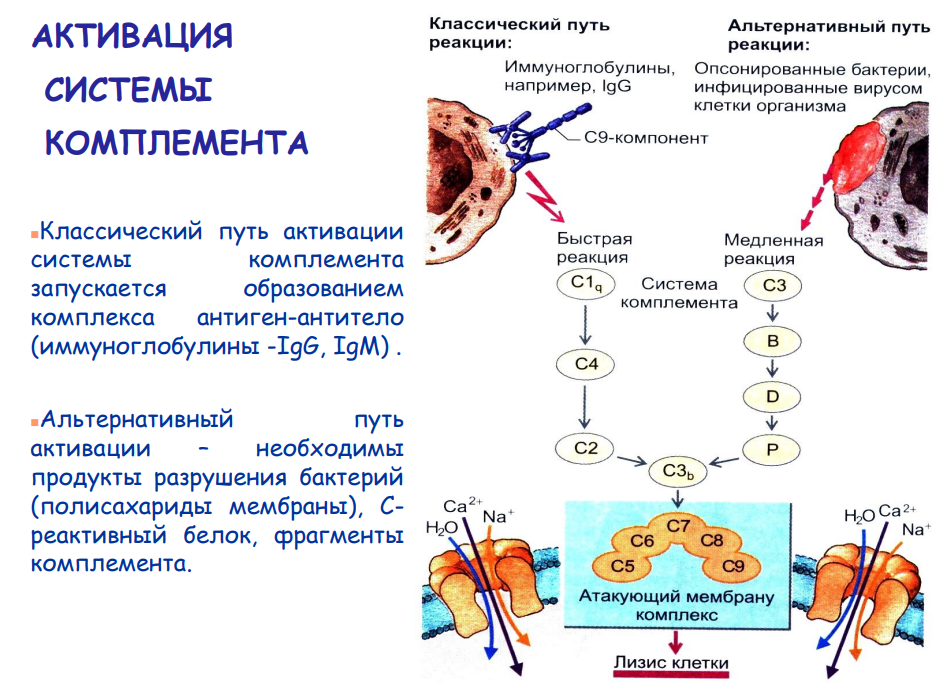 Некоторые другие функции системы комплемента: Опсонизация и фагоцитоз. Один из продуктов каскада комплемента — СЗЬ — мощно активирует фагоцитарную активность и нейтрофилов, и макрофагов, заставляя эти клетки поглощать бактерии, к которым прикрепляются комплексы антиген-антитело. Агглютинация. Продукты комплемента также изменяют поверхности внедряющихся организмов, способствуя их прилипанию друг к другу. Нейтрализация вирусов. Ферменты и другие продукты реакции комплемента могут атаковать структуры некоторых вирусов, в результате последние теряют свою вирулентность. Хемотаксис. Фрагмент С5а инициирует хемотаксис нейтрофилов и макрофагов, заставляя большое количество этих фагоцитов мигрировать в тканевые области, прилежащие к антигенному агенту. Активация тучных клеток и базофилов. Фрагменты СЗа, С4а и С5а активируют тучные клетки и базофилы, заставляя их выделять гистамин, гепарин и некоторые другие вещества в местные ткани. Эти вещества, в свою очередь, ведут к увеличению локального кровотока, усилению просачивания жидкости и плазменных белков в ткань и другие местные тканевые реакции, способствующие инактивации или обездвиживанию антигенного агента. Воспалительные эффекты. Кроме воспалительных эффектов, связанных с активацией тучных клеток и базофилов, вклад в местное воспаление вносят и некоторые другие продукты комплемента. Эти продукты ведут к: (I) еще большему увеличению уже повышенного кровотока; (2 ) усилению утечки белков из капилляров; (3) коагуляции белков интерстициальной жидкости в тканевых пространствах, что предотвращает движение внедрившихся организмов по тканям. Клеточный иммунитет. Клеточный неспецифический иммунитет образован гранулоцитами, а также мононуклеарной макрофагальной системой фагоцитов (она же-макрофагальная система). Основной неспецифического клеточного иммунитета является фагоцитоз, который осуществляется либо гранулоцитами (разные гранулоциты обладают разной фагоцитарной активностью), либо макрофагальной системой. Если в организм попал патогенный микроб, но первыми на поле битвы приходят именно клетки неспецифического иммунитета. Привлечение клеток осуществляется посредством хемотаксиса, запускаемого и поддерживающегося за счет градиентов концентраций химических веществ(существует очень много хемокинов, которые привлекают определенный тип клеток). После хемотаксиса происходит фагоцитоз.Фагоцитоз начинается с захвата микроорганизма и его связывания с фагоцитом (способность к связывания облегчается опсонизацией). Затем фагоцит образует псевдоподии, которые окружают чужеродное тело (образуется фагосома). Внутри фагоцита происходит слияние фагосомы с лизосомой, и образуется фаголизосома. Лизосомальные ферменты включают протеазы, липазы, оксидазы, дезоксирибонуклеазы, пептидазы. 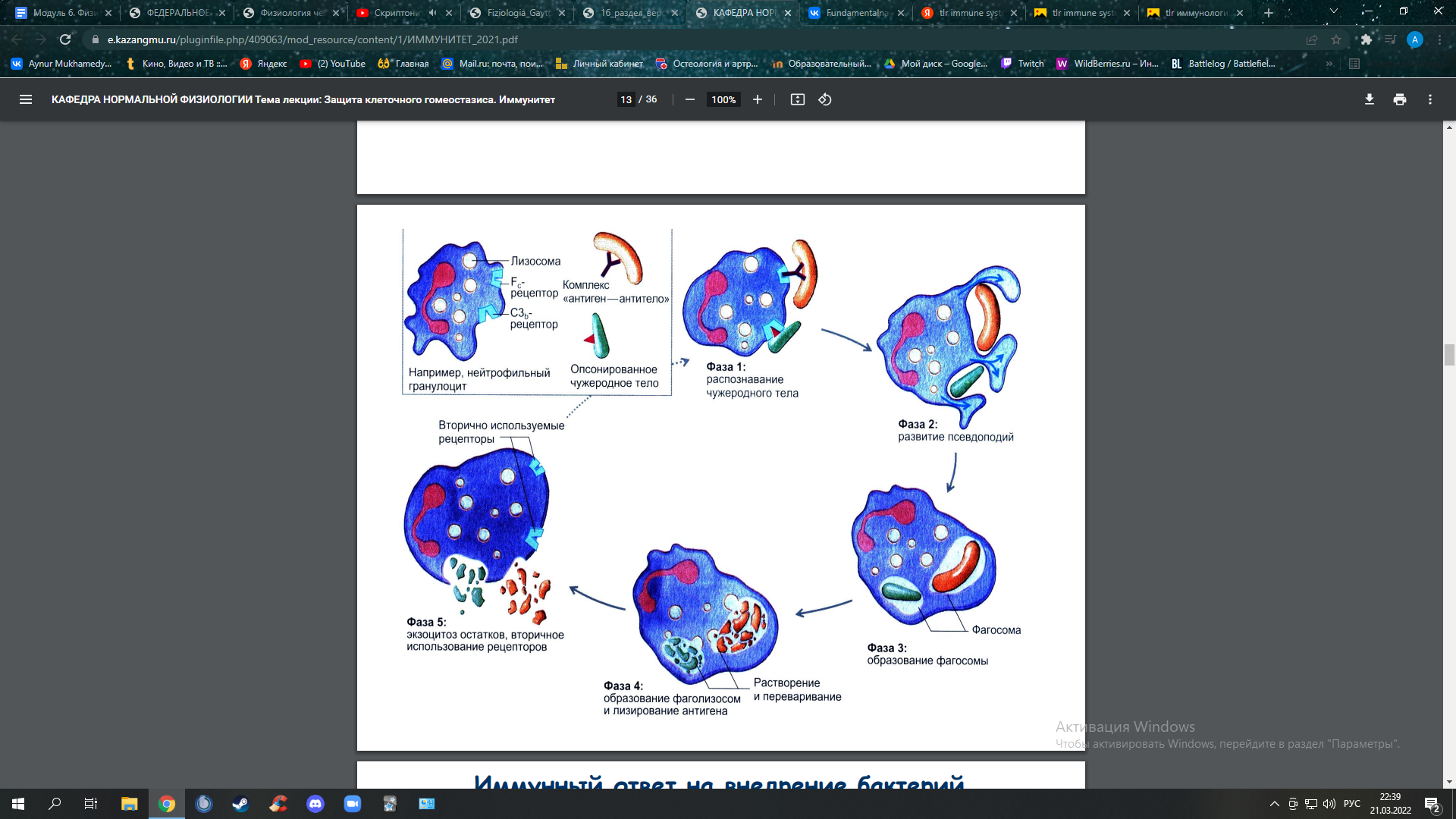 Немножко про то, как происходит связывание бактерии и фагоцита: Чтобы иметь возможность специфически реагировать на компоненты бактерий, у фагоцитов существуют toll-подобные рецепторы (TLR). Связывание бактерий с этими рецепторами и запускает защитные механизмы. Чуток примеров: 1) Многие бактерии экспрессируют на своей поверхности пептидогликаны, которые связываются с TLR-2 и тем самым активируют воспалительные клетки. 2) Определенные компоненты бактериальной ДНК могут связываться с TLR-9, что через такие же сигнальные пути, как и при связывании с TLR-4 или TLR-2, ведет к активации клеток. Другие TLR служат для связывания флагеллина (TLR-5) или определенных бактериальных липопротеинов (TLR-6). 3) У многих бактерий на поверхности присутствуют определенные липополисахариды (ЛПС). ЛПС с большим сродством связываются с рецептором CD14 (от англ. cluster of differentiation, более ста поверхностных белков клеток иммунной системы различаются соответствующей нумерацией, и CD14 является одним из них). Он активирует toll-подобный рецептор TLR-4. TLR-4 индуцирует экспрессию различных воспалительных белков и цитокинов. 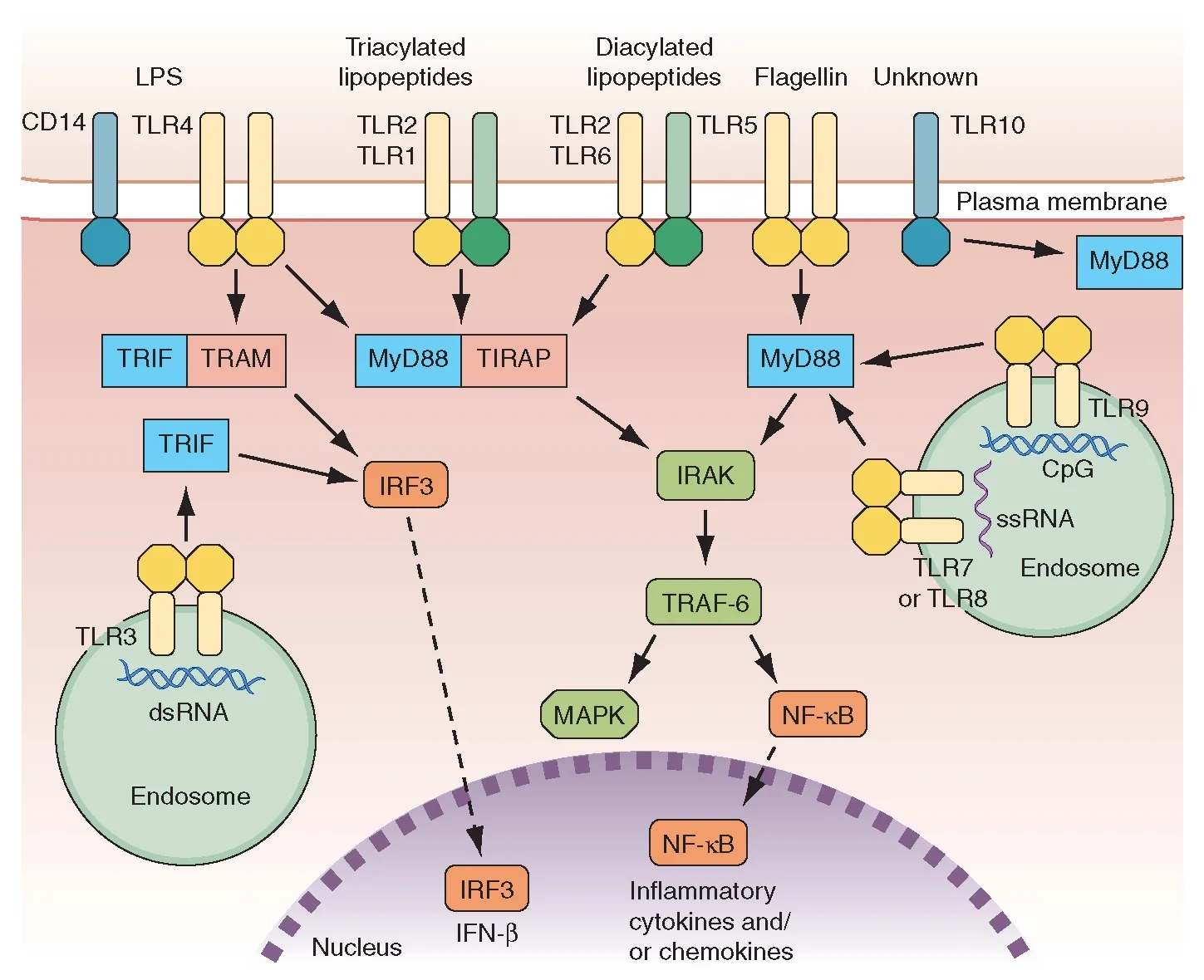 Немножко про фагоциты: Нейтрофильные гранулоциты. Нейтрофильные гранулоциты высвобождают различные ферменты, такие как лизоцим, расщепляющий пептидогликаны, кислые фосфатазы, кислые протеазы и коллагеназы. Ферменты убивают бактерии и расщепляют коллагены, что облегчает миграцию воспалительных клеток в ткани. За счет экспрессии НАДФ-Н-зависимой оксидазы гранулоциты могут образовывать активные формы кислорода, которые оказывают сильное токсическое действие на бактериальные мембраны. Остатки нейтрофильных гранулоцитов, бактерий и инфицированных тканей составляют то, что мы называем гноем. Эозинофильные гранулоциты. Эозинофильные гранулоциты высвобождают из внутриклеточных гранул эозинофильный катионный белок, главный основный белок (MBP, major basic protein), а также эозинофильный белок Х, которые оказывают токсическое действие на паразитов, особенно червей. Базофильные гранулоциты. При наличии инфекции базофильные гранулоциты в основном высвобождают гистамин и серотонин, что приводит к расширению сосудов и дальнейшей миграции воспалительных клеток. Виды лейкоцитов, количество (лейкоцитарная формула). Лейкоцитоз, лейкопения. Нейтрофилы, их разновидности и функции. Моноциты. Явление фагоцитоза. Функции базофилов и эозинофилов. Лимфоциты, их виды. Роль в клеточном и гуморальном иммунитете. Иммуноглобулины, их функции. Тромбоциты, их физиологическое значение. Тромбоцитарные факторы гемостаза. Остановка кровотечения в мелких сосудах. Первичный (сосудистотромбоцитарный) гемостаз, его характеристика. Тромбоциты (кровяные пластинки)-представляют собой мелкие дисковидные двояковыпуклые безъядерные постклеточные структуры диаметром 2-4 мкм, образующиеся в результате фрагментации мегакариоцитов в красном костном мозге. Вспомним чуток строение: Плазмолемма. Окружает тромбоцит и содержит многочисленные рецепторы, опосредующие действие веществ, активирующих и ингибирующих функции тромбоцитов, обусловливающие их прикрепление (адгезию) к эндотелию сосудов и агрегацию (склеивание друг с другом); Гиаломер. Состоит из системы трубочек: 1. Система канальцев, связанных с поверхностью (открытая система канальцев), представленная гладкими анастомозируюшими трубочками, которые открываются в инвагинации, образованные плазмолеммой. Ее функция заключается в захвате и выведении веществ (гранулы тромбоцитов, как пример). 2. Система плотных трубочек образуется комплексом Гольджи мегакариоцитов. Они накапливают и выделяют Са2 + , т.е. являются аналогом саркоплазматической сети мышечных клеток. 3. Цитоскелет, образованный микротрубочками, микрофиламентами и промежуточными филаментами; Грануломер. |
