Физиология-крови.. Кровь, как важнейшая часть внутренней среды организма. Роль системы крови в поддержании гомеостаза. Функции крови
 Скачать 3.08 Mb. Скачать 3.08 Mb.
|
|
α-гранулы: β-тромбоглобулин – ингибитор синтеза простациклина в эндотелии, выделяется до секреции других белков. Является маркером активированных тромбоцитов. тромбоцитарные факторы коагуляции, например, такие как фибриноген и фактор XIII (фибринстабилизирующий фактор, трансглутаминаза), ингибитор активатора плазминогена (PAI-1, рlasminogen activator inhibitor-1) – подавляет реакции фибринолиза тем, что инактивирует действие активатора плазминогена t-PA, фактор активации тромбоцитов (PAF, platelet-activating factor), который схож с фосфатидилхолином, но жирные кислоты заменены на алкильный остаток (при С1) и на ацетил (при С2), фактор Виллебранда – очень крупный мультимерный гликопротеин, выполняющий функции: прикрепления тромбоцита к субэндотелиальному коллагену в поврежденной стенке сосуда (адгезия) через тромбоцитарный рецептор GP1b, связывания и защиты фактора VIII в кровотоке от активного протеина С, доставки фактора VIII в зону повреждения (т.к. сам фактор Виллебранда здесь задерживается). фибронектин – гликопротеин, состоящий из двух практически идентичных полипептидных цепей. Фибронектин принадлежит к семейству адгезивных белков. Наличие связывающих доменов позволяет белку функционировать как молекулярный клей, образуя "мостики" между молекулами (например, рецепторы тромбоцита и коллаген). витронектин – полифункциональный гликопротеин, выполняет функции адгезии, как и фибронектин. Также активирует белок PAI-1, который при отсутствии витронектина не в состоянии выполнять свою функцию (т.е. подавлять фибринолиз),тромбоспондин – белок, опосредующий адгезию тромбоцитов к субэндотелию, тромбоцитарный фактор роста (PDGF, platelet-derived growth factor) – стимулятор роста эндотелиоцитов, фибробластов, гладких миоцитов. δ-гранулы (электронно-плотные гранулы): АТФ АДФ ГТФ ГДФ Неорганические фосфаты Кальций Серотонин λ-гранулы. Считаются лизосомами и содержат кислые гидролазы.   Функции тромбоцитов: Остановка кровотечения при повреждении стенки сосудов (первичный гемостаз) - основная функция тромбоцитов; Обеспечение свертывания крови - (гемокоагуляции) - вторичный гемостаз (совместно с эндотелием кровеносных сосудов и плазмой крови); Участие в реакциях заживления ран (в первую очередь, повреждений сосудистой стенки) и воспаления; Обеспечение нормальной функции сосудов, в частности, их эндотелиальной выстилки (ангиотрофическая функция). Тромбоцитарные факторы гемостаза: Фактор III – тромбоцитарный тромбопластин – фосфолипид, находящийся в мембране кровяных пластинок и их гранул. Освобождается после разрушения тромбоцитов и используется в I фазе свертывания. Фактор IV – антигепариновый - связывает гепарин и ускоряет процесс гемокоагуляции; Фактор V – свертывающий фактор или фибриноген определяет адгезию и агрегацию тромбоцитов; Фактор VI – тромбостенин – обеспечивает уплотнение и сокращение кровяного сгустка; Фактор X – сосудосуживающий (серотонин, который адсорбируется тромбоцитами из крови). Суживает поврежденные сосуды, уменьшает кровопотерю; Фактор XI – фактор агрегации (является АДФ и обеспечивает скучивание тромбоцитов в поврежденном сосуде ). Под гемостазом подразумевают комплекс физиологических процессов, обеспечивающих остановку кровопотери, в случае повреждения сосудистой стенки, а также поддержание крови в жидком состоянии. Процесс гемостаза состоит из нескольких этапов: Первичный спазм сосудов. В ответ на импульсы от болевых или других рецепторов в травмированном сосуде или рядом расположенных тканях происходит рефлекторное сужение сосуда. Но, по большей части первичный спазм сосудов связан с влиянием местных факторов, выделяющихся из травмированных тканей и тромбоцитов крови (тромбоксан А2, выделяющийся из тромбоцитов). Первичный гемостаз. Образуется тромбоцитарная пробка и вторично спазмируются сосуды. Вторичный гемостаз. Процесс свертывания крови. Фибринолиз. Первичный гемостаз (сосудисто-тромбоцитарный. Первичный спазм сосудов. В ответ на импульсы от болевых или других рецепторов в травмированном сосуде или рядом расположенных тканях происходит рефлекторное сужение сосуда. Но, по большей части первичный спазм сосудов связан с влиянием местных факторов, выделяющихся из травмированных тканей и тромбоцитов крови (тромбоксан А2, выделяющийся из тромбоцитов). Адгезия тромбоцитов. При повреждении сосудов обнажаются лежащие под эндотелием коллагеновые волокна. Тромбоциты начинают прикрепляться к волокнам соединительной ткани по краям раны. Это происходит благодаря белку-фактору фон Виллебранда, выделяющегося тромбоцитами, эндотелиальными клетками и из плазмы крови. Фактор фон Виллебранда образует мостики между волокнами коллагена и тромбоцитами, взаимодействуя с комплексом рецепторов на мембране последних. Активация тромбоцитов. Под действием секретируемых агонистов (АДФ, Са2+, тромбоксан А2) происходит активация тромбоцитов. Активированные пластинки увеличиваются в размерах и из круглых и дискообразных становятся круглыми с длинными отростками (псевдоподиями). Образование псевдоподий запускается Са2+, вследствие чего глобулярный актин переходит в фибриллярных. Обратимая агрегация тромбоцитов. Сократительные белки сокращаются, способствуя выделению из гранул секрета (содержимое гранул было выше мне лень опять писать). Уже на этой стадии выделяются вещества, которые запускают вторичный гемостаз по внешнему пути (тканевой фактор III, например). Кроме того, активированные тромбоциты выделяют тромбоксан А2, который совместно с АДФ и серотонином обеспечивают вазоконстрикцию (как я понял, это вторичный спазм сосудов). Кроме тогх2, активированные тромбоциты выделяют тромбоспондин, который укрепляет образованные фибринногенновые мостики между тромбоцитами. Кроме тогох3, активированные тромбоциты образуют вещества, которые в свою очередь их активируют. Примером может служить высвобождение АДФ, а также синтез тромбоксана А2. При воздействии этих медиаторов все большее число тромбоцитов лавинообразно вовлекается в процесс. Таким образом происходит образованием тромбоцитарного (белого) тромба и завершается первичный гемостаз. Доп: Чтобы агрегированные тромбоциты не распространялись за пределы поврежденной области сосуда, окружающий интактный эндотелий непрерывно выделяет простациклин, который связывается с ними. Простациклин препятствует агрегации тромбоцитов. Он активирует мембранную аденилатциклазу. Циклический АМФ усиливает обратный поток ионов Са2+ из цитозоля в электронно-плотные гранулы и таким образом стабилизирует тромбоциты. Доп2: Первичный гемостаз осуществляет остановку кровотечений только в достаточно мелких сосудах, так как образованный белый тромб может быть легко смыт кровотоком, и существует опасность нового кровотечения. В крупных же сосудах кровотечение останавливается с помощью вторичного гемостаза, благодаря которому сосуды окончательно замыкаются красным тромбом. 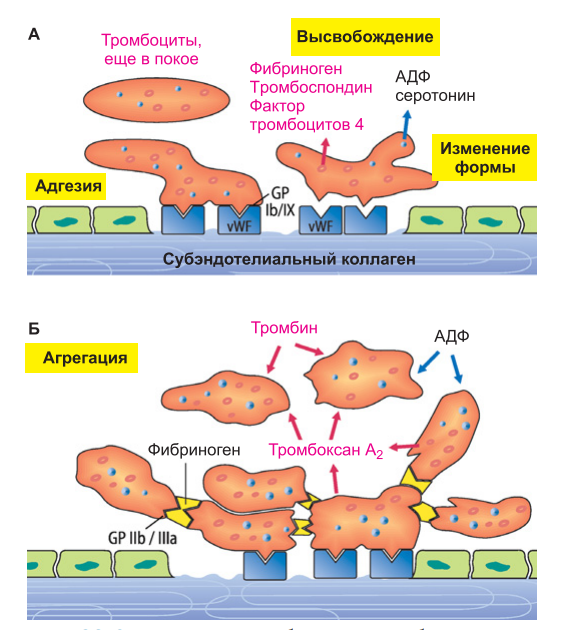 Вторичный гемостаз, гемокоагуляция. Плазменные факторы свертывания крови. Фазы гемокоагуляции. Внешний и внутренний пути активации процесса свертывания крови. Состав тромба. Под вторичным (коагуляционным s. плазменный) гемостазом (свертывание крови) понимают процесс образования сетей из нитей фибрина, которая содержит эритроциты и лейкоциты, под действием фактором свертывания крови. Плазменные факторы свертывания крови: Фактор I (фибриноген). Образуется в печени. Под влиянием тромбина переходит в фибрин. Принимает участие в агрегации тромбоцитов. ФII – протромбин – глюкопротеид, образуется клетками печени при участии витамина К. Под влиянием протромбиназы переходит в тромбин (фактор IIa). ФIII – тканевой тромбопластин – фосфолипид, входит в состав мембран всех клеток, необходим для образования тканевой протромбиназы. ФIV –Са2+ содержится в крови, наполовину в виде ионов или комплексов с белками плазмы. Ионы Са++ необходимы для всех фаз свертывания, участвует в образовании комплексов факторов свертывания крови, входит в состав протромбиназы. Способствует агрегации тромбоцитов. Связывает гепарин. Принимает участие в ретракции сгустка и образовании тромбоцитарной пробки. Тормозит фибринолиз. ФV и ФVI – проакцелерин и акцелерин. Фактор V (проакцелерин). Глобулин. Образуется в печени. Активируется тромбином. Усиливает действие фактора Ха на протромбин (входит в состав протромбиназы), участвует в 1 и 2 фазах гемокоагуляции. ФVII – конвертин синтезируется в печени, при участии витамина «К» требуется для образования тканевой протромбиназы. ФVIII – (антигемофильный глобулин А) – необходим для формирования кровяной протромбиназы. ФIX – фактор Кристмаса (антигемофильный глобулин В) – образуется в печени в присутствии витамина «К», требуется в I фазе гемокоагуляции. Ф X – фактор Стюарта – Прауэра. Синтезируется в печени, при участии витамина «К», участвует в формировании и входит в состав тканевой и кровяной протромбиназ. ФXI – плазменный предшественник тромбопластина. Образуется в присутствии витамина «К» в печени, требуется для образования кровяной протромбиназы, активирует фактор IX. При дефиците- гемофилия С. ФXII – фактор Хагемана – активируется при контакте с чужеродной поверхностью. Является инициатором образования кровяной протромбиназы и всего процесса гемокоагуляции. ФXIII – фибринстабилизирующий – содержится в плазме, клетках и тканях. Гликопротеид синтезируется в печени, необходим для образования окончательного (нерастворимого фибрина 1). Активируется тромбином и ионами Са2+. ФXIV (фактор Флетчера – прекалликреин). Участвует в активации факторов XII, IX и плазминогена. Переводит кининоген в кинин. Активируется фактором XIIa. ФXV (фактор Фитцжеральда, Фложек, Вильямса). Высокомолекулярный кининоген. Образуется в тканях. Активируется калликреином. Принимает участие в активации фактора XII и переводе плазминогена в плазмин. В целом все они относятся к протеолитическим ферментам, которые имеются в плазме в неактивной форме как проферменты и активируются только при запуске свертывания крови в каскаде реакций. Активная форма факторов обозначается буквой «а» (например, IIa). Фазы вторичного гемостаза: Фаза активации (Образование протромбиназы). Она может протекать либо по внешнему пути, либо по внутреннему пути: Внешний путь. Запускается тканевым фактором s. тканевым тромбопластином (ФIII), секретируемом поврежденной тканью. ТФ активирует ФVII, который вместе с фосфолипидами и Са2+ образует комплекс, активирующий ФХ. Внутренний путь. Запускается взаимодействием ФXII c отрицательной заряженной поверхностью сосуда в присутствии каллекреина и кининогена. Впоследствии активируются факторы XI и IX. Фактор IXa вместе с фосфолипидами, ионами Са2+ и ФVIII образует ферментативный комплекс, который протеолитически активирует фактор Х. Фаза активации заканчивается образованием активатора протромбина (протромбиназы), состоящей из факторов Xa, Va, Ca2+ и фосфолипида, который отщепляет из неактивного профермента протромбина ферментативно активный тромбин. Фаза коагуляции (Образование фибрина). В фазе коагуляции ферментативно активный тромбин отщепляет от фибриногена низкомолекулярные пептиды (фибринопептиды). Так образуются мономеры фибрина, которые через нековалентные связи (водородные мостики, например) полимеризуются в фибрин. НО! Для полной стабилизации требуется ФXIII (активируется тромбином), в присутствии которого возникают ковалентные связи между мономерами фибрина и тромб укрепляется. Доп: Помимо привычного для всех фагоцитоза нейтрофилы также продуцируют NET (Neutrophil extracellular traps), основной функцией которых является захват и обездвиживание микробов во внеклеточном пространстве. NET состоят из интактных хроматиновых волокон и антимикробных белков. Многоступенчатый процесс образования NET называется «нетоз» (NETosis). После активации некоторые ферменты переносятся из гранул в ядро, вызывают деконденсацию хроматина, разрушают ядерные мембраны и вызывают цитолиз. Активированный эндотелий совместно с нейтрофилами вызывает формирование NET, которые, в свою очередь, являются очень большими структурами и способствуют адгезии тромбоцитов. NET также стимулирует образование и осаждение фибрина. Путем расщепления ингибитора тканевого фактора, стимуляции Xa и связывания XII фактора NET стимулирует внутренний и внешний пути коагуляции. Но в нормальных условиях иммунка не участвует в гемостазе! Фаза ретракции. Нити фибрина укладываются над тромбоцитарным агрегатом и связываются через мембранный рецептор с тромбоцитами. В этом участвует также фибронектин. Пластинки содержат тромбостенин - белок, сходный с актомиозином, который может сокращаться при расщеплении АТФ. За счет сокращения тромбоцитов происходит сжатие тромба, который становится значительно меньше своего объема. Этот процесс и называние ретракцией тромба. Фаза фибринолиза. За процессами свертывания крови следует фаза фибринолиза, в ходе которой сгусток растворяется и сосуд снова становится проходимым. Он является важной защитной реакцией и предотвращает закупорку кровеносных сосудов фибриновыми сгустками, а также приводит к реканализации сосудов после остановки кровотечения. Основным ферментом, разрушающим фибрин, является плазмин (иногда его называют фибринолизин), который в циркуляции находится в неактивном состоянии в виде профермента плазминогена. Активация плазмина возникает в результате действия на него либо активаторов крови (внутренний путь), либо активаторов тканей (внешний путь). Активаторы плазминогена. Тканевые активаторы плазминогена непосредственно преобразуют плазминоген в плазмин. В моче содержится особенно эффективный активатор плазминогена-урокиназа. Она служит для растворения фибриновых сгустков в мочевыводящих путях. Кровяные активаторы (важнейших из них-ФXIIa) для расщепления плазминогена нуждаются в проактиваторах. Важнейшие проактиваторы (в том числе прекалликреин) представляют собой лизокиназы, которые высвобождаются из клеток крови при травматических или воспалительных повреждениях ткани. Как и плазминоген, так и его активаторы обладают высоким сродством к полимеризованному фибрину. Это своего рода “биохимическая ловушка”. 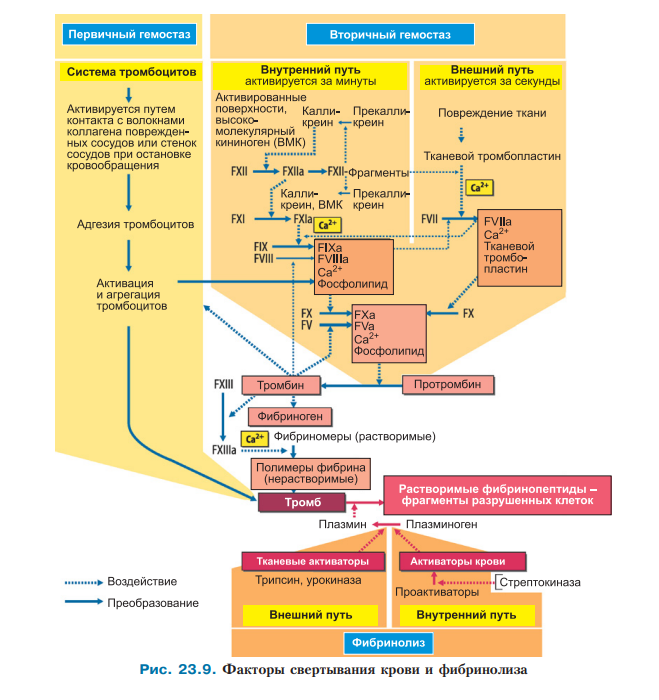 Ретракция кровяного сгустка. Роль тромбостенина. Фибринолиз, его фазы. Механизм действия плазмина. Взаимосвязь коагуляционной и антнкоагуляционной систем крови. Естественные антикоагулянты. Регуляция свертывания крови. Гипер- и гипокоагулемия. Группы крови. Понятие об агглютинации эритроцитов, ее причины и последствия для организма. Агглютинируемые и агглютинирующие факторы. Система АВО. Наследование групп крови. Агглютинируемые факторы=Агглютиногены-гликолипиды на поверхности мембраны эритроцитов, обладающие антигенными свойствами. Они обозначаются буквами А и В. Агглютинирующие факторы=Агглютинины-специфические антитела, находящиеся в плазме крови и реагирующие с мембранами эритроцитов. Они относятся к фракции γ-глобулинов и обозначаются как α и β (анти-А и анти-В). Агглютинация (изогемагглютинация) - процесс склеивания(агглютинирования) эритроцитов. Причиной агглютинации является реакция антиген–антитело. Например, анти-А (или анти-В) агглютинины плазмы смешиваются с эритроцитами, содержащими, А (или В) агглютиногены, эритроциты агглютинируют в результате присоединения к ним агглютининов. Кроме того, антитела по системе АВО относятся к IgM и имеют 10 участков связывания, то есть, агглютинин может связываться сразу с несколькими клетками. Связывание с эритроцитами ведет к образованию комков из клеток, что и ведет к агглютинации. В таких случаях происходит закупорка капилляров агглютинированными эритроцитами, обусловленная гемолизом блокада почечных канальцев и системные иммунные реакции, которые могут приводить к смерти. Мало ли: Одним из наиболее опасных осложнений трансфузионных реакций является почечная недостаточность, которая может начаться в течение нескольких минут или часов и продолжаться до тех пор, пока человек не умрет от этого осложнения. Почечная недостаточность является, вероятно, результатом трех причин. Во-первых, реакция антиген-антитело при трансфузионных осложнениях высвобождает из гемолизированной крови токсические вещества, вызывающие мощное сужение почечных сосудов. Во-вторых, потеря циркулирующих красных клеток крови реципиента наряду с выделением токсических веществ из гемолизированных клеток и в результате иммунной реакции часто ведет к циркуляторному шоку. Артериальное давление падает до очень низких значений, в связи с чем почечный кровоток и выделение мочи резко снижаются. В-третьих, если количество свободного гемоглобина, высвобождаемого в циркулирующую кровь, превышает его количество, которое может связаться с гаптоглобином (белком плазмы, связывающим небольшое количество гемоглобина), основная часть избытка фильтруется через гломерулярную мембрану в почечные канальцы. Небольшое количество гемоглобина может реабсорбироваться через канальцевый эпителий в кровь, не оказывая вреда; если лишнего гемоглобина много, тогда реабсорбируется только небольшой процент. Поскольку вода продолжает реабсорбироваться, внутриканальцевая концентрация гемоглобина резко повышается и происходит его осаждение, в результате блокируются многие из почечных канальцев. В течение следующих часов или дней физическая деформация клеток или атака их фагоцитирующими лейкоцитами разрушает мембраны агглютинированных клеток, высвобождая гемоглобин в плазму. Этот процесс называют гемолизом эритроцитов. Иногда при несовместимости крови реципиента и донора происходит немедленный гемолиз эритроцитов в циркулирующей крови. В этом случае антитела вызывают лизис красных клеток крови путем активации системы комплемента, в результате выделяются протеолитические ферменты (литический комплекс), разрушающие клеточные мембраны. Немедленный внутрисосудистый гемолиз бывает гораздо реже, чем агглютинация с последующим задержанным гемолизом, поскольку для немедленного гемолиза не только необходим высокий титр антител. Кровь каждого человека характеризуется определенным набором специфических антигенов эритроцитнов (белками наряду с гликолипидами). Этот набор и определяется группу крови человека. Наибольшее система значение для практической медицины имеют системы АВ0 и система Rh. |
