Курсовая работа методы обнаружения и количественного определения биологически активных веществ выполнил студент
 Скачать 0.6 Mb. Скачать 0.6 Mb.
|
|
Министерство образования и науки Российской Федерации Федеральное государственное бюджетное образовательное учреждение высшего образования «МУРМАНСКИЙ ГОСУДАРСТВЕННЫЙ Гуманитарный УНИВЕРСИТЕТ»
КУРСОВАЯ РАБОТА МЕТОДЫ ОБНАРУЖЕНИЯ И КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ БИОЛОГИЧЕСКИ АКТИВНЫХ ВЕЩЕСТВ Выполнил студент Студнева О.В., направление подготовки Биология, очная форма обучения Научный руководитель: Сагайдачная В.В., к.п.н., доцент кафедры естественных наук Мурманск 2015 СОДЕРЖАНИЕ стр. ВВЕДЕНИЕ…………………………………………………………..………. 3 ГЛАВА I. БИОЛОГИЧЕСКИ АКТИВНЫЕ ВЕЩЕСТВА В ОРГАНИЗМЕ ЧЕЛОВЕКА 1.1. Понятие о биологически активных веществах….…...……………..…. 5 1.2. Витамины как биологически активные вещества белкового строения……………………………………….……………………………14 ГЛАВА II. ПРИНЦИПЫ И МЕТОДЫ БИОХИМИЧЕСКОГО АНАЛИЗА БИОГЕННЫХ ВЕЩЕСТВ 2.1. Основные этапы проведения биохимического анализа……………………………………...………………………..…….... 19 2.2. Физико-химические методы исследования структуры вещества….30 2.3. Методы выделения биологически активных веществ белкового строения..………………………………………………………………..….. 34 ГЛАВА III. МЕТОДЫ ОБНАРУЖЕНИЯ И ОПРЕДЕЛЕНИЯ КОЛИЧЕСТВЕННОГО СОДЕРЖАНИЯ ВИТАМИНА С В ПРОДУКТАХ ПИТАНИЯ 3.1. Качественные методы определения аскорбиновой кислоты ………. 39 3.2 Количественные методы определения аскорбиновой кислоты …..… 43 ЗАКЛЮЧЕНИЕ ………………………………………….………………… 47 ВЫВОДЫ………………………………………………………..………….. 48 СПИСОК ЛИТЕРАТУРЫ …………………………………………….....…49 ВВЕДЕНИЕ Биологически активные вещества (БАВ) — это химические вещества, обладающие высокой физиологической активностью при небольших концентрациях по отношению к определённым группам живых организмов (в первую очередь — по отношению к человеку) или к отдельным группам их клеток. Физиологическая активность веществ может рассматриваться как с точки зрения возможности их медицинского применения, так и с точки зрения поддержания нормальной жизнедеятельности человеческого организма. Превышение установленных дозировок может привести к необратимым нарушениям в организме человека. Это особенно важно при приеме лекарственных средств. Так, при применении препаратов трёхвалентного железа (показания к лечению железодефицитной анемии) необходим дополнительно приём витамина С (аскорбиновой кислоты). Это приводит к изменению концентраций связанных с обменом аскорбиновой кислоты веществами (кобаламин, витамины А и Е и др.). Для применения на практике системы взаимодействующих биологически активных веществ как витаминоминеральной терапии необходимо точно рассчитать действующие концентрации и по возможности снизить избытки биологически активных веществ в лекарственных препаратах. Биологически активные вещества высокоспецифичны, поэтому для работы с ними требуются специализированные методы. Это обуславливает актуальность нашей работы. Предметом исследования являются методы качественного и количественного определения биологически активных веществ. Объектом исследования выступают витамины как представители биологически активных веществ, в частности витамин С. Цель работы – изучить методы количественного и качественного анализа биологически активных веществ на примере витамина С. В связи с поставленной целью нами были выдвинуты следующие задачи:
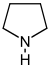
Выполнение поставленных задач обеспечит дальнейшую разработку витаминоминеральной диеты при лечении железодефицитной анемии, при которой приём железосодержащих препаратов необходимо сопровождать дополнительным приёмом аскорбиновой кислоты. ГЛАВА I. БИОЛОГИЧЕСКИ АКТИВНЫЕ ВЕЩЕСТВА В ОРГАНИЗМЕ ЧЕЛОВЕКА 1.1. Понятие о биологически активных веществах Жизнедеятельность организма обеспечивается двумя процессами - ассимиляцией и диссимиляцией, в основе которых лежит обмен веществ между внутренней (клетками организма) и внешней средой. Для нормального течения обменных процессов необходимо поддерживать постоянство химического состава и физико-химических свойств внутренней среды организма (гомеостаз). Оно зависит от определенных факторов, среди которых важное место занимают биологически активные вещества, поступающие с пищей (витамины, ферменты, минеральные соли, микроэлементы и др.) и осуществляющие гармоническую взаимосвязь и взаимозависимость всех физиологических и биохимических процессов в организме [4]. Нормализуя, регулируя все жизненные функции, биологически активные вещества оказывают также эффективное лечебное действие. В состав лекарственного сырья входят различные биологически активные вещества разнообразного фармакологического действия: алколоиды, витамины, ферменты, гормоны, гликозиды, эфирные масла, кумарины и микроэлементы. Алкалоиды - органические азотсодержащие соединения, преимущественно растительного происхождения, обладающие основными свойствами. Основания алкалоидов, нерастворимые в воде, с кислотами образуют хорошо растворимые в воде соли. Из водных растворов алкалоиды осаждаются дубильными веществами, солями тяжелых металлов, йодидами, и некоторыми другими соединениями и поэтому несовместимы с ними в лекарствах. Алкалоиды обладают очень высокой физиологической активностью и поэтому в больших дозах - это яды, а в малых - сильнодействующие лекарства различного действия: атропин, например, расширяет зрачок и повышает внутриглазное давление, а пилокарпин, наоборот, его суживает и понижает внутриглазное давление; кофеин и стрихнин возбуждают центральную нервную систему, а морфин угнетает ее; папаверин расширяет кровеносные сосуды и снижает артериальное давление, а эфедрин суживает сосуды и повышает артериальное давление и т.д. [13]. Алкалоиды представлены несколькими основными группами (табл. 1). Таблица 1 Основные классы мономерных алколоидов
Наличие аминогрупп в составе и синтез из аминокислот указывает на их белковое происхождение алколоидов, что необходимо учитывать при подборе методик определения и выделения других БАВ белковой структуры. Витамины - группа органических веществ разнообразной структуры, жизненно необходимых человеку и животным для нормального обмена веществ и жизнедеятельности организма. Многие из них входят в состав ферментов (каболамин, тиамин, фолат и т.д.) или принимают участие в образовании их (аскорбиновая кислота, флавоноиды), активизируют или тормозят активность некоторых ферментных систем [5]. В основном витамины синтезируются растениями и вместе с пищей поступают в организм, некоторые из них образуются микробами, живущими в кишечнике. Витамины группы D синтезируются из липоидов (жироподобных веществ) кожи под влиянием ультрафиолетовых лучей. Витамины делят на жирорастворимые - А, D, Е, F, К и водорастворимые - все остальные. Гликозиды - органические соединения из растений, обладающие разнообразным действием. Их молекулы состоят из двух частей: сахаристой части, называемой гликоном, и несахаристой - генина, или агликона (рис. 1).  Рисунок 1. Cтруктурная формула гликозидов Под влиянием ферментов или при кипячении с разбавленными кислотами гликозиды расщепляются. В качестве гликона они могут содержать различные моносахариды, чаще всего глюкозу, а иногда специфические сахара, которые в свободном виде в растениях не встречаются. В молекулу гликозида может входить как один, так и несколько сахаров. Чем больше сахаров в молекуле, тем более нестойкими являются гликозиды. Поэтому по своему гликозидному составу живые растения и лекарственное сырье могут отличаться, так как некоторые из сахаров при сушке могут отщепляться [11]. Гликоалкалоиды - родственные гликозидам соединения, у которых генинами служат алкалоиды. Такие соединения содержатся в растениях, не имеющих близкого ботанического родства. Например, чемерица из семейства лилейных, многие растения семейства пасленовых. Так, в траве паслена дольчатого найдены гликоалкалоиды соласолин и соламаргин, которые при кипячении с кислотами отщепляют алкалоид соласодин. Последний служит источником получения прогестерона, из которого затем на предприятиях вырабатывают гормональные препараты: кортизон, гидрокортизон и многочисленные другие. Такой способ получения лекарств называется полусинтетическим [18]. Дубильные вещества, или таниды, обладают вяжущим вкусом и способны превращать шкуру животного в дубленую кожу. На воздухе эти вещества окисляются, образуя флобафены - продукты, окрашенные в бурый цвет и не обладающие дубящими свойствами [15]. Выделенные из растений дубильные вещества представляют собой аморфные или кристаллические вещества, растворимые в воде и спирте. С солями тяжелых металлов они образуют осадки, а с солями трехвалентного железа - окрашенные соединения. Осаждают слизи, белки, клеевые вещества, алкалоиды, отчего несовместимы с ними в лекарствах. С белками они образуют нерастворимые в воде альбуминаты, на чем основано их применение в медицине (бактерицидное, противовоспалительное действие). Таким свойством не обладают флобафены, поэтому сушку сырья, содержащего дубильные вещества, нужно производить быстро, чтобы сохранить их максимальное количество. Кумарины (рис. 2) - природные соединения, в основе химического строения которых лежит кумарин или изокумарин. Сюда также относят фурокумарины и пиранокумарины.  Рисунок 2. Основные представители кумаринов Кумарины характерны в основном для растений семейств зонтичных, рутовых и бобовых. Здесь они находятся преимущественно в свободном виде и очень редко - в форме гликозидов. В зависимости от химического строения кумарины обладают различной физиологической активностью: одни проявляют спазмолитическое действие, другие - капилляроукрепляющую активность. Есть кумарины курареподобного, успокаивающего, мочегонного, противоглистного, обезболивающего, противомикробного и иного действия. Некоторые из них стимулируют функции центральной нервной системы, понижают уровень холестерина в крови, препятствуют образованию тромбов в кровеносных сосудах и способствуют их растворению [4]. Имеются кумарины, повышающие чувствительность кожи к ультрафиолетовым лучам (их используют для лечения лейкодермии), обладающие спазмолитическими и коронарорасширяющим действием, ускоряющие заживление язв, стимулирующие дыхание и повышающие артериальное давление. Микроэлементы имеют большое значение в жизни человека, так как входят в состав гормонов (стероидные гормоны), витаминов (каболамин), многих ферментов (метионин), дыхательных пигментов, образуют соединения с белками, накапливаются в некоторых органах и тканях человека, особенно в эндокринных железах. Микроэлементы содержатся в растительных и животных тканях в очень малых количествах (тысячных и меньших долях процента, но в некоторых случаях - в сотых и даже в десятых долях процента). Таких элементов насчитывают теперь 60, из них 24 входят в состав крови, 30 содержатся в молоке. Доказана роль йода, кобальта и брома в функции щитовидной железы [9]. При недостатке кобальта наблюдается разрастание этой железы вследствие новообразования клеток, а избыток брома препятствует накоплению йода в ней. Органические комплексы микроэлементов участвуют в процессах обмена веществ, оказывая влияние на рост и развитие, размножение, кроветворение. Экдизоны - вещества гормонального характера, обладают высокой биологической активностью. Так, экдизоны левзеи сафлоровидной проявляют стимулирующее и тонизирующее действие. Эти вещества, как и гликозиды женьшеня, элеутерококка, родиолы розовой и лигнаны лимонника, оказывают иммуностимулирующее действие. Эфирные масла - летучие ароматные жидкости сложного химического состава, главными компонентами которых являются терпеноиды. Эфирные масла содержат смесь различных органических веществ, как жидких, так и кристаллических, легко растворимых друг в друге. Так, в мятном масле содержится 50% и более кристаллического ментола, а в анисовом - до 80% анетола [11]. Выделенные из растений эфирные масла представляют собой бесцветные или слегка желтоватые маслянистые жидкости со своеобразным запахом. Исключение составляют ромашковое масло, окрашенное в темно-синий цвет, масло горькой полыни - сине-зеленое. Таким образом, все БАВ имеют сложное строение (не считая БАВ абиогенного характера – микроэлементы), чем обусловлена их высокая активность и роль в физиологических процессах как животных, так и растений. В основном все БАВ имеют белковую структуру, в том числе и витамины, изучение которых является задачей нашего исследования. 1.2. Витамины как биологически активные вещества белкового строения В клетках и тканях встречается свыше 170 различных аминокислот. В составе белков обнаруживаются лишь 26 из них; обычными же компонентами белка можно считать лишь 20 аминокислот. Растения синтезируют все необходимые им аминокислоты из более простых веществ. В отличие от них животные не могут синтезировать все аминокислоты, в которых они нуждаются; часть из них они должны получать в готовом виде, т. е. с пищей. Часть аминокислот синтезируются в самом организме человека, но существует, как известно, 10 незаменимых аминокислот (валин, лейцин, изолейцин, треонин, метионин, фенилаланин, триптофан, лизин, гистидин и аргинин), синтез которых в организме невозможен [17]. Незаменимые аминокислоты поступают в организм в составе белков пищи. Отсутствие или недостаток незаменимых аминокислот приводит к остановке роста, падению массы, нарушениям обмена веществ, при острой недостаточности — к гибели организма. Белки - это сложные органические соединения, состоящие из углерода, водорода, кислорода и азота. В некоторых белках содержится еще и сера. Часть белков образует комплексы с другими молекулами, содержащими фосфор, железо, цинк и медь. Существуют различные классификации. Определяющим в функционировании белков и белковых структур являются их состав. По классификации, представленной В.М.Степановым [17] белки делятся на простые и сложные. Простые белки состоят из аминокислот, а сложные включают в себя небелковую (простетическую) группу (табл. 2). Таблица 2 Классификация белков по составу
Белки, имеющие одинаковый аминокислотный состав, но разную последовательность аминокислот в молекуле белка, будут иметь разную форму и выполнять разные функции. Кроме того, как мы увидим в дальнейшем, идентичные белки могут или не могут выполнять сходную функцию в зависимости от их конформации. Пространственная ориентировка имеет большое значение при анализе структуры белка и веществ белкового происхождения. Выделяют четыре структуры белка ссылка (рис. 3).  Рисунок 3. Структуры белка. 1 – первичная, 2 – вторичная, 3 – третичная, 4 – четвертичная. Первичная структура, представляет собой последовательность аминокислотных остатков, соединенных друг с другом пептидными связями. Именно в таком виде белок образуется на рибосомах. Благодаря образованию водородных связей между радикалами отдельные участки белковой молекулы закручиваются в спираль или формируют складчатый слой. В результате образуется вторичная структура белка. Дополнительные связи определяют формирование третичной структуры белка. Многие (но не все) белки имеют четвертичную структуру, которая образуется, когда несколько молекул белка, имеющих третичную структуру, взаимодействуют друг с другом через радикалы аминокислот. В результате формируется молекула в виде шара (глобулярные белки) или нити (фибриллярные белки). Белки, которые обладают ферментативной активностью, чаще всего являются глобулярными. Структурные белки, например белки, входящие в состав волос или мышц, являются фибриллярными [16]. Витамины относятся к глобулярным белкам, но по составу могут относиться к различным группам. В ходе различных биохимических превращений витамины могут входить в состав или являться предшественниками различных эффекторов (ферментов, молекулы которых кроме каталитических центров содержат ещё и регуляторные участки). Например, В1 или тиамин входит в состав лиаз, декарбоксилирующих кетокислоты (пируватдегидрогеназа, кетоглутаратдегидрогеназа и т.д.), в виде эфира с пирофорной кислотой [14]. В результате монофосфорилирования фолиевой кислоты (витамин В6) образуется кофермент пиридоксальфосфат, принимающий участие во многих транс-процессах. Исследуемый нами витамин С или аскорбиновая кислота играет роль кофактора в реакции ферментативного гидроксилирования, при котором остатки пролина и лизина в коллагене соединительной ткани позвоночных превращаются в остатки 4-гидроксопролина и 5-гидроксолизина (рис. 4). Гидроксипролиновые и гидроксилизиновые остатки обнаружены только в коллагене и не встречаются ни в одном другом белке животных. Аскорбиновая кислота принимает обязательное участие в образовании основного компонента соединительной ткани высших животных, стимулирует заживление ран, но пока не ясно, является ли это ее единственной и даже главной функцией.  Рисунок 4. Продукты ферментативного гидроксилирования пролина По мнению ряда ученых (В.Эллиот, Р.Досон, Я.Кольман) витамин С принимает активное участие практически во всех биохимических процессах (переход проколлагена в коллаген, образование холестерина из жирных кислот и т.д.). Но, обладая рядом специфичных свойств предполагает использование сложных методов анализа. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||