Курсовая работа методы обнаружения и количественного определения биологически активных веществ выполнил студент
 Скачать 0.6 Mb. Скачать 0.6 Mb.
|
|
ГЛАВА III. МЕТОДЫ ОБНАРУЖЕНИЯ И ОПРЕДЕЛЕНИЯ КОЛИЧЕСТВЕННОГО СОДЕРЖАНИЯ ВИТАМИНА С В ПРОДУКТАХ ПИТАНИЯ 3.1. Качественные реакции определения аскорбиновой кислоты Для определения содержания аскорбиновой кислоты в овощах, фруктах и ягодах используется метод тонкослойной хроматографии [6] и количественный анализ. Хроматографирование проводится на силуфоловых пластинах, представляющих собой алюминиевую фольгу, покрытую тонким слоем широкопористого силикагеля, закреплённого крахмалом. Для анализа используют растворы исследуемых объектов. Для этого выдеренный методом гель-фильтрации материал помещают в буферный раствор с соляной кислотой. Оборудование: 5 силуфоловых пластин размером 5 х 7 см, капилляры, химические стаканы, раствор аскорбиновой кислоты, мерный цилиндр, спирт, гексан, стекло, аммиачный раствор нитрата серебра, пульверизатор. Проведение эксперимента. На силуфоловых пластинах отмечают линии старта и финиша. На стартовые линии наносят капилляром 1%-ный раствор аскорбиновой кислоты в качестве свидетеля и исследуемые образцы (диаметр наносимых проб составляет 4мм, расстояние между ними 15мм). Эти пластины опускают вертикально в химические стаканы с системой растворителей—спирт, гексан (1:3) с высотой в стаканах 3мм и закрывают их стеклом. Под действием капиллярных сил растворитель начинает двигаться вверх по пластинам. Он достигает пятен и увлекает их за собой. Молекулы каждого вещества при хроматографировании имеют характерную скорость движения. Расположение вещества на хроматограмме зависит от его хроматографической подвижности Rf, которая определяется отношением расстояния от старта до середины пятна к расстоянию от старта до финиша [12]. Rf аскорбиновой кислоты—0,71. Через какое-то растворители достиг линии финиша. Пластины достают и оставляют на несколько минут для испарения растворителя. Наличие в анализируемых веществах аскорбиновой кислоты мы обнаружили качественной реакцией с аммиачным раствором нитрата серебра. AgNO3+ NH4OH = Ag2O + H2O + NH4NO3 C6H8O6 + Ag2O = C6H6O6 + H2O + 2Ag Ещё один метод обнаружения аскорбиновой кислоты - реакция с метиленовой синью [19]. Аскорбиновая кислота на свету восстанавливает метиленовую синь в бесцветное соединение (лейкоформу), окисляясь в дегидроаскорбиновую кислоту (рис. 6).  Рисунок 6. Реакция аскорбиновой кислоты с метиленовой синью Реактивы: исследуемый образец, приготовленный аналогично первому методу; метиленовая синь, 0,01%-ный раствор; натрий углекислый, 5%-ныы раствор. Проведение эксперимента: К 1 мл исследуемого образца добавляют 1—2 капли раствора метиленовой сини и 2 - 3 капли раствора соды. Пробирку слегка подогревают. Наблюдают обесцвечивание синей окраски. Реакция с железосинеродистым калием. Аскорбиновая кислота, окисляясь, восстанавливает железосинеродистый калий до железистосинеродистого который с ионом трехвалентного железа образует в кислой среде берлинскую лазурь [12] (рис. 7). 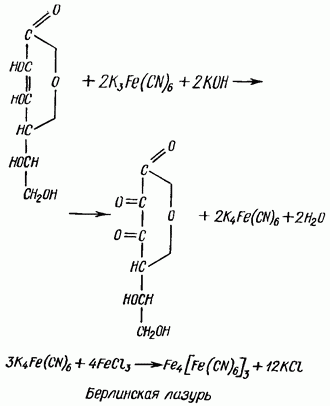 Рисунок 7. Двухступенчатая качественная реакция аскорбиновой кислоты сжелезосинеродистым калием. Реактивы: исследуемый образец в буферном растворе; железосинеродистый калий, 5%-ный раствор; едкое кали, 5%-ный раствор; соляная кислота, 10%-ный раствор; хлорное железо, 1%-ный раствор. Проведение эксперимента: К 1 мл исследуемого образца прибавляют 2 капли раствора едкого кали, столько же раствора железосинеродистого калия и встряхивают пробирку, после чего добавляют 6—8 капель 10%-ного раствора соляной кислоты и 1—2 капли раствора хлорного железа. Выпадает синий или зеленовато-синий осадок берлинской лазури. Наиболее простой и доступной является реакция аскорбиновой кислоты с метиленовой синью. При этом метод тонкослойной хроматографии является более чувствительным и применим для сложного по составу биологического материала. 3.1. Количественные методы определения аскорбиновой кислоты Наиболее простым и экономичным методом количественного определения аскорбиновой кислоты является метод йодометрии [11]. Йодат калия в кислой среде выделяет свободный йод по формуле: KJO3 + 5KJ + 6HCl = 6KCl + 3J2 + 3H2O В присутствии витамина С свободный йод восстанавливается в йодоводород, а аскорбиновая кислота окисляется до дегидроаскорбиновой. Реактивы: исследуемый образец, 2% раствора соляной кислоты, 1% раствора йодата калия, 1% раствора крахмала, Проведение эксперимента: В коническую колбу на 25 мл помещают 1 мл 2% раствора соляной кислоты, 0,5 мл 1% раствора йодата калия, 2-3 капли 1% раствора крахмала, 2 мл исследуемого раствора и доводят общий объем исследуемой жидкости дистиллированной водой до 10 мл. Титруют из бюретки 0,03 н раствором йодата калия до появления стойкого слабо-синего окрашивания. 1 мл 0,03 н йодата калия эквивалентен 0,00264 мг витамина С. Конец титрования определяется по появлению голубовато-синей окраски от избытка йодата калия после того, как вся аскорбиновая кислота окислена выделяющимся йодом (определение ведется в присутствии крахмала). Содержания аскорбиновой кислоты в мг% в исследуемых извлечениях вычисляли по формуле Х = 0,0026*а*100/ b где 0,00264 – эквивалент йодата калия по аскорбиновой кислоте (мг), a – количествово йодата калия в мл, израсходованного на титрование, b – количество исследуемого вещества в мл. Метод Тильманса основан на реакции с раствором 2,6 – дихлорфенолиндофенола (рис. 8).  Рисунок 8. Обесцвечивание реактива Тильманса аскорбиновой кислотой Реактивы: исследуемый образец; 0,001Н раствор 2,6 – дихлорфенолиндофенола (реактив Тильманса). Проведение эксперимента: Определение витамина С производится путем титрования испытуемого раствора указанным реактивом в кислой среде до появления слабо-розового окрашивания, указывающего, что вся аскорбиновая кислота вступила в реакцию. Избыток реактива приобретает в кислой среде красный цвет и окрашивает раствор. Определение проводится путём титрования исследуемой жидкости 0,001 н. раствором 2,6 – дихлорфенолиндофенола в условиях, предохраняющих аскорбиновую кислоту от разрушения (кислая среда, которую обеспечивает буферная система исследуемого образца). Одному миллилитру 0,001Н раствора 2,6 – дихлорфенолиндофенола соответствует 1 мл 0,001Н раствора (0,088 мг) аскорбиновой кислоты. Для расчёта содержания аскорбиновой кислоты (Х) используют следующие формулы. Х = 0,088*А*Б*1000 / В*Г (мг/кг); Х = 0,0005*А*Б*1000 / В*Г (ммоль/кг). Где: 0,088 (0,0005) – количество аскорбиновой кислоты (мг, ммоль), соответствующее 1 мл 0,001 н. раствора; А - количество раствора 2,6 – дихлорфенолиндофенола, израсходованное на титрование, мл; Б – общее количество вытяжки, мл; В – масса вещества, взятого для анализа; Г – количество вытяжки, взятое для титрования, мл; 1000 – коэффициент пересчёта на 1 кг продукта. Для статистической обработки результатов обоих методов следует использовать t-критерий Стьюдента, который докажет или опровергнет разницу концентраций витамина С в различных продуктах питания и витаминных комплексах. Повторяемость следует соблюсти не менее 30 повторений для одного объекта. Содержание аскорбиновой кислоты следует выразить в долях, формула для нахождения критерия: t = d / Sd, где d – разность долей, а Sd – ошибка разности; Sd в свою очередь находим по формуле:  Для оценки зависимости изменения концентрации активных веществ (кобаламин, витамин Е, железо и др.) от изменения концентрации аскорбиновой кислоты следует применить f-критерий Фишера, определяющийся как отношение дисперсий. Для оценки этим критерием количество опытов для каждой пары выборок должно быть не менее 20. Критерий находим по формуле: 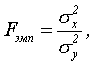 , где σ2х и σ2у - дисперсии первой и второй выборки соответственно. , где σ2х и σ2у - дисперсии первой и второй выборки соответственно.Максимальная достоверность эксперимента будет достигнута при использовании обоих количественных методов и независимой оценкой полученных результатов. ЗАКЛЮЧЕНИЕ Для работы с лекарственными препаратами и составления витаминоминеральных диет необходимо точно знать действующие дозировки биологически активных веществ, входящих в состав исследуемых и создаваемых в перспективе лекарств. Определённые в работе методы работы с витамином С помогут обеспечить точность и чистоту планируемых экспериментов на каждом этапе работы. Метод Гель-фильтрации позволят выделить витамин С. Качественные реакции в буферном растворе, содержащем витамин С, дают возможность обнаружить не только действующую аскорбиновую кислоту, но другие соединения, содержащие белковую, углеводную или липидную составляющие. Использование методов йодометрии и Тильманса независимо друг от друга даст возможность точно определить содержание аскорбиновой кислоты во всем исследуемом материале. Количественный анализ так же следует проводить несколькими методами, что повысит точность полученных результатов. При работе с лекарственными средствами от точности исследования зависит здоровье человека. При соблюдении всех правил получения и определения биологически активных веществ, а так же тщательном исследовании их взаимовлияния, можно создать поддерживающий и лечебный витаминоминеральные комплексы, оказывающие терапевтическое влияние при многих серьёзных заболеваниях, снизив при этом негативное воздействие лекарственных препаратов. ВЫВОДЫ 1. Биологически активные вещества (БАВ) являются высокоактивными соединениями, управляющими практически всеми физиологическими процессами живых организмов. По своей структуре биологически активные вещества делятся на биогенные (ферменты, витамины, алколоиды и т.д.) и абиогенные (минеральные вещества). Высокая реакционная способность биогенных БАВ обуславливается наличием специфических групп – алколоиды за счёт азотных групп, гликозиды за счёт сахаристой гликономной части, витамины за счёт перехода в ферментативные соединения. 2. При выборе метода работы с биогенными биологически активными веществами необходимо учесть строение и действующие группы (в т.ч. липидные, углеводные и др.) этих веществ и определить рациональность использования того или иного метода. 3. Для работы с витаминами как с белковыми структурами целесообразно применять точные и мягкие методы гель-фильтрации, которые сохранят активность вещества после выделения. Качественные реакции следует проводить в буферном растворе соляной кислоты для предохранения аскорбиновой кислоты от разрушения. 4. Качественная и количественная методика представлена рядом реакций, осуществление которых доступно в лабораторных условиях. Наиболее точны при определении содержания аскорбиновой кислоты является метод тонкослойной хроматографии. Количественно определять содержание витамина С эффективней независимым проведением йодометрии и реакции Тильманса. Количество повторений опята должно быть не менее 30 для достоверного подсчёта статистических критериев (Стьюдента и Фишера). Это обеспечит точность, применимую для фармакологических исследований. СПИСОК ЛИТЕРАТУРЫ
. |
