Курсовая работа Основные проблемы производства инъекционных лекарственных средств
 Скачать 0.57 Mb. Скачать 0.57 Mb.
|
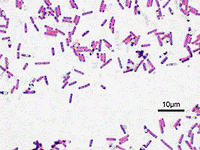 Газовая стерилизация. Использование биологических индикаторов необходимо при проведении всех процедур газовой стерилизации как при валидации циклов, так и при проведении рутинных операций. Рекомендуется использовать споры Bacillus subtilis (например, var. niger ATCC 9372, NCIMB 8058 или CIP 77.18) при использовании этилена оксида. Число жизнеспособных спор должно превышать 5 × 105 на носитель. Параметры устойчивости следующие: величина D составляет более 2,5 мин для испытания цикла при концентрации этилена оксида 600 мг/л, температуре 54 °С и 60 % относительной влажности. Следует убедиться, что после 60-минутного цикла стерилизации с указанными параметрами не наблюдается рост эталонных микроорганизмов, тогда как после 15 мин цикла стерилизации при более низкой температуре (600 мг/л, 30 °С, 60 % влажности) жизнеспособность спор сохраняется. Биологический индикатор должен позволять обнаруживать недоста-точную влажность в стерилизаторе и продукте: при воздействии на него этилена оксида концентрации 600 мг/л при температуре 54 °С в течение 60 мин без увлажнения должна сохраняться жизнеспособность спор.[2,4] .2 Апирогенность Апирогенностью называется отсутствие в инъекционных растворах продуктов метаболизма микроорганизмов - так называемых пирогенных веществ, или пирогенов. Свое название пирогены (от лат. руг - жар, огонь) получили за способность вызывать повышение температуры при попадании в организм. Пирогенные вещества хорошо растворимы и легко проходят сквозь фильтры, величина пор которых превышает 50 нм. Величина же самих пирогенов составляет 1-50 нм. В соответствии с требованиями ГФХ инъекционные растворы не должны содержать пирогенных веществ. Для обеспечения этого требования инъекционные растворы готовят на апирогенной воде для инъекций (или маслах) с использованием медикаментов и других вспомогательных веществ, не содержащих пирогенов.[5] Методы обнаружения пирогенов Для практических целей, наряду с методами удаления пирогенных компонентов, большое значение имеют методы их обнаружения: а) химические; б) физические; в) биологические. Химические методы основаны на проведении определенных цветных реакций. Физические методы основаны на измерении электропроводности и полярографических максимумов. Из-за ряда недостатков первых двух методов чаще всего применяют методы биопроб, которые введены в Фармакопеи различных стран мира. Биологические методы. До настоящего времени основным и официально принятым во всех странах методом испытания лекарственных средств на наличие пирогенных примесей считается метод, основанный на троекратном измерении температуры тела кролика после внутривенного введения исследуемого препарата. Повышение температуры на 0,6°С или более, согласно требованию фармакопей, считается доказательством наличия пирогенов. Специальные статьи Фармакопей оговаривают условия проведения этого испытания, поскольку факторы - химический, физический, физиологический - могут повлиять на результат испытания. И даже при самом строгом соблюдении требований к проведению испытаний невозможно избежать случайных ошибок, связанных с индивидуальной чувствительностью животных к пирогену и препарату, различными климатическими условиями, времени постановки опыта и т. п. Все это может отразиться на показателях температуры, измеренной с точностью до ±0,1°С. Согласно данным различных Фармакопей доза одного и того же препарата в ряде случаев колеблется в широких пределах. Очень часто при равных или весьма близких дозах препаратов объемы вводимых растворов различаются в 5 раз. Отмечено, что наблюдается большой разрыв между дозами для кроликов и человека. Нередко эти дозы различаются в 100-6000 раз. По мнению ученых, изучавших этот вопрос, тест-доза препарата при испытании пирогенности должна подбираться индивидуально, учитывая его фармакологию, переносимость кроликом, и ориентировочно должна составлять 1/10 максимальной суточной дозы для человека. Существует вариант условий признания препарата пирогенным либо апирогенным: воду или раствор лекарственного средства считают апирогенным, если сумма максимальных повышений температур у 3 кроликов не превышает 1,2°С, и пирогенным, если она равна или больше 2,2°С. Если сумма повышений температуры у 3 кроликов больше 1,2°С, но меньше 2,2°С, то испытание повторяют на 5 кроликах. Воду или раствор лекарственного средства считают пирогенным, если сумма повышений температуры у 8 кроликов равна или больше 3,8°С, в противном случае - апирогенным. В последнее время заметное распространение получает метод испытания лекарственных средств на пирогенность in vitro с использованием лизата амебоцитов краба Лимулюс. Этот метод имеет ряд преимуществ перед фармакопейным: он чувствительнее в 5-10 раз, результат получается быстрее, возможно количественное определение пирогена. Кроме того, с его помощью возможен контроль препаратов, которые нельзя испытать на кроликах. Одним из недостатков этого метода является его специфичность в отношении эндотоксина грамотрицательных бактерий, т. е. опасность не выявить наличие в лекарственных средствах пирогенов другого происхождения.[2,3,5] Методы удаления пирогенных веществ Методы депирогенизации подразделяются на: .химические; .физические; .энзиматические. Химические методы удаления пирогенов. Растворы, содержащие пирогены, нагревают при 100°С в течение 2 ч с добавкой 0,1 моля перекиси водорода. Эффективен способ нагрева растворов при температуре 116°С в течение 20 мин с добавкой 0,04 моля перекиси водорода. Ряд методов основан на применении раствора перманганата калия. Рекомендуется прибавлять к раствору небольшое количество гипохлорида (щавелевой воды): на 1 л добавляют 0,25 мл раствора гипохлорида натрия с содержанием активного хлора около 0,5%, смесь выдерживают 30 мин. Избыток гипохлорида удаляют с помощью активированного угля (из расчета 15% от объема воды). Для удаления пирогенов предлагается также обрабатывать растворы п-хиноном и антрахиноном, образующих с пирогенами комплексные соединения. Для уничтожения пирогенных веществ можно использовать подогрев раствора с 0,1Н раствором едкого натра или 0,1Н раствором соляной кислоты (при рН 4,0) в течение 1 ч. Происходит гидролитическое расщепление пирогенов с образованием моносахаридов, не обладающих пирогенными свойствами. Расход кислоты и щелочи при этом очень велик, поэтому данный метод следует назвать неэкономичным. Из-за возможного взаимодействия компонентов, химический и энзиматический методы мало приемлемы при промышленном изготовлении растворов для инъекций. Физические методы. Основываются на явлении адсорбции пирогенов активированным углем, каолином, асбестом, целлюлозой и т. п. Количество пирогенных веществ уменьшается после обработки активированным углем путем встряхивания в течение 15 мин, при этом эффективность очистки зависит от природы пирогенных веществ. Гранулированный уголь менее эффективен. Уголь, применяемый для очистки растворов, должен быть тщательно очищен, хорошо промыт водой, не содержать пирогенов и высушен при температуре 250°С в течение 2 ч. Однако обработка растворов активированным углем не всегда приводит к полной депирогенизации. Кроме того, данный метод нельзя применять для очистки растворов лекарственных веществ, легко адсорбируемых углем, например, солей алкалоидов, или легко окисляемых, например аскорбиновой кислоты. Ряд авторов рекомендуют для очистки от пирогенов использовать ионообменные смолы (например, для аминокислот), считая, что они более эффективны, чем активированный уголь. Депирогенизацию воды можно осуществить путем фильтрования через бактериальный фильтр Зейтца. Размер пор многих бактериальных фильтров такой же, как у фильтра Зейтца, но они не пригодны для удаления пирогенных веществ, поэтому нельзя объяснить эффективность удаления пирогенных веществ только малым диаметром пор. Рекомендуется, чтобы диаметр пор фильтра Зейтца не превышал 2,4 мкм. Фильтр Зейтца задерживает пирогенные вещества из раствора на 99,5%, даже когда они находятся в значительном количестве. Чем меньше концентрация пирогенных веществ в растворе, тем лучше они задерживаются на фильтре. Обработка раствора активированным углем с последующим фильтрованием через фильтр Зейтца обеспечивает более полное удаление пирогенных веществ. Для удаления пирогенных веществ из растворов аминокислот, применяемых для внутривенного вливания, предлагается их автоклавирование при температуре 120°С в течение 2-3 ч в атмосфере азота. Уменьшение пирогенных веществ происходит при термической стерилизации в течение 20 мин при 120°С, а при 140°С в течение 20 мин наступает их инактивация. Полное уничтожение пирогенных веществ достигается стерилизацией в сушильном шкафу при температуре 200°С в течение 45 мин или при 250°С в течение 30 мин. При температуре 120°С пирогенность уменьшается в процессе автоклавирования на следующие величины: в течение 30 мин на 25, 1 ч - на 70, 2 ч - на 95, 4 ч - на 100%. К физическим методам удаления пирогенов из растворов следует отнести уничтожение их с помощью ультразвука с частотой 2 МГц и интенсивностью 2 Вт/см2 в течение 10 мин. При этом достигается полное разрушение пирогенных веществ. В то же время ультразвук в 800 МГц и интенсивностью 1,5 Вт/см2 в течение 5- 10 мин незначительно снижает пирогенность воды. При действии ультразвука рН воды изменяется на ±0,75. [2,16] .3 Отсутствие механических включений Источники механических загрязнений растворов. Практически загрязнение препаратов может происходить на всех стадиях производства. Загрязнения парентеральных препаратов делят на три типа: химические (растворимые), микробные и механические. Два последних типа загрязнений тесно связаны между собой: часто одинаковы их источники, их одновременно показывает большинство современных приборов, аналогичны и методы борьбы с ними. Источники возможных загрязнений имеют широкий диапазон. Основные из них: воздух производственного помещения, исходное сырье и растворитель, технологическое оборудование, коммуникации, материалы первичной упаковки (флаконы, пробки), фильтрующие перегородки, обслуживающий персонал. Из названных источников в раствор могут попасть частицы металла, стекла, резины, пластмасс, угля, волокна асбеста, целлюлозы и т. д. На всех твердых частицах могут быть адсорбированы микроорганизмы. Одним из требований ГФ XI издания, предъявляемым к препаратам для инъекций, является полное отсутствие механических включений, видимых невооруженным глазом, при производстве растворов в ампулах (малые объемы). Для больших объемов растворов (100 мл и более) фармакопеи США, Великобритании, а также требования Австралии ограничивают содержание даже меньших частиц. Ужесточение требований к чистоте больших объемов растворов связано с тем, что с увеличением объема раствора большее количество механических включений поступает в организм больного. Степень тяжести неблагоприятных последствий в случае попадания инородных частиц зависит от их размера, природы и количества. Механические включения, находящиеся в инъекционном растворе, могут привести к образованию тромбов, гранулем, аллергических реакций и других патологических явлений. Так, содержащийся а асбесте хризотил может быть причиной злокачественных новообразований. В больших объемах внутривенных вливаний могут содержаться механические включения в виде волокон целлюлозы и частиц пластмасс, наличие которых служит причиной образования микротромбов в легких. И указанного выше следует, что введение в регламентирующие документы различных стран требований, ограничивающих количества невидимых невооруженным глазом механических частиц, является важным условием, обеспечивающим высокое качество инъекционного раствора. Инструментальный контроль содержания механических примесей в инъекционных растворах стал возможен благодаря использованию оптико-электронных приборов. Для количественной оценки содержания механических включений в жидкостях получил распространение метод фильтрации через мембранные фильтры, применяемый и в нашей стране. Основной недостаток данного метода - трудоемкость и большая погрешность субъективного измерения. Этих недостатков лишен телевизионный метод, благодаря системе PMS фирмы «Millipore» для подсчета и измерения частиц, основанный также на процессе фильтрации. Более совершенным устройством для определения содержания количества частиц в растворах служат приборы, основанные на кондуктометрическом и фотоэлектрическом методах регистрации частиц. [11,16] Итак, нормативно-техническая документация предъявляет высокие требования к чистоте инъекционных растворов, что достигается фильтрованием. Важнейшая часть любого фильтра - фильтровальная перегородка, задерживающая твердые частицы и легко отделяющая их. Она должна обладать достаточной механической прочностью, низким гидравлическим сопротивлением и химической стойкостью, обеспечивать возможность регенерации, а также быть доступной по стоимости, не изменяя при этом физико-химические свойства фильтрата. Требования, предъявляемые к фильтрам и фильтрующим материалам для инъекционных растворов, значительно выше перечисленных. Фильтрующие материалы должны максимально защищать раствор от контакта с воздухом; задерживать очень мелкие частицы и микроорганизмы; обладать высокой механической прочностью, чтобы препятствовать выделению волокон и механических включений; противодействовать гидравлическим ударам и не менять функциональные характеристики; не изменять физико-химический состав и свойства фильтрата; не взаимодействовать с лекарственными, вспомогательными веществами и растворителями; выдерживать тепловую стерилизацию. Фильтровальные материалы перед употреблением должны быть обязательно промыты до полного удаления растворимых веществ, твердых частиц или волокон. Выбор фильтрующих перегородок обусловливается физико-химическими свойствами фильтруемого раствора (растворяющая способность жидкой фазы, летучесть, вязкость, рН среды и др.), концентрацией и дисперсностью твердой фазы, требованиями к качеству фильтрата, масштабами производства и т. д. При производстве растворов чаще используют тонкое фильтрование как основное или предварительное, предшествующее микрофильтрованию. Фильтрующие перегородки, используемые для данной цели, могут задерживать частицы как на поверхности, так и в глубине фильтрующего материала. В зависимости от механизма задержания частиц различают фильтры глубинные (пластинчатые) и поверхностные, или мембранные. Глубинное фильтрование. При глубинном фильтровании частицы задерживаются на поверхности и, главным образом, в толще капиллярно-пористого фильтра. Улавливание частиц происходит за счет механического торможения и удержания в месте пересечения волокон фильтрующей перегородки; в результате адсорбции на фильтрующем материале или на участке капилляра, имеющего изгиб или неправильную форму; за счет электрокинетического взаимодействия. Эффективность фильтра зависит от диаметра, толщины волокна и плотности структуры фильтра. Этот способ фильтрации целесообразно применять для малоконцентрированных суспензий (с объемным содержанием твердой фазы менее 1%, так как постепенно происходит закупоривание пор и возрастает сопротивление перегородки). Глубинные фильтры производятся из волокнистого и зернистого материала, тканых, спрессованных, спеченных или другим образом соединенных, образующих пористую структуру. Примерами волокнистых материалов натурального происхождения могут служить шерсть, шелк, хлопчатобумажные ткани, вата, джут, льняная ткань, асбест, целлюлозное волокно. Среди искусственных волокон можно выделить: ацетатное, акриловое, фторуглеродное стекло, металлическое и металлокерамическое волокно, нейлон, капрон, лавсан. В фармацевтической промышленности, кроме того, используют бытовые и технические ткани: мадаполам, бельтинг, фильтробельтинг, миткаль, фильтромиткаль, хлорин, ткань ФПП, целлюлозно-асбестовые ткани. Из зернистых материалов наиболее распространены диатомит, перлит, активированный уголь и др. Диатомит получают из кремнеземных панцирей водорослей - диатомей. Перлит - это стекловидная горная порода вулканического происхождения, используется для изготовления патронных фильтров. Зернистые материалы нашли применение для фильтрования труднофильтруемых жидкостей (биологические жидкости, раствор желатина для инъекций и т. д.). Глубинные фильтры и префильтры, содержащие асбестовые и стеклянные волокна, не должны применяться для парентеральных растворов из-за возможности выделения вредных для организма или труднообнаруживаемых волокон. Большая поверхность адсорбции может привести к потерям действующих веществ на фильтре, а задержание в порах микроорганизмов - к их размножению и загрязненности фильтрата. Поэтому рекомендуется такие фильтры эксплуатировать не более 8 ч. Мембранное фильтрование. Поверхностное фильтрование происходит с образованием осадка на поверхности перегородки. Осадок образует дополнительный фильтрующий слой и постепенно увеличивает общее гидравлическое сопротивление продвижению жидкости. Роль перегородки в этом случае состоит в механическом задержании частиц. К этой группе относятся мембранные фильтры. При мембранном, или ситовом фильтровании, все частицы, имеющие размер больше, чем размер пор фильтра задерживаются на поверхности. Мембранные фильтры изготовлены из полимерных материалов. Фторопластовые мембраны устойчивы в разбавленных и концентрированных растворах кислот, щелочей, спиртов, эфиров, хлороформа и масел. Нейлоновые и полиамидные - в сильных Щелочах и хлороформе. Полиамидные ограниченно совместимы со спиртами. Заводы-изготовители указывают жидкости, не подлежащие фильтрованию, и предельные значения рН, которые выдерживают данный материал. Для ситового фильтрования используют мембраны сетчатого типа, называемые ядерными, или капиллярно-пористыми. Такие мембраны производят из прочных полимерных материалов (поликарбонат, лавсан и др.), которые подвергают бомбардировке в ядерном реакторе. Толщина таких фильтрующих перегородок составляет 5-10 мкм. В настоящее время в фармацевтической промышленности за рубежом используют мембраны сетчатого типа фирмы «Нуклепоре» и «Джелман» (из сополимеров акрилонитрила и винилилденхлорида). |
