лекарственное растительное сырье, содержащее дубильные вещества. курсовая сивикова. Курсовая работа по фармакогнозии лекарственное растительное сырье, содержащее дубильные вещества
 Скачать 1.14 Mb. Скачать 1.14 Mb.
|
|
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ОБРАЗОВАНИЯ КУРСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ МИНИСТЕРСТВА ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ Фармацевтический факультет КАФЕДРА ФАРМАКОГНОЗИИ И БОТАНИКИ  КУРСОВАЯ РАБОТА по фармакогнозии «ЛЕКАРСТВЕННОЕ РАСТИТЕЛЬНОЕ СЫРЬЕ, СОДЕРЖАЩЕЕ ДУБИЛЬНЫЕ ВЕЩЕСТВА» Исполнитель: Сивикова Анна Владимировна, 4 курс, 3 группа Руководитель: Сухомлинов Юрий Анатольевич, кандидат фармацевтических наук, доцент Дата сдачи курсовой работы___________________________________ Оценка____________________________________________________ Подпись руководителя________________________________________ Курск - 2019 Оглавление Введение…………………………………………………………………………..3 Глава 1. Дубильные вещества – объекты изучения фитохимического анализа лекарственного растительного сырья……………...……………………………………………………………….5 Понятие о дубильных веществах и история их открытия……………………………………………..……………………..5 Особенности строения, биосинтеза и физико – химических свойств объекта исследования………………..........................................................8 Растительные источники дубильных веществ……………………….....17 Применение дубильных веществ…………………………………….…..23 Глава 2. Фитохимический анализ лекарственного растительного сырья, содержащего дубильные вещества……………………………………………..25 2.1. Качественный анализ исследуемой группы БАВ…………………………25 2.2.Методики количественного определения дубильных веществ…………………………………………………………………………...27 Глава 3. Перспективные источники дубильных веществ из лекарственного растительного сырья………………………………..……………………………………….……32 3.1. Исследование содержания дубильных веществ корней шиповника собачьего…………………………………………………………………………32 3.2. Исследование содержания дубильных веществ растений семейства Hydrocharitaceae………………………………………………………………….34 Заключение……………………………………………………………………….36 Список литературы………………………………………………………………37 Введение В настоящее время в медицине применяется значительное количество лекарственных препаратов на основе растений. Их доля среди лекарстенных средств (ЛС) составляет около 30%, и в дальнейшем она будет только возрастать. Многолетний положительный опыт применения лекарственных растений в традиционной (народной) и научной медицине позволил растительным фармацевтическим аналогам занять достойное место среди современных лекарственных препаратов [20]. Исходя из выше описанного факта, следует отметить, что основной тенденцией развития фармацевтической промышленности в сфере изготовления фитопрепаратов является изучение имеющейся сырьевой базы, а также поиск и анализ новых свойств выделенных биологически активных веществ (БАВ) из лекарственного растительного сырья (ЛРС). В связи с сезонным возрастанием заболеваемости, связанной с инфекционным агентом, поражающим респираторную систему, наиболее часто применяемой группой в аптечной практике является ЛРС, содержащее дубильные вещества. Помимо антибактериальных, противовоспалительных, антигеморроидальных, местнораздражающих, вяжущих, а также кровоостанавливающих фармакологических свойств были обнаружены следующие виды активности: антирадикальная (антиоксидантная), противоопухолевая, детоксикационная, тонизирующая. Таким образом, целью научной работы является изучение разнообразия ЛРС, содержащего дубильные вещества. Объект исследования: дубильные вещества в ЛРС. В курсовой работе были использованы следующие методы исследования: - теоретические (анализ, классификация, обобщение, индукция, дедукция); - практические (сравнение, наблюдение, измерение, описание, эксперимент). Для достижения данной цели поставлен ряд задач, а именно: - изучить историю формирования научного представления о группе БАВ – дубильные вещества; - рассмотреть основные аспекты строения и свойств анализируемой группы веществ; - проанализировать растительные источники дубильных веществ; - выделить особенности фитохимического анализа объекта исследования; - рассмотреть перспективные растительные источники дубильных веществ на примере растений семейств Rosaceae и Hydrocharitaceae. Глава 1. Дубильные вещества – объекты изучения фитохимического анализа лекарственного растительного сырья Глава 1.1. Понятие о дубильных веществах и история их открытия Дубильные вещества (танниды) — это сложные смеси растительных высокомолекулярных полимеров фенольных соединений с молекулярной массой от 300 до 20000 (порядка 500-3000), обладающие вяжущим вкусом, осаждающие алкалоиды и способные образовывать прочные связи с белками, превращая невыделанную шкуру животных в дубленую кожу [3, 4, 15]. Дубление - это сложное химическое взаимодействие таннидов с молекулами коллагена - основного белка соединительной ткани. Дубящими свойствами обладают многоядерные фенолы, содержащие в молекуле более одного гидроксила. При плоском расположении таннида на белковой молекуле между ними возникают устойчивые водородные, эфирные, а также электровалентные связи, способствующие снижению ее растворимости и изменению конформационных свойств [3]. Этот процесс осуществляется за счет участия гидроксильных групп таннидов и аминогрупп, карбонильных групп, а также других полярных радикалов белковых молекул. Вследствие этого, наблюдается «сшивание» мономеров коллагена поперечными водородными связями, что способствует видоизменению пространственной и коллоидной структур, затвердеванию, уменьшению набухания и деформирования кожи. Это объясняет повышение ее термической, химической и микробиологической стойкости и появление водоотталкивающих свойств. Не все дубильные вещества способны к истинному дублению. Этим свойством отличаются соединения, имеющие молекулярную массу 1000 и более. Полифенольные соединения с массой менее 1000 не способны дубить кожу и обладают только вяжущим действием [3, 15]. 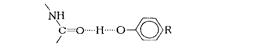 Рисунок 1. Взаимодействие молекул белка с таннидами Прочность взаимодействия таннида с белком зависит от числа водородных связей и лимитируется величиной молекулы полифенольного соединения (рис.1). Молекулярная масса дубильных веществ может составлять до 20000. При этом на 100 единиц молекулярной массы в танидах приходится по 1-2 фенольные оксигруппы. Поэтому количество образующихся водородных связей многочисленно и процесс дубления является необратимым. Гидрофобные радикалы, ориентированные во внешнюю среду, делают кожу недоступной для влаги и микроорганизмов, что объясняет антибактериальные свойства данной группы БАВ. Термин “дубильные вещества” сложился исторически, благодаря способности этих соединений превращать сырую шкуру животных в прочную кожу, устойчивую к воздействию влаги и микроорганизмов. Использовать этот термин официально предложил в 1796 году Сеген для обозначения в экстрактах некоторых растений веществ, способных осуществлять процесс дубления, о котором было упомянуто выше [3]. Сами же танниды были открыты ранее. Первые научные исследования в области химии дубильных веществ относятся ко второй половине XVIII века. Они были вызваны практическими запросами кожевенной промышленности. Первая опубликованная работа «Об использовании плодов черники как сырья для получения дубильных веществ» была опубликована Гледичем в 1754 году [15]. В 1793 году французский химик Николя Дейе впервые получил из растительных объектов танин и исследовал его дубящие свойства. Его работу продолжил Ян Берцелиус и в 1815 году выделил выше описанную субстанцию из коры дуба [3]. В 1891 году вяжущие вещества были выделены в отдельную группу, и профессор Генри Тримбл (США) дал им название танины [15]. Наиболее трудной оказалась задача получения чистой субстанции танинов, без сахаров. Первые очищенные субстанции отвечали по структуре дигалловой кислоте. В 1894 году Г. Проктером была осуществлена первая попытка классифицировать дубильные вещества. В виду многообразности химического строения данной группы веществ он предложил группировку по продуктам гидролиза, окрашивающие раствор хлорида окисного железа (FeCl3) в темно – синий (пирогаллоловая группа) или в темно – зеленый (пирокатехиновая группа) цвета. Позже, Андреащ провел аналогичные исследования, но со спиртовыми извлечениями [3, 12, 14]. Теоретическое обоснование и подтверждение полученных лабораторных данных было сделано в 1912 году: Эмиль Фишер и Карл Фрейденберг показали, что структура танина соответствует ангидриду галловой кислоты (рис.2) [3]. Впоследствии, Деккер, в 1913 году, объединил имеющиеся знания в данной области в одноименную монографию. 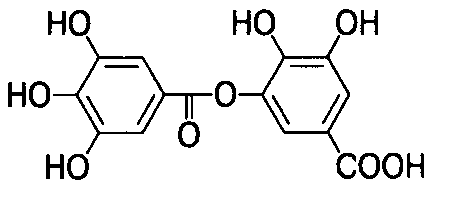 Рисунок 2. Структурная формула ангидрида галловой кислоты Гораздо позже, уже в 1933 году, на основе прошлых исследований, Карл Фрейденберг усовершенствовал предыдущую классификацию, взяв за основной критерий продукты распада танинов в результате кислотного гидролиза. На основании этого появилась более современная классификация, согласно которой различают гидролизуемые танины и конденсированные [3, 12, 14]. Детальная расшифровка строения танина была дана в 1961-1963 гг. В. Хэуорсом [15]. Поиском, выделением и установлением структуры, а также биосинтезом и систематизацией дубильных веществ занимались отечественные ученые Л.Ф. Ильин, A.Л. Курсанов, М.Н. Запрометов, Ф.М. Флавицкий, Г. Поварнин (участвовал в разработке классификации дубильных веществ), А.И. Опарин. Лишь в 2013 году группе французских учёных удалось впервые обнаружить растительную органеллу, получившую название танносома, в которой происходит синтез танинов – дубильных веществ. Она образуется в хлоропластах и после полимеризации танинов изолируется в мембранной оболочке. В таком виде происходит перемещение танносомы в вакуоль, где затем и остаются танины [13, 28]. 1.2. Особенности строения, биосинтеза и физико – химических свойств объекта исследования Так как дубильные вещества представляют собой смеси различных полифенолов с разнообразным химическим составом, классификация их затруднена. В связи с этим выделяют 2 основных классификации – по Проктеру и Фрейденбергу [3, 15, 18]. Классификация по Проктеру была предложена в 1894 году и основана на зависимости от природы продуктов их разложения при температуре 180-2000С (без доступа воздуха) подразделил на две основные группы: Пирогалловые (дают при разложении пирогаллол); Пирокатехиновые (образуется пирокатехин): Таблица 1. Классификационные признаки разделения дубильных веществ на подгруппы
В результате дальнейшего исследования химизма танидов Поварнин в 1911 году и Фрейденберг в 1933 году уточнил классификацию Проктера и рекомендовал обозначить первую группу (пирогалловые дубильные вещества) как гидролизуемые дубильные вещества, а вторую (пирокатехиновые дубильные вещества) – конденсированные [3, 15, 18]. Гидролизуемые дубильные вещества (пирогалловые) — это смеси сложных эфиров фенолкарбоновых кислот с сахарами и несахаридами. В водных растворах под действием кислот, щелочей и ферментов они способны гидролизоваться на составные части фенольной и нефенольной природы. Гидролизуемые дубильные вещества можно разделить на три группы – галлотаннины (депсиды и танниды), эллаготанниды (производные эллаговой кислоты или производные дифенилметилолида) и несахаридные эфиры фенолкарбоновых кислот [3, 18]. Галлотаннины – сложные эфиры кислоты галловой, дигалловой и других ее полимеров с циклическими формами cахаров (обычно D-глюкозой) (рис.3). Являются чаще всего гликозидными структурами. 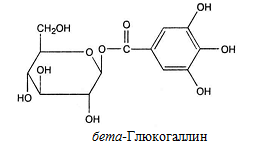 Рисунок 3. Структурная формула β - глюкогаллина Промышленными источниками галлотаннинов, применяемых в медицине (медицинского таннина), являются галлы турецкие – патологические наросты, образующиеся на дубе красильном (Quercus infectoria Oliv.), галлы китайские, образующиеся на сумахе китайском (Rhus chinensis Mill.), листья сумаха дубильного (Rhus coriaria L.) и листья скумпии кожевенной (Cotinus coggygria Scop.). Таннин представляет собой гетерогенную смесь веществ различного строения [15, 18]. Встречаются моно-, ди-, три-, тетра-, пента- и полигаллоильные эфиры, что представлено на рисунках (рис. 4, рис.5) 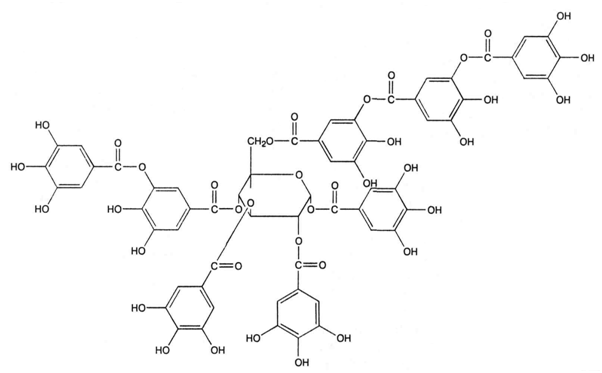 Рисунок 4. Структура китайского танина 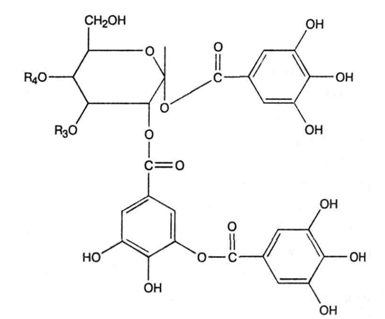 Рисунок 5. Структура турецкого танина (R3 = кислота галловая; R4 = кислота m-дигалловая) Дубильные вещества этой группы содержатся и преобладают в корневищах и корнях кровохлебки, корневищах змеевика, корневищах бадана, соплодиях ольхи, коре дуба. Гидролизуемые танниды подвергаются гидролизу ферментами (таназой) или кислотами с выделением фенольных соединений. Имеют гликозидный характер. Содержат эфиры ароматических оксикарбоновых кислот (галловой, эллаговой и др.) и сахарный компонент. С солями окисного железа образуют черно-синие осадки. Примером гидролизуемых дубильных веществ является танин [12, 18]. Эллаготаннины — эфиры кислоты эллаговой и других кислот (хебуловой, гидроксидифеновой), имеющих с ней биогенетическое родство, с циклическими формами cахаров (D-глюкозой) (рис.6, рис.7, рис.8). Эллаготаннины сложны по структуре и содержатся главным образом в тропических и субтропических растениях. Найдены в околоплоднике плодов гранатника, коре эвкалипта, околоплоднике грецкого ореха, коре дуба, соплодиях ольхи, листьях и соцветиях кипрея узколистного (иван-чая) [15, 18]. 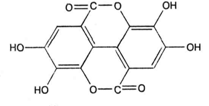 Рисунок 6. Структурная формула эллаговой кислоты 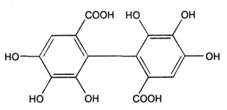 Рисунок 7. Структурная формула гидроксидифеновой кислоты 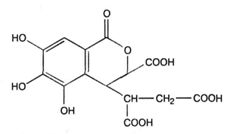 Рисунок 8. Структурная формула хебуловой кислоты Галлотаннины и эллаготаннины в растениях могут встречаться одновременно. Несахаридные эфиры фенолкарбоновых кислот представляют собой эфиры кислоты галловой с кислотами хинной, гидроксикоричными (хлорогеновой, кофейной, гидроксикоричной), а также с флаванами (катехингаллат). Эта группа широко распространена в растениях. Эфиры кислоты галловой и катехинов находятся в листьях чая китайского – Camellia sinensis (L.) Kuntze. Из зеленого чая выделен теогаллин, представляющий собой эфир кислот хинной и галловой (кислота 3-О-галлоилхинная) (рис.9) [12, 15, 18]. 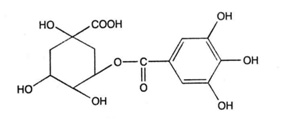 Рисунок 9. Структурная формула теогаллина Конденсированные дубильные вещества не обладающие химическими свойствами эфиров, полимерная цепь этих соединений образована посредством углерод-углеродных связей (-С-С-), что обусловливает их инертность и устойчивость к воздействию кислот, щелочей и ферментных агентов [15, 27]. Конденсированные дубильные вещества (пирокатехиновые производные, катехины) — это продукты конденсации катехинов (флаван-3-олов), лейкоантоцианидинов (флаван-3,4-диолов), реже гидроксистильбенов (фенилэтиленов) [3, 18]. Образование конденсированных дубильных веществ может идти двумя путями, изображенным на рисунках 10 и 11 [18]: По К. Фрейденбергу, оно сопровождается разрывом пиранового кольца катехинов, и С2-атом одной молекулы соединяется углерод-углеродной связью с С6— или С8-атомом другой молекулы. 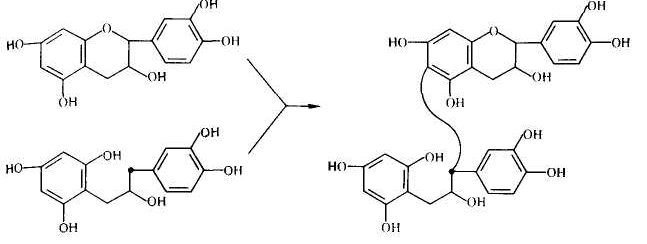 Рисунок 10. Образование конденсированных дубильных веществ по К. Фрейденбергу По Д. Е. Хатуэю, конденсированные дубильные вещества образуются в результате ферментативной окислительной конденсации молекул катехинов и лейкоантоцианидинов по типу «голова к хвосту» (кольцо А к кольцу В) или «хвост к хвосту» (кольцо В к кольцу В) по положениям 5’→8; 5’→2» и др. (рис. 11). 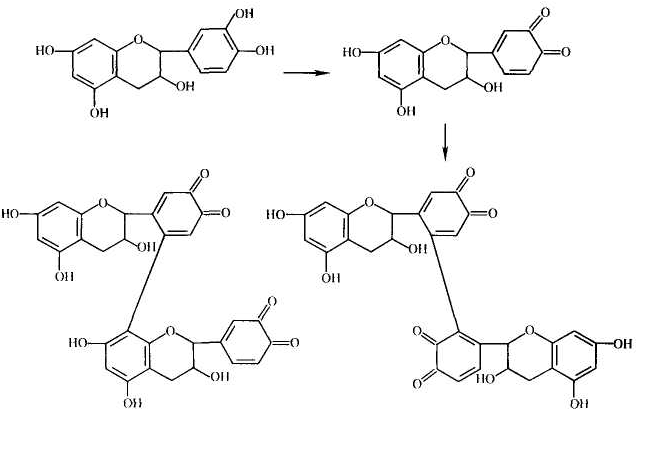 Рисунок 11. Образование конденсированных дубильных веществ по Хатуэю Конденсированные дубильные вещества содержатся и преобладают в коре калины, корневищах лапчатки, плодах черники, плодах черемухи, траве зверобоя, листьях чая [12, 15, 18]. В состав смесей дубильных веществ входят также простые фенолы (резорцин, пирокатехин, пирогаллол, флороглюцин и др.) и свободные фенолкарбоновые кислоты (галловая, эллаговая, протокатеховая и др.). Бензольные ядра соединены друг с другом посредством углеродных связей С-С; они являются производными главным образом катехинов и лейкоантоцианидов, с солями железа дают черно-зеленое окрашивание [18]. Чаще всего в растениях встречается смесь гидролизуемых и конденсированных таннидов с преобладанием той или иной группы, поэтому классифицировать лекарственное растительное сырье по типу дубильных веществ достаточно сложно. В некоторых видах сырья отмечено почти одинаковое содержание обеих групп дубильных веществ (например, корневища змеевика – Rhizomata Bistortae) [15, 18]. Физико – химические свойства: Дубильные вещества выделяются из растительного сырья в виде смеси полимеров и представляют собой аморфные вещества желтого или желто-бурого цвета, без запаха, вяжущего вкуса, очень гигроскопичные. Хорошо растворяются в воде (особенно в горячей) с образованием коллоидных растворов, растворимы также в спиртах этиловом и метиловом, ацетоне, этилацетате, бутаноле, пиридине. Нерастворимы в хлороформе, бензоле, диэтиловом эфире и других неполярных растворителях, оптически активны. Способны к микросублимации (возгонке) [12]. Легко окисляются на воздухе. Способны образовывать прочные межмолекулярные связи с белками и другими полимерами (пектиновые вещества, целлюлоза и др.). Под действием ферментов и кислот гидролизуемые дубильные вещества распадаются на составные части, конденсированные дубильные вещества — полимеризуются [15, 18]. Из водных растворов осаждаются желатином, алкалоидами (хинина хлоридом) – азотсодержащие компомненты, свинца основного ацетатом, калия бихроматом, кардиотоническими гликозидами [10, 15, 18]. Как вещества фенольной природы, дубильные вещества легко окисляются калия перманганатом в кислой среде и другими окислителями (концентрироанными растворами кислот, хлоратом калия), образуют окрашенные комплексы с солями тяжелых металлов, трехвалентного железа (железоаммонийными квасцами), бромной водой. Способны легко адсорбироваться на кожном порошке, целлюлозе, вате, в виду наличия полярных фенольных радикалов [10, 15, 18]. Локализация и наколение таннидов: Дубильные вещества находятся в растворенном состоянии в вакуолях растительных клеток, при старении клеток адсорбируются на клеточных стенках. Локализуются в клетках эпидермиса, обкладочных клетках, окружающих проводящие пучки (жилки листьев), в паренхимных клетках сердцевинных лучей, коры, древесины и флоэмы. Существуют специальные органоиды – танносомы, которые участвуют в транспорте дубильных веществ из хлоропластов в вакуоли. образуются из тилакоидных мембран, которые распадаются на множество пузырьков, заполненных танинами. Постепенно, эти пузырьки отпочковываются от мембраны тилакоида в виде крошечных везикул диаметром около 30 нм, в которых осуществляется транспорт танинов в большую вакуоль. При прохождении через мембрану хлоропласта группа танносом покрывается общей мембраной, образованной из внешней и внутренней мембраны хлоропласта. Такая группа попадает внутрь вакуоли в результате впячивания тонопласта. В результате группа танносом оказывается внутри вакуоли, окружённая двумя мембранами — внутренней, образованной из мембран хлоропласта, и наружной, образованной из мембраны вакуоли. Такие танины могут длительное время храниться внутри вакуоли в виде так называемых таниновых наслоений [13, 28]. Внутри танносом происходит полимеризация танинов и образование полифенолов. Запасание танинов помогает растению защитится от поедания травоядными животными, растительных патогенов и обеспечивает защиту от ультрафиолетовых лучей [13, 28] Дубильные вещества в больших количествах накапливаются, главным образом, в подземных органах многолетних травянистых растений (корневища бадана, змеевика, лапчатки, корневища и корни кровохлебки), в коре и древесине деревьев и кустарников (кора дуба, калины), в плодах (плоды черемухи, черники, соплодия ольхи), реже в листьях (листья скумпии, сумаха, чая). Накопление таннидов зависит от генетических факторов, климатических и экологических условий. У травянистых растений, как правило, минимальное количество дубильных веществ отмечается весной в период отрастания побегов, затем их содержание увеличивается и достигает максимума в период бутонизации и цветения (например, корневища лапчатки). К концу вегетации количество дубильных веществ постепенно снижается. У кровохлебки максимум дубильных веществ накапливается в фазу развития розеточных листьев, в фазу цветения их содержание снижается, а осенью вновь увеличивается. Фаза вегетации влияет не только на количество, но и на качественный состав дубильных веществ. Весной, в период сокодвижения в коре деревьев и кустарников и в фазу отрастания побегов у травянистых растений преимущественно накапливаются гидролизуемые танниды, а осенью в фазу отмирания растений — конденсированные танниды и продукты их полимеризации с оксистильбенами — флобафены (красени) [15, 18]. Наиболее благоприятными для накопления таннидов являются условия умеренного климата (лесная зона и высокогорный альпийский пояс). Наибольшее содержание дубильных веществ отмечено у растений, произрастающих на плотных известковых почвах, на рыхлых черноземных и песчаных почвах их содержание меньше. Способствуют накоплению дубильных веществ почвы, богатые фосфором, богатые азотом почвы снижают содержание таннидов [15, 18]. 1.3. Растительные источники дубильных веществ Дубильные вещества широко распространены в живой природе. Встречаются преимущественно в растениях, обнаружены также в водорослях, грибах и лишайниках. Наиболее распространены дубильные вещества среди представителей двудольных, в которых они накапливаются в максимальных количествах. Однодольные обычно не содержат дубильных веществ, в папоротниках дубильные вещества встречаются, а у хвощей, мхов, плаунов их практически нет, или они находятся в минимальных количествах [15, 18]. Разрешены к медицинскому применению 15 видов ЛРС, содержащего дубильные вещества, источником которых являются 17 производящих растений [9, 15, 18]: 1) Соплодия ольхи (Fructus Alni) – Alnus incana (Ольха серая), Alnus glutinosa (Ольха клейкая) – Betulaceae (Берёзовые); 2) Корневища лапчатки (Rhizomata Tormetillae) – Potentilla erecta (Лапчатка прямостоячая), Potentilla alba (Лапчатка белая) – Rosaceae (Розоцветные); 3) Корневища бадана (Rhizomata Bergeniae) – Bergenia grassifolia (Бадан толстолистный) – Saxifragaceae (Камнеломковые); 4) Листья бадана (Folia Bergeniae) – Bergenia grassifolia (Бадан толстолистный) – Saxifragaceae (Камнеломковые); 5) Листья скумпии (Folia Cotini) – Cotinus coggygria (Скумпия кожевенная) – Anacardiaceae (Сумаховые); 6) Листья гамамелиса (Folia Hamamelidis) – Hamamelis virginiana (Гамамелис вирджинский) – Hamamelidaceae (Гамамелисовые); 7) Кора гамамелиса (Cortex Hamamelidis) – Hamamelis virginiana (Гамамелис вирджинский) – Hamamelidaceae (Гамамелисовые); 8) Плоды черемухи (Fructus Padi) – Черемуха обыкновенная (Padus racemosa) – Rosaceae (Розоцветные); 9) Корневища змеевика (Rhizomata Bistortae) – Polygonum bistorta (Горец змеиный), Polygonum carneum (Змеевик мясо - красный) – Polygonaceae (Гречишные); 10) Кора дуба (Cortex Quercus) – Quercus robur (Дуб обыкновенный), Quercus petraea (Дуб скальный) – Fagaceae (Буковые); 11) Листья сумаха (Folia Rhois coriariae) – Rhus coriaria (Сумах дубильный) – Anacardiaceae (Сумаховые); 12) Корневища и корни кровохлебки (Rhizomata et radices Sanguisorbae) – Sanguisorba officinalis (Кровохлебка лекарственная) – Rosaceae (Розоцветные); 13) Плоды черники (Fructus Myrtilli) – Vaccinium myrtillus (Черника обыкновенная) – Ericaceae (Вересковые); 14) Кора гранатника (Cortex Punicae) – Punica granatum (Гранат обыкновенный) - Lythraceae (Дербенниковые); 15) Листья гранатника (Folia Punicae) – Punica granatum (Гранат обыкновенный) - Lythraceae (Дербенниковые); Наиболее высоким содержанием дубильных веществ отличаются семейства: Сумаховые — Anacardiaceae (сумах дубильный (Rhus coriaria), скумпия кожевенная (Cotinus coggygria (до 33% дубильных веществ в пересчете на сухое вещество) – являются официнальными источниками промышленного получения медицинского танина); Розоцветные — Rosaceae (кровохлебка лекарственная (Sanguisorba officinalis), черемуха обыкновенная (Padus racemosa), представители рода Potentilla: Лапчатка белая (Potentilla alba L.), Лапчатка прямая или лапчатка закаспийская (Potentilla recta L.), Лапчатка прямостоячая (Potentilla erecta L.), Potentilla rupestris (Лапчатка скальная) [23] 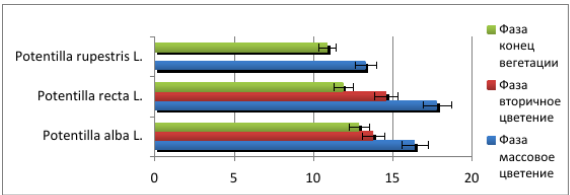 Рисунок 12 Содержание дубильных веществ в органах растений рода Potentilla в процентах (%) в абсолютно сухом сырье (в пересчете на танин) У представителей данного семейства обнаруживается до 23% дубильных веществ в пересчете на сухое вещество – корневища и корни кровохлебки. Буковые — Fagaceae (Дуб обыкновенный (Дуб черешчатый) – Quercus robur и Дуб скальный – Quercus petraea) до 12% [5]; Гречишные — Polygonaceae (змеевик большой и змеевик мясо-красный) до 36% дубильных веществ; Вересковые — Еricасеае (Arctostaphylos uva-ursi (Толокнянка обыкновенная, Vaccinium vitis – idaea (Брусника обыкновенная), Vaccinium myrtillus (Черника обыкновенная) до 41% дубильных веществ; Берёзовые — Betulaceae (ольха серая (Alnus incana) и ольха клейкая (Alnus glutinosa) до 30% дубильных веществ; Камнеломковые – Saxifragaceae (Bergenia grassifolia – Бадан толстолистный) – не менее 20% дубильных веществ [25]; Hypericaceae – растения рода Hypericum (зверобой продырявленный – Hypericum perforatum) – до 13% дубильных веществ; Hamamelidacece – Гамамелис вирджинский (Hamamelis virgiana) – до 10% дубильных веществ. Содержание таннидов в растениях доходит до 20-30 %, наивысшее содержание дубильных веществ найдено в патологических образованиях — галлах (до 50-70 %) [15]. Согласно информации, полученной из литературных источников, перспективные направления поиска сырьевой базы дубильных веществ осуществляются среди семейств: Lamiaceae – Дубровник белый (Teucrium polium) [1, 22]; Salicaceae – Salix gracilistyla (Ива тонкостолбиковая), Salix phylicifolia (Ива филиколистная), Salix pentandra (Ива пятитычинковая), Salix pyrolifolia (Ива грушанколистная), Salix rorida (Ива росистая) и Salix schwerinii (Ива Шверина) и т.д. (таблица 13) [17]; Hypericaceae – Hypericum perforatum (сорт «Золотодолинский») - первый в России сорт зверобоя продырявленного, выведенный Центральным сибирским ботаническим садом СО РАН [6, 16]; Punicacece – Punica granatum (Гранатовое дерево) [26]; Таблица 13. Содержание дубильных веществ и флавоноидов (%) в листьях некоторых видов растений рода Salix 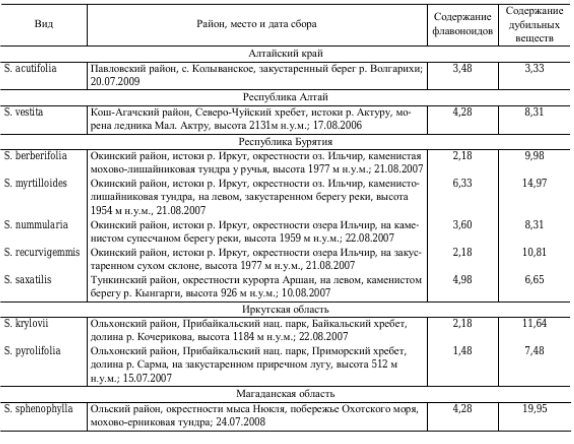 Hydrocharitaceae - Нуdrocharis morsusranae, Hydrilla verticillata, Stratiotes aloides, Egeria densa, Elodea Canadensis (таблица 14) [19]. Таблица 14. Содержание дубильных веществ в процентах (%) у некоторых представителей семейства Hydrocharitaceae.  Rosaceae – Шиповник собачий, растения рода Spiraea – Spiraea salicifolia (Спирея иволистная), Spiraea media var. media (Спирея средняя), Spiraea ussuriensis subsp. Ussuriensis (Спирея уссурийская), Spiraea betulifolia (Спирея березолистная), Spiraea beauverdiana (Спирея Бовера), Spiraea humilis (Спирея низкая) (таблица 15) [2, 24]. Таблица 15. Содержание биологически активных веществ (%) в растениях рода Spiraea 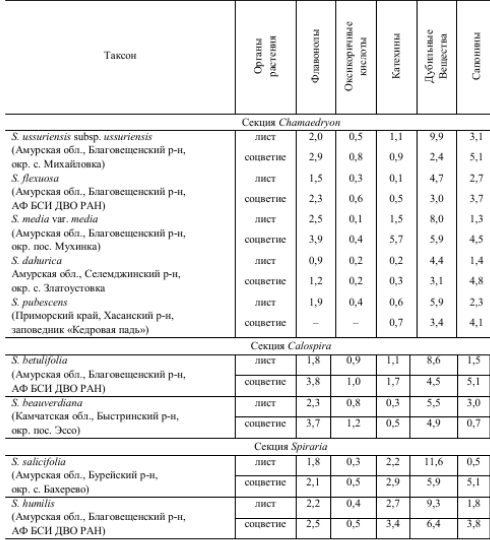 1.4. Применение дубильных веществ Лекарственное сырьё, содержащее дубильные вещества, применяют для получения препаратов, используемых как вяжущие, кровоостанавливающие, противовоспалительные, антимикробные средства. В свою очередь, разные классы дубильных веществ имеют разнообразную фармакологическую активность [2, 6, 12, 15]. Сырьё, содержащее конденсированные дубильные вещества, может применяться как антиоксидантное. Кроме того, установлено, что гидролизуемые и конденсированные дубильные вещества проявляют высокую Р-витаминную активность, антигипоксическое и антисклеротическое действие. Конденсированные дубильные вещества проявляют противоопухолевый эффект, они способны гасить цепные свободнорадикальные реакции, что объясняет их определённую эффективность в химиотерапии рака. Причём в больших дозах танниды проявляют противоопухолевое действие, в средних дозах -радиосенсибилизирующее, а в малых — противолучевое [15, 18, 21, 22]. Действие лекарственного растительного сырья и препаратов основано на способности дубильных веществ связываться с белками с образованием плотных альбуминатов, что способствует остановке кровотечений, снятию отеков и ускорению заживления поврежденных тканей [15, 18]. При соприкосновении с воспаленной слизистой оболочкой или раневой поверхностью образуются тонкая поверхностная пленка, защищающая от раздражения чувствительные нервные окончания. Происходит уплотнение клеточных мембран, сужение кровеносных сосудов, уменьшается выделение экссудатов, что приводит к уменьшению воспалительного процесса [15, 18]. Благодаря способности дубильных веществ образовывать осадки с алкалоидами, сердечными гликозидами, солями тяжелых металлов их используют как антидоты при отравлении этими веществами (детоксикационная терапия) [10, 15]. Наружно при заболеваниях полости рта, зева, гортани (стоматиты, гингивиты, фарингиты, ангины), а также при ожогах применяют отвары коры дуба, корневищ бадана, змеевика, лапчатки, корневищ и корней кровохлебки, и препарат «Альтан» [15, 18]. Внутрь при желудочно-кишечных заболеваниях (колитах, энтероколитах, поносах, дизентерии) применяют препараты танина («Танальбин», «Тансал», «Альтан», отвары плодов черники, черемухи (особенно в детской практике»), соплодий ольхи, корневищ бадана, змеевика, лапчатки, корневищ и корней кровохлебки [15, 18]. Как кровоостанавливающие средства при маточных, желудочных и геморроидальных кровотечениях применяют отвары коры калины, корневищ бадана, корневищ и корней кровохлебки, корневищ лапчатки, соплодий ольхи. Отвары готовят в соотношении 1: 5 или 1: 10. Нельзя применять сильно концентрированные отвары, так как при этом, пленка альбуминатов высыхает, появляются трещины и возникает вторичный воспалительный процесс [15, 18]. Экспериментально установлено противоопухолевое действие дубильных веществ водного экстракта экзокарпия плодов, а также сока гранатника (при лимфосаркоме, саркоме и других заболеваниях) и препарата «Ханерол», полученного основе соцветий кипрея обыкновенного (Иван-чай) при раке желудка и легких [15, 18, 26]. |
