Каталитическая очистка выхлопных газов. Клокова курсовая (1). Курсоваяработ а по физической химии химической кинетике каталитическая очистка выхлопных газов. Студент клокова алёна олеговна
 Скачать 0.96 Mb. Скачать 0.96 Mb.
|
|
ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ОБРАЗОВАНИЯ «БУРЯТСКИЙ ГОСУДАРСТВЕННЫЙ УНИВЕРСИТЕТ им. Доржи Банзарова» ХИМИЧЕСКИЙ ФАКУЛЬТЕТ К У Р С О В А Я Р А Б О Т А по физической химии: химической кинетике КАТАЛИТИЧЕСКАЯ ОЧИСТКА ВЫХЛОПНЫХ ГАЗОВ. СТУДЕНТ: КЛОКОВА АЛЁНА ОЛЕГОВНА КУРС: __ III__ ГРУППА 13190 РУКОВОДИТЕЛЬ: д. х. н., профессор ХАНХАСАЕВА СЭСЭГМА ЦЫРЕТОРОВНА Улан-Удэ 2022 Оглавлени Введение 4 Глава 1. Теоретическая часть. 5 1.1.Исторические аспекты. 5 1.2.Классификация выхлопных газов. 5 1.3.Методы очистки выхлопных газов. 8 1.4.Каталитический метод очистки. 9 1.4.1.Решения для транспортных средств. 10 1.4.2.Решения для промышленности. 11 1.4.3.Реверсивный метод каталитической очистки газа. 14 1.4.4.Особенности эксплуатации каталитических нейтрализаторов. 15 Глава 2. Практическая часть. 16 2.1. Гетерогенный катализ: разложение пероксида водорода на диоксиде марганца. 16 2.1.2. Теоретическая часть. 16 2.1.2. Методика выполнения эксперимента. 17 2.1.3. Обработка полученных данных. 18 Заключение. 24 Список литературы 25 Введение 3 Глава 1. Теоретическая часть. 5 1.1. Исторические аспекты. 5 1.2. Классификация выхлопных газов. 5 1.3. Методы очистки выхлопных газов. 8 1.4. Каталитический метод очистки. 9 1.4.1. Решения для транспортных средств. 10 1.4.2. Решения для промышленности. 11 1.4.3. Реверсивный метод каталитической очистки газа. 15 1.4.4. Особенности эксплуатации каталитических нейтрализаторов. 15 Глава 2. Практическая часть. 17 2.1. Гетерогенный катализ: разложение пероксида водорода на диоксиде марганца. 17 2.1.2. Теоретическая часть. 17 2.1.2. Методика выполнения эксперимента. 18 2.1.3. Обработка полученных данных. 19 Заключение. 25 Список литературы 26 ВведениеКаталитическая очистка газовых выбросов, неизбежно сопровождающих многие производственные процессы, является одним из наиболее эффективных методов химического обезвреживания содержащихся в них вредных веществ. Суть каталитических методов очистки газовых выбросов заключается в реализации химических взаимодействий, приводящих к конверсии подлежащих обезвреживанию вредных веществ в без- или маловредные вещества, в присутствии специальных катализаторов [5]. В составе выхлопных газов содержится много токсичных веществ. Для того чтобы, избежать попадание этих веществ в атмосферу используется специальное устройство, которое получило название «каталитический нейтрализатор» [9]. Каталитический нейтрализатор – элемент выхлопной системы мотора, предназначенный для очистки отработанных газов перед их выбросом в атмосферу. Актуальность: в настоящее время во многих странах идёт заметное ухудшение состояния атмосферы. Чтобы это предотвратить, нужна очистка газового потока, другими словами перевод в безвредную форму или отделение от него загрязняющих веществ, выбрасываемых в атмосферу. Каталитическая очистка выхлопных газов как раз и является одним из способов предотвращения загрязнения атмосферы. Цель работы: изучить каталитические реакции, применяемые в процессе очистке выхлопных газов. Задачи: 1. Изучить литературу по теме «Каталитическая очистка выхлопных газов». 2. Рассмотреть реакции методы очистки разных газов. 3. Изучить особенности протекания каталитических реакций при очистке выхлопных газов. 4. Провести кинетический эксперимент по гетерогенному катализу. 5. Подвести итоги по проделанной курсовой работе. Глава 1. Теоретическая часть.Исторические аспекты. До начала ХХ века в природе существовало экологическое равновесие, деятельность человека не нарушала природных процессов. В ХХ веке совместно с быстрым ростом технического прогресса, науки и промышленности росло и продолжает расти вредное воздействие выбросов в атмосферу. В результате происходит непредвиденное изменение экологических систем, разрушается экологическое равновесие [8]. История каталитической очистки химических соединений в отходящих газах началась примерно 40 лет назад и за последнее десятилетие получила развитие по всему миру. Существует несколько причин скачка в развитии такой очистки. Во – первых, предприятия стремятся к сокращению издержек на электроэнергию, энергоносители и капитальные расходы. Во – вторых, в Европе технология каталитического окисления отходящих газов была внесена в список наилучших доступных технологий в 1996 году. Это и дало стимул активному развитию и применению катализаторов для очистки выбросов [9]. Классификация выхлопных газов. Выхлопные газы (отходящие газы) – это отработавшее в двигателе рабочее тело или по-другому говоря – это продукт работы двигателей внутреннего сгорания. Выхлопные газы являются продуктами окисления и неполного сгорания углеводородного топлива. Зачастую выхлопными газами называют все выбросы в атмосферу, в их число входят, автомобили, самолеты, котельные, заводы и другие промышленные предприятия. На самом деле, правильней было бы называть выхлопными газами выбросы только транспортных средств [1]. В состав выхлопных газов разного топлива могут входить такое вещества, как: оксиды азота и углерода; диоксиды азота и серы; сернистый ангидрид; бензопирен; альдегиды; ароматические углеводороды; некоторое количество сажи; разные соединения свинца; взвешенные частицы. Таблица 1. Химический состав выхлопных газов автомобиля.
В данной таблице наблюдаем, что состав выхлопных газов очень разнообразный и большая часть этих компонентов токсична. По свойствам и химическому составу, а также по характеру влияния на организм человека все эти компоненты можно разделить на несколько групп. 1 группа. Это нетоксичные вещества, такие как азот, кислород, водород, водяной пар и другие компоненты, составляющие атмосферу воздуха. 2 группа. Это оксид углерода (угарный газ) – продукт неполного сгорания топлива. Угарный газ обладает наркотическим действием, раздражает кожу и слизистые оболочки. При вдыхании оксид углерода контактирует с гемоглобином в крови, вытесняя кислород, в результате этого у человека наступает кислородное голодание, которое, прежде всего, влияет на центральную нервную систему. Высокая концентрация угарного газа может привести к летальному исходу; небольшие дозы вызывают головокружение, головную боль, чувство усталости и замедленную реакцию. 3 группа. В её составе оксиды азота NO и NO2. Они вызывают сильное раздражение слизистых оболочек глаз, а высокие концентрации этих оксидов приводят к астматическим проявлениям и отёку лёгки. 4 группа. В эту группу входят различные углеводороды. Они обладают канцерогенными свойствами, то есть может способствовать появлению злокачественных опухолей. В особой категории находится бензапирен (C29H12), так как обладает высокой активностью канцерогенного действия. 5 группа. Эту группу составляют альдегиды. В выхлопных газах в основном содержатся такие альдегиды, как формальдегид, уксусный альдегид и акролеин. Эти соединения оказывают раздражающее действие органов зрения, дыхательных путей, а также поражают ЦНС, почки и печень. 6 группа. В состав этой группы входит сажа и другие дисперсные частицы. Сажа, как и любая мелкая пыль, действует на органы дыхания. Но самая главная опасность сажи в том, что на ней адсорбируются канцерогенные вещества, вследствие чего возрастает риск заболевания онкологическими заболеваниями. 7 группа. К этой группе относятся сернистые соединения – серный ангидрид, сероводород, которые имеют место в выхлопных газах, когда используется топливо с повышенным содержанием серы. Эти соединения оказывают раздражающее действие на слизистые оболочки горла, носа и глаз. Сернистый газ вызывает онкологические заболевания. А также при вдыхании сернистого газа и оксида серы нарушается деятельность нервной системы и опасно для людей, страдающих сердечнососудистыми заболеваниями. 8 группа. В эту группу входят свинец и его соединения. Эти компоненты появляются в выхлопных газах при использовании этилового бензина. Соединения свинца разрушают органы и ткани организма, нервную систему, желудочно-кишечный тракт, приводят к появлению онкологических заболеваний и нарушаются обменные процессы. Соединения свинца, как и канцерогены, не выводятся из организма, а накапливаются, как в почве и растениях. В организме человека свинец удерживается в белках эритроцитов, в дальнейшем попадает в плазму крови, затем достигает почки, печень и другие органы. В костях у человека свинец накапливается и надолго остается [2]. Методы очистки выхлопных газов. Технические мероприятия, направленные на снижение выбросов автотранспорта, являются самыми главными в работе природоохраны. Такие мероприятия можно разделить на три группы: Градостроительные мероприятия: а) строительство автомагистралей в обход городов и населенных пунктов; б) изоляция зданий от дорог, тротуаров при помощи посадки разных кустов и деревьев; в) размещение жилых особенно детских учреждений подальше от дорог. Организация движения городского транспорта: а) ограничение поездок грузовых машин по городу; б) организация оптимальной работы светофоров и транспортных развязок; в) оптимизация скорости движения машин (при 60 км/ч – наименьшие загрязнения); г) расширение перевозок пассажиров на электротранспорте. Технические мероприятия: а) регулировка двигателей внутреннего сгорания; б) снижение, замена и полное исключение свинца в топливе; в) добавление в топливо присадок, снижающих содержание угарного газа, альдегидов, сажи в выхлопных газах; г) замена бензина метанолом, сжатым и сжиженным газом, а ещё лучше – водородом; д) нейтрализация (обезвреживание) выхлопных газов; е) фильтрация выхлопных газов дизелей от сажи; ж) замена обычных автомобилей электромобилями [7]. Для обезвреживания отходящих газов от газообразных и парообразных токсичных веществ, применяют методы: абсорбции (физической и хемосорбции), адсорбции, каталитические, термические, конденсации и компримирования. Каталитический метод очистки. Каталитическая очистка газов основана на гетерогенном катализе и служит для превращения примесей либо в безвредные соединения, либо в соединения, которые легко удаляются из газовой смеси. Достоинства метода: - высокая степень очистки; - компактность; - небольшая металлоёмкость; - высокая производительность; - лёгкость автоматического управления. Недостатки метода: - образование новых веществ, которые часто надо удалять из газа; - высокая стоимость катализаторов. Особенностью каталитической очистки выхлопных газов является то, что очищаются большие объёмы отходящих газов с малым содержанием примеси. Кроме того, в газах могут содержаться несколько вредных компонентов. Суть каталитических процессов газоочистки заключается в реализации химических взаимодействий, приводящих к конверсии подлежащих обезвреживанию примесей в другие продукты в присутствии специальных катализаторов. Каталитические взаимодействия в гетерогенном катализе происходят на границе раздела фаз конвертируемой газовой смеси и катализатора. Решения для транспортных средств. Выхлопной газ, состоящий из токсичных веществ, проходит через структуру нейтрализатора. Вещества – катализаторы вызывают химические реакции, преобразовав вредные вещества в безвредные вещества. В результате реакций при каталитической очистке образуются углекислый газ, азот и вода. В настоящее время пользуются тремя типами катализаторов. Первый тип – это катализатор окисления. Он уменьшает выбросы вредных загрязнений, таких как угарный газ (CO) и углеводороды (CH). Тем не менее, катализатор окисления уменьшает лишь небольшую часть загрязняющих выбросов. Второй тип – это двухступенчатый каталитический нейтрализатор, который является усовершенствованным. Работает он в два этапа. На первом этапе происходит окисление оксида углерода до диоксида углерода: 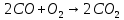 . .На втором этапе проходит окисление углеводородов (несгоревшего или частично сгоревшего топлива) до диоксида углерода и воды: 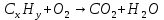 (реакция горения). (реакция горения).Данный тип автомобильных катализаторов часто используется в транспорте с дизельным двигателем для снижения выбросов углеводородов и угарного газа. Эти катализаторы так же использовались для бензинового двигателя около 40 лет назад, но из – за того, что у них не было способности контролировать оксиды азота их заменили трёхступенчатым каталитическим нейтрализатором. Итак, третий тип - это трёх ступенчатый каталитический нейтрализатор. Он преобразовывает вредные вещества, содержащиеся в выхлопных газах, в безвредные вещества. Такой катализатор преобразует опасные вещества в менее вредный углекислый газ, воду и азот. Очистка таким катализатором проходит в три этапа. Восстановление оксидов азота до азота: 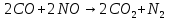 ; ;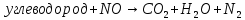 ; ;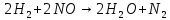 . .Окисление угарного газа до углекислого газа: 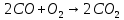 . .Окисление несгоревших углеводородов до углекислого газа и воды: 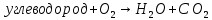 . .Трёхступенчатый катализатор является единственным устройством, которое уменьшает выбросы всех трёх загрязнителей, а также такой способ является наиболее экономичный [3]. Решения для промышленности. Известно несколько разновидностей каталитических методов очистки, отличающихся по механизму, природе используемых катализаторов и применяемых в зависимости от типа преобладающего вредного вещества в газовых выбросах производства: пиролюзитный, озонокаталитический, жидкостно-контактный и радикально-каталитический. Для снижения выбросов в атмосферу вредных веществ, содержащихся в промышленных выбросах, например, металлургических производств, а это в основном NOx, могут быть использованы как первичные, так и вторичные меры. Первичные меры направлены на предотвращение образования вредных веществ на этапе подготовки производства (использование новых современных технологий, переход на альтернативные расходные материалы и энергоносители), они достаточно эффективны, но весьма затратные. Вторичные меры включает удаление вредных веществ путем очистки газовых выбросов, образующихся на различных стадиях производства. Использование этих мер не требует каких-либо структурных изменений и не влияет на ход принятого технологического процесса производства продукции. При выборе подходящих мер, как правило обращают внимание на экологический и экономический аспект, то есть, будут ли инвестиционные затраты, связанные с сокращением выбросов вредных веществ, адекватны прибыли от производства. На рынке представлен широкий спектр оборудования, реализующего различные методы каталитической очистки газовых выбросов, которые позволяют эффективно уменьшить концентрацию выбрасываемых вредных веществ. В зависимости от объема производства и финансовых возможностей компании предприниматель должен решить, может ли он использовать вторичные меры – каталитические методы очистки газовых выбросов, или использовать первичные меры, при которых он будет использовать возобновляемые энергоресурсы и не столкнется с проблемой управления отходами. Для минимизации концентрации вредных веществ в газовых выбросах могут быть использованы различные химические реакции, такие как абсорбция и адсорбция, а также каталитическое восстановление и каталитическое окисление. Каталитический нейтрализатор, представляющий собой систему очистки отработавших газов, установленный на генераторной станции, специальной технике обеспечивает степень очистки отработавших газов: по оксиду углерода (CO) – 90-97%; по углеводородам (CH) – 85-95%; по оксидам азота (NOx) – 65-95%; по содержанию твердых частиц (саже) – 85-95%. Система очистки отработавших (выхлопных) газов может состоять из трех последовательных ступеней, в зависимости от требований производства: Сажевый фильтр. Сажа, осаждаемая на фильтре, состоит в основном из частиц углерода (C) и углеводородов. Существует два основных метода по удалению частиц: Сгорание кислородом: 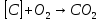 ; ;Сгорание с диоксидом азота: 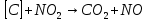 . .Таблица 2. Характеристики двух методов.
Оборудование для селективного каталитического восстановления оксидов азота (NOx). Этот процесс используется для уменьшения оксидов азота, образующихся во время процесса сгорания углеводородного топлива, сопровождающегося выделением энергии. NO (оксид азота) представляет собой бесцветный газ, который окисляется в воздухе с образованием NO2 (диоксид азота). В высоких концентратах он вызывает симптомы паралича нервной системы. NO2 - красно-коричневый газ с резким запахом. Под воздействием солнечного света и углеводородами, образует смог. Оксиды азота восстанавливаются в кислородсодержащих выхлопных газах с помощью процесса SCR (Selective Catalytic Reduction, селективное/выборочное каталитическое восстановление). Отработавший газ, обработанный дозированным реагентом мочевины, проходит через тонкостенные сотовые преобразователи, восстанавливая оксиды до воды и азота. Процесс с мочевиной – выгодная альтернатива аммиаку в качестве реагента для снижения уровня отравляющих веществ в выхлопных газах двигателя. По сравнению с аналогом реагент обладает значительными преимуществами в отношении транспортировки, хранения и обработки, при этом она значительно дешевле. Оборудование для каталитического окисления СО и несгоревших углеводородов. Этот процесс используется для снижения уровня окиси углерода и несгоревших углеводородов в выхлопных газах. Это достигается путем каталитического окисления. Такой катализатор может быть установлен после стадии SCR. Несгоревшие углеводороды могут быть обнаружены в выхлопных газах двигателей внутреннего сгорания. Реверсивный метод каталитической очистки газа. Среди каталитического дожигания можно выделить реверсивный метод каталитической очистки газа, который благодаря низкому энергопотреблению особенно подходит для очистки газов от органических загрязнителей, выбрасываемых промышленностью в атмосферу. Установки обратного типа изготавливаются в соответствии с типовой серией с диапазоном производительности от 300 до 15 000 м3/ч для концентраций органических соединений от нескольких сотен мг до нескольких грамм на м3. Эффективность очистки зависит от типа загрязнения и составляет до 98%. При концентрациях органических соединений выше 0,7 г/м3 установка работает автотермически (без затрат энергии для нагрева реактора). Побочные продукты – азот и вода нейтральны для окружающей среды. Способ более экономичен, чем термическое сгорание, так как работает при более низких температурах. Недостаток – высокие затраты на внедрения по причине стоимости каталитически активных металлов [5]. Особенности эксплуатации каталитических нейтрализаторов. Каталитический нейтрализатор использует каталитическое химическое преобразование для преобразования оксида углерода (CO) и несгоревших углеводородов (CH) в нетоксичный диоксид углерода и воду. Это преобразование осуществляется на металлической сотовой подложке, покрытой активным каталитическим материалом. Катализатор способен обеспечить степень очистки загрязняющих веществ – до 90% при оптимальной рабочей температуре от 250°C. Сфера применения. Катализатор подходит для любых дизельных двигателей, использующихся на такой технике, как генераторные агрегаты с первичной мощностью или резервные генераторы, землеройное и погрузочно-разгрузочное оборудование (спецтехника, погрузчики). В частности, катализаторные установки применяют для оснащения техники, используемой в ограниченном пространстве, таком как туннели, склады и шахты. Установка. Важно монтировать узел как можно ближе к выпускному коллектору двигателя. Для обеспечения максимальной каталитической эффективности катализатора требуется достаточно высокая температура. Срок эксплуатации. В основе работы каталитического нейтрализатора лежит осуществление каталитической реакции, следовательно, срок службы катализатора теоретически не ограничен. Узел может выйти из строя в результате ошибок при эксплуатации (повышенная вибрация двигателя, погрешности монтажа, абразивное воздействие выхлопных газов). Глава 2. Практическая часть.2.1. Гетерогенный катализ: разложение пероксида водорода на диоксиде марганца.2.1.2. Теоретическая часть.Применение пероксида водорода в химии, медицине и других областях основывается на её окислительных свойствах. Характерный для пероксида водорода окислительный распад протекает с выделением тепла: 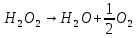 Гораздо реже (только под действием сильных окислителей) протекает восстановительный распад: 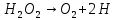 . .Окислительный распад H2O2 идёт со значительной скоростью в присутствии веществ, способных окисляться кислородом. Разложение перекиси ускоряется гетерогенными катализаторами (стекло, многие металлы, соли, окислы металлов, уголь). Механизм гетерогенного разложения пероксида водорода протекает с промежуточным образованием перекисных соединений. По Виланду реакция идёт в две стадии: 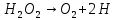 (медленно) (медленно)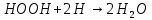 (быстро) (быстро)Суммарная скорость реакции определяется первой стадией и потому реакция идёт по первому порядку. 2.1.2. Методика выполнения эксперимента.Оборудование и реактивы: Пероксид водорода ( 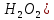 – 1,5 % 200 мл. – 1,5 % 200 мл.Диоксид марганца ( 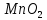 ) – по 0,015 г. ) – по 0,015 г.Волюмометрическая установка. Выполнение работы: Приготовили раствор 1,5% перекиси водорода разбавлением 30% пероксида водорода. При разложении 1 г Н2О2 выделяется около 360 см3 кислорода. Поэтому волюмометрический метод слежения за кинетикой этой реакции обладает весьма высокой чувствительностью. Перед началом опыта собранную волюмометрическую установку проверяют на герметичность. Для этого опускают уравнительную склянку ниже бюретки. Уровень воды в бюретке опустится и установится на некотором делении. Если это положение не изменится в течении 5 минут, установку можно считать герметичной. В противном случае уровень воды в бюретке будет непрерывно опускаться. Перед началом опыта в реактор наливают 20 мл рабочего раствора. Реактор помещают в термостат. Уравнивая высоты воды в бюретке и уравнительной склянке, приводят давление внутри прибора к атмосферному давлению. Спустя 20 мин, когда рабочий раствор примет температуру термостата, открывают реактор, всыпают в него примерно 0,015 г заранее взвешенного катализатора диоксида марганца и быстро закрывают пробку. В этот же момент включают секундомер и производят первый замер по газовой бюретке. По мере понижения уровня жидкости в бюретке уравнительную склянку опускают так, чтобы в моменты измерений высоты жидкостей в бюретке и уравнительной склянки были одинаковыми. Объём выделившегося кислорода – V фиксируют через каждые 2-3 минуты. Опыт можно считать законченным, когда объём выделившегося О2 составит примерно 40-45 мл [10]. 2.1.3. Обработка полученных данных.Реакция 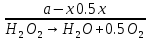 Имеет первый порядок по пероксиду водорода, получаем, что 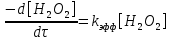 , ,где kэфф – эффективная константа скорости реакции; (a-2x) – количество молей Н2О2 в растворе в момент времени t; a – исходное количество Н2О2 в растворе, моль; x – число молей О2, образовавшегося к моменту времени t. 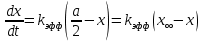 , ,где, 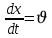 - скорость образования кислорода; - скорость образования кислорода; 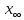 - число молей О2, которое можно получить при полном разложении - число молей О2, которое можно получить при полном разложении 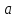 молей Н2О2. молей Н2О2.Поскольку при фиксированных температурах и давлении x пропорционально объему выделившегося кислорода V, имеем 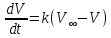 Интегрируем уравнение 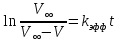 Полный объем кислорода равен 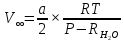 где R – 62360 мм. рт. ст.*см3/(моль*град), T – температура газовой бюретки, °К; Р – атмосферное давление по барометру, мм. рт. ст. (23,75 мм. рт. ст. при 25°С) При 25°С: 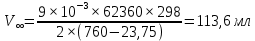 Таблица 3.
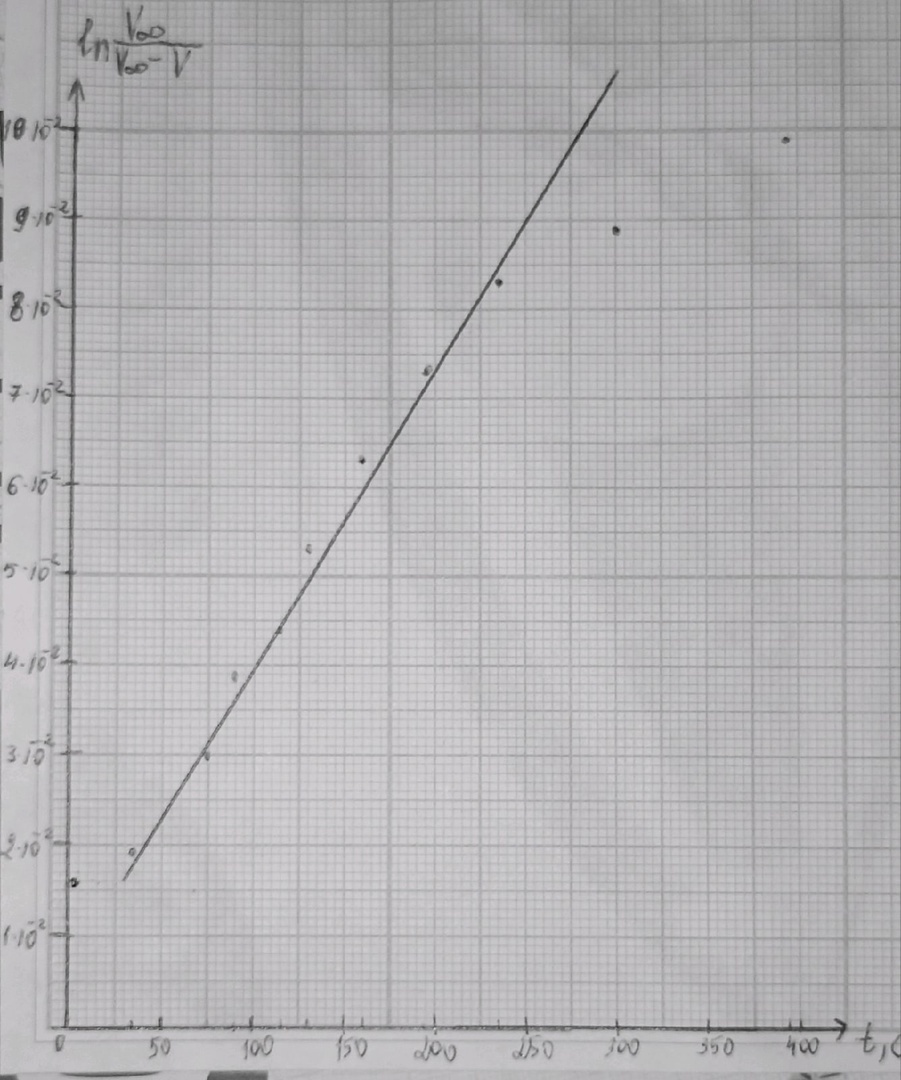 Рис 1. Зависимость 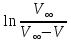 от времени. от времени.По графику найдём тангенс угла, который равен kэфф: 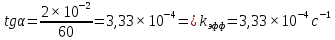 При 35°С: 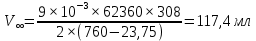 Таблица 5.
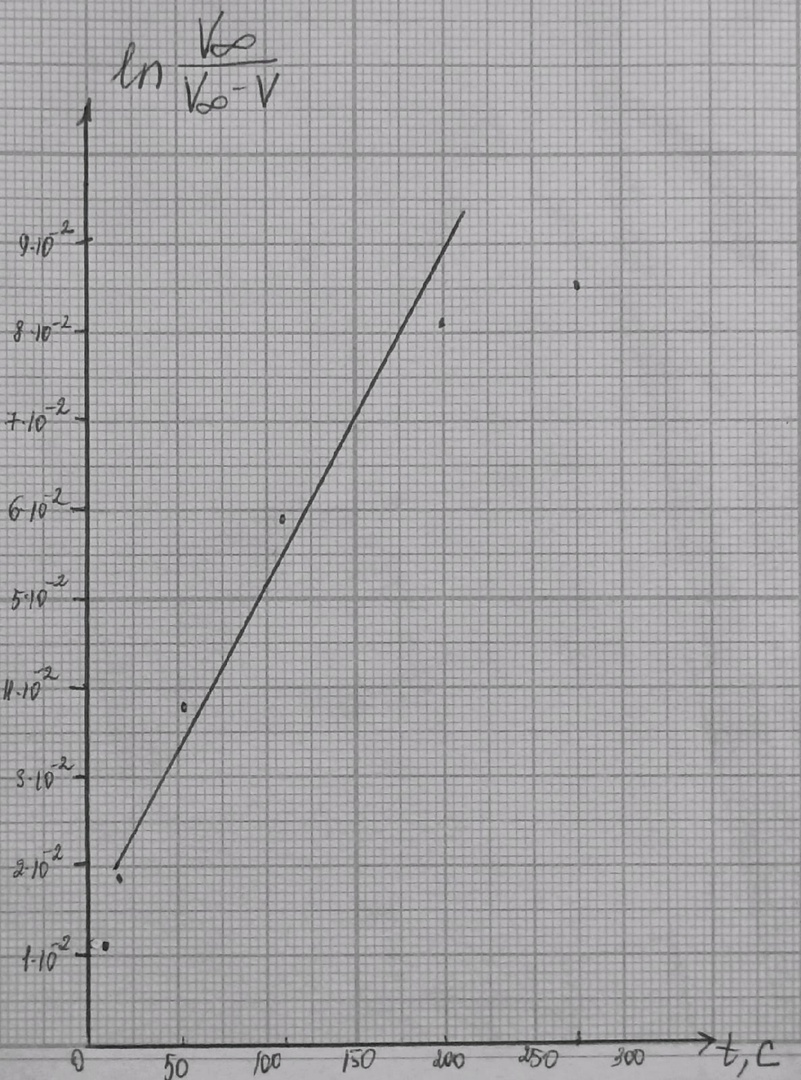 Рис 2. Зависимость 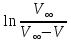 от времени при 35°С. от времени при 35°С.По графику найдём тангенс угла, который равен kэфф: 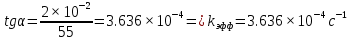 Уравнение Аррениуса показывает зависимость константы скорости реакции от температуры 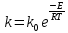 Предэкспоненциальный множитель (k0) и энергия активации (Е) – константы, не зависящие от температуры. Их можно рассчитать, если известно значение коэффициента Вант Гоффа (γ) для исследуемой реакции 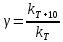 где kT+10 и kT– константы скорости реакции при температурах (Т+10) и Т соответственно. Температура должна быть выражена в градусах Кельвина. Используя значение температуры опыта (T), рассчитанную ранее величину константы скорости реакции (k) и γ, заполняют таблицу. Таблица 9.
Аналитический метод. 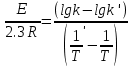 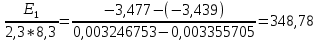 Дж/моль Дж/моль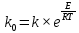 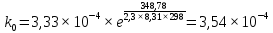 Расчет энергии активации графическим методом. 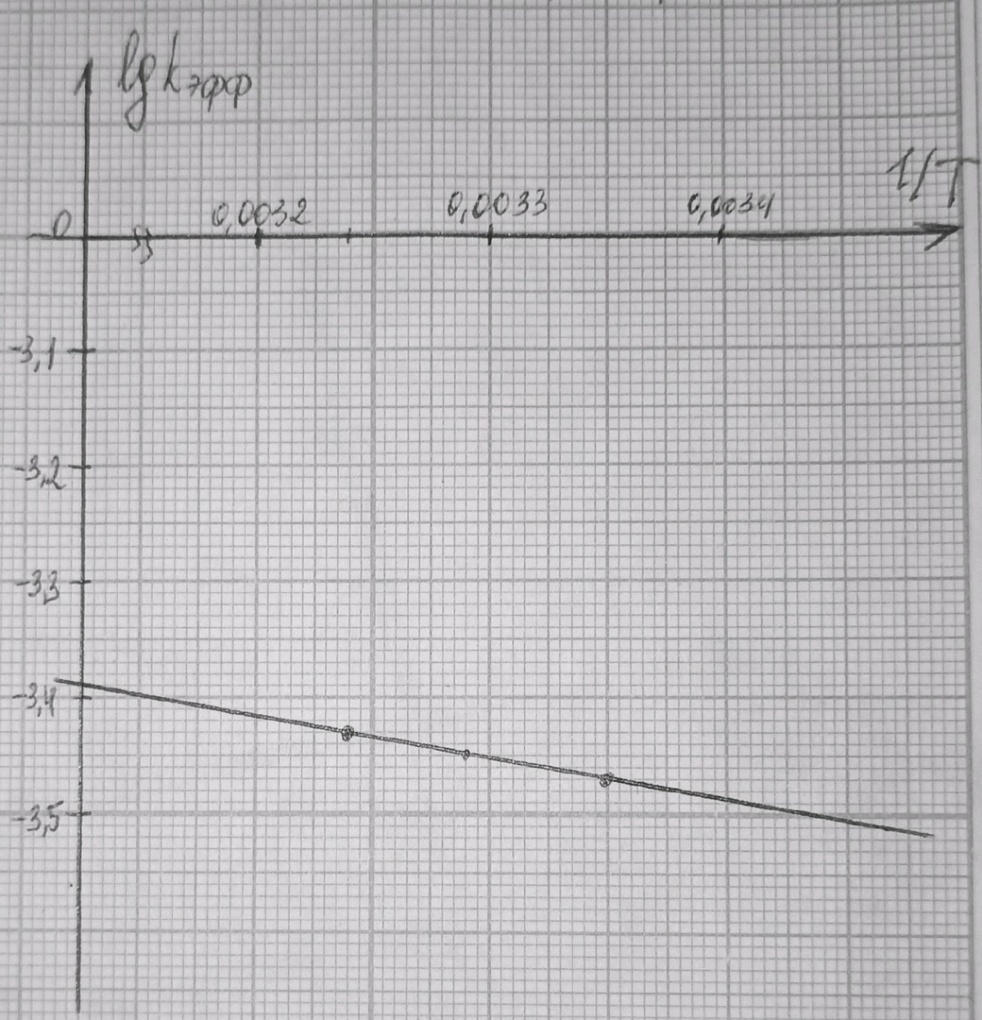 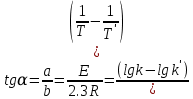 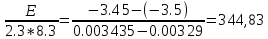 Дж/моль. Дж/моль.Заключение.В результате поиска источников информации в виде научной литературы, включающей в себя научные статьи, учебники и некоторые данные из сети Интернет был получен и усвоен материал по теме «Каталитическая очистка выхлопных газов». В курсовой работе проведен анализ и изучен каталитический метод очистки отходящих газов. Этот метод очистки основан на химических превращениях токсичных компонентов в нетоксичные на поверхности твердых катализаторов. Каталитические методы используются для очистки газов от оксидов азота, серы, углерода и от органических примесей. Также мы рассмотрели классификацию выхлопных газов и методы их очистки в следующих отраслях: транспортных средствах и промышленности. В практической части курсовой работы была выполнена работа по гетерогенному катализу на основе реакции разложения пероксида водорода на диоксиде марганца. С увеличением температуры увеличивается скорость реакции. Определены константы скоростей реакции при разных температурах. Итак, на основании проведённых исследований можно сделать вывод, что проведённая работа помогла изучить углубленно каталитическую очистку выхлопных газов, а также изучить влияние гетерогенного катализа на скорость разложения пероксида водорода. Были получены новые знания в области физической химии, химической кинетике. Список литературыВлияние выхлопных газов на здоровье человека.// TION. -2018. URL: https://tion.ru/blog/vyhlopnye-gazy/ (Дата обращения: 18. 05. 2022) – Текст: электронный. Вяткин М. Ф., Куимова М. В. О влиянии выхлопных газов автомобилей на здоровье человека. // Молодой учёный. 2015. – № 10. – С. 87 – 88. Катализатор автомобильный: работа, типы, конструкция. URL: https://elm3.ru/wiki/kataliticheskij-nejtralizator (Дата обращения: 18. 05. 2022) – Текст: электронный. Каталитический нейтрализатор: устройство и принцип работы. URL: https://techautoport.ru/dvigatel/vypusknaya-sistema/kataliticheskiy-neytralizator.html (Дата обращения: 11.05.2022). - Текст: электронный. Каталитическая очистка газовых выбросов: методы и технологии – фильтр каталитической очистки // ГК «ЭКОЭНЕРГОТЕХ» - 2019. URL: https://eet-msk.ru/posts/12 (Дата обращения: 12. 05. 2022) – Текст: электронный. Колбасина Н. И., Котов М. М. Химический состав выхлопных газов автотранспорта, его влияние на здоровье человека. // Материалы студенческой научной конференции «Студенческий научный форум». URL – href="https://scienceforum.ru/2018/article/2018004431">https://scienceforum.ru/2018/article/2018004431 (дата обращения: 14.05.2022 ). – 2018. Очистка выбросов автотранспорта. URL: https://studopedia.su/7_41220_ochistka-vibrosov-avtotransporta.html (Дата обращения: 14. 05. 2022). – Текст: электронный. Пимнева Л. А., Загорская А. А., Иванько А. Н. Использование каталитической очистки для подавления газовых выбросов Уренгойского НГКМ.// Фундаментальные исследования. – 2016. - №5 (часть 2). – С. 279 – 283. Тарасенко А. Каталитическая и термическая очистка отходящих газов – что лучше?// TOPSOE. – 2020 №3 – 38 с. Ханхасаева С. Ц. Руководство к практическим работам по химической кинетике. / С. Ц. Ханхасаева, Э. Ц. Дашинамжилова, Л. Б. Буянтуева. – Улан-удэ : Изд-во Бурятского университета, 2003 – 85 с. |

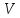 , мл
, мл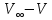 , мл
, мл