Получение стирола 1. Курсовой проект 57 с., 14 табл., 8 рис., 20 источников
 Скачать 0.69 Mb. Скачать 0.69 Mb.
|
 Реферат РефератКурсовой проект 57 с., 14 табл., 8 рис., 20 источников. СТИРОЛ, ЭТИЛБЕНЗОЛ, ДЕГИДРИРОВАНИЕ, ВОДЯНОЙ ПАР, МАТЕРИАЛЬНЫЙ БАЛАНС, ТЕПЛОВОЙ БАЛАНС, РЕАКТОР, КАТАЛИЗАТОР, ОКСИД ЖЕЛЕЗА. Целью данного курсового проекта является изучение процесса производства стирола дегидрированием этилбензола. Курсовой проект содержит обзор катализаторов процесса, аппаратурное оформление и описание основных методов производства стирола. Рассмотрены характеристики сырья и продуктов. Описан химизм процесса дегидрирования этилбензола. Дано подробное описание технологической схемы дегидрирования этилбензола. Проект содержит расчет материального баланса получения стирола из этилбензола мощностью 350 000 т/год. Графическая часть включает технологическую схему производства стирола – один лист формата А1, особенности и тенденции технологического оформления процессп – один лист А1.  Содержание СодержаниеВведение……………………………………………………….…………........………..5 1. Аналитический обзор с элементами патентной проработки……………..…...........6 1.1 Физико-химические основы процесса получения стирола ………...............6 1.2 Обзор технологического оформления процесса……………….…………10 1.2.1 Технология совместного получения стирола и пропиленоксида ………………………………………………………10 1.2.2 Дегидрирование этилбензола..............................................….............13 1.3 Библиографический обзор и патентный поиск................................................21 2 Технологическая часть……………………………………………..………..............27 2.1 Характеристика сырья и производимой продукции………………………27 2.2 Описание технологической схемы……………………………………...........31 3 Расчет материального и теплового балансов………………………………………33 3.1 Материальный баланс установки……………………...……………………..33 3.2 Расчет теплового баланса …………………………………….........................40 3.2.1 Тепловой расчет первой ступени катализа .......................................40 3.2.2 Тепловой расчет межступенчатого теплообменника........................42 3.2.3 Тепловой расчет второй ступени катализа .......................................43 4 Технологический расчет и подбор основного и вспомогательного оборудования………………………………………………………………….............46 4.1 Расчет реактора. …...…….................................................................................46 4.2 Расчет реактора первой ступени ……………………………........................47 4.3 Расчет межступенчатого теплообменника ......................................................48 4.4 Расчет и подбор насоса ...............................................................................53 Заключение……………………………………………………………………………56 Список использованных источников…………………………………………….........57  Введение ВведениеСтирол является одним из основных мономеров для производства полимерных материалов, без которых в настоящее время не может обойтись ни одна отрасль промышленности, как в России, так и за рубежом, Стирол используется для получения полистирола, термоэластопластов, различных лакокрасочных композиций. В настоящее время производство стирола – крупнотоннажное, единичная мощность современных агрегатов составляет 150-300 тысяч тонн стирола в год. Первоначально стирол в США получали дегидрохлорированием монохлорэтилбензола, в свою очередь получавшегося хлорированием этилбензола. Этилбензол синтезировали путем алкилирования бензола хлористым этилом по Фриделю – Крафтсу. Полученный таким способом продукт, содержал атом хлора в ядре, что приводило к окрашиванию. Кроме того, себестоимость продукта тоже была высокой. Существует множество способов получения стирола, но эти способы не востребованы, так как применение высоких температур и давлений приводит к удорожанию продукта, а выход составляет не более 50% от теоретического. Основным промышленным способом производства стирола в настоящее время является дегидрирование этилбензола. Перспективным может быть получение стирола из фракции C8 пиролизной смолы. В данной работе описаны свойства стирола, его применение, основные методы получения и технологические процессы. Целью работы является рассмотрение технологии получения стирола дегидрированием этилбензола, как основного метода получения рассматриваемого мономера.  1 Аналитический обзор с элементами патентной проработки 1 Аналитический обзор с элементами патентной проработки1.1 Физико-химические основы процесса получения стирола Большую часть стирола (около 85 %) в промышленности получают дегидрированием этилбензола при температуре 600 – 650°С, атмосферном давлении и разбавлении перегретым водяным паром в 3 – 10 раз. Используются оксидные железо-хромовые катализаторы с добавкой карбоната калия. Другой промышленный способ, которым получают оставшиеся 15 %, заключается в дегидратации метилфенилкарбинола, образующегося в процессе получения оксида пропилена из гидропероксида этилбензола. Гидропероксид этилбензола получают из этилбензола некаталитическим окислением воздухом. Разрабатываются альтернативные способы получения стирола. Каталитическая циклодимеризация бутадиена в винилциклогексен, с его последующим дегидрированием. Окислительное сочетание толуола с образованием стильбена; метатезис стильбена с этиленом приводит к стиролу. Взаимодействием толуола с метанолом также может быть получен стирол. Кроме того, активно разрабатывались способы выделения стирола из жидких продуктов пиролиза. На сегодняшний день ни один из этих процессов не является экономически выгодным и в промышленном масштабе не реализован [1]. В лабораторных условиях может быть получен нагреванием до 320 °С полистирола с его моментальным отведением. 1) Термическое декарбоксилирование коричной кислоты проводится при температуре 120-130 °С и атмосферном давлении. Выход стирола составляет около 40% 2) Дегидратация фенилэтилового спирта. Реакция может быть реализована как в газовой, так и в жидкой фазе. Жидкофазная дегидратация фенилэтилового спирта осуществляется в присутствии фосфорной кислоты или бисульфита калия. Дегидратация в паровой фазе проводится над катализаторами: оксидами алюминия, тория или вольфрама. При использовании оксида алюминия выход стирола составляет до 90% от теории. 3) Синтез из ацетофенона. Стирол можно получить по реакции ацетофенона с этиловым спиртом над силикагелем: Выход составляет около 30%. 4) Получение стирола из галогенэтилбензола:  5) Получение стирола дегидрированием этилбензола.  6 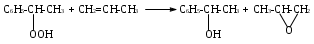 ) Метод производства из этилбензола через гидропероксид этилбензола с одновременным получением оксида пропилена (халкон-процесс):  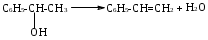 7   )Получение стирола метатезисом этилена со стильбеном, полученным окислением толуола: 8) Получение стирола каталитической циклодимеризацией бутадиена:  Все приведенные методы получения стирола (за исключением дегидрирования) многостадийны, используют повышенное давление и высокую температуру, что приводит к усложнению и удорожанию производства. Для некоторых методов используется не очень доступное сырье. Небольшие выходы. Основным методом промышленного производства стирола является каталитическое дегидрирование этилбензола. Этим методом получают более 90% мирового производства этилбензола. Дегидрирование этилбензола осуществляется в присутствии водяного пара на катализаторе марки К-28У, содержащим оксид железа и небольшое количество соединений калия, рубидия, циркония. Водяной пар вводится для снижения парциального давления процесса, что способствует сдвигу равновесия реакции в сторону образования стирола, сокращению побочных реакций на поверхности катализатора. Реакция дегидрирования этилбензола производится в двухступенчатом адиабатическом реакторе с промежуточным подводом тепла через межступенчатый подогреватель. Содержание стирола после первой ступени – не менее 23 %, после второй – не менее 47 %. Температура процесса 550-6400С, соотношение этилбензол: пар равно 1:3-3, 5, давление над слоем катализатора не более 1 атм. Основная реакция дегидрирования: 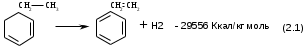 Побочные реакции: 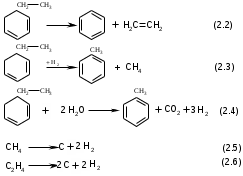 Изопропилбензол, содержащийся в этилбензоле, в процессе дегидрирования превращается в α-метилстирол:  Дивинилбензол полимеризуется с образованием нерастворимых полимеров в колоннах ректификации. Наличие бензола приводит к образованию дивинила:  О дновременно идут реакции дегидроконденсации с получением полициклических соединений – двухзамещенных стильбенов, фенантренов, нафталинов. Углерод, образующийся при разделении углеводородов, удаляется с катализатора водяным паром:  Для предотвращения полимеризации стирола в процессе его получения используются также ингибиторы: парахинондиоксим (ДОХ), 4-нитрофенол – отход (ПХФ), 2, 6-дитретбутил-4-диметиламинометилфенол (основание Манниха). В качестве катализаторов дегидрирования применяются сложные композиции на основе оксидов цинка или железа. Раньше наиболее распространенным был катализатор стирол-контакт на основе ZnO. В последнее время используют, главным образом, железо-оксидные катализаторы, содержащие 55-80% Fe2O3; 2-28% Cr2O3; 15-35% K2CO3 и некоторые оксидные добавки. В частности широко используется катализатор НИИМСК К-24 состава Fe2O3 – 66-70%; K2CO3 – 19-20%; Cr2O3 – 7-8%; ZnO2 – 2,4-3,0%; K2SiO3 – 2,0-2,6%. Значительное содержание K2CO3 в катализаторе обусловлено тем, что он способствует дополнительной саморегенерации катализатора за счет конверсии углеродистых отложений водяным паром. Катализатор работает непрерывно 2 месяца, после чего его регенерируют, выжигая кокс воздухом. Общий срок службы катализатора – 2 года [2]. 1.2 Обзор технологического оформления процесса 1.2.1 Технология совместного получения стирола и пропиленоксида Общая технологическая схема совместного получения стирола и пропиленоксида представлена на рисунке 1.1.  1 – колонна окисления; 2 – конденсатор; 3,7-10,18 – ректификационные колонны; 4 – скруббер щелочной очистки; 5,12,14 – теплообменники; 6 – колонна эпоксидирования; 11 – испаритель смешения; 13,15 – реакторы дегидратации; 16 – холодильник; 17 – флорентийский сосуд; I – воздух; II – этилбензол; III – пропилен; IV – раствор щелочи; V – газы; VI – катализаторный раствор; VII – оксид пропилена; VIII – смолы; IX – водный слой; X – стирол; XI – на дегидрирование; XII – пар; Рисунок 1.1. Технологическая схема совместного получения стирола и оксида пропилена В данной технологии окисление этилбензола проводится в тарельчатой колонне 1. При этом как подогретый этилбензол, так и воздух подаются в низ колонны. Колонна снабжена змеевиками, расположенными на тарелках. Тепло отводится водой, подаваемой в эти змеевики. Если для интенсификации процесса использовать катализатор, то процесс необходимо проводить в ряде последовательно соединенных барботажных реакторов, в которые подают противотоком к воздуху этилбензольную шихту (смесь свежего и возвратного этилбензола с катализаторным раствором). При этом продукты окисления проходят последовательно через реакторы, в каждый из которых подают воздух. Парогазовая смесь из верхней части реактора поступает в конденсатор 2, в котором конденсируется главным образом унесённый этилбензол, а также примеси бензойной и муравьиной кислот. После отделения конденсата от газов он направляется в скруббер для нейтрализации кислот щелочью. После нейтрализации этилбензол возвращается в реактор 1. Туда же подается этилбензол из колонны 10. Газы выводятся из системы. Оксидат из нижней части колонны 1, содержащий около 10% гидропероксида, направляют в ректификационную колонну 3 для концентрирования. Концентрирование гидропероксида проводят при глубоком вакууме. Несмотря на большие затраты энергии, этот процесс лучше проводить на установке двойной ректификации. При этом на первой колонне отгоняется часть этилбензола при более низком вакууме, а во второй колонне при более глубоком вакууме отгоняется остальная часть этилбензола с примесями. Дистиллят этой колонны возвращается в первую колонну, а в кубе получается концентрированный (до 90 %) гидропероксид, который направляется на эпоксидирование. Предварительно оксидат охлаждается в теплообменнике 5 исходным этилбензолом. В колонне 3 отгоняется этилбензол с примесями кислот, поэтому верхний продукт также направляется в скруббер 4. Из куба колонны 3 сконцентрированный гидропероксид поступает в колонну эпоксидирования 6. (Эпоксидирование можно также проводить в каскаде реакторов.) В нижнюю часть колонны подается катали - заторный раствор из куба колонны 9. Туда же проводится подпитка свежим катализатором. Свежий и возвратный (из колонны 7) пропилен также подается в нижнюю часть колонны. Продукты реакции вместе с катализаторным раствором выводят из верхней части колонны и направляют в ректификационную колонну 7 для отгонки пропилена. Газы выводят из верхней части колонны и из системы для утилизации или сжигания. Кубовый продукт колонны 7 поступает в ректификационную колонну 8 для выделения в качестве дистиллята продуктового оксида пропилена. Кубовая жидкость колонны 8 поступает в колонну 9 для отделения продуктов синтеза от катализаторного раствора. Катализаторный раствор из куба колонны возвращается в колонну эпоксидирования 6, а верхний продукт поступает в ректификационную колонну для отделения этилбензола от метилфенилкарбинола и ацетофенона. Смесь метилфенилкарбинола (МФК) и ацетофенона подается в испаритель 11, в котором с помощью перегретого пара испаряются и отделяются от смол метилфенилкарбинол и ацетофенон. Смесь паров, перегретая до 300 °С, поступает в реактор 13 для дегидратации метилфенилкарбинола. В этом реакторе частично проходит дегидратация. Так как реакция дегидратации является эндотермической, то прежде чем продукты дегидратации поступают в другой реактор (реактор 15), продукты дегидратации перегреваются в теплообменнике 14. Конверсия метилфенилкарбинола после двух реакторов достигает 90%. Продукты дегидратации охлаждаются водой в холодильнике 16 и поступают во флорентийский сосуд 17, в котором органический слой отделяется от водного. Верхний углеводородный слой поступает в ректификационную колонну 18 для отделения стирола от ацетофенона. Ацетофенон затем гидрируется на отдельной установке в метилфенилкарбинол, который поступает в отделение дегидратации. Селективность процесса по оксиду пропилена составляет 95 – 97 %, а выход стирола достигает 90 % по этилбензолу. При этом из 1 т пропиленоксида получается 2,6 – 2,7 т стирола. Таким образом, рассмотренная технология представляет сложную систему, включающую множество рециклов по этилбензолу, пропилену и катализатору. Эти рециклы приводят, с одной стороны, к увеличению затрат энергии, а с другой, позволяют вести процесс в безопасных условиях (при низкой концентрации гидропероксида – 10 – 13%) и достигать полной конверсии реагентов: этилбензола и пропилена. Следовательно, данный процесс необходимо оптимизировать. В предложенной технологической схеме достаточно полно используется тепло реакций и потоков. Однако вместо холодильника 16 лучше использовать котел-утилизатор, в котором можно получать пар низкого давления. Для этого в котел-утилизатор необходимо подавать водный конденсат, из которого будет получаться пар. Кроме того, следует предусмотреть более полное использование отходящих газов и смолы, щелочного раствора солей из скруббера 4, а также до- очистку водного слоя флорентийского сосуда. Наиболее существенным усовершенствованием технологической схемы может служить замена реакторов дегидратации на колонну, в которой можно организовать совмещенный реакционно-ректификационный процесс. Этот процесс протекает на ионообменном катализаторе в парожидкостном варианте, т. е. при температуре кипения смесей, проходящих через колонну, и может быть представлен схемой (рисунок 1.2).  Рисунок 1.2. Принципиальная схема оформления совмещенного процесса В таком варианте процесса конверсия и селективность могут достигать 100 %, так как процесс протекает при низких температурах и малом времени пребывания продуктов синтеза в реакторе. Преимущество данного варианта процесса заключается еще и в том, что стирол не попадает в куб колонны, а выделяется в виде гете- роазеотропа с водой (температура кипения ниже 100 °С), что позволяет исключить его термополимеризацию [4]. Технология производства стирола и оксида пропилена использует в качестве сырья доступные, производимые в больших количествах этилбензол и пропилен. Этот процесс нельзя отнести к мало - стадийным, поскольку он включает в себя несколько химических реакций: окисление этилбензола в гидропероксид, эпоксидирование пропилена, дегидратация метилфенилкарбинола, гидрирование ацетофенона. Тем не менее, даже такая многоступенчатая структура технологии дает возможность получать целевые продукты с селективностью по оксиду пропилена 95—97 % и выходом стирола по этилбензолу до 90%. Таким образом, рассматриваемое производство можно отнести к высокоэффективным. Более того, такая технология является ярким примером «сопряженных» производств, обеспечивающих одновременное получение нескольких целевых продуктов, позволяет выпускать стирол с качеством более высоким, чем при дегидрировании (с точки зрения процессов полимеризации) и заменить экологически грязное производство оксида пропилена хлоргидринным способом. В связи с многостадийным характером технологии следует выделить в ней узлы, обеспечивающие высокие конверсии за один проход — эпоксидирование, дегидратация, гидрирование, и не обладающие таким характером — получение гидропероксида этилбензола. В этом случае ограничения по конверсии этилбензола связаны с последовательным характером побочных реакций и взрывоопасностью гидропероксида при высоких концентрациях в температурных условиях (140-160 °С) протекания реакции. Соответственно, рециркуляционные потоки, направленные на полное использование исходного сырья, имеют большие объемы на стадии окисления и меньшие для остальных стадий (рецикл по катализаторному раствору стадии эпоксидирования; рецикл по возвратному этилбензолу. Данная технология из-за многостадийности требует реализации в полной мере принципа полноты выделения продуктов из реакционной массы, поскольку именно чистые соединения, поступающие на каждую из стадий химического превращения, обеспечивают высокие показатели процесса в целом. Экзотермичный характер процессов окисления и эпоксидирования дает возможность применять получаемые на этих стадиях энергоресурсы (пар) для процессов разделения и, тем самым, обеспечить реализацию принципа полноты использования энергии системы. В целом разработанное и реализованное в нашей стране технологическое решение обладает высокой эффективностью [4]. |
