Получение стирола 1. Курсовой проект 57 с., 14 табл., 8 рис., 20 источников
 Скачать 0.69 Mb. Скачать 0.69 Mb.
|
|
Расчет основных расходных коэффициентов Для получения 42896,82 кг/ч стирола-ректификата расходуется по реакциям 1-4 52049,71 кг/ч этилбензола. Расходный коэффициент по этилбензолу: 52049,71/42896,82 = 1,213 кг/кг. Дополнительно образуется (кг на 1 т стирола-ректификата): толуола: 4336,82/42896,82 = 0,101; бензола: 2267,40/42896,82 = 0,053 [17]. 3.2 Расчет теплового баланса Исходные данные: в реактор дегидрирования подают 288142,28/(3600∙2) = 40,02 кг/с парогазовой смеси; состав потоков 6, 7 и потока на выходе их реактора приведены в таблицах 2.6 и 2.7.; температура парогазовой смеси, °С: на входе в реактор – 610; на выходе из первой ступени (уточняется расчетом) – 530-540; на входе во вторую ступень реактора – 610; на выходе из реактора (уточняется расчетом) – 570-590; температура водяного пара на выходе из промежуточного теплообменника 655°С. 3.2.1 Тепловой расчет первой ступени катализа Цель расчета – определение температуры парогазовой смеси на выходе из первой ступени катализа. Уравнение теплового баланса в общем виде: Ф1 = Ф2 +Ф3+ Фпот где Ф1, Ф3 – тепловые потоки парогазовой смеси на входе в реактор и выходе из первой ступени катализа соответственно, кВт; Ф2 – теплота, расходуемая на осуществление химических реакций, кВт; Фпот – теплопотери в окружающую среду, кВт. Тепловой поток парогазовой смеси на входе в реактор рассчитывают, используя определенные ранее значения средней энтальпии парогазовой смеси и энтальпии водяного пара после смешения: Ф1=[111454,46/(2∙3600)] ∙1740,72+[176687,82/(2∙3600)] ∙3725,8] = = 118377,03 кВт. Для расчета Ф2 определяют теплоту реакции дегидрирования (реакция1); 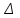 H 0298 = 147,36 – 29,79 = 117, 57 кДж/моль; H 0298 = 147,36 – 29,79 = 117, 57 кДж/моль;Ф2 = (276,99/(2∙3600)) ∙117, 57∙103 = 4522,96 кВт, где 273,57 – расход этилбензола на первой ступени катализа, кмоль/ч. Для определения температуры парогазовой смеси на выходе из первой ступени катализа, используя данные о составе смеси, рассчитывают средние энтальпии парогазовой смеси при температурах 530 и 540°С. Таблица 3.8 – Расчет средней энтальпии парогазовой смеси
Значения энтальпий органических соединений и перегретого водяного пара находят по справочнику [19], предварительно рассчитывают парциальное давление водяного пара (молярную долю водяного пара): рH2О = р · хH2О = 0,4 ∙ 0,8953 = 0,36 МПа. Принимают, что теплопотери в окружающую среду составляют 1,5 % от общего прихода теплоты: Фпот = 0,015 ∙ 118377,03 = 1775,66 кВт. Тепловой поток парогазовой смеси на выходе из первой ступени находят из уравнения теплового баланса: Ф3 = Ф1 – Ф2 – Фпот = 118377,03 – 4522,96 – 1775,66 = 112078,41 кВт. Энтальпия парогазовой смеси: hг = Ф3/mг = 112078,41/40,02 = 2800,58 кДж/кг, где mг – количество парогазовой смеси, проходящей через слои катализатора, кг/с. Температура парогазовой смеси: 813+((2800,58 – 2781,65)/(2781,65 – 2758,38)) ∙ (813-803) = 816 К или 543 °С. Температура парогазовой смеси на выходе из первой ступени катализа соответствует оптимальному технологическому режиму реактора, следовательно, степень конверсии этилбензола принята верно. 3.2.2 Тепловой расчет межступенчатого теплообменника Цель расчета – определение температуры перегретого водяного пара на входе в теплообменник. Рассчитывают среднюю энтальпию парогазовой смеси на входе во вторую ступень катализа ( на выходе из теплообменника) при температуре Е= 610+273 = 883 К Таблица 3.9 – Состав парогазовой смеси на входе во вторую ступень катализа
Тепловая нагрузка теплообменника: 40,02 (2943,17 – 2800,58) = 5706,66 кВт, Тепловой поток водяного пара на выходе из теплообменника при температуре 650ºС: Фп=176687,82∙3821, 0/(2∙3600) = 93767,25 кВт, где 176687,82 – расход водяного пара, поступающего в узел смещения при температуре 650 ºС, кДж/кг. Тепловой поток водяного пара на входе в теплообменник: 93767,25 + 5706,66 = 99473,91 кВт. Энтальпия водяного пара на входе в теплообменник: 99473,91∙2∙3600/176687,82=4053,55 кДж/кг, что при давлении 0,9 МПа соответствует температуре водяного пара 760 ºС. 3.2.3 Тепловой расчет второй ступени катализа Цель расчета – определение температуры парогазовой смеси на выходе из реактора дегидрирования. Уравнение теплового баланса в общем виде идентично уравнению теплового баланса первой ступени катализа. Тепловой поток парогазовой смеси на входе во вторую ступень катализа: Ф1 = 40,02 ∙ 2943,17 = 117785,07 кВт. Для определения количества теплоты реакций 2 – 3, 5 – 8. теплотой реакции образования дибензилидена (реакция 4) пренебрегают; теплота реакции 1 рассчитана ранее. Расчет теплот реакций (в кДж/моль):
Количество теплоты расходуемой на химические реакции: Ф2=[1000/(2∙3600)](135,48 ∙ 117,52 – 47,14 ∙ 54, 64 + 29,07 ∙ 105, 44 – – 2,36 ∙ 127, 15+27,62 ∙ 131, 28+ 61,69 ∙ 206,13 – 88,41 ∙ 41,17) = = 0,139 ∙ 25601,51 = 3558,61 кВт. Ориентировочное понижение температуры во второй ступени катализа: (610 – 543) – 3558,61/4522,96 = 66˚С. Температура на второй ступени катализа: 610 – 66 = 544 ˚С Для определения температуры контактного газа на выходе из реактора рассчитывают его средние энтальпии при температурах 550 и 570˚С, используя данные о составе газа (поток 7). Значение энтальпии водяного пара принято при давлении 0, 35 · 0, 8983 = 0,314 МПа. Так как содержание в контактном газе бензола, этилена, метана, диоксида углерода, оксида углерода, водорода и тяжелых продуктов незначительно, при расчете средней энтальпии эти компоненты не учитывают Таблица 2.10- Расчет средней энтальпии контактного газа
Принимают, что теплопотери в окружающую среду составляют 1, 5% от общего прихода теплоты: Фпот = 0,015 ∙ 116149,14 =1742,24 кВт. Тепловой поток контактного газа на выходе из реактора находят из уравнения теплового баланса: Ф3=Ф1 – Ф2 – Фпот = 116149,14 – 3942,02 – 1742,24 = 110464,87 кВт. Энтальпия контактного газа: hг = 110464,78/39,46 = 2799,33 кДж/кг. Температура контактного газа: 843 + (2799,33 – 2789,73)20/(2789,73 – 2744,50) = 847 К или 574˚С. Определяют суммарную теплоту, расходуемую на осуществление химических реакций (на обеих ступенях катализа): 4467,13 + 3942,02 = 8409,16 кВт [17]. Таблица 2.11- Составляют тепловой баланс дегидрирования
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||