Получение стирола 1. Курсовой проект 57 с., 14 табл., 8 рис., 20 источников
 Скачать 0.69 Mb. Скачать 0.69 Mb.
|
600°С. Это позволяет устранить обратимость и эндотермичность реакции, повысить степень конверсии этилбензола при сохранении хорошей селективности и снизить энергетические затраты [16]. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Компоненты | C6H5 – C2H5 | C6H6 | 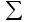 |
| wi, % | 99,965 | 0,035 | 100 |
| m 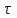 , кмоль/ч , кмоль/ч | 52125,48 | 18,25 | 52143,73 |
| n 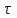 , кмоль/ч , кмоль/ч | 491,75 | 0,23 | 491,98 |
| хi, % | 99,952 | 0,048 | 100 |
Рассчитываем состав возвратного (циркуляционного) этилбензола (поток 2):
Таблица 3.2 – Состав возвратного этилбензола
| Компоненты | C6H5-C2H5 | C6H5-C2H3 | C6H5-CH3 | 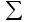 |
| wi, % | 93,94 | 2,76 | 3,30 | 100,00 |
| m 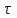 , кг/ч , кг/ч | 42586,13 | 1251,20 | 1496,00 | 45333,32 |
| М, г/моль | 106 | 104 | 92 | - |
| n 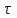 , кмоль/ч , кмоль/ч | 401,76 | 12,03 | 16,26 | 430,05 |
| хi, % | 93,42 | 2,80 | 3,78 | 100,00 |
Для снижения температуры кипения в жидкую этилбензольную фракцию в испарителе добавляют водяной пар. Массовую долю водяного пара в образующейся парогазовой смеси находят по формуле:
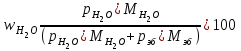 ,
,где рH2О и рэб – парциальные давления паров воды и этилбензольной фракции при температуре кипения;
MH2O и Мэб – молярные массы воды и этилбензольной фракции, кг/кмоль.
Так как этилбензольная фракция состоит в основном из этилбензола, молярную массу фракции принимают равной молярной массе этилбензола.
Парциональное давление паров воды при температуре кипения 155°С составляет 0,5579 МПа, парциональное давление этилбензольной фракции при общем давлении в испарителе 1,2000 МПа равно
1, 2000 – 0,5579 = 0,6421МПа.
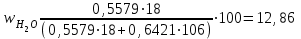 %.
%.Общее количество подаваемого в реактор этилбензола:
52125,48 + 42586,13 = 94711,60 кг/ч.
Расход водяного пара в испаритель (поток 3):
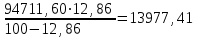 кг/ч.
кг/ч.Рассчитывают по суммарному содержанию компонентов в потоках 1, 2, 3 состав парогазовой смеси после испарителя (поток 4):
Таблица 3.3 – Состав парогазовой смеси после испарителя
| Компоненты | C6H5-C2H5 | C6H5-C2H3 | C6H5-CH3 | C6H6 | Н2О | 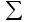 |
| m 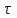 , кмоль/ч , кмоль/ч | 94711,60 | 1251,20 | 1496,00 | 18,25 | 13977,41 | 111454,46 |
| wi, % | 84,98 | 1,12 | 1,34 | 0,02 | 12,54 | 100, 00 |
| n 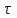 , кмоль/ч , кмоль/ч | 893,51 | 12,03 | 16,26 | 0,23 | 776,52 | 1698,55 |
| хi, % | 52,60 | 0,71 | 0,96 | 0,01 | 45,72 | 100,00 |
В сырьевой поток на входе в реактор дегидрирования вводят водяной пар для снижения парциального давления этилбензола, повышения его степени конверсии и подавления побочных реакций. Расход водяного пара определяют из уравнения теплового баланса узла смешения:
mп (hп′ – hп′′)= mг (hг′′– hг′),
где mп и mг – массовый расход газовой смеси и поступающего водяного пара, кг/ч;
hг′ и hп′ – энтальпия газовой смеси и водяного пара до смешения, кДж/кг;
hг′′ и hп′′ – энтальпия газовой смеси и водяного пара после смешения, кДж/кг.
Принимают следующие значения температуры, °С: парогазовой смеси после перегревателя – 550; водяного пара, поступающего из промежуточного теплообменника – 655; парогазовой смеси на входе в реактор – 610.
Рассчитывают среднюю энтальпию парогазовой смеси:
Таблица 3.4 – Средняя энтальпия парогазовой смеси
| Компоненты | wi, % | T = 550+273=823 К | Т = 610+273=883 К | |||
| hi, кДж/кг | wihi/100, кДж/кг | hi, кДж/кг | wihi/100, кДж/кг | |||
| C6H5-C2H5 | 85,12 | 1294,2 | 1101,62 | 1458 | 1241,05 | |
| C6H5-C2H3 | 1,05 | 1223,3 | 12,84 | 1375,8 | 14,45 | |
| C6H5-CH3 | 1,25 | 1224,3 | 15,30 | 1381,2 | 17,27 | |
| C6H6 | 0,02 | - | - | - | - | |
| Н2О | 12,56 | 3594,5 | 451,47 | 3725,8 | 467,96 | |
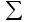 | 100 | - | 1581,24 | - | 1740,72 | |
Предварительно определяют парциальное давление паров воды в парогазовой смеси:
ρH20 = 0,46 ∙ 0,4572 = 0,21 МПа,
где 0,46 – давление парогазовой смеси, МПа; 0,4572 – молярная доля паров воды в смеси.
Энтальпия водяного пара (ρ = 0,9 МПа):
до смешения (t = 655°С): hп′ = 3821,0 кДж/кг;
после смешения (t = 610°С): hп′′ = 3720,4 кДж/кг.
Определяем расход водяного пара в узел смешения (поток 5):
mп (3821,0 – 3720,4) = 111454,46 · (1740,72 – 1581,24),
mп = 176687,82 кг/ч.
Количество водяного пара на входе в реактор дегидрирования:
176687,82 + 13977,41 = 190655,23 кг/ч.
Массовое отношение водяной пар : этилбензол:
190655,23/94711,60 = 2,01,
что соответствует оптимальному технологическому режиму.
Суммируя содержание компонентов в потоках 4 и 5, определяют состав парогазовой смеси на входе в реактор дегидрирования (поток 6):
Таблица 3.5 – Состав парогазовой смеси на входе в реактор дегидрирования
| Компоненты | C6H5-C2H5 | C6H5-C2H3 | C6H5-CH3 | C6H6 | Н2О | 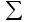 |
| m 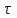 , кмоль/ч , кмоль/ч | 94711,60 | 1251,20 | 1496,00 | 18,25 | 190665,23 | 288142,28 |
| wi, % | 32,87 | 0,43 | 0,52 | 0,01 | 66,17 | 100,00 |
| n 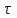 , кмоль/ч , кмоль/ч | 893,51 | 12,03 | 16,26 | 0,23 | 10592,51 | 11514,54 |
| хi, % | 7,76 | 0,10 | 0,14 | 0,00 | 91,99 | 100,00 |
Для упрощения расчета принимают, что на первой ступени протекает только основная (целевая) реакция конверсии этилбензола, при этом расходуется этилбензола:
893,51 ∙ 0,31 = 276,99 кмоль/ч или 276,99 ∙ 106 = 29360,60 кг/ч,
где 0, 31 – степень конверсии этилбензола в стирол на первой ступени дегидрирования.
Образуется:
стирола: 276,99 кмоль/ч или 28806,62 кг/ч;
водорода: 276,99 кмоль/ч или 553,97 кг/ч.
В парогазовой смеси после первой ступени содержится:
стирола: 12,03 + 276,99 = 289,02 кмоль/ч или 30057,82 кг/ч;
непрореагировавшего этилбензола:
893,51 – 276,99 = 616,52 кмоль/ч или 65351,01 кг/ч.
Рассчитывают состав парогазовой смеси после первой ступени катализа:
Таблица 3.6 – Состав парогазовой смеси после первой ступени катализа
| Компоненты | m 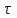 , кмоль/ч , кмоль/ч | wi, % | n 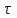 , кмоль/ч , кмоль/ч | хi, % |
| C6H5-C2H5 | 65351,01 | 22,68 | 616,52 | 5,23 |
| C6H5-C2H3 | 30057,82 | 10,43 | 289,02 | 2,45 |
| C6H5-CH3 | 1496,00 | 0,52 | 16,26 | 0,14 |
| C6H6 | 18,25 | 0,01 | 0,23 | - |
| Н2О | 190665,23 | 66,17 | 10592,51 | 89,83 |
| Н2 | 553,97 | 0,19 | 276,99 | 2,35 |
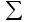 | 288142,28 | 100,00 | 11791,53 | 100,00 |
Массовая доля стирола в контактном газе (в расчете на органические соединения):
 %,
%,что соответствует нормам оптимально технологического режима (30 – 32 %).
На второй ступени дегидрирования по реакции 1 реагирует этилбензола:
412,47 – 276,99 = 135,48 или 14361,16 кг/ч;
Образуется:
стирола: 135,48 кмоль/ч или 14090,19 кг/ч;
водорода: 135,48 кмоль/ч или 270,97 кг/ч.
Количество стирола на выходе из реактора дегидрирования:
289,02 + 135,48 = 424,50 кмоль/ч или 44148,02 кг/ч.
Расход этилбензола по реакциям 1 – 4 составляет 511,43 кмоль/ч, следовательно, по реакциям 2 – 4 расходуется этилбензола:
491,03 – 412,47 = 78,57 кмоль/ч или 8327,95 кг/ч.
По реакции 2 реагирует 60% этилбензола, что составляет:
78,57 ∙ 0,6 = 47,14 кмоль/ч или 4996,77 кг/ч;
расходуется водорода: 47,14 кмоль/ч или 94,28 кг/ч;
Образуется:
толуола: 47,14 кмоль/ч или 4336,82 кг/ч;
метана: 47,14 кмоль/ч или 754,23 кг/ч.
Всего содержится толуола в контактном газе:
47,14 + 16,26 = 63,40 кмоль/ч или 5832,82 кг/ч.
По реакции 3 реагирует 37% этилбензола, что составляет:
78,57 ∙ 0,37 = 29,07 кмоль/ч или 3081,34 кг/ч;
Образуется:
бензола: 29,07 кмоль/ч или 2267,40 кг/ч;
этилена: 29,07 кмоль/ч или 81394 кг/ч.
Всего содержится бензола в контактном газе:
29,07 + 0,23 = 29,30 кмоль/ч или 2285,65 кг/ч.
По реакции 4 реагирует 3% этилбензола, что составляет:
78,57 ∙ 0,03 = 2,36 кмоль/ч или 249,84 кг/ч.
Образуется:
дибензилидена: 2,36/2 = 1,18 кмоль/ч или 212,13 кг/ч;
метана: 2,36 кмоль/ч или 37,71 кг/ч.
Образовавшийся при дегидрировании этилен разлагается по реакции:
С2Н4
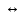 СН4 + С (5)
СН4 + С (5)При степени разложения этилена 0,95 его расход составит:
29,07 ∙ 0,95 = 27,62 кмоль/ч или 773,24 кг/ч.
Остается этилена в контактном газе:
29,07 – 27,62 = 1,45 кмоль/ч или 40,70 кг/ч
Образуется:
метана: 27,62 кмоль/ч или 441,85 кг/ч;
углерода: 27,62 кмоль/ч или 331,39 кг/ч.
Образовавшийся углерод конвертируют водяным паром по реакции:
С + Н2О
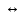 СО + Н2 (6)
СО + Н2 (6)Расходуется водяного пара: 27,62 кмоль/ч или 497,08 кг/ч;
Образуется:
оксида углерода: 27,62 кмоль/ч или 773,24 кг/ч;
водорода: 27,62 кмоль/ч или 55,23 кг/ч.
Всего образуется метана по реакциям 2, 4, 5:
47,14 + 2,36 + 27,62 = 77,11 кмоль/ч или 1233,79 кг/ч.
Метан конвертируют водяным паром по реакции:
СН4+ Н2О
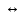 СО + 3Н2 (7)
СО + 3Н2 (7)При степени конверсии метана 0,8 расходуется:
метана: 77,11 ∙ 0, 8 = 61,69 кмоль/ч или 987,04 кг/ч;
водяного пара: 61,69 кмоль/ч или 1110,41 кг/ч
Образуется:
оксида углерода: 61,69 кмоль/ч или 1727,31 кг/ч;
водорода: 3 ∙ 61,69 = 185,07 кмоль/ч или 370,14 кг/ч.
Остается метана в контактном газе:
77,11 – 61,69 = 15,42 кмоль/ч или 246,76 кг/ч.
Всего образуется оксида углерода по реакциям 6 и 7:
27,62 + 61,69 = 89,31 кмоль/ч или 2500,55 кг/ч.
Оксид углерода конвертируют водяным паром по реакции:
СО + Н2О
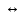 СО2 + Н2 (8)
СО2 + Н2 (8)При степени конверсии оксида углерода 0, 99 расходуется:
оксида углерода: 89,31 ∙ 0,99 = 88,41 кмоль/ч или 2475,55 кг/ч;
водяного пара: 88,41 кмоль/ч или 1591,42 кг/ч;
Образуется:
диоксида углерода: 88,41 кмоль/ч или 3890,15 кг/ч;
водорода: 88,41 кмоль/ч или 176,82 кг/ч.
Остается оксида углерода в контактном газе:
89,31 – 88,41 = 0,89 кмоль/ч или 25,01 кг/ч.
Общий расход водяного пара по реакциям 6-8:
27,62 + 61,69 + 88,41 = 177,72 кмоль/ч или 3198,92 кг/ч.
Остается водяного пара в контактном газе:
10592,51 – 177,72 = 10414,79 кмоль/ч или 187466,31 кг/ч.
Образуется водорода по реакциям 1, 6-8:
135,48 + 27,62 + 185,07 + 88,41 = 436,58 кмоль/ч или 873,16 кг/ч.
Расходуется водорода по реакции 2:
47,14 кмоль/ч или 94,28 кг/ч.
Остается водорода в контактном газе:
276,99 + 436,58 – 47,14 = 666,43 кмоль/ч или 1332,85 кг/ч.
Рассчитывают состав контактного газа на выходе из реактора дегидрирования (поток 7). Результаты расчетов приведены в таблице 3.7.
Таблица 3.7 – Состав контактного газа на выходе из реактора дегидрирования
| Компоненты | m 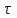 , кмоль/ч , кмоль/ч | wi, % | n 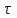 , кмоль/ч , кмоль/ч | хi, % |
| C6H5-C2H5 | 42661,89 | 14,81 | 402,47 | 3,32 |
| C6H5-C2H3 | 44148,02 | 15,32 | 424,50 | 3,51 |
| C6H5-CH3 | 5832,82 | 2,02 | 63,40 | 0,52 |
| C6H6 | 2285,65 | 0,79 | 29,30 | 0,24 |
| C2H4 | 40,70 | 0,01 | 1,45 | 0,01 |
| CH4 | 246,76 | 0,09 | 15,42 | 0,13 |
| CО2 | 3890,15 | 1,35 | 88,41 | 0,73 |
| CО | 25,01 | 0,01 | 0,89 | 0,01 |
| Н2О | 187466,31 | 65,06 | 10414,79 | 86,01 |
| Н2 | 1332,85 | 0,46 | 666,43 | 5,50 |
| Тяжелые продукты | 212,13 | 0,07 | 1,18 | 0,01 |
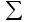 | 288142,28 | 100 | 12108,26 | 100,00 |
Материальный баланс сводим в таблицу 3.8.
Таблица 3.8 Сводная таблица материального баланса
| Приход | кмоль/ч | кг/ч | Расход | кмоль/ч | кг/ч |
| Свежий этилбензол, в т.ч.: | 491,98 | 52143,73 | Продуктовая смесь | 12108,256 | 288142,28 |
| Этилбензол | 491,750 | 52125,48 | C6H5-C2H5 | 402,471 | 42661,89 |
| Бензол | 0,234 | 18,25 | C6H5-C2H3 | 424,500 | 44148,02 |
| | | | C6H5-CH3 | 63,400 | 5832,82 |
| Возвратный этилбензол | 430,048 | 45333,32 | C6H6 | 29,303 | 2285,65 |
| Этилбензол | 401,76 | 42586,13 | C2H4 | 1,453 | 40,70 |
| Стирол | 12,031 | 1251,20 | CH4 | 15,422 | 246,76 |
| Толуол | 16,261 | 1496,00 | CО2 | 88,412 | 3890,15 |
| | | | CО | 0,893 | 25,01 |
| | | | Н2О | 10414,795 | 187466,31 |
| Водяной пар | 10592,513 | 190665,23 | Н2 | 666,427 | 1332,85 |
| | | | Тяжелые продукты | 1,178 | 212,13 |
| Всего: | 922,031 | 288142,28 | Всего | 12108,256 | 288142,28 |



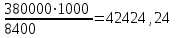 кг/ч;
кг/ч; кг/ч или
кг/ч или 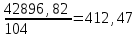 кмоль/ч.
кмоль/ч.