лекции токса. Лекции по токсикологической химии
 Скачать 5.01 Mb. Скачать 5.01 Mb.
|
Применение органических реагентов в дробном анализе“металлических ядов” В дробном методе анализа широко применяются различные органические реагенты: диэтилдитиокарбаминаты натрия и свинца (в анализе на катионы меди, цинка, кадмия, висмута), дитизон (в анализе на катионы свинца, таллия, цинка, серебра, ртути), 8-оксихинолин ( в анализе на катион висмута), малахитовый зеленый из группы трифенилметановых красителей (при анализе на катионы сурьмы и висмута), дифенилкарбазид (при анализе на катион хрома), тиомочевина (при анализе на катион висмута) и др. В основном, образуются окрашенные комплексные соединения или ионные ассоциаты. Ионные ассоциаты (ионные пары) представляют собой неполностью диссоциированные солеобразные соединения, образующиеся в результате ассоциации противоположно заряженных ионов, при этом характер связи колеблется от ионной (электростатической) до ковалентной. Реакции с органическими реагентами используются для следующих целей:
Применение диэтилдитиокарбаминовой кислотыи её солей Диэтилдитиокарбаминовая кислота – соединение, неустойчивое в водных растворах, поэтому в аналитической практике используют её соли, натриевая, аммониевая, свинцовая. Эти реагенты образуют более чем с 20 металлами внутрикомплексные соединения – диэтилдитиокарбаминаты (ДДТК металлов). В большинстве случаев они используются для целей селективной экстракции катионов из минерализата. Свойства ДДТК металлов
4 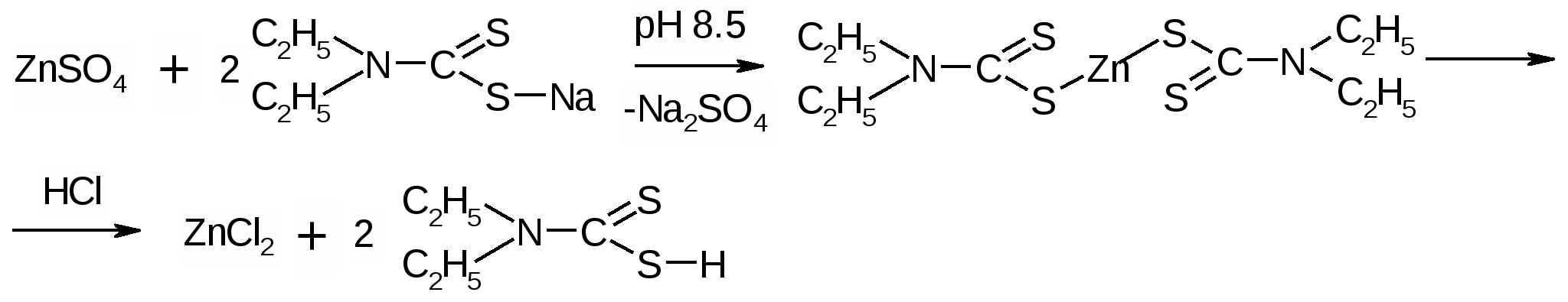 . Устойчивость ДДТК металлов также связана с рН среды. Те комплексы, которые образуются в щелочной среде – неустойчивы в кислой и разрушаются под действием кислот. Это свойство используется для реэкстракции металлов из их комплексов и переведения в водную фазу с целью проведения подтверждающих реакций. Например, ДДТК цинка и кадмия можно разрушить действием хлористоводородной кислоты, а ДДТК висмута – азотной. 5.Для тех ДДТК металлов, которые устойчивы в широком интервале рН (медь), выделение катиона в водную фазу основано на использовании правила рядов среди диэтилдитиокарбаминатов. Согласно этому правилу каждый предшествующий катион, находящийся в водной фазе, вытесняет последующие катионы из их комплексов, растворенных в хлороформе. Ряд ДДТК токсикологически важных катионов можно представить следующим образом: Hg > Ag > Cu > Ni > Co > Pb > Bi > Cd > Tl > Sb > Zn > Mn > Fe Например, Hg2+ способна вытеснять Cu из (ДДТК)2Cu, в свою очередь Cu2+ вытесняет Pb из (ДДТК)2Pb. 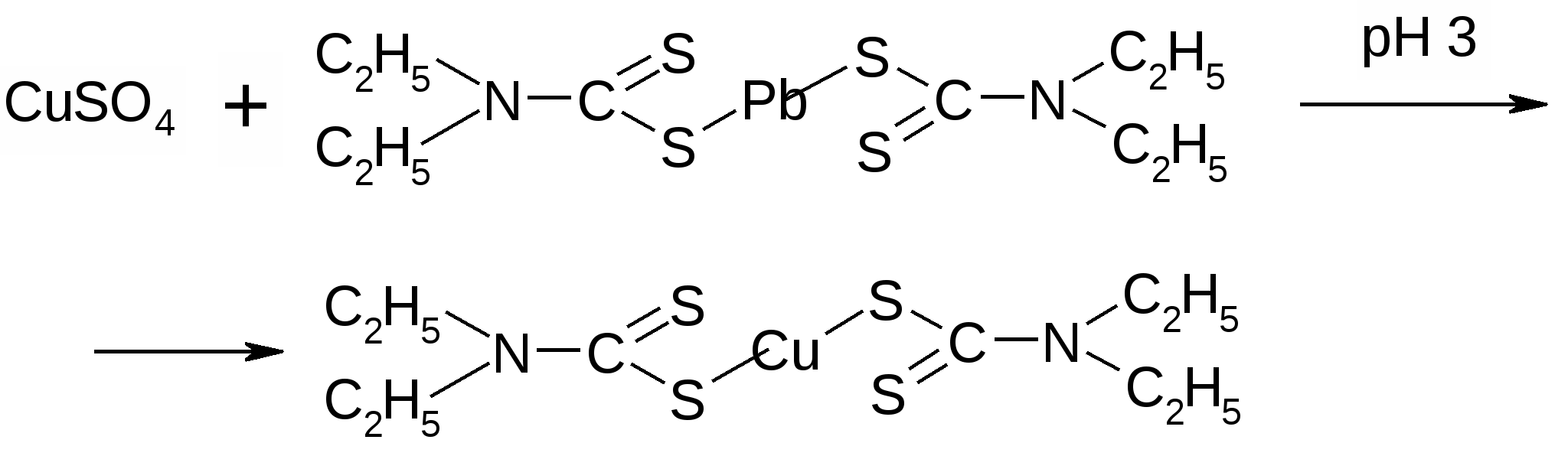 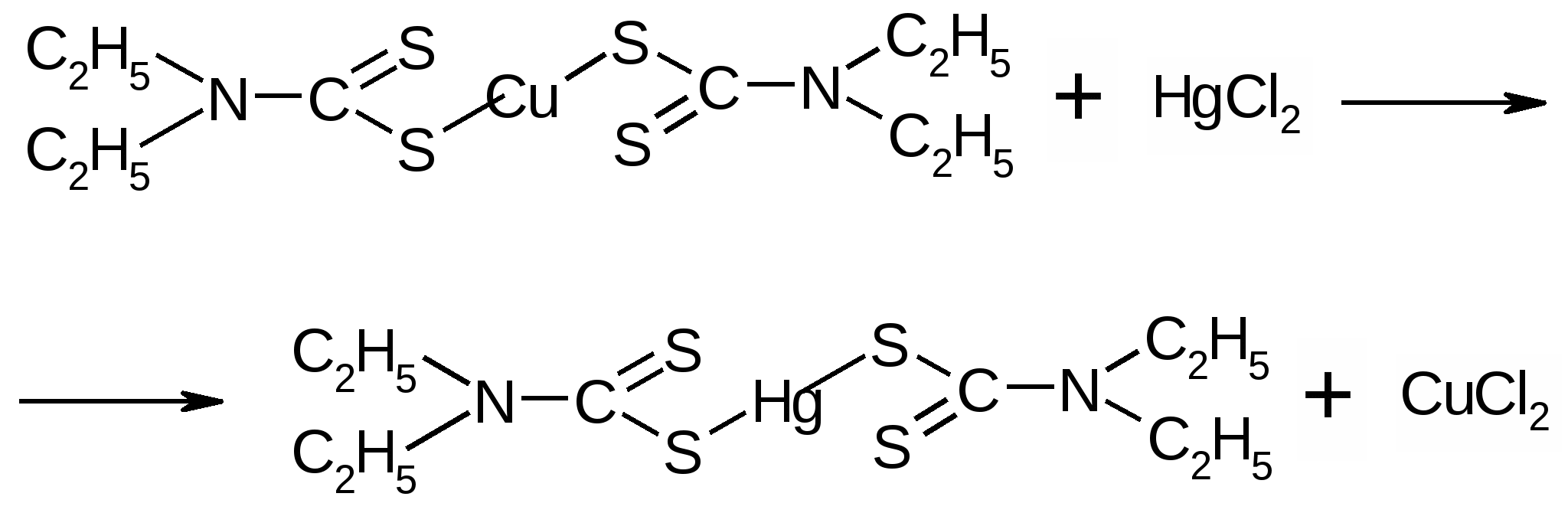 Катионы цинка, кадмия, висмута и меди называют экстракционными катионами и их анализ проводят по следующей схеме:
|
