М.И.Кузин. Хирургические болезни. Литература для студентов медицинских вузов Хирургические болезни Под редакцией
 Скачать 10.27 Mb. Скачать 10.27 Mb.
|
28.8. Пересадка сердце—легкиеНекоторые пациенты одновременно нуждаются в пересадке сердца и легких в связи с тяжелым заболеванием обоих органов. В последние годы сделаны успешные операции одновременной пересадки сердца и легких. Успешная трансплантация этих органов единым комплексом была разработана Reitz и сотрудниками. Метод постепенно внедряется в клиники. Основное препятствие — недостаток подходящих доноров. Показания к пересадке сердца и легких: 1) первичная легочная гипертензия, синдром Эйзенменгера, 2) кистозный фиброз легких, 3) дефицит а, -антитрипсина. Выбор донора. Донор по размерам, по возможности, должен соответствовать реципиенту или быть немного меньше, иметь здоровые легкие (по данным рентгенологического исследования), нормальные показатели по газообмену. Естественно, донор должен соответствовать реципиенту по группе крови и по гистосовместимости. Выбор реципиента. Возраст — не старше 50 лет. В качестве реципиента выбирают пациентов с заболеванием сосудов легких или паренхимы в сочетании с конечной стадией декомпенсации сердца. У реципиента не должно быть необратимых заболеваний или дисфункции других органов и ранее перенесенных торакотомии или стернотомии. Операцию начинают так же, как при пересадке сердца. Легкие удаляют поодиночке с помощью сшивающего аппарата, накладываемого на корень легкого. Затем мобилизуют трахею с проксимальными культями бронхов и пересекают ее над кариной. После удаления легких и сердца реципиента подготовленный консервированный трансплантат помещают в грудную полость реципиента и последовательно соединяют швами. Сначала накладывается анастомоз на трахею (бронх при односторонней пересадке), после создания которого легкие начинают вентилировать. Затем накладывают анастомозы между аортой донора и правым предсердием. Выживаемость после успешной трансплантации сердца и легких такая же, как при пересадке сердца. Иммуносупрессию проводят по тем же правилам. Возможные осложнения — реакция отторжения, кровотечение, обтурирующий бронхолитиаз, который сдерживает широкое распространение метода. 28.9. Трансплантация печениЭто одна из наиболее сложных и длительных операций, тем не менее она стала часто применяться в специальных центрах пересадки органов. Показанием к пересадке печени является терминальная стадия развития цирроза печени, вызванного неумеренным употреблением алкоголя, гепатитом С или В, аутоиммунным гепатитом. Часто показанием к операции является первичная холестатическая болезнь печени, фульминантная печеночная недостаточность, атрезия желчных путей. Значительно реже трансплантацию печени производят при доброкачественных и злокачественных опухолях, у детей — при атрезии желчных путей и некоторых метаболических заболеваниях (рис. 28.3). Выбор реципиента. Успешность трансплантации печени зависит от корректного выбора реципиента. Главным является состояние его здоровья к моменту пересадки, способность перенести тяжелую операцию. Реципиент не должен иметь других тяжелых заболеваний в конечной фазе их развития. За 6 мес до операции больной не должен употреблять алкоголя и наркотиков. Операция не показана при наличии внепеченочного онкологического заболевания и не поддающейся излечению инфекции. 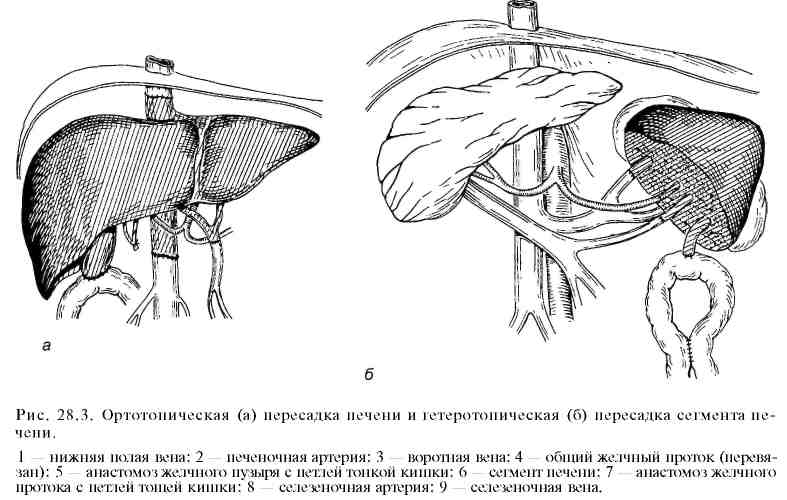 Кандидат на пересадку печени должен быть тщательно обследован специалистами разных областей медицины, включая психиатра. До операции необходимо провести лечение имеющихся заболеваний, которые могут повлиять на успешность трансплантации. Выбор донора. Пересаженная печень должна немедленно выполнять свою синтетическую функцию. В противном случае наступит смерть в ближайшие 72 ч, так как для поддержания ее функции нет никаких устройств, подобных искусственной почке. Нефункционирующую после трансплантации печень удаляют и производят повторную пересадку. Только здоровая печень донора способна выполнять свою функцию сразу после пересадки. Печень необходимо брать у донора с мозговой смертью и нормально функционирующим сердцем. Трансплантат должен по размерам соответствовать или быть немного меньше печени реципиента. При значительной величине печени донора предпочтение отдают пересадке левой доли (2, 3, иногда 4 сегмента) печени. Трансплантат считается малопригодным, если при биопсии выявляется, что 40% и более паренхимы печени замещено жиром. Пробы на совместимость органов донора и реципиента при трансплантации печени отличаются от тех проб, которые обычно проводят при пересадке почек и сердца. Проба на совместимость по HLA-антигенам не имеет того значения, как при пересадке почки, сердца, поджелудочной железы. HLA-антигены имеют физиологическое свойство представлять вирусные пептиды Т-лимфоцитам для начала процесса деструкции клеток, зараженных вирусом. Таким образом, HLA-совместимость будет потенцировать воспаление при наличии у реципиента вирусной инфекции или аутоиммунного процесса, увеличивать шанс рецидива указанных заболеваний. Не производят и перекрестную цитолитическую пробу с лимфоцитами для прогнозирования возможности развития сверхострой реакции отторжения, так как корреляция между результатами перекрестной пробы и реакцией отторжения печени минимальная. Вместе с тем сверхострая реакция отторжения изредка наблюдается даже при обнаружении у реципиента преформированных антител против HLA донорских тканей и отсутствии совместимости по АВО антигенам. Пробу на совместимость по АВО-антигенам проводят обычно при плановой трансплантации, В экстренных случаях иногда пересаживают даже несовместимую по АВО-антигенам печень. Пятилетняя выживаемость пациентов после такой пересадки на 15% хуже, чем при пересадке АВО совместимых органов. Отмечено также, что пересаженная печень от донора женского пола мужчине приживает хуже мужской донорской печени. Острое отторжение, так же как и при пересадке других органов, осуществляется с помощь сложной реакции деструкции печени при участии Т-лимфоцитов. Без иммуносупрессии избежать такой реакции невозможно. Для Т-лимфоцитов первичной мишенью для распознавания HLA-антигенов являются антигены, расположенные на поверхности клеток желчных протоков и эндотелия сосудов. Острая реакция отторжения печени похожа на таковую после пересадки почки и сердца. Она возникает через 6 мес, но часто развивается в течение 4 нед после пересадки. Симптомы отторжения неспецифичны. Они проявляются слабостью, повышением температуры, ухудшением функциональных печеночных тестов — повышением в крови билирубина, щелочной фосфатазы, трансаминаз, клиническими симптомами печеночной недостаточности. Диагноз подтверждается с помощью биопсии печени. Хроническое отторжение происходит в период от нескольких месяцев до нескольких лет. Иммуносупрессивную терапию проводят по общим правилам, подбирая препараты различного механизма действия. Существует несколько схем (протоколов) иммуносупрессии, что позволяет выбирать наиболее подходящую из них. Возникающие после трансплантации печени осложнения разделяют на 4 степени тяжести. Для лечения каждой из них предусмотрена соответствующая схема лечения. Выживаемость после операции составляет 90%. Выживаемость в течение одного года равна 73%, в течение 5 лет приблизительно 60%. Реципиенты нуждаются в постоянном наблюдении и контроле. Применяют в основном ортотопическую, реже гетеротопическую трансплантации (см. рис. 28.3). При ортотопической трансплантации печень реципиента удаляют, а на ее место пересаживают аллогенную печень донора. При этом соединяют выделенные кровеносные сосуды печени донора с нижней полой веной, воротной веной и печеночной артерией реципиента. Желчный проток донорской печени соединяют анастомозом с выключенной по Ру петлей тощей кишки реципиента. При гетеротопической трансплантации печень реципиента не удаляют. Поскольку удаление нескольких сегментов левой доли печени стало безопасным, некоторые центры отдают предпочтение пересадке левой доли (2—3, иногда 4 сегмента) печени от живого родственного донора, соединяя сосуды трансплантируемой части печени с сосудами селезенки реципиента, а желчный проток — с выключенной по Ру петлей тощей кишки. Это вмешательство менее сложно, дает отличное приживление трансплантата и отличные функциональные результаты вследствие лучшей гистосовместимо-сти и уменьшения времени ишемии пересаживаемого органа. Сложными являются этические проблемы. Ради жизни ребенка мать часто пойдет на риск для собственного здоровья. В связи с улучшением иммунодепрессив-ной терапии многие специалисты считают взятие левой доли печени у живого родственного донора неоправданным риском, поскольку левая доля печени донора с мозговой смертью может дать столь же хорошие конечные результаты. |
