|
|
Материаловедение
9
Железоуглеродистые сплавы. Диаграмма состояния железо – углерод.
Структуры железоуглеродистых сплавов
Компоненты и фазы железоуглеродистых сплавов
Процессы при структурообразовании железоуглеродистых сплавов
Структуры железоуглеродистых сплавов
Структуры железоуглеродистых сплавов
Железоуглеродистые сплавы – стали и чугуны – важнейшие металлические сплавы современной техники. Производство чугуна и стали по объему превосходит производство всех других металлов вместе взятых более чем в десять раз.
Диаграмма состояния железо – углерод дает основное представление о строении железоуглеродистых сплавов – сталей и чугунов.
Начало изучению диаграммы железо – углерод положил Чернов Д.К. в 1868 году. Чернов впервые указал на существование в стали критических точек и на зависимость их положения от содержания углерода.
Диаграмма железо – углерод должна распространяться от железа до углерода. Железо образует с углеродом химическое соединение: цементит – . Каждое устойчивое химическое соединение можно рассматривать как компонент, а диаграмму – по частям. Так как на практике применяют металлические сплавы с содержанием углерода до , то рассматриваем часть диаграммы состояния от железа до химического соединения цементита, содержащего углерода.
Диаграмма состояния железо – цементит представлена на рис. 9.1.
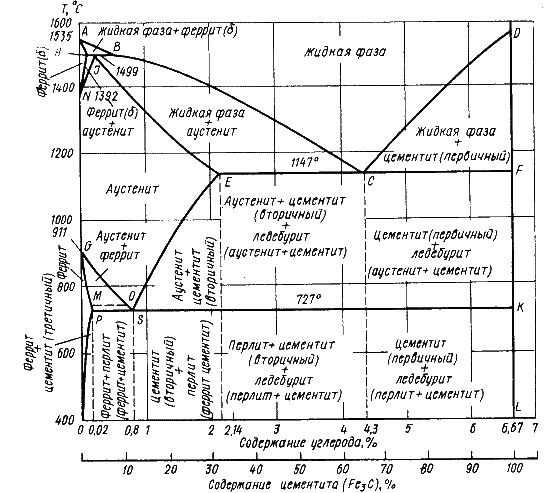
Рис. 9.1. Диаграмма состояния железо - цементит
Компоненты и фазы железоуглеродистых сплавов
Компонентами железоуглеродистых сплавов являются железо, углерод и цементит.
1. Железо – переходный металл серебристо-светлого цвета. Имеет высокую температуру плавления – 1539o С5o С.
В твердом состоянии железо может находиться в двух модификациях. Полиморфные превращения происходят при температурах 911o С и 1392o С. При температуре ниже 911o С существует с объемно-центрированной кубической решеткой. В интервале температур 911…1392o С устойчивым является с гранецентрированной кубической решеткой. Выше 1392o С железо имеет объемно-центрированную кубическую решетку и называется или высокотемпературное . Высокотемпературная модификация не представляет собой новой аллотропической формы. Критическую температуру 911oС превращения обозначают точкой , а температуру 1392o С превращения - точкой А4.
При температуре ниже 768o С железо ферромагнитно, а выше – парамагнитно. Точка Кюри железа 768o С обозначается А2.
Железо технической чистоты обладает невысокой твердостью (80 НВ) и прочностью (предел прочности – , предел текучести –) и высокими характеристиками пластичности (относительное удлинение – , а относительное сужение – ). Свойства могут изменяться в некоторых пределах в зависимости от величины зерна.
Железо характеризуется высоким модулем упругости, наличие которого проявляется и в сплавах на его основе, обеспечивая высокую жесткость деталей из этих сплавов.
Железо со многими элементами образует растворы: с металлами – растворы замещения, с углеродом, азотом и водородом – растворы внедрения.
2. Углерод относится к неметаллам. Обладает полиморфным превращением, в зависимости от условий образования существует в форме графита с гексагональной кристаллической решеткой (температура плавления – 3500 0С, плотность – 2,5 г/см3) или в форме алмаза со сложной кубической решеткой с координационным числом равным четырем (температура плавления – 5000 0С).
В сплавах железа с углеродом углерод находится в состоянии твердого раствора с железом и в виде химического соединения – цементита (Fe3C), а также в свободном состоянии в виде графита (в серых чугунах).
3. Цементит (Fe3C) – химическое соединение железа с углеродом (карбид железа), содержит 6,67 % углерода.
Аллотропических превращений не испытывает. Кристаллическая решетка цементита состоит из ряда октаэдров, оси которых наклонены друг к другу.
Температура плавления цементита точно не установлена (1250, 1550o С). При низких температурах цементит слабо ферромагнитен, магнитные свойства теряет при температуре около 217o С.
Цементит имеет высокую твердость (более 800 НВ, легко царапает стекло), но чрезвычайно низкую, практически нулевую, пластичность. Такие свойства являются следствием сложного строения кристаллической решетки.
Цементит способен образовывать твердые растворы замещения. Атомы углерода могут замещаться атомами неметаллов: азотом, кислородом; атомы железа – металлами: марганцем, хромом, вольфрамом и др. Такой твердый раствор на базе решетки цементита называется легированным цементитом.
Цементит – соединение неустойчивое и при определенных условиях распадается с образованием свободного углерода в виде графита. Этот процесс имеет важное практическое значение при структурообразовании чугунов.
В системе железо – углерод существуют следующие фазы: жидкая фаза, феррит, аустенит, цементит.
1. Жидкая фаза. В жидком состоянии железо хорошо растворяет углерод в любых пропорциях с образованием однородной жидкой фазы.
2. Феррит (Ф) (C) – твердый раствор внедрения углерода в -железо.
Феррит имеет переменную предельную растворимость углерода: минимальную – 0,006 % при комнатной температуре (точка Q), максимальную – 0,02 % при температуре 727o С ( точка P). Углерод располагается в дефектах решетки.
При температуре выше 1392o С существует высокотемпературный феррит () ((C), с предельной растворимостью углерода 0,1 % при температуре 1499o С (точка J)
Свойства феррита близки к свойствам железа. Он мягок (твердость – 130 НВ, предел прочности –) и пластичен (относительное удлинение –), магнитен до 768o С.
3. Аустенит (А) (С) – твердый раствор внедрения углерода в -железо.
Углерод занимает место в центре гранецентрированной кубической ячейки.
Аустенит имеет переменную предельную растворимость углерода: минимальную – 0,8 % при температуре 727o С (точка S), максимальную – 2,14 % при температуре 1147o С (точка Е).
Аустенит имеет твердость 200…250 НВ, пластичен (относительное удлинение – ), парамагнитен.
При растворении в аустените других элементов могут изменяться свойства и температурные границы существования.
4. Цементит – характеристика дана выше.
В железоуглеродистых сплавах присутствуют фазы: цементит первичный (ЦI), цементит вторичный (ЦII), цементит третичный (ЦIII). Химические и физические свойства этих фаз одинаковы. Влияние на механические свойства сплавов оказывает различие в размерах, количестве и расположении этих выделений. Цементит первичный выделяется из жидкой фазы в виде крупных пластинчатых кристаллов. Цементит вторичный выделяется из аустенита и располагается в виде сетки вокруг зерен аустенита (при охлаждении – вокруг зерен перлита). Цементит третичный выделяется из феррита и в виде мелких включений располагается у границ ферритных зерен.
Процессы при структурообразовании железоуглеродистых сплавов
Линия АВСD – ликвидус системы. На участке АВ начинается кристаллизация феррита (), на участке ВС начинается кристаллизация аустенита, на участке СD – кристаллизация цементита первичного.
Линия AHJECF – линия солидус. На участке АН заканчивается кристаллизация феррита (). На линии HJB при постоянной температуре 14990С идет перетектическое превращение, заключающееся в том, что жидкая фаза реагирует с ранее образовавшимися кристаллами феррита (), в результате чего образуется аустенит:
На участке JЕ заканчивается кристаллизация аустенита. На участке ECF при постоянной температуре 1147o С идет эвтектическое превращение, заключающееся в том, что жидкость, содержащая 4,3 % углерода превращается в эвтектическую смесь аустенита и цементита первичного:
Эвтектика системы железо – цементит называется ледебуритом (Л), по имени немецкого ученого Ледебура, содержит 4,3 % углерода.
При температуре ниже 727o С в состав ледебурита входят цементит первичный и перлит, его называют ледебурит превращенный (ЛП).
По линии HN начинается превращение феррита () в аустенит, обусловленное полиморфным превращением железа. По линии NJ превращение феррита () в аустенит заканчивается.
По линии GS превращение аустенита в феррит, обусловленное полиморфным превращением железа. По линии PG превращение аустенита в феррит заканчивается.
По линии ES начинается выделение цементита вторичного из аустенита, обусловленное снижением растворимости углерода в аустените при понижении температуры.
По линии МО при постоянной температуре 768o С имеют место магнитные превращения.
По линии PSK при постоянной температуре 727o С идет эвтектоидное превращение, заключающееся в том, что аустенит, содержащий 0,8 % углерода, превращается в эвтектоидную смесь феррита и цементита вторичного:
По механизму данное превращение похоже на эвтектическое, но протекает в твердом состоянии.
Эвтектоид системы железо – цементит называется перлитом (П), содержит 0,8 % углерода.
Название получил за то, что на полированном и протравленном шлифе наблюдается перламутровый блеск.
Перлит может существовать в зернистой и пластинчатой форме, в зависимости от условий образования.
По линии PQ начинается выделение цементита третичного из феррита, обусловленное снижением растворимости углерода в феррите при понижении температуры.
Температуры, при которых происходят фазовые и структурные превращения в сплавах системы железо – цементит, т.е. критические точки, имеют условные обозначения.
Обозначаются буквой А (от французского arret – остановка):
А1 – линия PSK (7270С) – превращение П А;
A2 – линия MO (7680С, т. Кюри) – магнитные превращения;
A3 – линия GOS ( переменная температура, зависящая от содержания углерода в сплаве) – превращение Ф А;
A4 – линия NJ (переменная температура, зависящая от содержания углерода в сплаве) – превращение ;
Acm – линия SE (переменная температура, зависящая от содержания углерода в сплаве) – начало выделения цементита вторичного (иногда обозначается A3).
Так как при нагреве и охлаждении превращения совершаются при различных температурах, чтобы отличить эти процессы вводятся дополнительные обозначения. При нагреве добавляют букву с, т.е , при охлаждении – букву r, т.е. .
Структуры железоуглеродистых сплавов
Все сплавы системы железо – цементит по структурному признаку делят на две большие группы: стали и чугуны.
Особую группу составляют сплавы с содержанием углерода менее 0,02% (точка Р), их называют техническое железо. Микроструктуры сплавов представлены на рис.9.2. Структура таких сплавов после окончания кристаллизации состоит или из зерен феррита (рис.9.2 а), при содержании углерода менее 0,006 %, или из зерен феррита и кристаллов цементита третичного, расположенных по границам зерен феррита (рис.9.2.б), если содержание углерода от 0,006 до 0,02 %.
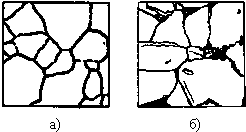
Рис.9.2. Микроструктуры технического железа: а – содержание углерода менее 0,006%; б – содержание углерода 0,006…0,02 %
Углеродистыми сталями называют сплавы железа с углеродом, содержащие 0,02…2,14 % углерода, заканчивающие кристаллизацию образованием аустенита.
Они обладают высокой пластичностью, особенно в аустенитном состоянии.
Структура сталей формируется в результате перекристаллизации аустенита. Микроструктуры сталей представлены на рис. 9.3.

Рис. 9.3. Микроструктуры сталей: а – доэвтектоидная сталь ; б – эвтектоидная сталь (пластинчатый перлит); в – эвтектоидная сталь (зернистый перлит); г – заэвтектоидная сталь .
По содержанию углерода и по структуре стали подразделяются на доэвтектоидные , структура феррит + перлит (рис.9.3 а); эвтектоидные , структура перлит (П), перлит может быть пластинчатый или зернистый (рис. 9.3 б и 9.3 в); заэвтектоидные, структура перлит + цементит вторичный (П + ЦII), цементитная сетка располагается вокруг зерен перлита.
По микроструктуре сплавов можно приблизительно определить количество углерода в составе сплава, учитывая следующее: количество углерода в перлите составляет 0,8 %, в цементите – 6,67 %. Ввиду малой ратворимости углерода в феррите, принимается, что в нем углерода нет.
Сплавы железа с углеродом, содержащие углерода более 2,14 % (до 6,67 %), заканчивающие кристаллизацию образованием эвтектики (ледебурита), называют чугунами.
Наличие легкоплавкого ледебурита в структуре чугунов повышает их литейные свойства.
Чугуны, кристаллизующиеся в соответствии с диаграммой состояния железо – цементит, отличаются высокой хрупкостью. Цвет их излома – серебристо-белый. Такие чугуны называются белыми чугунами.
Микроструктуры белых чугунов представлены на рис. 9.4.

Рис. 9.4. Микроструктуры белых чугунов: а – доэвтектический белый чугун; б – эвтектический белый чугун (Л); в – заэвтектический белый чугун .
По количеству углерода и по структуре белые чугуны подразделяются на: доэвтектические , структура перлит + ледебурит + цементит вторичный ; эвтектические , структура ледебурит (Л) (рис. 9.4 б); заэвтектические , структура ледебурит + цементит первичный (рис. 9.4 в).
В структуре доэвтектических белых чугунов присутствует цементит вторичный, который образуется в результате изменения состава аустенита при охлаждении (по линии ES). В структуре цементит вторичный сливается с цементитом, входящим в состав ледебурита.
Фазовый состав сталей и чугунов при нормальных температурах один и тот же, они состоят из феррита и цементита. Однако свойства сталей и белых чугунов значительно различаются. Таким образом, основным фактором, определяющим свойства сплавов системы железо – цементит является их структура.
10
Стали. Классификация и маркировка сталей.
Влияние углерода и примесей на свойства сталей
Влияние углерода.
Влияние примесей.
Назначение легирующих элементов.
Распределение легирующих элементов в стали.
Классификация и маркировка сталей
Классификация сталей
Маркировка сталей
Углеродистые стали обыкновенного качества (ГОСТ 380).
Качественные углеродистые стали
Качественные и высококачественные легированные стали
Легированные конструкционные стали
Легированные инструментальные стали
Быстрорежущие инструментальные стали
Шарикоподшипниковые стали
Стали являются наиболее распространенными материалами. Обладают хорошими технологическими свойствами. Изделия получают в результате обработки давлением и резанием.
Достоинством является возможность, получать нужный комплекс свойств, изменяя состав и вид обработки. Стали, подразделяют на углеродистые и легированные.
Влияние углерода и примесей на свойства сталей
Углеродистые стали являются основными. Их свойства определяются количеством углерода и содержанием примесей, которые взаимодействуют с железом и углеродом.
Влияние углерода.
Влияние углерода на свойства сталей показано на рис. 10.1
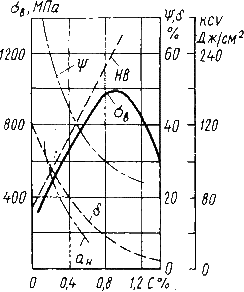
Рис.10.1. Влияние углерода на свойства сталей
С ростом содержания углерода в структуре стали увеличивается количество цементита, при одновременном снижении доли феррита. Изменение соотношения между составляющими приводит к уменьшению пластичности, а также к повышению прочности и твердости. Прочность повышается до содержания углерода около 1%, а затем она уменьшается, так как образуется грубая сетка цементита вторичного.
Углерод влияет на вязкие свойства. Увеличение содержания углерода повышает порог хладоломкости и снижает ударную вязкость.
Повышаются электросопротивление и коэрцитивная сила, снижаются магнитная проницаемость и плотность магнитной индукции.
Углерод оказывает влияние и на технологические свойства. Повышение содержания углерода ухудшает литейные свойства стали (используются стали с содержанием углерода до 0,4 %), обрабатываемость давлением и резанием, свариваемость. Следует учитывать, что стали с низким содержанием углерода также плохо обрабатываются резанием.
Влияние примесей.
В сталях всегда присутствуют примеси, которые делятся на четыре группы. 1.Постоянные примеси: кремний, марганец, сера, фосфор.
Марганец и кремний вводятся в процессе выплавки стали для раскисления, они являются технологическими примесями.
Содержание марганца не превышает 0,5…0,8 %. Марганец повышает прочность, не снижая пластичности, и резко снижает красноломкость стали, вызванную влиянием серы. Он способствует уменьшению содержания сульфида железа FeS, так как образует с серой соединение сульфид марганца MnS. Частицы сульфида марганца располагаются в виде отдельных включений, которые деформируются и оказываются вытянутыми вдоль направления прокатки.
Содержание кремния не превышает 0,35…0,4 %. Кремний, дегазируя металл, повышает плотность слитка. Кремний растворяется в феррите и повышает прочность стали, особенно повышается предел текучести, . Но наблюдается некоторое снижение пластичности, что снижает способность стали к вытяжке
Содержание фосфора в стали 0,025…0,045 %. Фосфор, растворяясь в феррите, искажает кристаллическую решетку и увеличивает предел прочности и предел текучести , но снижает пластичность и вязкость.
Располагаясь вблизи зерен, увеличивает температуру перехода в хрупкое состояние, вызывает хладоломкость, уменьшает работу распространения трещин, Повышение содержания фосфора на каждую 0,01 % повышает порог хладоломкости на 20…25oС.
Фосфор обладает склонностью к ликвации, поэтому в центре слитка отдельные участки имеют резко пониженную вязкость.
Для некоторых сталей возможно увеличение содержания фосфора до 0,10…0,15 %, для улучшения обрабатываемости резанием.
S – уменьшается пластичность, свариваемость и коррозионная стойкость. Р–искажает кристаллическую решетку.
Содержание серы в сталях составляет 0,025…0,06 %. Сера – вредная примесь, попадает в сталь из чугуна. При взаимодействии с железом образует химическое соединение – сульфид серы FeS, которое, в свою очередь, образует с железом легкоплавкую эвтектику с температурой плавления 988oС. При нагреве под прокатку или ковку эвтектика плавится, нарушаются связи между зернами. При деформации в местах расположения эвтектики возникают надрывы и трещины, заготовка разрушается – явление красноломкости.
Красноломкость – повышение хрупкости при высоких температурах
Сера снижает механические свойства, особенно ударную вязкость аи пластичность (и ), а так же предел выносливости. Она ухудшают свариваемость и коррозионную стойкость.
2. Скрытые примеси - газы (азот, кислород, водород) – попадают в сталь при выплавке.
Азот и кислород находятся в стали в виде хрупких неметаллических включений: окислов (FeO, SiO2, Al2O3 ) нитридов (Fe 2N), в виде твердого раствора или в свободном состоянии, располагаясь в дефектах (раковинах, трещинах).
Примеси внедрения (азот N, кислород О) повышают порог хладоломкости и снижают сопротивление хрупкому разрушению. Неметаллические включения (окислы, нитриды), являясь концентраторами напряжений, могут значительно понизить предел выносливости и вязкость.
Очень вредным является растворенный в стали водород, который значительно охрупчивает сталь. Он приводит к образованию в катанных заготовках и поковках флокенов.
Флокены – тонкие трещины овальной или округлой формы, имеющие в изломе вид пятен – хлопьев серебристого цвета.
Металл с флокенами нельзя использовать в промышленности, при сварке образуются холодные трещины в наплавленном и основном металле.
Если водород находится в поверхностном слое, то он удаляется в результате нагрева при 150…180, лучше в вакууме мм рт. ст.
Для удаления скрытых примесей используют вакуумирование.
3. Специальные примеси – специально вводятся в сталь для получения заданных свойств. Примеси называются легирующими элементами, а стали - легированные сталями.
Назначение легирующих элементов.
Основным легирующим элементом является хром (0,8…1,2)%. Он повышает прокаливаемость, способствует получению высокой и равномерной твердости стали. Порог хладоломкости хромистых сталей - (0…-100)oС.
Дополнительные легирующие элементы.
Бор - 0.003%. Увеличивает прокаливаемость, а такхе повышает порог хладоломкости (+20…-60 oС.
Марганец – увеличивает прокаливаемость, однако содействует росту зерна, и повышает порог хладоломкости до (+40…-60)oС.
Титан (
0,1%) вводят для измельчения зерна в хромомарганцевой стали.
Введение молибдена (0,15…0,46%) в хромистые стали увеличивает прокаливаемость, снихает порог хладоломкости до –20…-120oС. Молибден увеличивает статическую, динамическую и усталостную прочность стали, устраняет склонность к внутреннему окислению. Кроме того, молибден снижает склонность к отпускной хрупкости сталей, содержащих никель.
Ванадий в количестве (0.1…0.3) % в хромистых сталях измельчает зерно и повышает прочность и вязкость.
Введение в хромистые стали никеля, значительно повышает прочность и прокаливаемость, понижает порог хладоломкости, но при этом повышает склонность к отпускной хрупкости (этот недостаток компенсируется введением в сталь молибдена). Хромоникелевые стали, обладают наилучшим комплексом свойств. Однако никель является дефицитным, и применение таких сталей ограничено.
Значительное количество никеля можно заменить медью, это не приводит к снижению вязкости.
При легировании хромомарганцевых сталей кремнием получают, стали – хромансиль (20ХГС, 30ХГСА). Стали обладают хорошим сочетанием прочности и вязкости, хорошо свариваются, штампуются и обрабатываются резанием.Кремний повышает ударную вязкость и температурный запас вязкости.
Добавка свинца, кальция – улучшает обрабатываемость резанием. Применение упрочнения термической обработки улучшает комплекс механических свойств.
Распределение легирующих элементов в стали.
Легирующие элементы растворяются в основных фазах железоуглеродистых сплавов ( феррит, аустенит, цементит), или образуют специальные карбиды.
Растворение легирующих элементов в происходит в результате замещения атомов железа атомами этих элементов. Эти амомы создают в решетке напряжения, которые вызывают изменение ее периода.
Изменение размеров решетки вызывает изменение свойств феррита – прочность повышается, пластичность уменьшается. Хром, молибден и вольфрам упрочняют меньше, чем никель, кремний и марганец. Молибден и вольфрам, а твкже кремний и марганец в определенных количествах, снижают вязкость.
В сталях карбиды образуются металлами, расположенными в таблице Менделеева левее железа (хром, ванадий, титан), которые имеют менее достроенную d – электронную полосу.
В процессе карбидообразования углерод отдает свои валентные электроны на заполнение d – электронной полосы атома металла, тогда как у металла валентные электроны образуют металлическую связь, обуславливающую металлические свойства карбидов.
При соотношении атомных радиусов углерода и металла более 0,59 образуются типичные химические соединения: Fe3C, Mn3C, Cr23C6, Cr7C3, Fe3W3C – которые имеют сложную кристаллическую решетку и при нагреве растворяются в аустените.
При соотношении атомных радиусов углерода и металла менее 0,59 образуются фазы внедрения: Mo2C, WC, VC, TiC, TaC, W2C – которые имеют простую кристаллическую решетку и трудно растворяются в аустените.
Все карбиды обладают высокой твердостью и температурой плавления.
4. Случайные примеси.
|
|
|
 Скачать 1.75 Mb.
Скачать 1.75 Mb.