курстык жумыс. Мазмны 1 Кондуктометрияны теориялы негізі 2 Кондуктометрлік дістердін жіктелуі 3 Кондуктометрлік титрлеу
 Скачать 233.24 Kb. Скачать 233.24 Kb.
|
|
Мазмұны 1 Кондуктометрияның теориялық негізі 2 Кондуктометрлік әдістердін жіктелуі 3 Кондуктометрлік титрлеу 4 Қышқыл мен негіздің өзара әсерлесу реакциялары 5 Қолдаланған әдебиеттер Кондуктометрия Кондуктометрия Электролиттердің концентрациясын кондуктометрлік әдіспен анықтау талданатын ерітіндінің электр өткізгіштігін елшеуге негізделген. Кондуктометрия - ең қарапайым және талдап сұрыптаудын электрохимиялық әдісі. Кондуктометрлік әдістердің барлығы жылдамдығымен, өлшеуіш аспаптарының оңай табылуымен, жұмысының ыңғайлылығымен, қанағаттанарлық дәлдігімен, өндірістік, технологиялық және лабораториялык жағдайларда талдауды автоматты түрде, әрі қашықтықған жүргізу мүмкіндігімен сипатталады. Тікелей кондуктометрлік анықтаудын қателігі - 1-2 %. Ал белгілі бір арнайы жағдайды сақтаганда талдау қателігі 0.2 %-ке дейін азаяды. Кондуктометрлік ұяшықтарды термостатсыз өлшегенде, бұл қателіктер 3 %-ке артады, өйткені температураның бір градусқа жоғарылауы электр өткізгіштікті 2 не 3 проценттей өзгертеді. Демек, ерітінділерді термостаттау кондуктометрлік талдау әдісінің дәлдігін арттырады. Кондуктометрияның теориялық негізі Кондуктометрияның теориялық негізі Электролит ерітінділерінің электр өткізгіштігі - осы ерігіндінің кедергісіне кері шама, әрі ол сыртқы электр өрісінің әсерінен еріген заттыіі электр тогын өткізу қабілетіне байланысты. Ендеше бүл эдіс электрдің негізгі заңдарының бірі Ом заңына бағынады: I = Е / R мұндағы I - ток күші, Е - потенциал айырымы, R - кедергі. Кондукгометрияда өлшенетін шама ерітіндінің кедергісі немесе электр өткізгіштігі болуы мүмкін. Электр өткізгіштігінің бірлігі - кедергісі 1 Ом өткізгіштің өткізгіштік қабілеті. Электролит ерітіндісінің электр өткізгіштігі - сыртқы кернеу көзі әсерінен заттың электролиттік диссоциациялануы және иондар қозғалуының нәтижесі. Электр тогы өрісінде ерітіндідегі қозғалған иондар еріткіш молекуласы және өзін қоршаған кері зарядталған иондар тарапынан тежеу осеріне ұшырайды. Бұл әсер релаксациялык және электрофореттік эффект деп аталады, ал бұл тежеудің нәтижесі ерітінді кедергісі болып табылады. Сөйтіп, ерітіндінін электр өткізгіштігі негізінен миграциялық иондардың санымен және жылдамдығымен (қозғалғыштығымен), оларды тасымалдайтын заряд санымен анықталады. Электр өткізгіштік температураға және еріген электролит пен еріткіштің табиғатына тәуелді. Электролит арқылы ток өткенде, оң зарядталған болшекіер катодка (теріс зарядталған электродқа), ал теріс зарядталған бөлшектер анодқа (оң зарядталған электродқа) қарай жылжиды. Демек, электролиттегі әрбір зарядталған бөлшек электр өткізгіштік сияқты жалпы процеске қатысады. Электролит ерітіндісі - үш өлшемді өткізгіш. Ал кез келген ерітінді кедергісінің шамасы ұяшықтың құрамына, материалына, шамасына және электродтардың кеңістіктегі орналасуына тәуелді. Барлық белгілі және табиғатта кездесетін немесе қолдан жасалған өткізгішгер олар арқылы электр тогы өткен кездегі электрдің тасымалдану механизміне тәуелділігіне қарай үш топқа бөлінеді : электрондык, иондық, аралас. Элекптрондық өткізгіштер. Мұнда өткізгіштердегі электрді тасымзлдаушылар - электрондар. Электрондық өткізгіштерге металдар, жартылай еткізгіштер, металл құймалары, көміртек және кейбір тұздар мен тотықтар жатады. Иондық өткізгіштер. Мұндағы электр тасымалдауыштар - иондар. Өткізгіштердің бұл тобына газдар мен электролиттер, олардың ерітінділері жатады. Аралас откізгіштер әрі электрондық, әрі иондық қасиетке ие болады. Бұған сұйық аммиактағы сілтілік жер элементтердің ерітінділері, кейбір сұйық (балқыма) құймалар мен тұздар жатады. Мұндай өткізгіштердегі ток өткізу сипаты температураның белгілі бір аралықтарында өзгереді. Электр өткізгіштікті өлшеуге арналған иондық немесе аралас ток өткізгіиі электролштерге мына заттардың типтері жатады: қатты күйдегі таза заттар (күміс, барий, қорғасын және металдардың галогенидтері); сұйық күйдегі заттар (су, спирттер, қышқылдар, т.б.); балқыған тұздар мен гидридтер: қатты және балқыма күйдегі бірнеше заттың ерітіндісі; сулы және сусыз, яғни анорганикалық және органикалық нағыз (молекулалық) және коллоидты ерітінділер; оксидтердің, тұздар мен негіздердің және кейбір жекеленген заттар ерітінділері. Әр түрлі ерітінділердің электр өткізгіштігін салыстыру үшін менілікті электр өткізгіштігін пайдалану қолайлы, ол мына теңдеумен беріледі: {\displaystyle X={\frac {1}{RS}}}  мұндағы I - ұзындығы өгкізгіштің көлденең кимасының ауданы. Менпіікті электр өткізгіштік дегеніміз - ауданы 1 м2, ара қашықтығы 1 м болатын өзара параллель орналасқан екі электрод арасындағы 1 м3 ерітіндінің өткізгіштігі. Меншікті (к), эквивалентті (λ) және мольдік А электр өткізгіштік деп бөлінеді, соңғысында ерітіндінің меншікті электр өткізгіштігі оның мольдік концентрациясымен анықталады. Жалпы электр өгкізгіштік электр тасымалдау процесіне қатынасатын әрбір ионның концентрация және ұяшық сияқты параметрлері арқылы өрнектеледі: 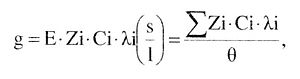 Шексіз сұйылтқандағы катиондар мен аниондардың ионды эквиваленттік электр өткізгіштігі (25° С) Меншікті электр өткізгіштік ерітіндінің концентрациясы өскен сайын артып, өзінін ең жоғарғы шегіне жетеді де, содан кейін төмендейді. Ерітіндідегі электролит концентрациясының артуымен меншікті электр өткізгіштігінің артуы ерітіндідегі ион санының көбеюімен байланысты. Концентрацияланған ерітіндіде ионаралық өзара әсерлесу артады да. осының нэтижесінде ионаралық ассоциагтар немесе ион суы пайда болады, ток өткізгіштікті төмендететін ерітіндінің тұтқырлығы көбейеді; нондардың қозғалыс жылдамдықтарын азайтатын басқадай эффектілер туады. Осындай факторлар қосыла келіп, электр өткізгіштіктің қисығында максимум пайда болады. Әдетте аналитикалық мақсат үшін осы қисықтың өсімді учаскесін пайдаланады, яғни ерітіндінщ орташа концентрация аймағы. Алайда, меншікті электр өткізгіштік концентрацияға сандық тұрғыда тым бағынатындықтан, оның орнына эквиваленттік электр откізгіштікті пайдаланған орынды. Сонымен, ерітіндінің эквиваленттік электр өткізгіштігі дегеніміз - беткі ауданы 1 см2, ара қашықтығы 1 см параллель орншіасқан екі электрод арасында, құрамында заттың 1 моль эквиваленті болатын ерітіндінің электр өткізгіштігі, ол см · см2/моль · экв бірлігімен өлшенеді. Әдетте, концентрациясы төмен болатын аймақта А ерітінді концентрациясы азайған сайын өсе түседі. Ал күшті электролитгер үшін, концентрация шамасы < 10−3 моль/л, ол келесі теңдеумен өрнектелінеді: Ерітінді концентрациясының өсуімен эквиваленттік электр өткізгіштіктің төмендеуі Дебай-Хюккель-Онзагер эффектісі бойынша, ион айналасында кері зарядталған иондардан иондық атмосфераның туындауымен және оған байланысты найда болатын электрофоретті релаксациялық тежеу әсерімен түсіндіріледі. Электрофореттік эффекті орталық ион бір бағытта жылжыса, оны қоршаған кері ионның оған қарама-қарсы қозғалуымен байланысты. Ал релаксациялық тежеу ион жылжыған кездегі иондық қоршаудың бұзылып, қайта құрылуымен байланысты. Осы теорияның концентрациялық тәуелділігі мына теңдеумен сипатталады: мұндағы А мен В - электрофореттік және релаксациялық эффектілерді сипаттайтын коэффициенттер, олардың шамасы ерітіндідегі температураға, тұтқырлыққа, диэлектрлікке тэуелді, әрі теориялық тұрғыда есептелінеді. Шекті эквивалентті электр өткізгіштік иондардың шекті электр өткізгіштіктерінің қосындысына (немесе иондардың қозғалғыштығына) тең: Бұл тендеуді Ф. Кодьрауш (1879 жылы) заңы, кейде иондардың тәуелсіз қозғалу заңы дейді. Қалыпты жағдайда су ерітіндісіндегі иондардын қозғалтқыштық мэні 30-70 см · см2/моль әкв. аралығында болады, ал сутек пен гидроксид иондарынікі 350 мен 199 см · см2 моль · экв.-ке тең. Бұл осы иондардың электр өрісінде ерекше қозғалуымен түсіндіріледі. Әлсіз электролиттердің электр өткізгіштігінің концентрациялық тәуелділігі аса күрделі сипат алады. Бұл жоғарыда айтылған эффектілермен қатар, әлсіз электролитті сұйылтқан кезде оның диссоциациялану дәрежесі өсіп, осы сүйытылған ерітінді аймағында оның жылдам артуын туғызатын диссоциациялану дәрежесінің айтарлықтай ықпалымен түсіндіріледі. Әлсіз электролиттің электр өткізгіштігін пайдаланып, оның диссоциация түрақтысын есептейді. Сусыз ерітінділердегі электр өткізгіштіктің бірқатар ерекшеліктері бар. Диэлектрлік өтімділігі жоғары болатын органикалық ерітінділердегі электр өткізгіштігінің конценфацияға тәуелділігі өрнектегідей. Егер диэлектрлік өтімділік аз болса (пириндинде, диоксонда, хинолинде жэне т.б.), онда электр өткізгіштік қисығында максимум және минимумдар пайда болады. Бұл иондардын еріткішпен өзара әсерлесу сипатының күрделілігімен түсіндіріледі. Анықтама кестелеріндегі деректерді және соңғы теңдеулерді пайдаланып, кез келген ерітінділердің электр өткізгіштігін есептеуге болады. Көп жағдайларда алынған деректердің дәлдігі өлшеу жүргізуге қажетті тәжірибе жағдайын дұрыс бағалауға жеткілікгі. Мұндай есептеулер титрлеу барысында байқалатын электр өткізгіштіктін өзгеруін алдын ала болжауға пайдалы. Иондық эквивалентті электр өткізгіштігі жоғары болатын иондарды ерітіндіде титрлеу барысында не косып, не алғаннан оньш өткізгіштігі өзгереді. Бұдан басқа реакция кезінде түзілетін жаңа өнім иондалмауы мүмкін, демек, ол нашар еткізгіш болуы мүмкін. 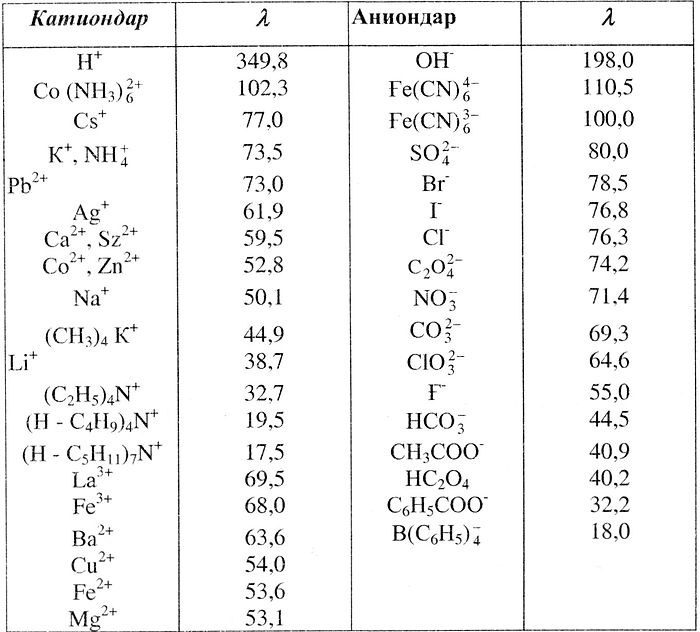 Кондуктометрлік әдістердін жіктелуі[өңдеу | қайнарын өңдеу] Кондуктометрлік әдістердін жіктелуі Тура және жанама кондуктометрия. Талдаудың кондукто метрлік әдістерін қолдану ауқымына қарай үш топқа бөлуге болады: таза заттын, ерігіндінін құрамын және физикалық-химиялық өзгерістердің кинетикасын зерттеу; ғылымдық, технологиялық және өндірістік процестерде бақылау үшін қолданылатын талдау кондуктометриясы; эквиваленттік нүктені (э.н.) анықтау үшін пайдаланылатын кондуктометрлік (автоматтық) титрлеу. Аналитикалык кондуктометрияны тура және жанама деп жіктейді. Тікслей кондуктометрия әдісінде зат концентрациясын ерітіндінің электр өткізгіштігі бойынша анықтайды, онда да бұл екеуінің арасындағы тура пропорционалдық тэуелділіктін болуына байланысгы. Бұл әдіс негізінен бір кұрамдас бөлікті ерітінді үшін немесе оның құрамындағы өзге қосылыстардың концентрациясы өзгеріссіз қалатын жағдайда тиімді. Анықталатын құрамдас бөліктің концентрациясы электр өткізгіштіктің ерітіпді концентрациясына тәуелділігін сипаттайды. Реттеуші график бойынша бұл тәуелділік тура сызықты сипат алуы керек. Талданатын ерітіндінің электр өткізгіштігін репеуші осы график бойынша өлшеп, іздеп отырған құрамдас бөліктін концентрациясын (немесе мөлшерін) табады. Тура кондуктометрлік талдау әдісі өте карапайым болғанымен, ол өте шектеулі қолданылады, өйткені болмашы ғана кездейсок электролит қоспасы ерітіндінің электр өткізгіштігін едәуір езгертуге бейім тұрады. Бұл эдіс ғылыми лабораторияда сирек колданылғанымен, өндірістегі процесс барысын бақылауға қажет, әрі талдау химиясындағы маңызды мәселелерді шешуге көмектеседі, мысалы: технологиялық процестерді бақылау, тұз елшеуіш көмегімен тұзды ерітінділердін концентрациясын анықтау, су тазалыгын анықтау, таза және ағын, калдықты сулар бақылау, өзен, көл, теңіз суындагы минералды анықтау, тұнбаны шайып, тазалау және иониттерді қайта тұтыну, тамақ, дәрі-дәрмек сапасын бақылау. Жанама кондуктометрия әдісі. Бұл әдіс көп кұрамды ерітіндідегі тек бір ғана құрамдас бөлікті талдаған кезде, кондуктометриямен қатар талдаудың басқа да физикалық-химиялық әдістерін қолдануга негізделген. Сол сияқты жанама кондуктометрия әдісіне ерітіндідегі ойтеуір бір қосылыс немесе сумен әрекеттесіп, электр өткізгішті өзгертуге себепші болатын газдың концентрациясын анықтау да енеді, мысалы, С02, NH3, S02, S03, N02 және т.б. Кондуктометрлік титрлеу Кондуктометрлік титрлеу Титрлеу процесін бақылау үшін электр өткізгіштікті өлшеу әдісін колдануды берілген ерітіндінің электр өткізгіштігі реагент не реакция өнімінікінен айтарлықтай өзгеше болған жағдайда қолдануға болады. Титрлеу кезінде ұяшык тұрактысын білу шарт емес, өйткені ә.н.-ді табу үшін салыстырмалы шамалар да жеткілікті. Алайда электродтар арасы өзгеріссіз қалғаны абзал, яғни олар кеңістікте мықты орналасуы керек. Кез келген ион ерігіндісінің электр өткізгіштігіне қосар үлесі, оның концентрациясы мен эквиваленттік электр өткізгіштігіне тура пропорционал, бірақ титрлеу барысында реагенттің қосылуына қарай ерітіндінің көлемі артып отырады. Бұған электр өткізгіштікті есептеу кезінде ерітіндіні сұйылтқанда өзгеріс енгізу керек. Сызықты тәуелділіктен ауытқу іс жүзінде реакцияға түсуші зат не өнімнің гидролизденуі немесе тұнбанын ішінара еруі не тұрақтануы салдарынан байкалады. Титрлеу қисығының пішінін теориялық тұрғыдан болжауға болады. Титрлеу кезінде жүйелі нүктелердегі әр ионының концентрациясын стехиометрия, тепе-теңдік, сұйылту заңдарына, тендеуіне негізделген белгілі әдіспен есептейді. Концентрацияны шамасына көбейгіп, әрбір ионның cалыстырмалы үлесін алсақ, онда олардың қосындысы титрлеу қисығын береді. Сұйығылған ерітіндінің электр өткізгіштігін есептегенде, иондардың қозғалткыштығының мәнін жиі пайдалануға тура келеді Ерітіндідегі әр түрлі иондар бір-бірінен қозғалғыштығымен өзгешеленеді. Кейбір иондардың қозғалғыштығы Катиондар Қозғалғыштық Аниондар Козғалғыштық 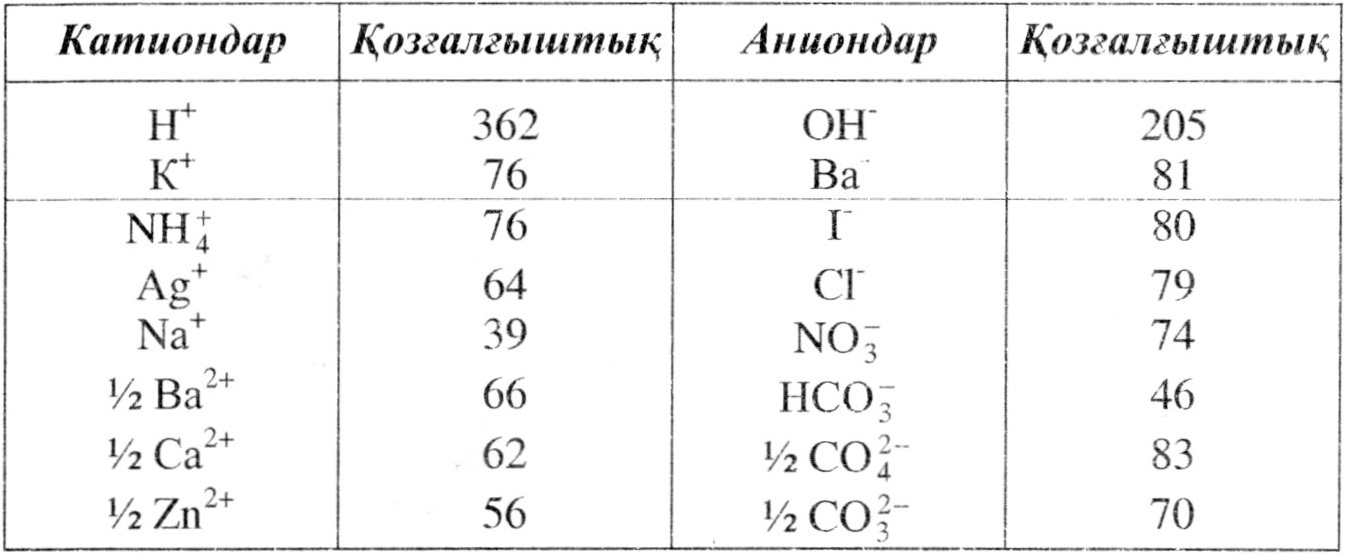 Жеке және қосиада кездесетін заттарды кондуктометрлік әдіспен талдағанда, әр түрлі химиялық реакциялар пайдаланылады: бейтараптау, тұндыру, сулы және сусыз ерітінділерде кешенді қосылыс түзілу. Ерітіндідегі иондардың саны мен сапасы кондуктометрлік титрлеу кезінде өзгереді, сондықтан да титранпы белгілі бір уақыт аралығында тұракты жылдамдыкпен беру арқылы оның электр өткізгіштігін өлшей отырып, титрлеу барысын мұқият бақылайды. Әдетте. титранттың үлесін әлсін-әлі коса отырып, ерітіндінің электр өткізгіштігін өлшейді. Ерітінді электр өткізгіштігінің титрант көлеміне тэуелділігі график арқылы кескінделеді. Алынған график кондуктометрлік титрлеу қисығы деп аталады. Қисықтың сынуы эквивалент нүктеге сәйкес келеді. Титрлеу кезінде ерітінді электр өткізгіштігінің өзгерісі әркез түзу сызықты бола бермейтінін ескерген жөн. Титрлеу қисығының сызықты емес сипаты титрлеу процесі кезінде диссоциация дәрежесі немесе зат реакциясына қатысатын гидролиз дәрежесі өзгерген жағдайларда байқалады. Егер титранттың белгілі бір стандартты ерітіндісімен талданатын зат кондуктометрлік титрлеу нәтижесінде нашар диссоциацияланатын немесе аз полюсті қосылыс түзетін болса, онда бұл жағдай ерітіндінің электр өткізгііитігін едәуір азайтады. Титрлеудің соңғы нүктесіне кондуктометрлік титрлеу қисығындағы электр өткізгіштіктің төменгі моні сәйкес келеді. Реагентті одан әрі косу ерітінді өткізгіштігін арттырады. Мұндай қисықтар жоғарыда келтірілген реакциялардың бәріне де тән. Күшті қышқылды күшті негізбен, күшті негізді күшті қышқылмен титрлеу қисығы, тұндыру реакциясы бұған мысал болады. Кондуктометрлік титрлеу реакциясы жүргенде, яғни эквиваленттік нүктеге дейін және одан кейін титрлеу қисығында электр өткізгіштіктің өзгеруі салыстырмалы түзу сызықты болуы мүмкін. Осы түзу учаскелерді қиылысқанша экстрополюстей отырып, титрлеудің сонғы нүктесін табады, яғни екі түзудің қиылысы, осы ә.н. болады. Бұл жағдайда талдау дәлдігі қанағаттанарлық дәрежесіне жетеді. Қайсыбір жағдайларда реакцияның мөлшерлі егуі титрлеу қисығының түзу сызықты болмауы кезінде де, мәселен, әлсіз қышқылды күшті негізбен титрлегенде байқалады. Мұндай қисыктарды эквиваленттік нүктені графикпен анықтау ушін сиректеу қолдануға тура келеді, яғни оны э.н. манайында сызықтың түзу болатын учаскесі айқын көрінгенде ғана пайдаланады. Басқа жағдайларда мұндай қисықтарды электронды есептегіш машиналар (ЭЕМ) көмегімен өңдеу қажет. Қышқыл мен негіздің өзара әсерлесу реакциялары Қышқыл мен негіздің өзара әсерлесу реакциялары Мұндай әрекеттесу кезінде титриметрлік кисықтың пішіні мен олардың тармақтары арасындағы бұрыштын шамасы титрлейтін жүйеде кездесетін иондардың қозғалгыштыгына ғана емес, қышқыл мен негіздің дәрежесіне, олардың ерітіндідегі концентрацнясына тәуелді болады. Қышқылды-негізді титрлеу кезінде аса қозғалғыш сутек пен гидроксид иондарынан аз диссоциацияланған қосылыс - су және күшті диссоциацияланатын тұз түзіледі, алайда тұз ионда- рының қозғалі ыштығы сутек пен гидроксид иондарыныкінен аз: Н+ + A- + Ме+ + ОН- -> Н20 + Ме+ + А- Егер едәуір концентрленген титрантты пайдаланса, ерітіндінің сұйылуы шамалы болады, оны теориялық есептеулерде ескермегенмен, талдаудағы есептеуде ескерген жөн. Күшті қышкыл - күшті негіз. Кондуктомегрлік қисық екі түзу сызықты тармақтан тұрады. AC тармағын нейтралдау қисығы дейді және ол электр өткізгіштігінің қосынды эффектісін көрсетеді. Бұл қисықты екі құраушыға жіктеуге болады: қышқыл концентрациясыпың азаюы (AF қышқылдық қисығы) және тұз концентрациясының артуы (EC тұз түзу қисығы). СВ кескіні де қосынды эффектіні көрсетеді: ерітінді көлемінің өзгерісін ескермеген жағдайда түзілетін тұз концентрациясы (CD кесіндісі) мен эквиваленттік нүктеден кейінгі қосылған сілті концентрациясы (СВ кесіндісі). Эквиваленттік нүктеге жақындаганда кондуктометрлік титрлеу қисығы әр кезде де түзу сызықты тәуелділіктен ауытқиды, бұл әр ионның электр өткізгіштікке қосқан үлесімен түсіндіріледі. Орташа күшті қышқыл - күшті негіз. Бұл жағдайда титрлеу қисығының минимумы болады да, аналитикалық мәні бола бермейді. Титрлеудің бірінші сәтінде әлсіз қышқыл мен күшгі негізден түзілетін тұздың пайда болуы нәтижесінде электр өткізгіштік кемиді, өйткені бұл тұз жақсы диссоциацияланған және қышқылмен ортақ анионы болғандықтан, оның дисеоциациялануын басады, яғни сутек иондары конценграциясының кемуі басталады. Мұнан кейінгі сілтінің қосылуы тұздағы электр өткізгішгікті арттырады. Эквиваленттік нүктеден кейін ерітіндінің электр өткізгіштігі гидроксид иоидарының көбейіп кетуі салдарынан тез өседі. Диссоциацияланбаған молекулалар (НА) концентрациясы монотонды түрде э.н.-гe дейін, кейде нөлге дейін төмендейді. Титрлеудің басында (Н+) иондарының конценфациясына тең болатын анион (А-) концентрациясы титрлеу кезінде э.н.-ге дейін өсіп, сосын тұрақты болып қалады, ал сутек ионының концентрациясы э.н.-де нөлге дейін төмендейді, ал калий иондарыныц концентрациясы титрант көлеміне сәйкес өседі. Ерітіндінің меншікті электр өткізгіштігі э.н.-ге дейін әуелі төмендеп, сосын реакция барысында К+ мен А- иондарының саны артуына байланысты өседі. Әлсіз қышқыл ерітіндісіндегі H+ ионда- рының және оның тұзының концентрациясы аса жоғары емес, ал оның титрлеу барысындағы азаюы электр өткізгішке көп әсер ете қоймайды. Әлсіз қышқыл - күіиті негіз. Бұл жұпта тұздан түзілетін гидролиздің ықпалы э.н. маңайында қисықтың баяу иілуімен кескінделеді Бұл жағдайда эквиваленттік нүктені кәдімгі графиктік тәсілмен анықтау мүмкін бола бермейді. Әлсіз қышқыл - әлсіз негіз. Бұл жағдайда титрлеу қисығы э.н.- ге біршама баяу өгетіндіктен, оны ЭЕМ көмегінсіз байқау мүмкін емес. Ал кондуктометрлік титрлеуді белгілі бір дәрежеде, тек оның жоғарғы рКНА шегінде ғапа жүргізуге болады, оны мына деректермен шектейді:  Қышқыл қоспасын немесе екі негізді қышқылды титрлеу. Күшті негізді қышқылдар қоспасын (күшті және әлсіз) тигрлегенде алынатын қисықты екі рет имелі қисықпен өрнектеуге болады. Бірінші име күшті кышқылды титрлеуге сәйкес келеді. Күшті қышқылда әлсіздің диссоциациялануы басылыңқы болатындықтан, ол электр өткізгіштікке ықпал етпейді. Ерітіндінің бірінші эквиваленттік нүктесінде күшті қышқыл орі күшті негіздің тұзы, сондай-ақ әлсіз қышқыл болады. Бұдан әрі титрлегенде, ерітіндінің электр өткізгіштігі жаңадан түзілген және түзілетін тұз концентрациясымен анықталады. Әлсіз қышқыл мен күшті негіз тұзының қосымша түзілуі есебінен ол болмашы ғана өзгереді. Бірінші және екінші эквиваленттік нүктелер арасында әлсіз қышқыл титрленеді. Екінші гитрлеу нүктесінен кейін электр өткізгіштік сілтінің артық мөлшерімен анықталады да, күрт өседі. Күшті қышқыл мөлшеріне эквивалент сілті мөлшері сілтінің бірінші эквиваленттік нүктеге дейін қосылған көлемімен (концентрациясымен) анықталады. Әлсіз қышқылдын мөлшері бірінші және екінші э.н. арасында титрлеуге кеткен сілті мөлшерімен өлшенеді. Әлсіз екі қышқыл қоспасын титрлегенде, егер, олардағы рК мәні 2-ден артық болса, онда қанағаттанарлық нәтиже алуға болады. Ал олардың концентрацияларының айырмашылығы тым көп болса, онда олардың ΔрК ≥ 3 болу қажет. Бұл жағдайларда қышқылдарды жеке титрлеуге негіз болатын бірден-бір талап. ол осы кышқылдар аниондары қозғалғыштықтарының арасында біраз айырмашылықтың болуына саяды. Көп негізді қышқылдарды титрлеу де қышқыл қоспалардағыдай (диссоциация кезіндегі) Δ рК айырымына байланысты. Қышқылдарды күшті негіздермен титрлегенде алынатын деректер мен дәйектемелердің дәлдігіне көмір қышқыл газы мен карбонаттардың ықпалы мол. Карбонат және бикарбонат иондары да күшті негізбен титрленеді. Демек, негіз ерітіндісінің тазалығына мән бөлген жөн. Мұндайда барий гидроксидінің ерітіндісін қолданған жақсы, өйткені оның құрамында карбонат жоқ, ол нашар ериді, әрі сүзгенде оңай бөлінеді. Негізді титрлеу. Негізді қышқылмен титрлеу қисығының сипаты жоғарыда қарастырылған қышқылды негізбен титрлегендегі қисыққа ұқсас. Өзгешелігі мұнда ОН- иондарының қозғалғыштығы Н+ ионына қарағанда аз, сондықтан қисықтың сонғы учаскесіндегі көлбеулік үлкен болады, яғни ерітіндідегі электр откізгіштік эквиваленітік нүктеден кейін бірден өседі. Ал э.н. маңындағы қисықтың бір қалыты озгерісі қышқылды тигрлегенге қарағанда айқынырақ кескінделеді. Тұздарды титрлеу. Олсіз қышқылдың тұзын күшті қышқыл ерітіндісімен титрлегенде, олсіз қышқыл ығыстырылады, ал әлсіз негіздің тұзын күшті негізбен титрлегенде, әлсіз негіз (көбінесе тұндыру) түзіледі. Әлсіз қышқыл мен әлсіз негізден түзілген тұздарды қышқылмен де, негізбен де титрлеуге болады. Кондуктометрлік титрлеу қисығында эквиваленттік нүктедегі күрт иілу мына жағдайда іске асады:  Егер әлсіз негізбен (және күшті қышқылмен) түзілген тұзды күшті негізбен титрлесе және осы кезде катион толық гидролизге душар болса, онда бұл жағдайда титрлеу қисығы U тәріздес болады. Гидролиз дәрежесі азайған сайын кондуктомеірлік титрлеу қисығының түрі өзгереді. Бұған семикарбазиттік гидрохлориді (рКи = 10,6) жақсы мысал болады. Бұл ортадағы катионның қозғалғыштығы натрий мен калий иондарынікінен жоғары. Егер тұз рКв < 9 аз болатын негізбен түзілсе, онда гидролиз ықпалы байкалмайды және тифлеу қисығының екі тармағы түзу сызықты болады. Қолдаланған әдебиеттер 1. Құлажанов Қ.С.Аналитикалық химия: II томдық оқулық . II - том. Оқулық. Алматы:«ЭВЕРО» баспаханасы, 2005. - 464 б. 2. Орысша-қазақша түсіндірме сөздік: Физика / Жалпы редакциясын басқарған э.ғ.д,, профессор Е. Арын – Павлодар: С. Торайғыров атындағы Павлодар мемлекеттік университеті, 2006. 3. Тугамбаева Т.Б., Масакбаева С.Р. Талдаудың физика-химиялық әдістері. Оқу құралы. Кереку. 2011. – 75б. 4. Б.Өтелбаева- Химия, 2-том, 1999ж, Шымкент, 413 бет. 5. Өтелбаев.Б.Т. Химия - Шымкент.: ОҚМУ, 2000г. 3 том - 6. А.Б.Адиходжаева, Р.А.Рустамбекова. Лабораторный практикум по аналитической химии.- Шымкент, ЮКГУ, 2010. 7. А.П. Крешков. Основы аналитической химии. Кн. 1,2,3 -М., Химия, 1977 8. В.Р. Алексеев. Курс качественного химического полумикроанализа.- М., Химия,1973. 9. В.И. Посыпайко, Н.А.Козырева, Ю.П. Логачева. Химические методы анализа.- М., Высшая школа,1989 10. Ю.С. Ляликов, Ю.А. Клячко. Теоретические основы современного качественного анализа.- М., Химия, 1978 |
