Суммативное оценивание за раздел 8.1С «Сравнение активности металлов»
|
Цель обучения
|
Описывать реакции взаимодействия активных металлов с холодной водой, горячей водой или паром
Исследовать факторы, влияющие на возникновение коррозии металлов
8.2.2.5 Составлять уравнения реакций металлов с кислотами
8.2.4.6 Разработать план и провести реакции металлов с растворами солей
8.2.4.8 Прогнозировать возможность протекания незнакомых реакций замещения металлов, используя ряд активности металлов
|
Критерий оценивания
|
Обучающийся
Записывает уравнения химических реакций магния с холодной водой и водяным паром.
Определяет факторы, влияющие на возникновение коррозии металлов, анализируя результаты исследования.
Составляет уравнения возможных реакций между раствором кислоты и металлами.
Заполняет таблицу, используя символы, для прогнозирования возможности протекания реакции
Записывает уравнения возможных реакции замещения металлов с растворами солей.
|
Уровень мыслительных навыков
|
Знание и понимание Навыки высокого порядка
|
Время выполнения
|
20 минут
|
Задания
|
|
1. Магний медленно реагирует с холодной водой, немного быстрее с горячей водой. В атмосфере водяного пара магний горит ярким пламенем.
Запишите уравнения реакций
(а) вода(ж) + магний (тв) →
(b) вода (пар) + магний (тв) →
|
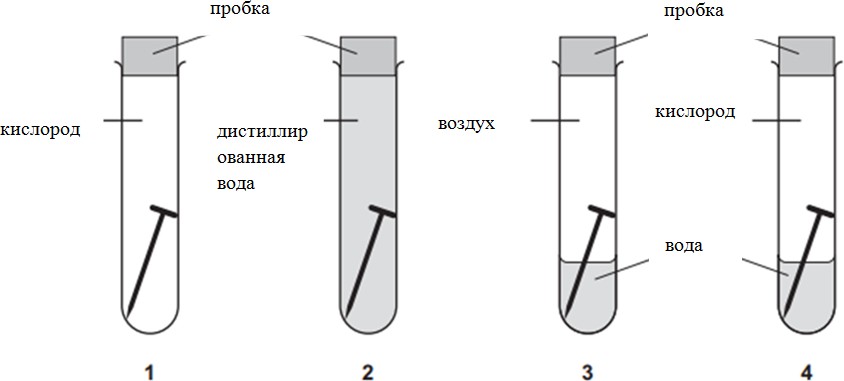 В четырёх пробирках показаны результаты исследования факторов, влияющих на возникновение коррозии металлов. В каждой из четырёх пробирок содержится железный гвоздь и указанны реагенты. В четырёх пробирках показаны результаты исследования факторов, влияющих на возникновение коррозии металлов. В каждой из четырёх пробирок содержится железный гвоздь и указанны реагенты.
(а) Предскажите порядок появления ржавчины в пробирках.
(b) Объясните свой прогноз.
В четыре одинаковые пробирки налили равные
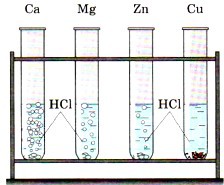 объёмы раствора соляной кислоты и поместили в них разные металлы. объёмы раствора соляной кислоты и поместили в них разные металлы.
Запишите уравнения протекающих реакций.
(а) кальций + соляная кислота →
магний + соляная кислота →
цинк + соляная кислота →
медь + соляная кислота →
(а) Заполните таблицу знаками «+» или «-» для прогнозирования возможности реакции.
соль \металл
|
железо
|
магний
|
медь
|
цинк
|
хлорид железа (II)
|
|
|
|
|
хлорид магния
|
|
|
|
|
хлорид меди (II)
|
|
|
|
|
хлорид цинка
|
|
|
|
|
число возможных реакций
|
|
|
|
|
Выведите ряд активности металлов, на основе вашего прогноза.
Запишите два уравнения протекающих реакций.
Критерий оценивания
|
№ задания
|
Дескриптор
|
Балл
|
Обучающийся
|
Записывает уравнения химических реакций магния с холодной водой и водяным
паром.
|
1
|
записывает словесное уравнение химической
реакции магния с холодной водой;
|
1
|
записывает словесное уравнение химической реакции магния с водяным паром;
|
1
|
Определяет факторы, влияющие на возникновение коррозии металлов, анализируя
результаты исследования.
|
2
|
определяет последовательность появления
ржавчины в пробирках;
|
1
|
объясняет предложенную последовательность появления ржавчины в пробирках;
|
1
|
Составляет уравнения возможных реакций между раствором кислоты и металлами.
|
3
|
записывает уравнение реакции между
раствором соляной кислоты и кальцием;
|
1
|
записывает уравнение реакции между
раствором соляной кислоты и магнием;
|
1
|
записывает уравнение реакции между
раствором кислоты и цинком;
|
1
|
определяет невозможность протекания реакции
между раствором соляной кислоты и медью;
|
1
|
Заполняет таблицу, используя символы, для прогнозирования возможности протекания реакции
|
4(а)
4(b)
|
заполняет таблицу, используя символы «+» или
«-» для прогнозирования возможности протекания реакции
|
4 (по 1 баллу для
каждого металла)
|
выводит ряд активности металлов, на основе
своего прогноза;
|
1
|
Записывает уравнения возможных реакции
замещения металлов с растворами солей
|
4(с)
|
записывает первое уравнение реакции;
|
1
|
записывает второе уравнение реакции;
|
1
|
Всего баллов
|
|
15
|                Рубрика для предоставления информации родителям по итогам суммативного оценивания за раздел 8 1С «Сравнение активности металлов» Рубрика для предоставления информации родителям по итогам суммативного оценивания за раздел 8 1С «Сравнение активности металлов»
ФИО обучающегося _
Критерий оценивания
|
Уровень учебных достижений
|
Низкий
|
Средний
|
Высокий
|
Записывает уравнения химических реакций магния с холодной водой и водяным паром.
|
Затрудняется при записи уравнений химических реакций магния с холодной водой и водяным паром
|
Допускает ошибки при записи уравнений химических реакций магния с холодной водой / с водяным паром
|
Записывает уравнения химических реакций магния с холодной водой и водяным паром.
|
Определяет факторы,
влияющие на
возникновение коррозии металлов, анализируя результаты исследования.
|
Затрудняется определить факторы, влияющие на возникновение коррозии металлов.
|
Допускает ошибки при определении порядка появления ржавчины в пробирках/ объяснении выбранного порядка
|
Определяет факторы, влияющие на появление ржавчины в пробирках
|
Составляет уравнения
возможных реакций между раствором кислоты и металлами.
|
Затрудняется при составлении возможных уравнений реакций между раствором кислоты и металлами.
|
Допускает ошибки при записи уравнения реакции между раствором соляной кислоты и кальцием/ магнием/ цинком/ медью
|
Записывает уравнения
возможных химических реакций между раствором соляной кислоты и металлами
|
Заполняет таблицу, используя символы, для прогнозирования возможности протекания реакции
|
Затрудняется прогнозировать возможности протекания реакции
|
Допускает ошибки при прогнозировании протекания реакции железа /магния/меди / цинка с растворами солей/ при составлении ряда активности металлов
|
Прогнозирует возможности протекания реакции
|
Записывает уравнения возможных реакции замещения металлов с растворами солей.
|
Затрудняется в записи возможных реакций замещения металлов с растворами солей
|
Допускает ошибки в записи первого / второго уравнения реакции
|
Записывает уравнения реакций замещения металлов с растворами солей
|    Задания по суммативному оцениванию за 2 четверть Задания по суммативному оцениванию за 2 четверть
Суммативное оценивание за разделы
8.2А «Количество вещества», 8.2В «Стехиометрические расчёты»
|
Цель обучения
|
8.1.1.2 Вычислять массу, количество вещества и число структурных частиц
Вычислять массу, количество вещества по уравнениям химических реакций
Знать закон Авогадро и использовать молярный объем для расчета объема газов при нормальных и стандартных условиях
|
Критерий оценивания
|
Обучающийся
Сопоставляет число структурных частиц в определённой массе и количестве вещества (n) и обосновывает ответ
Вычисляет массу вещества по известному количеству вещества (n) по уравнениям химических реакций
Применяет закон Авогадро для расчёта объёма газа при нормальных условиях по уравнению реакции
|
Уровень мыслительных навыков
|
Знание и понимание Применение
|
Время выполнения
|
20 минут
|
Задания
|
|
1. Определите, где содержится больше атомов. Ответ обоснуйте.
[Впишите в прямоугольник нужный знак: больше (>), меньше (<) или равно (=).]
(а) в 1 моль железа в 1 моль натрия, так как
в 1 г железа в 1 г натрия, так как
в 64 г меди в 0.5 моль кислорода, так как
2. Определите, одинаковые ли массы кислорода можно получить при разложении 1 моль оксида серебра (I) и 1 моль оксида ртути (II).
Уравнение химической реакции разложения оксида серебра (I): 2Ag2O → 4Ag + O2 Уравнение химической реакции разложения оксида ртути (II): 2HgO → 2Hg + O2
|
(а) Вычислите количество вещества кислорода при:
разложении оксида серебра (I): разложении оксида ртути (II):
Вычислите массу кислорода, полученного при:
разложении оксида серебра (I): разложении оксида ртути (II):
Ответ
Хватит ли 2,8 л кислорода для полного сжигания 8 г серы, если в результате образуется оксид серы (IV)? Если кислорода недостаточно, рассчитайте необходимый объем (условия нормальные).
(а) Уравнение химической реакции горения серы в кислороде: S + O2 → SO2
Вычислите количество вещества серы:

Вычислите количество вещества кислорода:

Вычислите объём (н.у.) кислорода, применяя Закон Авогадро.

(b) Ответ:
Критерий оценивания
|
№ задания
|
Дескриптор
|
Балл
|
Обучающийся
|
Сопоставляет число структурных частиц в определённой массе и количестве вещества (n) и обосновывает ответ.
|
1
|
определяет число атомов в первой паре
веществ, сопоставляет полученные значения и обосновывает ответ;
|
1
|
определяет число атомов во второй паре
веществ, сопоставляет полученные значения и обосновывает ответ;
|
1
|
определяет число атомов в третьей паре
веществ, сопоставляет полученные значения и обосновывает ответ;
|
1
|
Вычисляет массу
вещества по известному количеству вещества
(n) по уравнениям химических реакций.
|
2
|
вычисляет количество вещества оксида
серебра (I) и оксида ртути (II);
|
1
|
вычисляет массу кислорода, полученного
при разложении оксида серебра (I) и оксида ртути (II);
|
1
|
Применяет закон
Авогадро для расчёта объёма газа при нормальных условиях по уравнению реакции.
|
3
|
вычисляет количество вещества серы;
|
1
|
вычисляет количество вещества кислорода;
|
1
|
вычисляет объём (н.у.) кислорода, применяя
Закон Авогадро;
|
1
|
Всего баллов
|
8
|          Рубрика для предоставления информации родителям по итогам суммативного оценивания за раздел 8.2А «Количество вещества» 8.2В «Стехиометрические расчёты» Рубрика для предоставления информации родителям по итогам суммативного оценивания за раздел 8.2А «Количество вещества» 8.2В «Стехиометрические расчёты»
ФИО обучающегося _
Критерий оценивания
|
Низкий
|
Средний
|
Высокий
|
Сопоставляет число структурных частиц в определённой массе и количестве вещества (n) и обосновывает ответ.
|
Затрудняется определить и сопоставить число атомов веществ и обосновать свой ответ
|
Допускает ошибки при определении числа атомов в первой паре / второй
/ третьей паре веществ, сопоставляет полученные значения и обосновывает ответ
|
Определяет число атомов в определённой массе и количестве вещества (n) и обосновывает ответ
|
Вычисляет массу вещества по известному количеству вещества (n) по уравнениям химических реакций.
|
Затрудняется вычислить массу вещества по известному количеству вещества (n) по уравнениям химических реакций
|
Допускает ошибки при вычислении количества вещества оксида серебра
(I) и оксида ртути (II)/ массы кислорода, полученного при разложении оксида серебра (I) и разложении оксида ртути (II)/при записи ответа
|
Определяет массы кислорода при разложении одинакового количества оксида серебра (I) и оксида ртути (II)
|
Применяет закон Авогадро для расчёта объёма газа при нормальных условиях по уравнению реакции.
|
Затрудняется рассчитать объём газа при нормальных условиях по уравнению реакции, используя закон Авогадро
|
Допускает ошибки при вычислении количества вещества серы/ кислорода/ объёма (н.у.) кислорода, применяя Закон Авогадро/ при записи ответа
|
Вычисляет объём газа по уравнению реакции при нормальных условиях, применяя закон Авогадро
|
Суммативное оценивание за раздел
8.2С «Знакомство с энергией в химических реакциях»
|
Цель обучения
|
Понимать, что продуктами реакций горения являются оксиды, и что при горении углеродсодержащего горючего в кислороде могут образовываться углекислый газ, угарный газ или углерод
Объяснять причины парникового эффекта и предлагать пути решения
Знать, что экзотермические реакции идут с выделением теплоты, а эндотермические реакции с поглощением теплоты
|
Критерий оценивания
|
Обучающийся
Определяет, что для реакции горения необходим кислород и продуктами реакций горения являются оксиды
Называет причину образования углерода при реакции горения и составляет сбалансированное уравнение реакции
Объясняет причины парникового эффекта и предлагает меры по сокращению выбросов углекислого газа
Сравнивает количество энергии, потребляемой и выделяющейся во время реакции
|
Уровень мыслительных навыков
|
Знание и понимание Применение
|
Время выполнения
|
20 минут
|
Задания
|
|
Провели реакцию А с участием металла и неметалла. На рисунке показана реакция А.

Реакция А является примером реакции окисления.
(а) Назовите вещество, реагирующее с магнием в реакции A.
Назовите белое твердое вещество, полученное в реакции А.
Запишите уравнение реакции А.
Бензин - жидкое углеводородное топливо.
При избытке воздуха многие углеводороды сгорают почти невидимым пламенем.
(а) Предположите, почему при горении бензина образовалось облако черного дыма.
Сбалансированное уравнение на рисунке показывает полное сгорание углеводорода (этена).
Вещества, участвующие в уравнении реакции изображены структурными формулами.
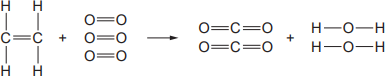
(b) Запишите, сбалансированное уравнение реакции полного сгорания этена, используя молекулярные формулы.
С2Н4 + ……. → …….. + ……..
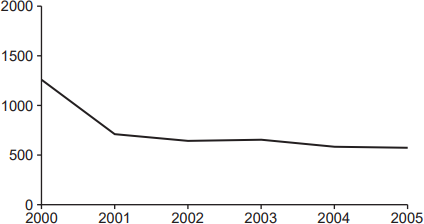 На рисунке показано количество углекислого газа, выброшенного в атмосферу крупным промышленным предприятием в период с 2000 по 2005 год. На рисунке показано количество углекислого газа, выброшенного в атмосферу крупным промышленным предприятием в период с 2000 по 2005 год.
Выбросы углекислого газа/ тысячи тонн
Год
(а) Опишите, как выбросы углекислого газа компании изменились между 2000 и 2005.
Промышленное предприятие заявило, что выбросы углекислого газа связаны с использованием электрической энергии. Объясните, как использование электроэнергии может влиять на выбросы углекислого газа.
Помимо уменьшения использования электроэнергии, предложите другой способ, с помощью которого промышленное предприятие могло бы сократить выбросы углекислого газа.
В 1997 году, на встрече в городе Киото в Японии, многие страны мира подписали соглашение о сокращении выбросов углекислого газа. Соглашение вступило в законную силу в 2005 году.
Объясните, почему нам необходимо сокращать выбросы углекислого газа.
(а) Рассмотрите типичную химическую реакцию: сгорание природного газа (метана) в кислороде воздуха.
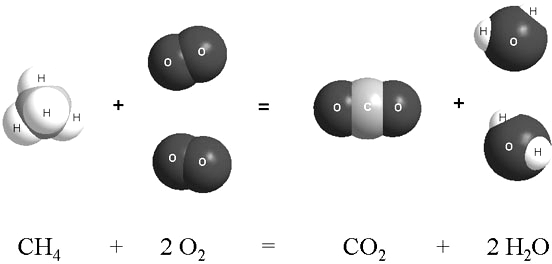
Определите тип химической реакции по тепловому эффекту.
(b) Рассмотрим другую реакцию – превращение гидроксида кальция (гашеная известь) в оксид кальция СаО (негашёная известь) и воду.

Определите тип химической реакции по тепловому эффекту.
Критерий оценивания
|
№ задания
|
Дескриптор
|
Балл
|
Обучающийся
|
Определяет, что для реакции горения необходим кислород и продуктами реакций горения являются оксиды
|
1
|
называет вещество необходимое для
реакции горения;
|
1
|
называет белое твёрдое вещество,
полученное в реакции;
|
1
|
записывает сбалансированное уравнение
реакции;
|
1
|
Называет причину
образования углерода при реакции горения и составляет сбалансированное уравнение реакции
|
2
|
предсказывает причину образования
углерода при горении бензина;
|
1
|
записывает сбалансированное уравнение реакции;
|
1
|
Объясняет причины
парникового эффекта и предлагает меры по сокращению выбросов углекислого газа
|
3
|
описывает изменения выбросов, как
выбросы углекислого газа, используя график;
|
1
|
объяснят влияние электроэнергии на
выбросы углекислого газа;
|
1
|
предлагает способ, с помощью которого
можно сократить выбросы углекислого газа;
|
1
|
объясняет необходимость сокращения
выбросов углекислого газа;
|
1
|
Сравнивает количество энергии, используемой и высвобождаемой во время реакции
|
4
|
рисует одну стрелку на стороне реагента, а другую на стороне продукта доказывая, что реакция экзотермическая;
|
1
|
рисует одну стрелку на стороне реагента, а другую на стороне продукта доказывая, что реакция эндотермическая;
|
1
|
Всего баллов
|
11
|             Рубрика для предоставления информации родителям по итогам суммативного оценивания за раздел 8.2С «Знакомство с энергией в химических реакциях» Рубрика для предоставления информации родителям по итогам суммативного оценивания за раздел 8.2С «Знакомство с энергией в химических реакциях»
ФИО обучающегося _
Критерий оценивания
|
Низкий
|
Средний
|
Высокий
|
Определяет, что для реакции горения необходим кислород и продуктами реакций горения являются оксиды
|
Затрудняется определить, что для реакции горения необходим кислород и продуктами реакции горения являются оксиды
|
Допускает ошибки при определении кислорода, необходимого для реакции горения
/ вещества, полученного в реакции/ при записи сбалансированного уравнения реакции
|
Определяет наличие кислорода для реакции горения и продукты реакции горения – оксиды
|
Называет причину образования углерода при реакции горения и составляет сбалансированное уравнение реакции
|
Затрудняется назвать причину образования углерода при горении бензина и составлении сбалансированного уравнения реакции.
|
Допускает ошибки в предсказании причины образования углерода при горении бензина/ составлении сбалансированного уравнения реакции.
|
Называет причину образования углерода при горении бензина и составляет сбалансированное уравнение реакции.
|
Объясняет причины парникового эффекта и предлагает меры по сокращению выбросов углекислого газа
|
Затрудняется объяснить причины парникового эффекта, предложить меры по сокращению выбросов углекислого газа.
|
Допускает ошибки при описании выбросов/ объяснении влияния электроэнергии на выбросы углекислого газа/ при выборе способа для сокращения выбросов углекислого газа/ при объяснении необходимости сокращения выбросов углекислого газа
|
Объясняет причины парникового эффекта и предлагает меры по сокращению выбросов углекислого газа
|
Сравнивает количество энергии, используемой и высвобождаемой во время реакции
|
Затрудняется определить изменение количества энергии во время реакции.
|
Допускает ошибки при определении изменения количества энергии, используемой / высвобождаемой во время реакции.
|
Определяет изменение количества энергии во время реакции.
| |
 Скачать 400.27 Kb.
Скачать 400.27 Kb. В четырёх пробирках показаны результаты исследования факторов, влияющих на возникновение коррозии металлов. В каждой из четырёх пробирок содержится железный гвоздь и указанны реагенты.
В четырёх пробирках показаны результаты исследования факторов, влияющих на возникновение коррозии металлов. В каждой из четырёх пробирок содержится железный гвоздь и указанны реагенты. объёмы раствора соляной кислоты и поместили в них разные металлы.
объёмы раствора соляной кислоты и поместили в них разные металлы.













 Рубрика для предоставления информации родителям по итогам суммативного оценивания за раздел 8 1С «Сравнение активности металлов»
Рубрика для предоставления информации родителям по итогам суммативного оценивания за раздел 8 1С «Сравнение активности металлов» 

 Задания по суммативному оцениванию за 2 четверть
Задания по суммативному оцениванию за 2 четверть 










 Рубрика для предоставления информации родителям по итогам суммативного оценивания за раздел 8.2А «Количество вещества» 8.2В «Стехиометрические расчёты»
Рубрика для предоставления информации родителям по итогам суммативного оценивания за раздел 8.2А «Количество вещества» 8.2В «Стехиометрические расчёты» 
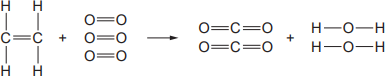
 На рисунке показано количество углекислого газа, выброшенного в атмосферу крупным промышленным предприятием в период с 2000 по 2005 год.
На рисунке показано количество углекислого газа, выброшенного в атмосферу крупным промышленным предприятием в период с 2000 по 2005 год.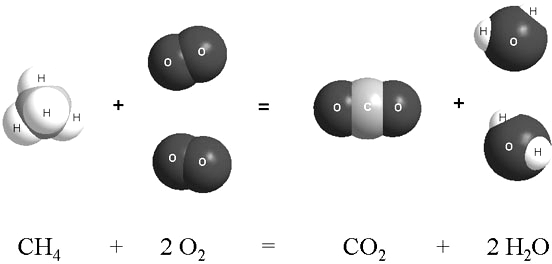












 Рубрика для предоставления информации родителям по итогам суммативного оценивания за раздел 8.2С «Знакомство с энергией в химических реакциях»
Рубрика для предоставления информации родителям по итогам суммативного оценивания за раздел 8.2С «Знакомство с энергией в химических реакциях» 