Алкалоиды. Лекция 8. Алколоиды. Название алкалоиды происходит, по одним источникам, от
 Скачать 168.58 Kb. Скачать 168.58 Kb.
|
|
Алкалоиды Название «алкалоиды» происходит, по одним источникам, от alkali (позднелат.) -щелочь, eidos(греч.) –вид; по другим – от араб. al-qali – щелочь. Алкалоиды – обширная группа азотсодержащих гетероциклических соединений преимущественно растительного происхождения, обладающих основным характером (что и подчеркивается в названии). В растениях алкалоиды содержатся в виде солей с органическими кислотами (лимонной, яблочной, винной, янтарной, щавелевой). Извлекают их методом экстракции. Содержание алкалоидов в растениях невелико (0,001-2,0%), но есть уникальные растения с большим (10-18%) содержанием алкалоидов, это хинное дерево и табак. Алкалоиды – бесцветные кристаллические вещества горького вкуса, практически нерастворимые в воде, но хорошо растворимые в органических растворителях (CHCl3, C2H5-O-C2H5, C6H6). Многие алкалоиды ядовиты, и способность обнаруживать их по вкусу помогла человеку избежать отравлений. Высказывалось даже предположение о том, что практически полное отсутствие у рептилий способности ощущать горький вкус явилось одной из причин вымирания динозавров, которое случилось примерно в то же время, что и развитие покрытосемянных (пестичных) растений, содержащих алкалоиды. Обычно алкалоидам присваивают тривиальные названия, используя видовые или родовые названия растений-алкалоидоносов, с прибавлением суффикса –ин. Например: атропин (Atropa belladonna), стрихнин (Strychnos nux Vomica), кофеин (Coffea Arabica) и т.д. Ранняя классификация алкалоидов по ботаническому (филогенетическому) признаку объединяла в одну группу все алкалоиды, выделенные из растений одного рода, например: - алкалоиды дафнифиллума - алкалоиды элаокарпуса - алкалоиды ипекакуаны и т.д. Сейчас наиболее принятой является классификация, основанная на строении гетероцикла (пуриновые алкалоиды, алкалоиды группы пиридина, пиперидина и пирролидина и т.д.), см.таблицу: Таблица : Классификация алкалоидов по строению гетероцикла
Рассмотрим строение и свойства важнейших представителей каждой группы. 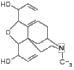 МОРФИН, бесцветное кристаллическое вещество, tпл.=254ºС, оптически активен (левовращающий). Выделен из опийного (снотворного) мака PapaverSomniferum в 1806г. французским фармацевтом Сегэном. Только в 1925г. английский химик-органик Р.Робинсон установил его строение. Пространственное строение установлено в 1955 г. (Д.Ходжкин). Обладает мощным обезболивающим действием (в виде соли с HCl). МОРФИН, бесцветное кристаллическое вещество, tпл.=254ºС, оптически активен (левовращающий). Выделен из опийного (снотворного) мака PapaverSomniferum в 1806г. французским фармацевтом Сегэном. Только в 1925г. английский химик-органик Р.Робинсон установил его строение. Пространственное строение установлено в 1955 г. (Д.Ходжкин). Обладает мощным обезболивающим действием (в виде соли с HCl). Морфин, как, впрочем, и большинство других алкалоидов, имеет довольно сложное строение. В одной молекуле представлены фрагменты различных классов органических соединений. Поэтому алкалоиды используются в качестве модельных структур при изучении взаимосвязи строения со свойствами органических соединений, их физиологической активностью. В частности, молекула морфина содержит функциональные группы следующих классов: алканы, циклоалканы, алкены, вторичные спирты, фенолы, арены, простые эфиры, третичные амины. Следовательно, все характерные реакции перечисленных классов будут протекать и для морфина. Например, наличие фенольного гидроксила придает морфину способность растворяться в щелочах, тогда как атом азота является местом протонирования в реакциях солеобразования с кислотами. Производными морфина являются кодеин и героин:
Кодеин уменьшает возбудимость кашлевого центра, используется как эффективное противокашлевое средство. В отличие от морфина, не растворим в щелочах и не дает характерного окрашивания с FeCl3, так как не содержит фенольного гидроксила. Героин хуже, чем морфин, растворяется в воде, но лучше в жирах. Поэтому, хотя героин и вводят внутривенно, он быстро попадает в мозг, практически недоступный для больших водорастворимых молекул. По этой причине героин более эффективен (более «героичен»), но его действие менее продолжительно. В организме героин превращается в морфин.  ХИНИН, белое кристаллическое вещество, выделяют из коры южно-американского хинного дерева. Оптически активен, левовращающий. 2-х кислотное основание, образует 2 вида солей с минеральными кислотами. Применяется для лечения малярии, связывается с ДНК зараженной клетки и ингибирует ее репликацию. Применяется для лечения малярии, связывается с ДНК зараженной клетки и ингибирует ее репликацию. ХИНИН, белое кристаллическое вещество, выделяют из коры южно-американского хинного дерева. Оптически активен, левовращающий. 2-х кислотное основание, образует 2 вида солей с минеральными кислотами. Применяется для лечения малярии, связывается с ДНК зараженной клетки и ингибирует ее репликацию. Применяется для лечения малярии, связывается с ДНК зараженной клетки и ингибирует ее репликацию.Применяется также в акушерстве для усиления родовой деятельности и стимуляции выкидыша. Входит в состав напитков «тоник» и ароматизированного вина «дюбонне». Местом протонирования в молекуле хинина является атом азота третичной аминогруппы. Характерные реакции: АЕ (радикал винил СН2=СН-), SE (ароматическая система хинолина), SN (вторичная спиртовая группа, простая эфирная группа и пиридиновый цикл), SR (фрагменты с насыщенными атомами С).  ПАПАВЕРИН ПАПАВЕРИНОдин из главных алкалоидов опийного мака PapaverSomniferum (0,5-1,0%). Гипотензивное средство.  НО-ШПА (дротаверин). Синтетический препарат. Имеет структурное сходство с папаверином НО-ШПА (дротаверин). Синтетический препарат. Имеет структурное сходство с папаверином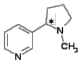 НИКОТИН НИКОТИНОсновной алкалоид табака и махорки (NicotianatabacumL., N.rusticaL). Бесцветная маслянистая жидкость с запахом табака. tºкип.=246º С. Хорошо растворим в Н2О и органических растворителях. Оптически активен, левовращающий. Воздействует на вегетативную нервную систему, сужает кровеносные сосуды. Ядовит, смертельная доза 40 мг/кг  АНАБАЗИН АНАБАЗИНСодержится в ежовнике безлистном (AnabasisaphyllaL). Гидрохлорид анабазина снижает влечение к курению. Сырье для получения никотиновой кислоты.  КОНИИН КОНИИН Выделен из семян болиголова крапчатого (Coniummaculatum). Парализует окончания двигательных и чувствительных осязательных нервов, участвующих в иннервации кожи.  ЛОБЕЛИН ЛОБЕЛИН Обнаружен в растении лобелия (Lobeliainflate, Северная Америка). В виде гидрохлорида используется как аналептическое средство.  КОФЕИН (1,3,7-триметилксантин). Бесцветное кристаллическое вещество без запаха, tº пл.=235ºС. Выделен из зерен растения CoffeaArabica, содержится также в чае (до 5%). Оказывает возбуждающее действие на центральную нервную систему, усиливает сердечную деятельность, стимулирует диурез. Входит в состав напитка «Cola». КОФЕИН (1,3,7-триметилксантин). Бесцветное кристаллическое вещество без запаха, tº пл.=235ºС. Выделен из зерен растения CoffeaArabica, содержится также в чае (до 5%). Оказывает возбуждающее действие на центральную нервную систему, усиливает сердечную деятельность, стимулирует диурез. Входит в состав напитка «Cola».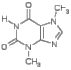  Теобромин (3,7-диметилксантин) и теофиллин (1,3-диметилксантин) Теобромин (3,7-диметилксантин) и теофиллин (1,3-диметилксантин)Природные источники те же, что у кофеина. Обладают менее выраженным общестимулирующим действием, но являются сильными диуретиками. Теобромин - основной алкалоид какао-бобов шоколадного дерева. В отличие от других алкалоидов, у метилированных ксантинов основные свойства выражены очень слабо, их соли с минеральными кислотамигидролизованы. За счет пиррольного атома азота теофиллин и теобромин обладают кислотными свойствами, они способны образовывать нерастворимые соли с ионами некоторых металлов, что используется для их идентификации и количественного определения в фармацевтическом анализе. Так водонерастворимый теофиллин, предварительно превращенный в растворимую натриевую соль, осаждается ионами кобальта (II) в виде соли светло-розового цвета.  Теобромин при такой же обработке дает соль серовато-голубого цвета; анион этой соли представлен ниже в виде резонансных структур, соответствующих лактамной и лактимной формам теобромина. Кофеин не обладающий кислотными центрами, подобной соли не образует.  На использовании кислотных свойств пуриновых алкалоидов основано получение водорастворимых препаратов. Примером может служить эуфиллин – соль теофиллина с этилендиамином.  Эуфиллин ЭуфиллинВсе три метилированных ксантина устойчивы к щелочам только при обычной температуре, а при нагревании подвергаются частичному (теобромин) или полному разрушению с раскрытием пиримидинового кольца. Синтез метилированных ксантинов. Простой и эффективный способ превращения мочевой кислоты в ксантин состоит в кипячении ее с формамидом. В качестве промежуточного образуется соединение с раскрытым имидазольным циклом, которое затем отщепляет аммиак и диоксид углерода.  Алкилирование ксантина диметилсульфатом при рН 8-9 приводит преимущественно к образованию кофеина, при рН 4-7 – теобромина.  Атомы азота в молекуле ксантина подвергаются алкилированию в последовательности N-3, N-7, N-1, поэтому теофиллин прямым алкилированием ксантина синтезировать не удается, его получают другими методами.  ПИЛОКАРПИН выделен из африканских растений рода PilocarpusVahl.. Синтезирован А.Е.Чичибабиным и Н.А.Преображенским. Используется в офтальмологии при лечении глаукомы, снижает внутриглазное давление. ПИЛОКАРПИН выделен из африканских растений рода PilocarpusVahl.. Синтезирован А.Е.Чичибабиным и Н.А.Преображенским. Используется в офтальмологии при лечении глаукомы, снижает внутриглазное давление.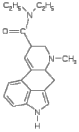 ЛСД (ЛСД-25, делизид) – диэтиламид лизергиновой кислоты. ЛСД (ЛСД-25, делизид) – диэтиламид лизергиновой кислоты.Получен в 1938 г. А.Гофманом из диэтиламина С2Н5-NH-C2H5 и лизергиновой кислоты, выделенной из спорыньи (микрогриб-паразит на ржи и других зерновых культурах, вызывающий заболевание, известное под древним названием «Антонов огонь»). Синтезирован в 1954 г. Р.Вудвордом. Бесцветное кристаллическое вещество без вкуса и запаха, не растворимое в воде, но растворимое в органических растворителях. Гидролизуется по амидной связи при кипячении в 7% водном КОН за 1 час. Вызывает галлюцинации, продолжающиеся до суток и сопровождающиеся вегетативными расстройствами. Вызывает отклонения от нормального развития зародыша. Механизм действия – конкурентный антагонист серотонина, нарушает баланс серотонина в мозге.  Серотонин. Один из основных нейромедиаторов. По химическому строению серотонин относится к биогенным аминам, классу триптаминов. Серотонин часто называют «гормоном хорошего настроения» и «гормоном счастья». Серотонин. Один из основных нейромедиаторов. По химическому строению серотонин относится к биогенным аминам, классу триптаминов. Серотонин часто называют «гормоном хорошего настроения» и «гормоном счастья». РЕЗЕРПИН. Выделяют из растения Rauvolfiaserpentine. Применяют для лечения артериальной гипертензии, при легких формах сердечной недостаточности с тахикардией. РЕЗЕРПИН. Выделяют из растения Rauvolfiaserpentine. Применяют для лечения артериальной гипертензии, при легких формах сердечной недостаточности с тахикардией. СТРИХНИН. Выделен в 1818 г. из рвотных орешков (семян чилибухи Strychnosnux-vomica). Чрезвычайно токсичен, антагонист глициновых рецепторов. Применяется как тонизирующее средство (экстракт, настойки). СТРИХНИН. Выделен в 1818 г. из рвотных орешков (семян чилибухи Strychnosnux-vomica). Чрезвычайно токсичен, антагонист глициновых рецепторов. Применяется как тонизирующее средство (экстракт, настойки).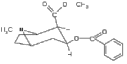 КОКАИН. Извлекают из листьев кустарника Coca. Первый синтез кокаина осуществлен в 1909 г. (Р.Вильштеттер). Конфигурация молекулы определена в 1953 г. (Г.Фодор, С.П.Финдлей). Бесцветные кристаллы горького вкуса, tºпл.=98º С. Хорошо растворим в воде и этаноле. Оказывает сильное местное анестезирующее действие (в виде соли с HCl). Большие дозы кокаина вызывают паралич дыхательного центра. КОКАИН. Извлекают из листьев кустарника Coca. Первый синтез кокаина осуществлен в 1909 г. (Р.Вильштеттер). Конфигурация молекулы определена в 1953 г. (Г.Фодор, С.П.Финдлей). Бесцветные кристаллы горького вкуса, tºпл.=98º С. Хорошо растворим в воде и этаноле. Оказывает сильное местное анестезирующее действие (в виде соли с HCl). Большие дозы кокаина вызывают паралич дыхательного центра. СКОПОЛАМИН содержится в растениях семейства пасленовых (скополия, красавка, белена, дурман). Применяется в офтальмологии, для подготовки к наркозу в хирургии, как успокаивающее в психиатрии. Средство от воздушной и морской болезни (таблетки «Аэрон»). СКОПОЛАМИН содержится в растениях семейства пасленовых (скополия, красавка, белена, дурман). Применяется в офтальмологии, для подготовки к наркозу в хирургии, как успокаивающее в психиатрии. Средство от воздушной и морской болезни (таблетки «Аэрон»). АТРОПИН содержится в красавке (Atropabelladonna), белене, дурмане, скополии и других растениях семейства пасленовых. Впервые выделен в 1833 г. Синтез осуществлен в 1901 г. (Р.Вильштеттер). Бесцветное кристаллическое вещество tºпл.=115-116º С. Один из сильнейших ядов. По химическому строению является сложным эфиром спирта тропин и (±)троповой кислоты и представляет собой рацемическую смесь (+) и (-) изомеров. АТРОПИН содержится в красавке (Atropabelladonna), белене, дурмане, скополии и других растениях семейства пасленовых. Впервые выделен в 1833 г. Синтез осуществлен в 1901 г. (Р.Вильштеттер). Бесцветное кристаллическое вещество tºпл.=115-116º С. Один из сильнейших ядов. По химическому строению является сложным эфиром спирта тропин и (±)троповой кислоты и представляет собой рацемическую смесь (+) и (-) изомеров.В растениях содержатся лишь следы атропина. Главной формой алкалоида является гиосциамин – сложный эфир тропина и (-)троповой кислоты. При выделении из растений гиосциамин при tº=114-116ºС подвергается рацемизации и превращается в атропин. В медицине атропин применяется как спазмолитическое средство; в глазной практике (еще в древности было открыто, что употребление красавки вызывает мидриаз – расширение зрачков, женщина с расширенными зрачками – красивая женщина – belladonna); как антидот при отравлениях снотворными и наркотиками (в том числе морфином). Все вышеперечисленные алкалоиды условно называют «истинными», то есть такими, в основе структуры которых находится гетероцикл с атомом азота. Однако, есть немалая группа алкалоидов, не содержащих гетероциклов, их относят к «протоалкалоидам», например, эфедрин, капсаицин, колхицин, колхамин (учебник, ч.2, с.308-312). |