Обмен липидов. обмен липидов. Обмен липидов Обмен липидов
 Скачать 4.54 Mb. Скачать 4.54 Mb.
|
|
Окисление жирной кислоты с образованием ацетильных групп (в форме ацетил-SКоА). Сгорание ацетил-SКоА в цикле лимонной кислоты или синтез (только в печени) кетоновых тел. Первое, что происходит при использовании нейтрального жира во время голодания и физической нагрузки – это активация ферментов, отвечающих за отщепление жирных кислот от триацилглицерола. Первый активируемый фермент называется триацилглицерол-липаза или ТАГ-липаза. Кроме ТАГ-липазы, в адипоцитах имеются еще диацилглицерол-липаза (ДАГ-липаза) и моноацилглицерол-липаза (МАГ-липаза), которые постоянно активны, однако в покое их активность не проявляется из-за отсутствия субстрата. Активация триацилглицерол-липазы Гормонзависимая активация липолиза в адипоцитах адреналином и глюкагоном происходит при напряжении организма (голодание, длительная мышечная работа, охлаждение). Активность ТАГ-липазы зависит, главным образом, от соотношения инсулин / глюкагон. 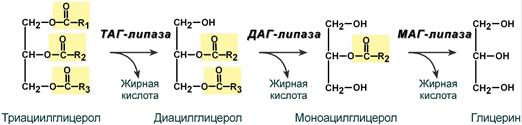 Снижение активности ТАГ-липазы Инсулин препятствует активации липолиза другими гормонами, т.к. : он активирует фермент фосфодиэстеразу активирует протеинфосфатазы, дефосфорилирующие ТАГ-липазу . Распад глицерофосфолипидов осуществляется в различных тканях двумя альтернативными путями. В ходе первого пути гидролитический распад глицерофосфолипидов начинается с отщепления жирных кислот под влиянием фосфолипаз А1 или А2. Распад глицерофосфолипидов по второму пути начинается с гидролиза эфирной связи между диацилглицеринами и замещенной фосфорной кислотой под действием фосфолипазы С с образованием диацилглицерина и фосфорилированной формы спиртового основания. Распад глицерофосфолипидов Распад фосфолипидов осуществляется тканевыми фосфолипазами. Различают несколько видов фосфолипаз (фосфолипазы А1, А2, С, D), которые разрывают различные связи в фосфолипидах. 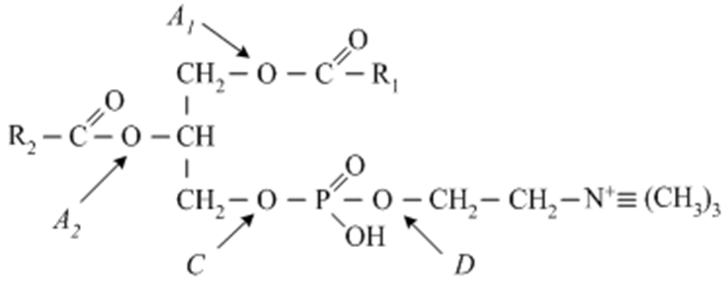 При ряде патологических состояний наблюдается активация тканевой фосфолипазы А2. Это сопровождается образованием продуктов неполного распада фосфолипидов ‒ лизофосфолипидов. Гепатозы ‒ это группа заболеваний печени, в основе которых лежит нарушение обмена веществ в гепатоцитах и развитие в этих клетках дистрофических изменений. Различают жировые и пигментные гепатозы, имеющие острое и хроническое (чаще) течение. Наиболее распространённым гепатозом является хронический стеатогепатоз (жировой гепатоз, жировая инфильтрация печени, жировая дистрофия печени). Стеатоз печени ‒ это наиболее распространённый гепатоз, при котором в печёночных клетках происходит накопление жира. Это состояние, при котором более 5 % массы печени составляет жир, преимущественно триглицериды. Главной причиной жировой инфильтрации печени является метаболический блок синтеза ЛПОНП, ответственных за транспорт ТАГ из печени. Так как ЛПОНП включают разнородные соединения, то блок может возникнуть на разных уровнях синтеза: нарушение секреции липопротеинов в кровь, 2) часто причиной может быть относительная недостаточность апобелков и фосфолипидов при избытке ТАГ 3) недостаток апобелков, 4) снижение синтеза фосфолипидов, 5) блок сборки липопротеиновых частиц в ЭПР при воздействии токсинов (хлороформ, мышьяк, свинец). Причинами стеатоза печени могут также быть: нарушение обмена веществ действие токсических факторов несбалансированное питание хронические заболевания пищеварительной системы с синдромом нарушенного всасывания и др. синдром Кушинга микседема дефицит лизосомальной кислой липазы Липотропные вещества являются важными факторами, способствующими нормализации обмена липидов и холестерола в организме, стимулируют мобилизации жира из печени и его окисление, что ведёт к уменьшению степени выраженности жировой инфильтрации печени К липотропным факторам относятся: 1. Структурные компоненты фосфолипидов: полиненасыщенные жирные кислоты, инозитол, серин, холин, этаноламин. 2. Метионин – в виде S-аденозилметионина является донором метильных групп для синтеза холина и фосфатидилхолина. 3. Витамины: пиридоксин (В6), способствующий образованию ФЭА из ФС. цианкобаламин (В12) и фолиевая кислота, участвующие в реакциях обмена серина, глицина и метионина, при ресинтезе метионина из гомоцистеина. 7.Синтез холестерола; реакции образования мевалоновой кислоты. Экскреция холестерола. Желчные кислоты (первичные и вторичные) Биосинтез холестерина ‒ это образование в живом организме органического спирта холестерола стероидной природы. Холестерин (холестерол) – это, природный полициклический липофильный спирт 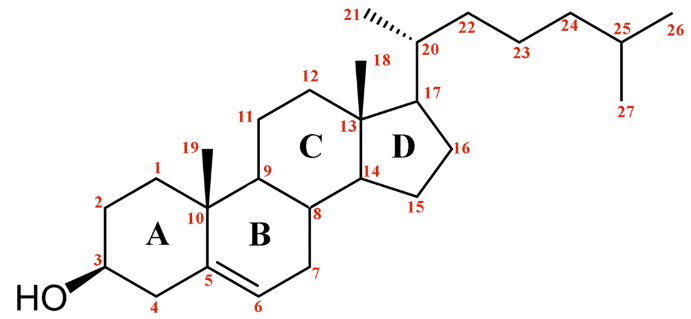 В настоящее время установлена цепь биосинтеза холестерина, включающая в себя несколько ступеней. Превращение трёх молекул активного ацетата в пятиуглеродный мевалонат. Превращение мевалоната в активный изопреноид – изопентилпирофосфат. Образование тридцатиуглеродного изопреноидного сквалена из шести молекул изопентенилдифосфата. Циклизация сквалена в ланостерин. Последующее превращение ланостерина в холестерин. Синтез холестерола На первой стадии образуется мевалоновая кислота (а). На второй стадии мевалоновая кислота превращается в изопентенилпирофосфат («активный изопрен»), 6 молекул которого конденсируются в сквален (б). На третьей стадии сквален превращается в холестерол (в). Биологическая роль холестерола Холестерин в составе клеточной (плазматической) мембраны играет роль модификатора бислоя, придавая ему определённую жёсткость за счёт увеличения плотности «упаковки» молекул фосфолипидов. Таким образом, холестерин – это стабилизатор текучести плазмалеммы. Холестерин открывает цепь биосинтеза стероидных половых гормонов и кортикостероидов, служит основой для образования желчных кислот и витаминов группы D, участвует в регулировании проницаемости клеток и предохраняет эритроциты крови от действия гемолитических ядов. 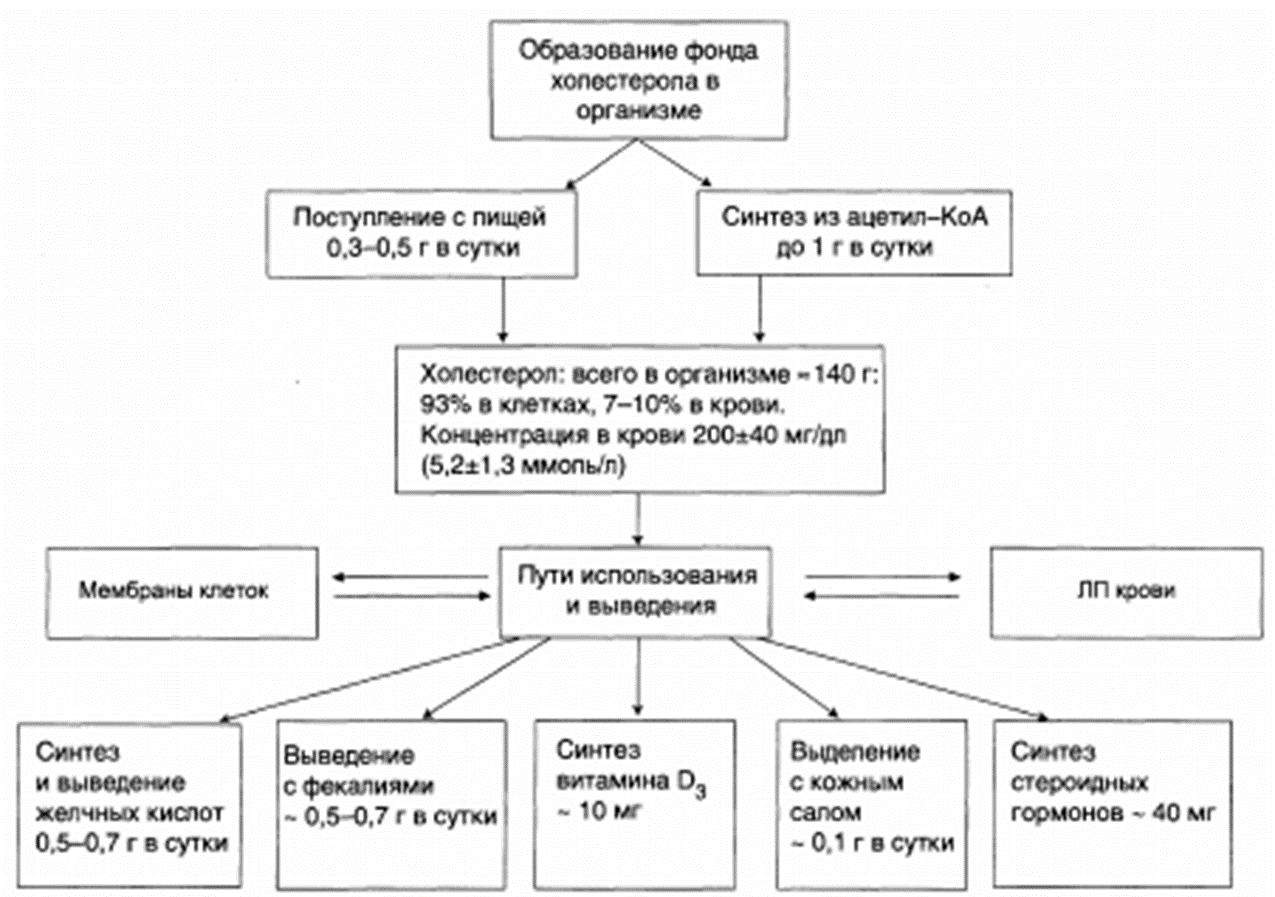 Жёлчные кислоты – это монокарбоновые гидроксикислоты из класса стероидов (холевые кислоты, холиевые кислоты, холеновые кислоты). Жёлчные кислоты – производные холановой кислоты (С23Н39СООН), отличающиеся тем, что к её кольцевой структуре присоединены гидроксильные группы. Печень человека выделяет в сутки до 2 л жёлчи Основными типами жёлчных кислот, имеющимися в организме человека, являются так называемые первичные жёлчные кислоты (первично секретируемые печенью): холевая кислота и хенодезоксихолевая кислота, а также вторичные (образуются из первичных жёлчных кислот в толстой кишке под действием кишечной микробиоты: дезоксихолевая кислота, литохолевая, аллохолевая и урсодезоксихолевая кислоты. Жёлчные кислоты, содержащиеся в жёлчи, эмульгируют жиры и участвуют в мицеллообразовании, активизируют моторику тонкой кишки, стимулируют продукцию слизи и гастроинтестинальных гормонов: холецистокинина и секретина, предупреждают адгезию бактерий и белковых агрегатов за счёт взаимодействия с эпителиальными клетками жёлчных путей. Жёлчь также участвует в выполнении выделительной функции. Жёлчь активирует киназоген, превращая его в энтеропептидазу, которая в свою очередь активирует трипсиноген, превращая его в трипсин, то есть, она активирует ферменты, необходимые для переваривания белков. 8.Транспортные липопротеины: строение, образование, функции Липопротеины представляют собой комплексы, состоящие из белков (аполипопротины – апо-ЛП) и липидов, связь между которыми осуществляется посредством гидрофобных и электростатических взаимодействий. 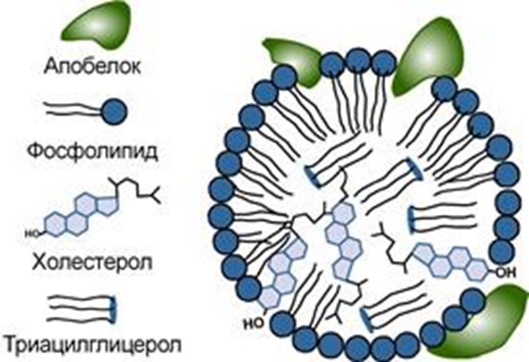 Различают четыре основных класса липопротеинов: липопротеины высокой плотности (ЛПВП, α-липопротеины, α-ЛП), липопротеины низкой плотности (ЛПНП, β-липопротеины, β-ЛП), липопротеины очень низкой плотности (ЛПОНП, пре-β-липопротеины, пре-β-ЛП), хиломикроны (ХМ). Хиломикроны и ЛПОНП ответственны, в первую очередь, за перенос жирных кислот в составе триацилглицеролов. Липопротеины высокой и низкой плотности – за транспорт свободного холестерола и жирных кислот в составе его эфиров. Апопротеины выполняют несколько функций: формируют структуру липопротеинов; взаимодействуют с рецепторами на поверхности клеток и таким образом определяют, какими тканями будет захватываться данный тип липопротеинов; служат ферментами или активаторами ферментов, действующих на липопротеины. 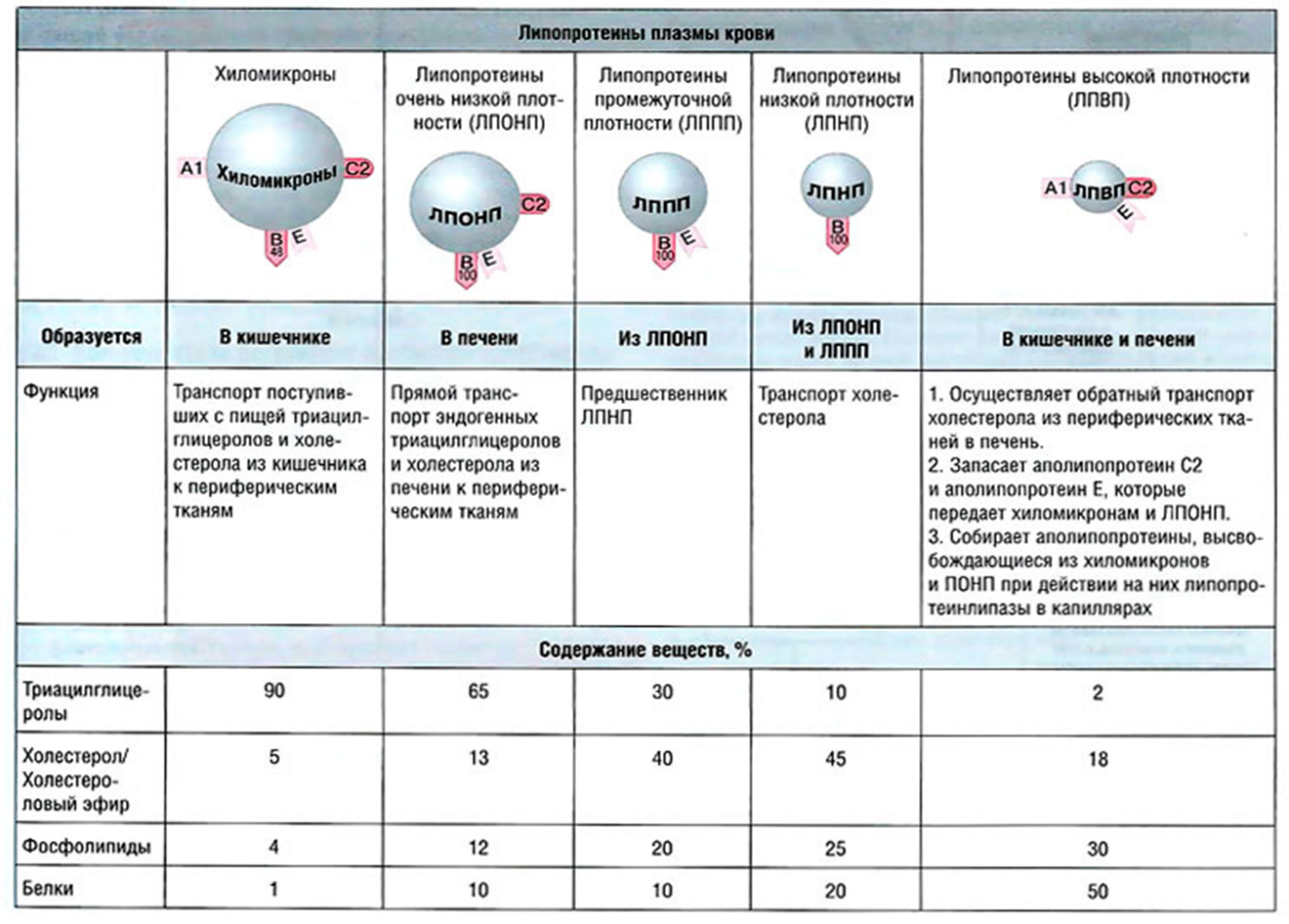 Обмен липопротеинов ЛПВП ‒ липопротеин высокой плотности; ЛПНП ‒ липопротеин низкой плотности; ЛПОНП ‒ липопротеин очень низкой плотности; ХМ ‒ хиломикрон; ТГ ‒ триацилглицерол; ХС ‒ холестерол; ЭХС ‒ эфир холестерола; ЛПЛ-аза ‒ липопротеинлипаза; ЛХАТ ‒ лецитин: холестерол-ацилтрансфераза.  9. Атеросклероз. Коэффициент атерогенности Атеросклероз – это хроническое заболевание артерий эластического и мышечно-эластического типа, возникающее вследствие нарушения липидного и белкового обмена и сопровождающееся отложением холестерина и некоторых фракций липопротеинов в просвете сосудов. Отложения формируются в виде атероматозных (холестериновых) бляшек. Последующее разрастание в них соединительной ткани (склероз), и кальциноз стенки сосуда приводят к деформации и сужению просвета вплоть до обтурации (закупорки сосуда). Выдвигаются следующие варианты, а также их сочетания: теория липопротеидной инфильтрации ‒ первично накопление липопротеидов в сосудистой стенке, теория дисфункции эндотелия ‒ первично нарушение защитных свойств эндотелия и его медиаторов, аутоиммунная ‒ первично нарушение функции макрофагов и лейкоцитов, инфильтрация ими сосудистой стенки, моноклональная ‒ первично возникновение патологического клона гладкомышечных клеток, вирусная ‒ первично вирусное повреждение эндотелия (герпес, цитомегаловирус и др.), перекисная ‒ первично нарушение антиоксидантной системы, генетическая ‒ первичен наследственный дефект сосудистой стенки, хламидиозная ‒ первичное поражение сосудистой стенки хламидиями, в основном, Chlamydia pneumoniae. гормональная ‒ возрастное повышение уровня гонадотропных и адренокортикотропных гормонов приводит к повышеному синтезу строительного материала для гормонов ‒ холестерина. При атеросклерозе сосуды поражаются неравномерно. Чаще страдают сосуды нижних конечностей в местах разветвлений, аорта и коронарные сосуды, поверхностная бедренная и подколенная артерии. Коэффициент атерогенности ‒ это показатель состава крови, который отражает соотношение между липопротеидами высокой плотности и низкомолекулярными липопротеидами. Для того чтобы результаты атерогенности, были максимально правильными, необходимо знать концентрацию в составе крови всех фракций липопротеидов: концентрация общего холестерина в составе крови; индекс липопротеидов высокомолекулярных (ЛПВП); низкомолекулярные липиды (ЛПНП); липиды очень низкой плотности (ЛПОНП); молекулы триглицеридов. Факторы риска возникновения атеросклероза Курение (наиболее опасный фактор) Употребление алкоголя Гиперлипопротеинемия (общий холестерин > 5 ммоль/л, ЛПНП > 3 ммоль/л, ЛП(а) > 50 мг/дл) Артериальная гипертензия (систолическое АД > 140 мм рт. ст. диастолическое АД > 90 мм рт. ст.) Сахарный диабет Ожирение Малоподвижный образ жизни (гиподинамия) Эмоциональное перенапряжение Неправильное питание Наследственная предрасположенность Постменопауза Гиперфибриногенемия Гомоцистеинурия и гомоцистеинемия Гипотиреоз. Формула расчета Для выявления коэффициента атерогенности существует формула расчёта: КТ = (общий ХС минус ХСЛПВП) и разделить на показатель ХС ЛПВП ХС ‒ это коэффициент общего холестерина в составе плазме крови; ХСЛПВП ‒ это концентрация в крови высокомолекулярного холестерина. Показания атерогенности Нормативный показатель коэффициента атерогенности ‒ от 2,0 до 3,0; Отклонения коэффициента в сторону повышения до 4,0; При коэффициенте выше 4,0 также необходима диета с низким содержанием холестерина в продуктах питания. 10. Гормональная регуляция липолиза и липогенеза Липолиз является важнейшим энергетическим процессом в клетке, который обеспечивает синтез самого большого количества АТФ. На процесс липолиза оказывают стимулирующее воздействие гормоны глюкагон, адреналин и тироксин (у взрослых). Противоположное действие оказывает инсулин, который стимулирует фосфодиэстеразу, расщепляющую цАМФ ‒ молекулу вторичного посредника, что тормозит процесс липолиза. Липогенез ‒ это процесс, посредством которого ацетил-КоА превращается в жирные кислоты. Липогенез включает как процесс синтеза жирных кислот, так и синтез ТАГ. Гормональная регуляция Инсулин стимулирует липогенез, главным образом, путем активации двух ферментативных путей. Пируватдегидрогеназа (ПДГ) превращает пируват в ацетил-КоА. Ацетил-КоА-карбоксилаза (АКК) превращает ацетил-КоА, продуцируемый ПДГ, в малонил-КоА. Малонил-КoA обеспечивает двухуглеродистые строительные блоки, которые используются для синтеза жирных кислот. Инсулиновая стимуляция липогенеза также происходит путем стимулирования поглощения глюкозы жировой тканью. Гормон, который препятствуют стимуляции липогенеза в жировых клетках, это гормон роста. Он приводят к потере жира, но стимулирует усиление роста мышц. Соматотропин оказывает мощное анаболическое и анти-катаболическое действие, усиливает синтез белка и тормозит его распад, а также способствует снижению отложения подкожного жира, усилению сгорания жира и увеличению соотношения мышечной массы к жировой Заключение Одна из важных функций липидов – источник энергии. β-Окисление жирных кислот является одним из главных источников АТФ. Этот процесс протекает только в аэробных условиях в матриксе митохондрий. При таких состояниях, как голодание, сахарный диабет I типа, длительные физические нагрузки, клетки органов и тканей испытывают жёсткий дефицит энергии. В этом случае печень начинает синтезировать кетоновые тела (ацетоацетат, 3-гидроксибутират, ацетон), которые, кроме ацетона, могут служить источником АТФ. Процесс повышения содержания кетоновых тел в крови называется гиперкетонемией. Увеличение уровня кетоновых тел в крови приводит к ацидозу. Ацидоз – это смещение кислотно-щелочного баланса организма в сторону увеличения кислотности (уменьшению рН). Кетонурия, ацетонурия – это состояние, когда кетоновые тела появляются в моче. В состоянии покоя или после еды очень активно происходит биосинтез жирных кислот в цитозоле клеток печени, кишечника, жировой ткани. Синтез жирных кислот осуществляется с помощью ферментного комплекса – синтазы жирных кислот. Эйкозаноиды – окисленные производные полиненасыщенных жирных кислот, содержащих 20 углеродных атомов, участвуют во множестве процессов, таких как рост мышечной ткани, раздражение и реакциях иммунитета на введенные токсины и патогены. Некоторые эйкозаноиды являются нейромедиаторами. Выделяют несколько семейств эйкозаноидов. Реакции биосинтеза липидов (липогенез) могут идти при участии ферментов гладкой эндоплазматической сети клеток всех органов. Субстратом для синтеза жиров de novoявляется глюкоза. Начальные реакции синтеза триацилглицеролов и фосфолипидов совпадают и происходят при наличии глицерола и жирных кислот. Триацилглицеролы – основная форма запасания энергии. Фосфолипиды – основной структурный компонент биомембран. Распад триацилглицеролов (липолиз) идет в жировых клетках постоянно и может активироваться в результате эмоционального стресса, мышечной работы, голодании, а также при таких патологических состояниях, как сахарный диабет I типа, гипертиреозе и др. Нарушения липидного обмена приводят к возникновению целого ряда заболеваний. Гепатозы ‒ это группа заболеваний печени, в основе которых лежит нарушение обмена веществ в гепатоцитах и развитие в этих клетках дистрофических изменений. Различают жировые и пигментные гепатозы, имеющие острое и хроническое течение. Липотропные вещества (структурные компоненты фосфолипидов, метионин, пиридоксин, цианкобаламин) являются важными факторами, способствующими нормализации обмена липидов и холестерола в организме, стимулируют мобилизации жира из печени и его окисление, что ведёт к уменьшению степени выраженности жировой инфильтрации печени. Холестерол – важное соединение липидной природы, придающее биомембранам жёсткость, играющее роль предшественника стероидных гормонов, витаминов группы D, жёлчных кислот. Жёлчные кислоты – это производные холановой кислоты, содержащиеся в жёлчи, эмульгируют жиры и участвуют в мицеллообразовании, активизируют моторику тонкой кишки, стимулируют продукцию слизи и гастроинтестинальных гормонов. Транспортной формой липидов в крови являются липопротеины, которые представляют собой комплексы, состоящие из белков и липидов. Различают 4 класса липопротеинов (ЛПОНП, ЛППП, ЛПНП, ЛПВП, ХМ), каждый из которых выполняет специфические функции. Вследствие нарушения липидного и белкового обмена может возникнуть такое хроническое заболевание артерий эластического и мышечно-эластического типа, как атеросклероз. Существует несколько предположений относительно возможных причин возникновения атеросклероза. Процессы синтеза и распада липидов находятся под контролем эндокринной системы. На процесс липолиза оказывают стимулирующее воздействие гормоны глюкагон, адреналин и тироксин (у взрослых). Противоположное действие оказывает инсулин, который стимулирует фосфодиэстеразу, расщепляющую цАМФ ‒ молекулу вторичного посредника, что тормозит процесс липолиза. Инсулин стимулирует липогенез. Гормон, который препятствуют стимуляции липогенеза в жировых клетках, это гормон роста. Он приводят к потере жира, но стимулирует усиление роста мышц. |
