Общие сведения о высокомолекулярных соединениях
 Скачать 0.64 Mb. Скачать 0.64 Mb.
|
РАДИКАЛЬНАЯ ПОЛИМЕРИЗАЦИЯПо этому механизму полимеризуются, как правило, мономеры типа I и, прежде всего, соединения со связью С=С. Наиболее типичные мономеры - монозамещенные этилена СН2=СН(Х) (винильные мономеры) и 1,1-дизамещенные этилена СН2=СХ(Y), где Х,Y – алкильные, арильные, гетарильные фрагменты, разнообразные функциональные группы (в случае самого этилена Х=Н). А. ИнициированиеСуть процесса инициирования – превращение молекулы мономера в радикал; для этого в молекуле мономера должен произойти гомолитический разрыв какой-либо связи. Инициирование может осуществляться: а) одноступенчато, т.е. неким энергетическим воздействием непосредственно на мономер, в результате которого он превращается в радикал; б) двухступенчато – воздействием на специальную добавку – инициатор –, который легко образует радикалы (1-я ступень); далее радикал, образовавшийся из инициатора, присоединяется к мономеру, превращая его в радикал (2-я ступень). Инициирование путем непосредственного воздействия на мономер. Непосредственное превращение мономера (как любой другой молекулы) в радикал можно осуществить:
Термическое инициирование протекает с достаточной скоростью, как правило, лишь при температурах порядка 200 оС; исключение составляют лишь немногие мономеры, в частности, стирол. Предполагается (в качестве одного из вариантов), что инициирование происходит путем диспропорционирования двух молекул мономера с передачей атома водорода и образованием двух радикалов: 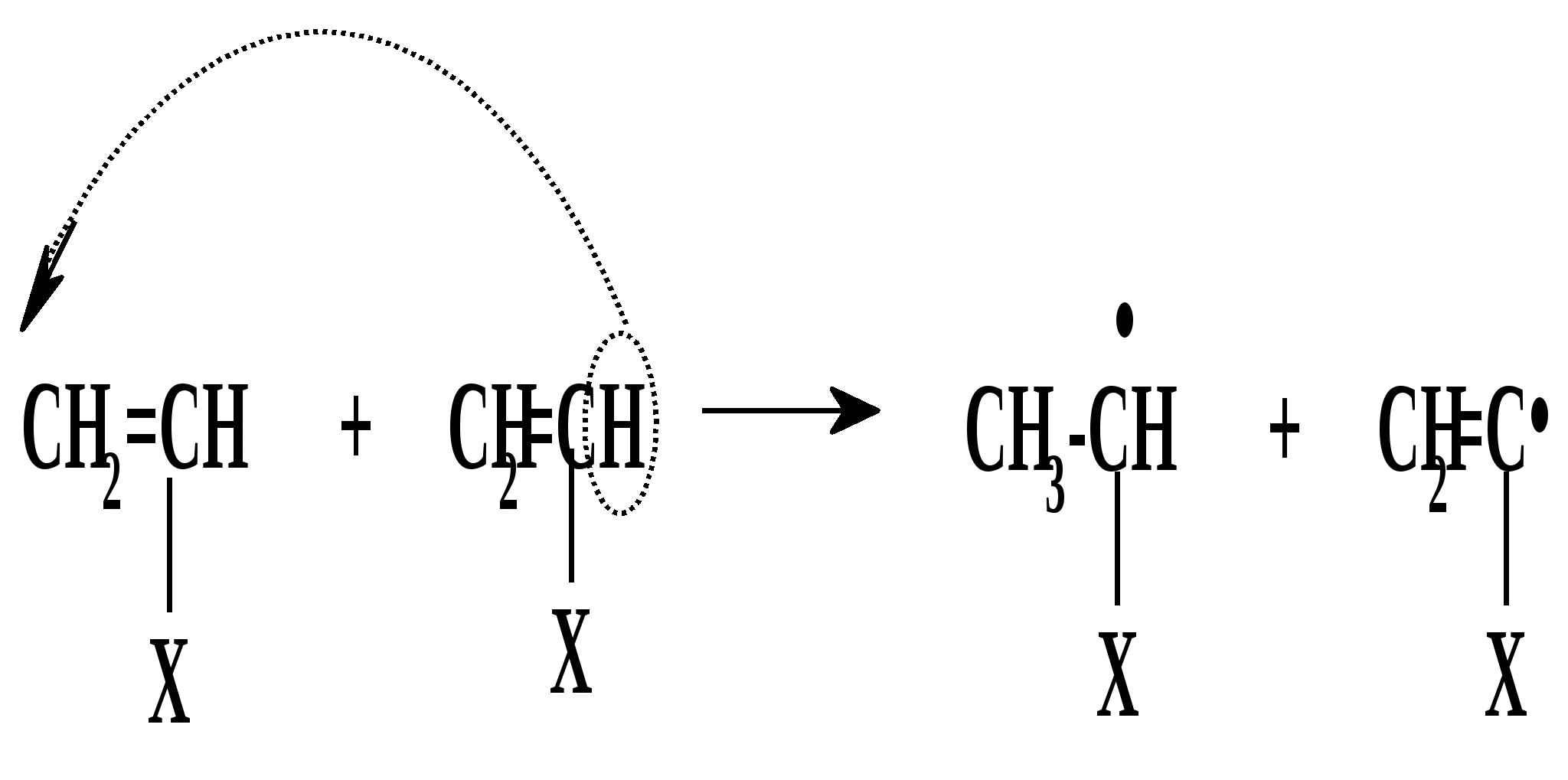 Как будет ясно из последующего, полимеризация при столь высоких температурах крайне неблагоприятно сказывается на качестве получаемых полимеров (падает молекулярная масса и, что особенно существенно, нарушается регулярность строения макромолекул). Поэтому термическая полимеризация непосредственно мономеров не имеет практического использования и осуществляется только в научных исследованиях. Фотохимическое инициирование обычно проводят, облучая мономер светом с длиной волны порядка 300 нм. При этом вначале происходит фотовозбуждение молекул мономера, а затем образование радикалов. Предполагается, что такое образование может происходить по той же бимолекулярной схеме, что и при термическом инициировании, а, кроме того, по мономолекулярным схемам: В 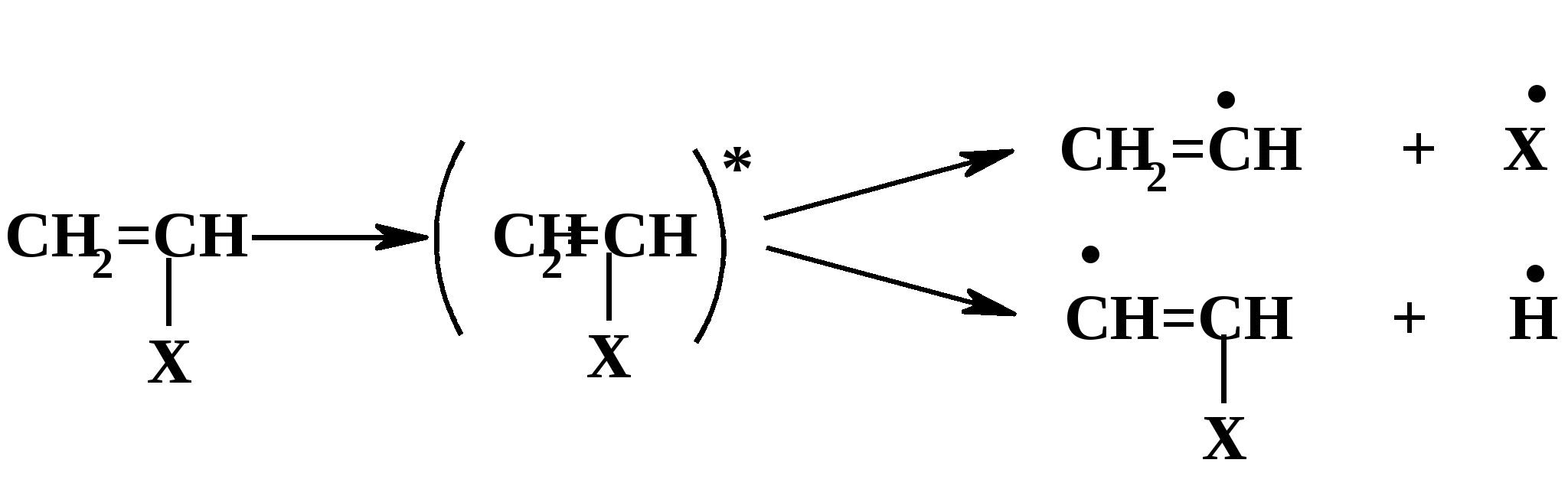 отличие от термического инициирования, этой вариант пригоден для практического использования: инициирование можно проводить при обычных температурах; дозируя интенсивность излучения, можно регулировать скорость инициирования (v), используя простое соотношение: v = kI1/2 где I – интенсивность излучения, k – константа, зависящая от природы мономера. Используя инициирование с помощью лазерного излучения, можно значительно сузить интервал частот излучения. Фотоиницирование иногда используют в промышленных процессах, но все же наиболее часто – в лабораторной практике при изучении процессов полимеризации. Радиационное инициирование протекает под воздействием α-, β-, γ-излучений, нейтронов. Кинетические закономерности радиационного инициирования во многом напоминают фотоинициирование. Радикалы, в принципе, могут образовываться по тем же схемам, что и при фотоиницировании, но, вследствие более высоких энергий ионизирующих излучений, могут возникать также ион-радикалы и ионы («выбивание» электрона из молекулы мономера с образованием катион-радикала или захват электрона молекулой мономера с образованием анион-радикала; далее ион-радикалы могут фрагментировать): Т 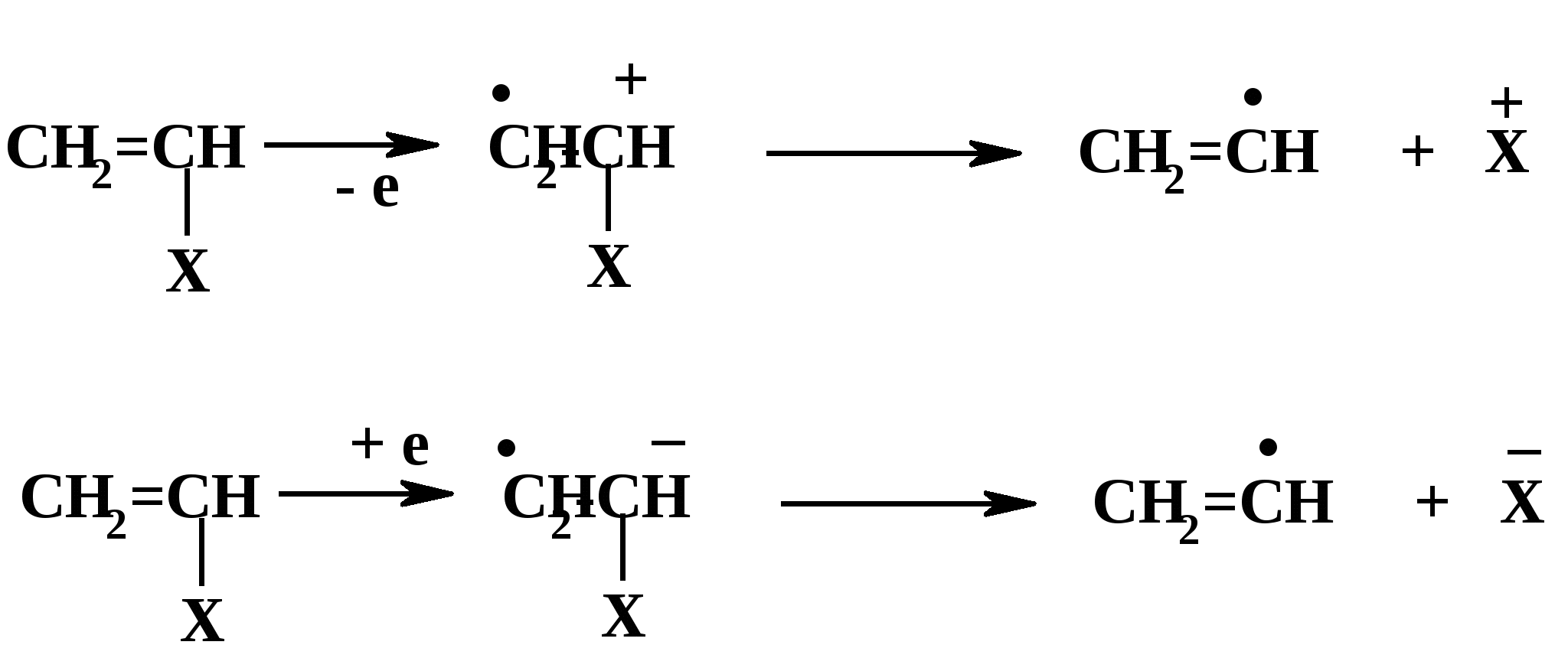 аким образом, в принципе, при радиационном инициировании возможна не только радикальная, но и ионная полимеризация, однако чаще всего протекает радикальная; ионную можно осуществить только при низких температурах. 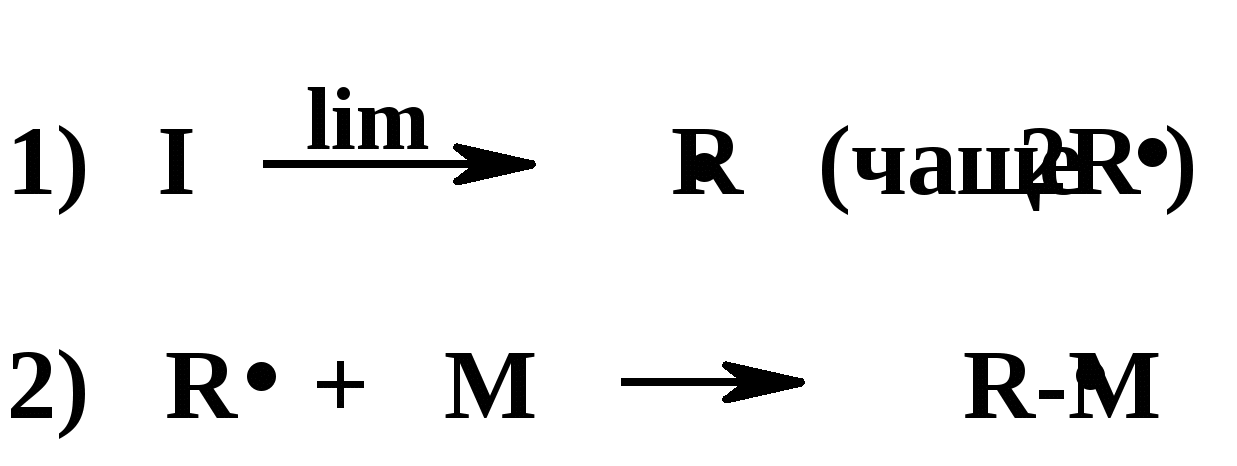 Инициирование с использованием инициаторов. Радикальная полимеризация с использованием инициаторов применяется наиболее часто. Инициирование осуществляется в две стадии по общей схеме: I – инициатор, который легко генерирует радикалы. На первой стадии происходит генерация радикалов из молекулы инициатора; в большинстве случаев из молекулы инициатора образуется два радикала. На второй стадии радикал, образованный из инициатора, присоединяется к молекуле мономера, превращая ее в радикал. Скоростьопределяющей (лимитирующей) чаще всего является первая стадия. Первая стадия. Генерация радикалов из инициатора может идти фотохимически, радиационно, электрохимически (при реакции Кольбе – электролизе солей карбоновых кислот). Но чаще всего используют термический распад инициаторов; такой распад происходит при относительно невысоких температурах (обычно не превышающих 100 оС); при таких температурах полимеризация протекает удовлетворительно. В отдельных случаях инициирование может происходить и при обычных температурах. Наиболее часто используемые инициаторы – пероксидные соединения и азосоединения. 1) Пероксидные соединения – пероксиды и гидропероксиды. Используются: А) Неорганические соединения: пероксид водорода НО–ОН, персульфаты KO-SO2-O–O-SO2-OK; эти инициаторы используются для проведения полимеризации в водных средах (например, эмульсионной полимеризации). Б) Органические: бензоилпероксид PhCO-O–O-COPh, трет-бутилгидропероксид t-BuO–OH, гидропероксид кумола PhC(CH3)2O–OH и некоторые другие; они используются для проведения полимеризации в среде чистого мономера (в блоке) или в среде органических растворителей, а также при суспензионной полимеризации. Легкость образования радикалов из пероксидных соединений обусловлена наличием «слабой» связи О–О, которая легко разрывается гомолитически (энергия активации порядка 110-170 кДж/моль): Б 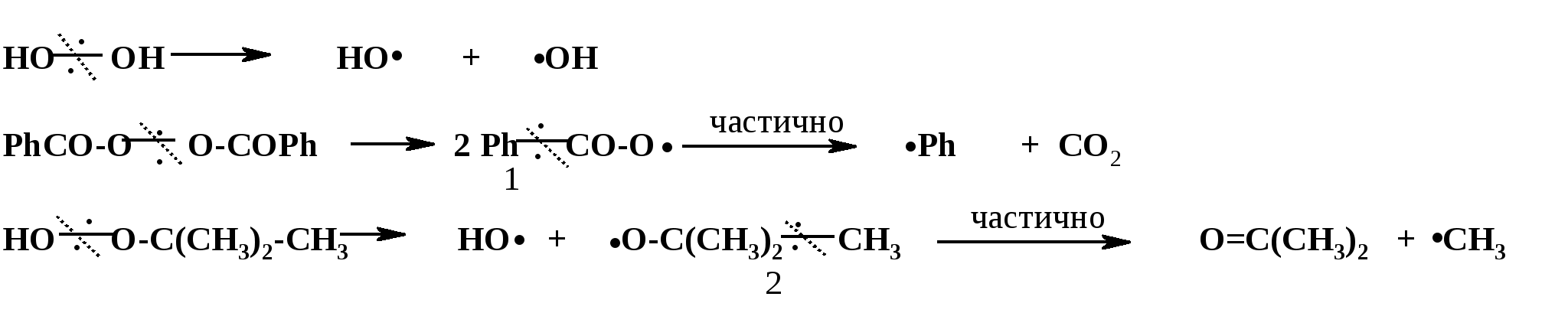 ензоилокси- (1) и алкилокси- (2) радикалы, по крайней мере, частично подвергаются фрагментации с образованием соответственно арильных и алкильных радикалов. Бензоилпероксид эффективно распадается при 80-90 оС, трет-бутилгидропероксид – около 100 - 110 оС. 2. Азосоединения склонны к гомолитическому распаду с выделением термодинамически весьма стабильной молекулы азота, что и обусловливает легкость образования радикалов. Наиболее широко используемый инициатор этого типа – легкодоступный азобисизобутиронитрил (АИБН):  АИБН Этот инициатор эффективен при 50-70 оС и используется для проведения полимеризации в неводных средах. Окислительно-восстановительное инициирование. Температуру инициирования можно снизить до комнатной и даже до более низких значений, если применять комбинацию пер- оксидного инициатора с одноэлектронным восстановителем. Наиболее простой пример – смесь пероксида водорода и иона Fe2+, применяемая для полимеризации в водных средах: НО-ОН + Fe2+ → HO‾ + • OH + Fe3+ Распад инициатора здесь происходит заметно легче (Е активации порядка 50 кДж/моль), потому что образуется гидроксид-анион, более устойчивый, чем гидроксид-радикал. Для полимеризации в органических средах используют смесь бензоилпероксида и вторичного или третичного ароматического амина: З 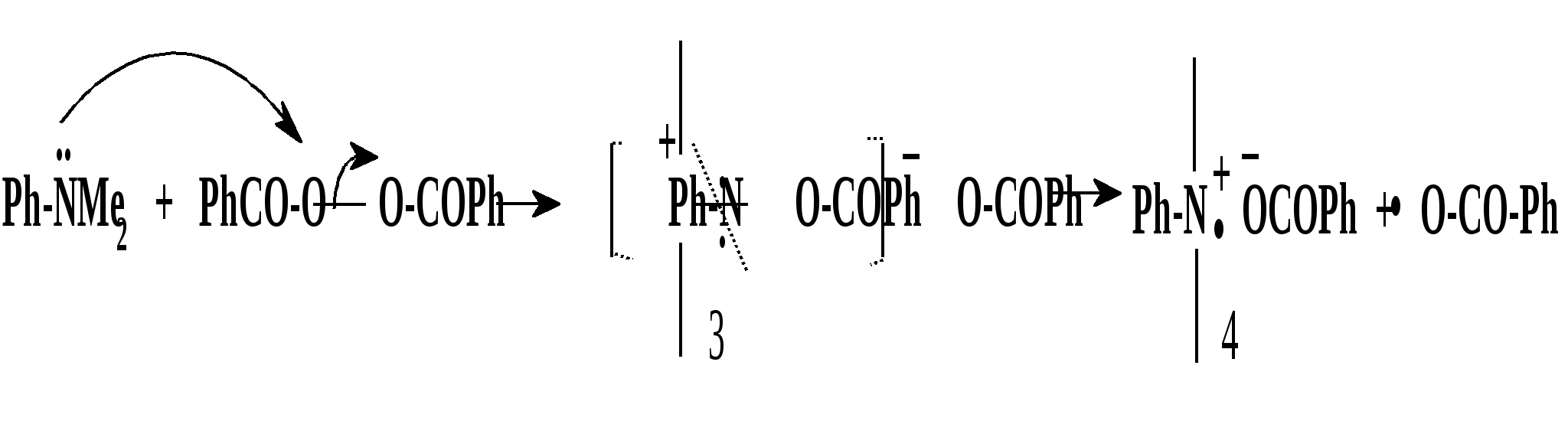 десь промежуточно образуется четвертичная соль (3), которая далее гомолитически распадается с образованием анион-радикальной соли (4) и бензоилокси-радикала; образование устойчивого бензоат-аниона способствует легкому распаду бензоилпероксида. В последнее время помимо традиционных инициаторов используют инициаторы новых типов – полифункциональные пероксиды и инифертеры. Особенности их использования будут рассмотрены позднее (т.к. они участвуют не только в инициировании, но и в последующих процессах). 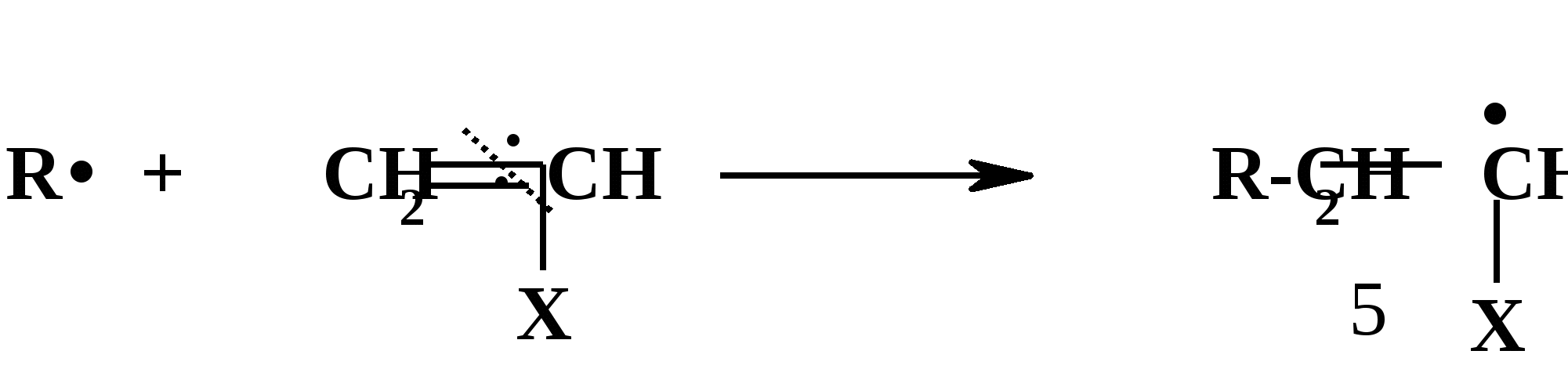 Вторая стадия протекает по схеме (для винильных мономеров): Радикал, образовавшийся из инициатора, присоединяется к винильному мономеру с гомолизом π-связи, превращая его в мономерный радикал (5). Во второй стадии участвуют не все радикалы, образовавшиеся из инициатора; часть этих радикалов вступает в побочные реакции, самой распространенной из которых являетcя рекомбинация в момент образования (первичная рекомбинация), например, образование бифенила при использовании бензоилпероксида: Ph▪ + ▪Ph → Ph–Ph Доля первично образовавшихся радикалов, которая принимает участие во второй стадии инициирования (т.е. присоединяется к мономеру), называется эффективностью инициатора и обозначается символом f; для большинства инициаторов 0,3 < f < 0,8. Для успешного протекания полимеризации необходимо, чтобы концентрация инициирующих радикалов была малой (10-6 – 10-8); только при этом условии может быть достигнуто необходимое соотношение скоростей реакций роста и обрыва цепи (см. ниже). Таким образом, скорость распада инициатора должна быть малой; единовременно распадается лишь очень малая его доля. В связи с этим концентрация инициатора в реакционной смеси обычно невелика (порядка 1%). Рост кинетической цепи Это – главный этап радикальной ( и любой цепной) полимеризации – здесь формируется полимерная цепь. Суть роста цепи – последовательное присоединение радикалов к молекулам мономеров: Р 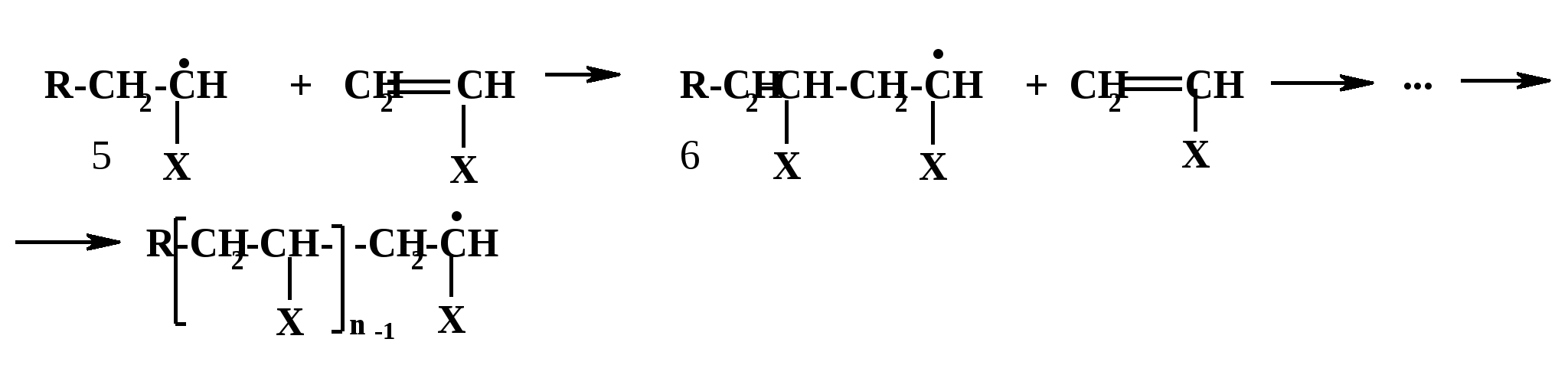 адикал (5), возникший при инициировании, присоединяется к молекуле мономера; образовавшийся при этом димерный радикал (6) присоединяется к следующей молекуле мономера; аналогичные элементарные реакции многократно повторяются. Таким образом, рост кинетической цепи сопровождается ростом молекулярной цепи. Растущая полимерная цепь представляет собой радикал с неспаренным электроном на концевом атоме («концевой» радикал). При достаточном числе звеньев это полимерный радикал (макрорадикал). Для макрорадикалов (как «концевых», и «неконцевых») и для других полимерных активных центров (макроионов и др.) принят термин «живые полимеры» или «живые цепи». Если мономер несимметричный (а таких явное большинство), возникает вопрос о региоселективности и регионаправленности реакций роста цепи. Действительно, взаимодействие несимметричного радикала с несимметричным мономером может протекать по нескольким вариантам: 1. Более замещенный радикал присоединяется к менее замещенному атому мономера; так изображен рост цепи на приведенной выше схеме [см., например, образование (6)]. При этом мономерные звенья соединяются по типу «голова к хвосту» (head to tail), если считать менее замещенный атом звена «головой», а более замещенный – «хвостом». 2. Более замещенный радикал присоединяется к более замещенному атому мономера; возникает соединение по типу «хвост к хвосту» (7). 3. Менее замещенный радикал (возникший по варианту 2) присоединяется к менее замещенному атому мономера; это приводит к соединению по типу «голова к голове» (8). 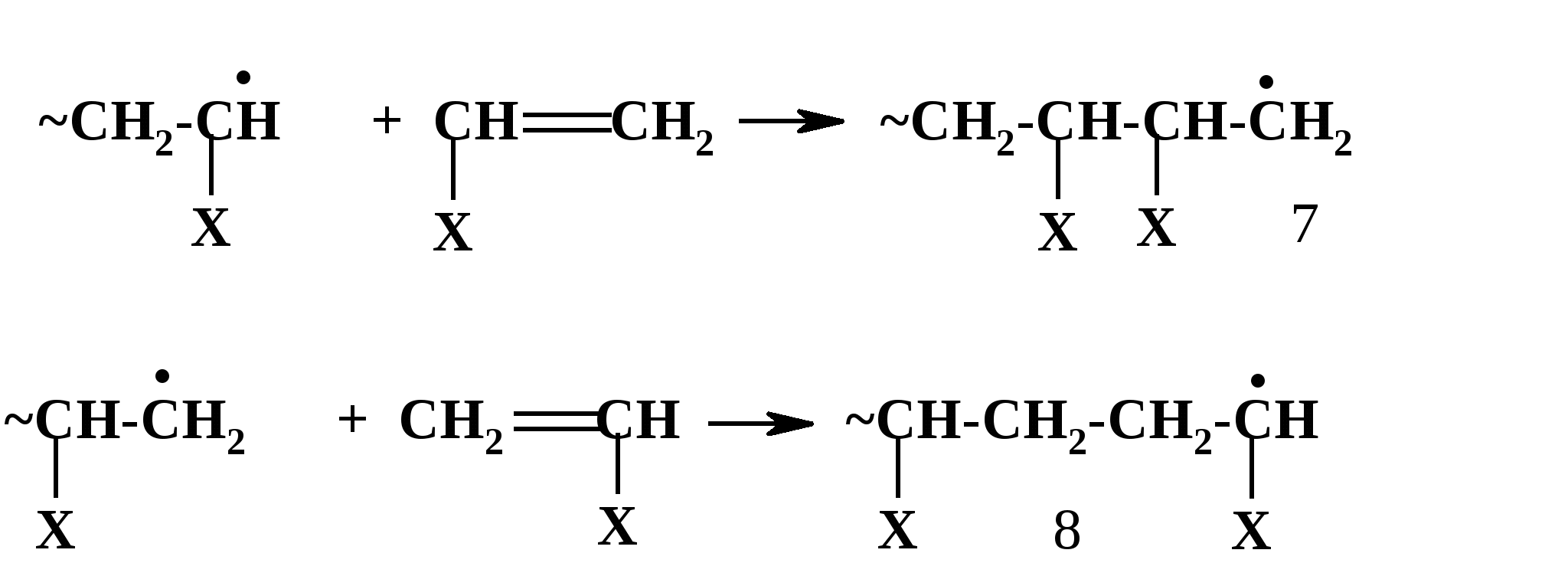 Нетрудно заметить, что вариант 1 энергетически предпочтительнее варианта 2: во-первых, потому, что при этом образуется более замещенный (т.е. более устойчивый) радикал, а во-вторых, потому, что в соединении звеньев «хвост к хвосту» пространственное напряжение выше, чем в соединении «голова к хвосту». Поэтому в ходе роста цепи вариант 1 преобладает (вариант 3 требует предварительного протекания варианта 2), и в итоге большинство звеньев соединяются по схеме «голова к хвосту». Такая региоселективность обеспечивает достаточную регулярность строения макромолекулы, а это благоприятно сказывается на свойствах полимера. Все же некоторое количество «нестандартных» сочленений звеньев включается в полимерные цепи; их число возрастает при повышении температуры полимеризации; таким образом, чем выше температура полимеризации, тем менее регулярно построена макромолекула. Энергия активации реакций роста цепи весьма невелика – от 10 до 40 кДж/моль; это связано с тем, что одной из реагирующих частиц является весьма реакционноспособный радикал. Поэтому скорости реакций весьма высоки: величины констант скоростей роста (kp) составляют 102 – 104 л/моль∙сек. Сами скорости роста в зависимости от строения мономеров могут довольно заметно различаться ( чем более устойчивый радикал образуется из мономера, тем меньше скорость роста); однако в любом случае они остаются очень высокими. Обычно за время порядка 10 секунд может образоваться цепь, содержащая сотни и даже тысячи звеньев. Иными словами, время формирования отдельной макромолекулы намного меньше продолжительности полимеризации; иными словами, макромолекулы с очень большой молекулярной массой образуются уже с самого начала процесса (при малых глубинах конверсии мономера); это – специфическая особенность радикальной полимеризации. Обрыв кинетической цепи 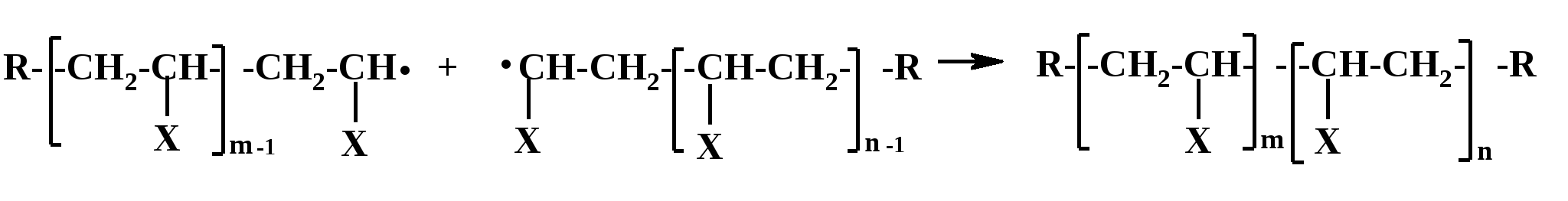 Этот этап завершает формирование полимерной цепи. В результате этих реакций исчезают активные центры – радикалы; «живые» полимеры (цепи) превращаются в стабильные («мертвые») макромолекулы. Обрыв кинетической цепи радикальных цепных реакций происходит при встрече двух радикалов. В большинстве случаев происходит встреча двух растущих («живых») цепей. При этом возможны два варианта их взаимодействия: 1. Рекомбинация – соединение двух радикалов: При этом из двух «живых» цепей образуется одна стабильная («мертвая») макромолекула. На обоих концах этой макромолекулы находятся осколки инициатора (R). 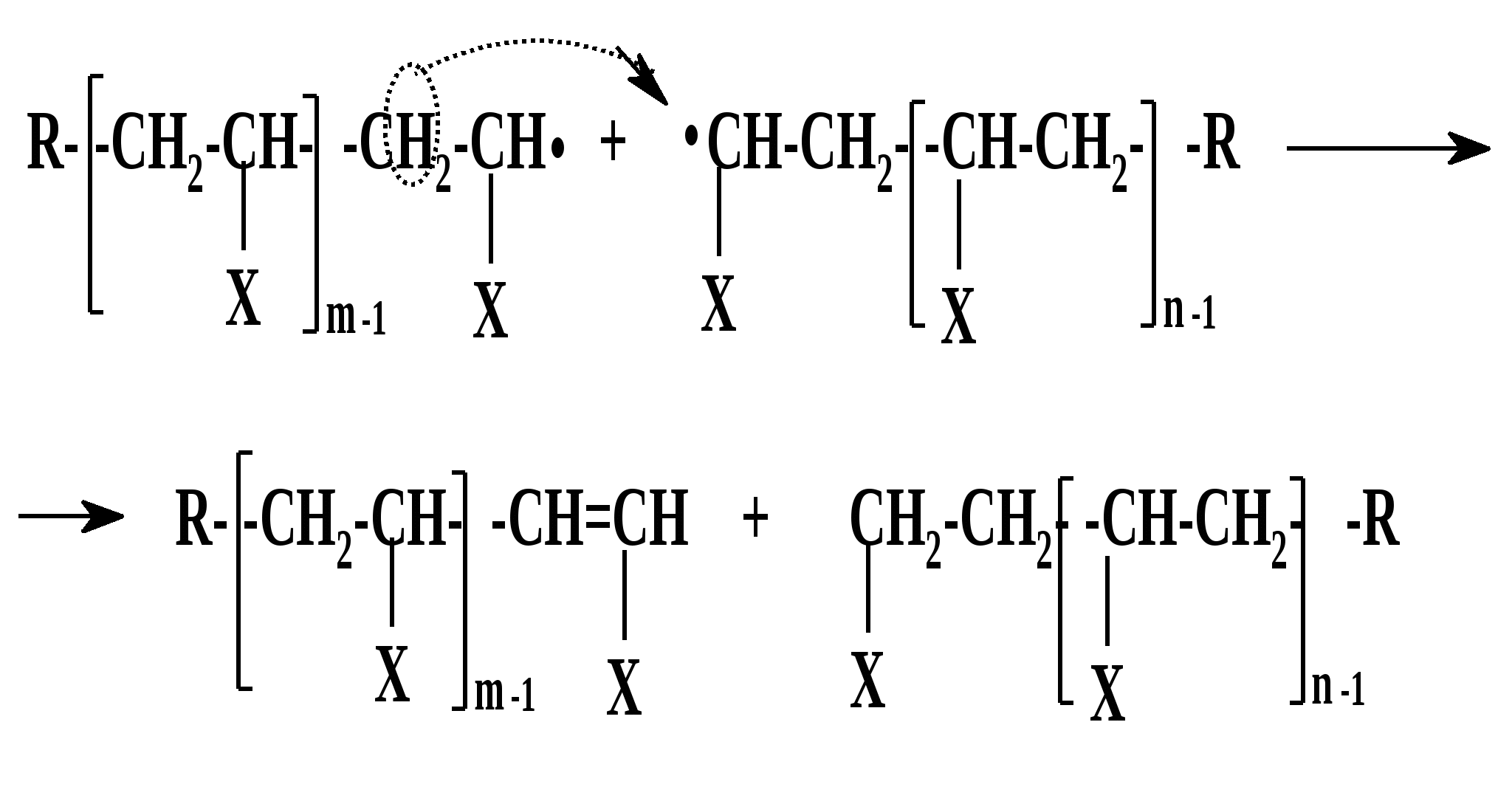 2. Диспропорционирование – передача атома водорода от одной «живой» цепи к другой: При этом из двух «живых» цепей образуется две стабильные макромолекулы. На одном конце такой макромолекулы находится осколок инициатора, на другом – двойная связь или насыщенное звено. Рекомбинация кажется более выгодным вариантом и, действительно, происходит чаще, чем диспропорционирование. Однако, если рекомбинация связана со стерическими затруднениями (например, при полимеризации 1,1-дизамещенных производных этилена), диспропорционирование становится «конкурентоспособным»; например, при полимеризации стирола преобладает рекомбинация, а при полимеризации метилметакрилата СН2=С(СН3)СООСН3 в заметной степени протекает диспропорционирование. Доля реакций диспропорционирования повышается также с ростом температуры. Но и та и другая реакция протекают с исключительно высокими скоростями (энергия активации составляет всего 2-6 кДж/моль); это естественно, поскольку здесь реагируют две активные частицы. Константы скоростей реакций обрыва цепи намного (на несколько порядков) выше констант скоростей роста цепи. Тем не менее, кинетические цепи могут достигать очень большой длины, потому что вероятность встречи двух радикалов на много порядков меньше вероятности встречи радикала с молекулой мономера. Такая малая вероятность обусловлена малой единовременной концентрацией радикалов в реакционной смеси (см. выше), а также тем, что при встрече двух макрорадикалов (фактически двух полимерных клубков, содержащих атом с неспаренным электроном) должно произойти сближение именно тех атомов, при которых находятся неспаренные электроны, что происходит отнюдь не при каждом столкновении, а лишь при их малом числе.Поэтому скорости реакций обрыва цепи обычно на несколько порядков меньше, чем скорости роста цепи. Длина кинетической цепи определяется соотношением скоростей роста и обрыва цепи: d = vp/vo  Средняя степень полимеризации (Р) равна удвоенной длине цепи при обрыве путем рекомбинации (из двух цепей образуется одна макромолекула) или длине цепи при обрыве путем диспропорционирования; в общем случае: d < P ≤ 2d Теперь можно посмотреть на весь процесс радикальной полимеризации в дифференциальном и интегральном аспектах Дифференциальный аспект – как выглядит формирование единичной макромолекулы. Если попытаться представить изменения энергии (энергетический профиль) формирования единичной макромолекулы, то это выглядит примерно так (рис.2):   Рис. 2 Энергетический профиль формирования полимерной цепи при радикальной полимеризации. Инициирование (точнее его первая стадия – распад инициатора) требует наибольшей энергии активации («пусковая кнопка» процесса); растущая кинетическая цепь – набор растущих по величине радикальных интермедиатов; обрыв цепи практически не требует энергии активации. Энергетический профиль формирования цепи для так называемых ступенчатых процессов (ступенчатой полимеризации и поликонденсации), совсем иной, как будет показано ниже. Интегральный аспект – как меняется вся реакционная система в ходе процесса. Учитывая: 1) постепенный, медленный распад инициатора; 2) весьма малую единовременную концентрацию растущих цепей; 3) очень малое время роста единичной цепи, можно представить общую картину протекания радикальной полимеризации. Реакционная смесь практически от начала до конца процесса полимеризации представляет собой смесь непрореагировавшего мономера, «мертвого» полимера и очень малого количества «живых» цепей. По мере протекания процесса на смену оборвавшимся цепям возникают новые «живые» цепи, которые столь же быстро обрываются; количество «мертвого полимера постепенно растет, количество мономера уменьшается. При этом уже в начале процесса образуются полимеры с высокой молекулярной массой; поэтому можно останавливать реакцию на малых глубинах и выделять полноценный полимер (это часто используется при исследовании, например, процессов сополимеризации). В приведенную картину вносят коррективы рассмотренные ниже реакции передачи цепи и кинетические отклонения (гель-эффект и др.), но в своей основе ее суть не меняется. Такая картина принципиально отличается от ступенчатых процессов, в которых вначале образуются лишь олигомеры, и полимерные цепи постепенно растут по ходу процесса. Реакции передачи цепи при радикальной полимеризации. 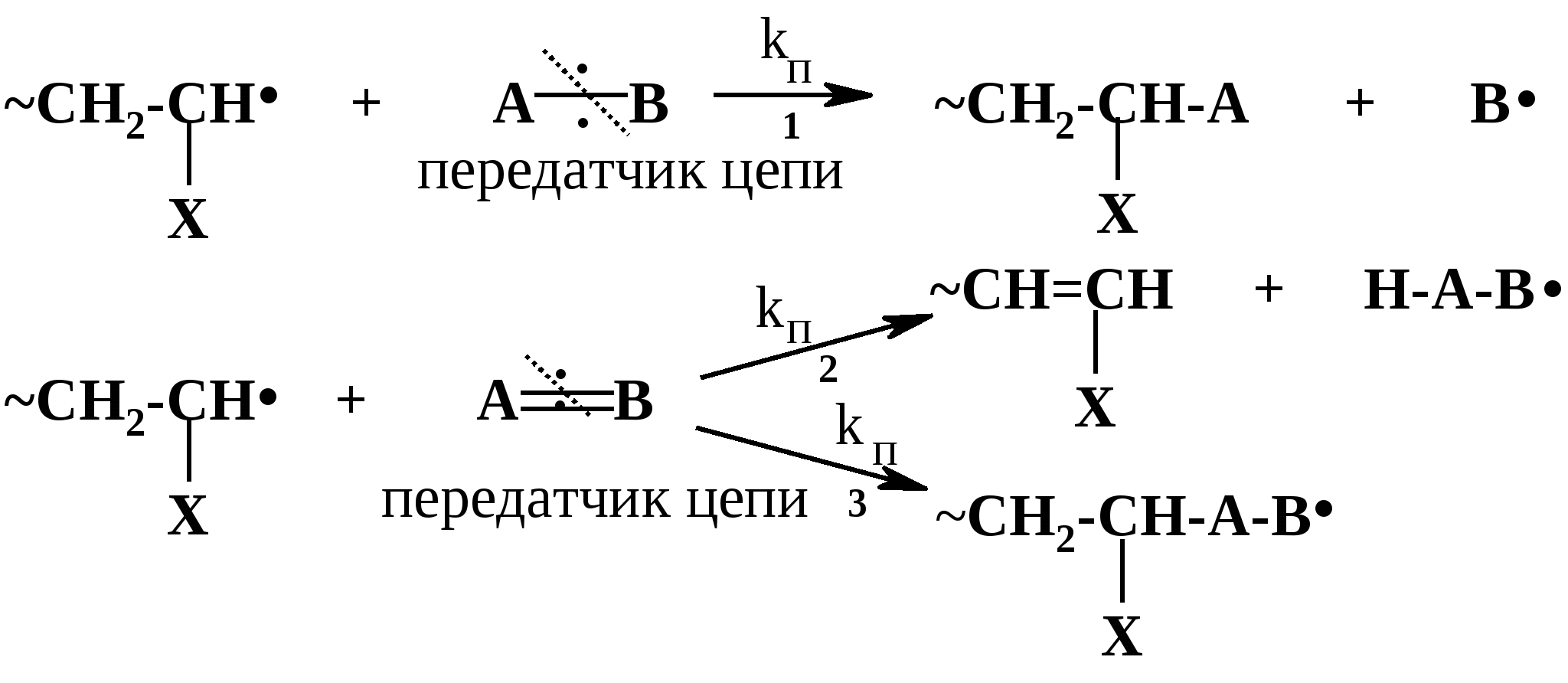 В подавляющем большинстве случаев протекание радикальной полимеризации не ограничивается тремя рассмотренными выше процессами – инициированием, ростом кинетической цепи по схеме присоединения радикала к мономеру и обрывом цепи. Реакции роста кинетической цепи обычно сопровождаются побочными процессами – реакциями передачи цепи. Суть этих реакций – взаимодействие растущей цепи с какими-либо молекулами (называемыми передатчиками цепи или агентами передачи цепи), причем активный центр (неспаренный электрон) передается на такую молекулу. Процессы передачи цепи (для полимеризации винильных мономеров) могут быть представлены общими схемами: Пожалуй, наиболее часто реакции идут по схеме 1. В зависимости от мономера и присутствия передатчиков реакции передачи цепи могут играть разную роль – от относительно небольшой до доминирующей. Следствием передачи цепи по схемам 1 и 2 является обрыв молекулярной цепи при сохранении кинетической (т.е. активного центра). Таким образом, эти реакции ведут к уменьшению длины полимерной цепи, т.е. молекулярноймассы полимера. Это уменьшение тем больше, чем чаще идут реакции передачи цепи; степень этого уменьшения может меняться в весьма широких пределах – вплоть до полного ингибирования полимеризации. Степень участия реакций передачи цепи на тот ли иной агент выражается константой передачи цепи, равной отношению констант скоростей передачи цепи (kп) и роста цепи (kр): Сп = kп/kр Как влияют процессы передачи цепи на скорость полимеризации? Это зависит от характера того радикала, который образуется при передаче цепи. Здесь возможны два основных варианта: 1) При передаче цепи возникает активный радикал, который способен легко присоединяться к мономеру. В этом случае он и присоединяется к мономеру и тем самым инициирует новую молекулярную цепь, например, для передачи по пути 1: 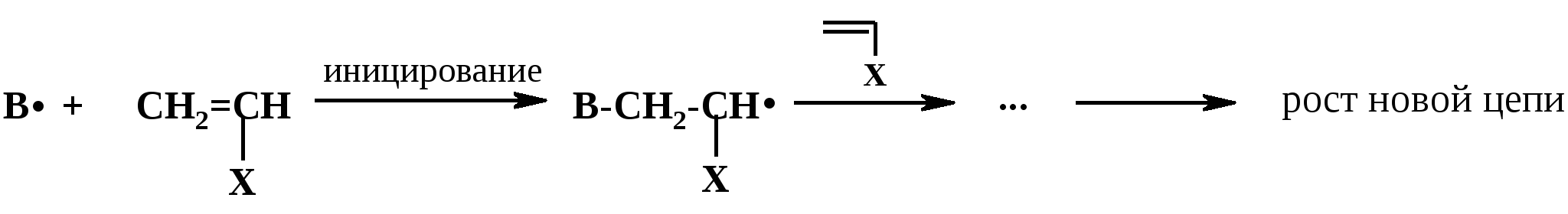 В этом случае скорость полимеризации не падает, уменьшается только молекулярная масса полимера. 2) Радикал, возникший при передаче цепи, малоактивен или совсем неактивен; он либо с трудом присоединяется к мономеру, либо вовсе не присоединяется к нему. В этом случае скорость полимеризации уменьшается. Если такие реакции передачи идут очень легко (Сп>>1), а возникший радикал не способен присоединяться к мономеру, то агент передачи «перехватывает» радикалы, возникшие из инициатора (или образовавшиеся иным путем), и полимеризация вообще не происходит – она ингибируется. Возникшие малоактивные радикалы либо существуют как таковые (если они долгоживущие), либо подвергаются рекомбинации или диспропорционированию; таким образом, вслед за передачей цепи следует непосредственно обрыв кинетической цепи. В качестве передатчиков цепи могут выступать: 1) молекулы инициатора; 2) молекулы мономера; 3) молекулы посторонних веществ (случайно попавших или специально введенных в реакционную смесь); 4) макромолекулы «мертвого» полимера. 1) Передача цепи на инициатор. Эта реакция может происходить при использовании пероксидных инициаторов:  Радикал RO·, возникший при передаче, естественно, активен (это обычный инициирующий радикал), поэтому на скорости полимеризации такая передача не отражается. Передача на инициаторы – азосоединения – не происходит. Передача на инициатор – пожалуй, наименее важная из реакций передачи цепи. 2) Передача цепи на мономер. Это – реакции взаимодействия «живой» цепи с мономером, идущие не по схеме роста цепи. Наиболее типичный вариант – передача атома водорода от растущей («живой») цепи к молекуле мономера: Э 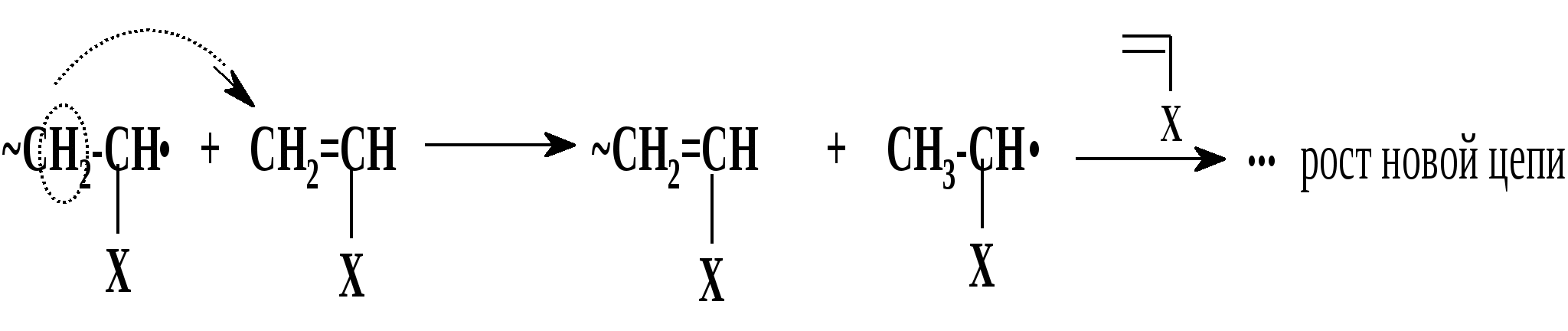 то соответствует схеме 2 (стр. 18). Образовавшийся при этом радикал аналогичен «оборвавшемуся», поэтому немедленно инициируется новая цепь, и скорость полимеризации не меняется. В традиционных системах такие реакции передачи идут с малой скоростью (kп << kр) и не препятствуют формированию больших молекулярных цепей. Однако картина резко меняется при добавлении в систему некоторых катализаторов, в частности, комплексных соединений кобальта. Эти катализаторы служат «передатчиками» атомов водорода от растущих цепей к молекулам мономеров и резко ускоряют передачу цепи. При этом молекулярная масса может уменьшиться настолько, что образуются не высокополимеры, а олигомеры. Поэтому такие катализаторы могут использоваться для регулирования молекулярной массы полимеров или для синтеза олигомеров. Особый случай передачи цепи на мономер наблюдается при полимеризации «аллильных» мономеров, содержащих связь С-Н рядом со связью С=С: З 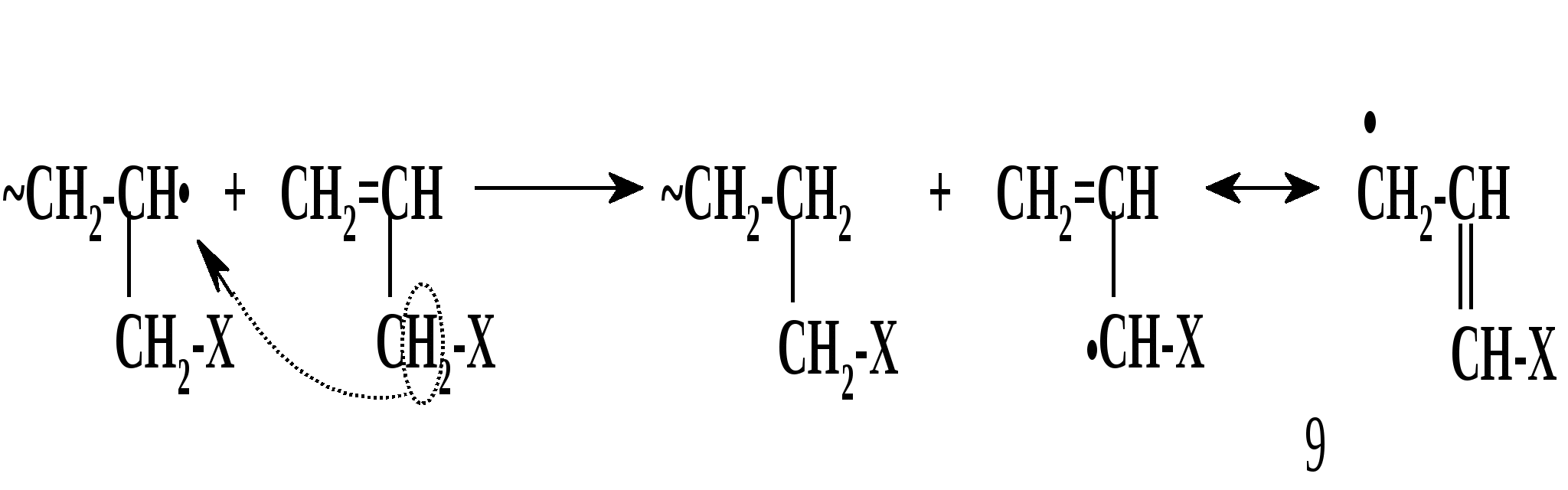 десь, в противоположность предыдущему варианту, происходит передача атома водорода от мономера к растущей цепи (по схеме 1, стр. 18). При этом образуется аллильный радикал (9), стабилизированный резонансной делокализацией неспаренного электрона. Такие радикалы (особенно если группа Х – арильная, винильного типа или ацильная) обычно малоактивны и не могут инициировать рост новой цепи. Этот вариант называется деградационной передачей цепи; он приводит к замедлению или прекращению полимеризации; этот эффект называют аутоингибированием полимеризации аллильных мономеров (мономер ингибирует собственную полимеризацию). 3) Передача цепи на посторонние молекулы. Посторонние молекулы могут попасть в реакционную смесь случайно, но при корректно проводимых процессах полимеризации, передача на такие молекулы не играет сколько-нибудь заметной роли. Гораздо более существенную роль играют реакции передачи цепи на специально введенные соединения; это могут быть добавки или растворители. Использование таких передатчиков преследует одну из двух целей: 1) Регулирование молекулярной массы (точнее, ее регулируемое уменьшение). Это, в основном, необходимо: А) Когда слишком высокая молекулярная масса полимера затрудняет его переработку (например, затрудняет его перевод в расплав или в раствор); Б) Когда нужно получить олигомерные продукты. Передатчики цепи, используемые для регулирования молекулярной массы, называют регуляторами полимеризации. 2) Замедление или чаще ингибирование полимеризации. Ингибирование необходимо для предотвращения полимеризации мономеров при хранении. Передатчики цепи, способствующие достижению этой цели, называют соответственно замедлителями и ингибиторами полимеризации. 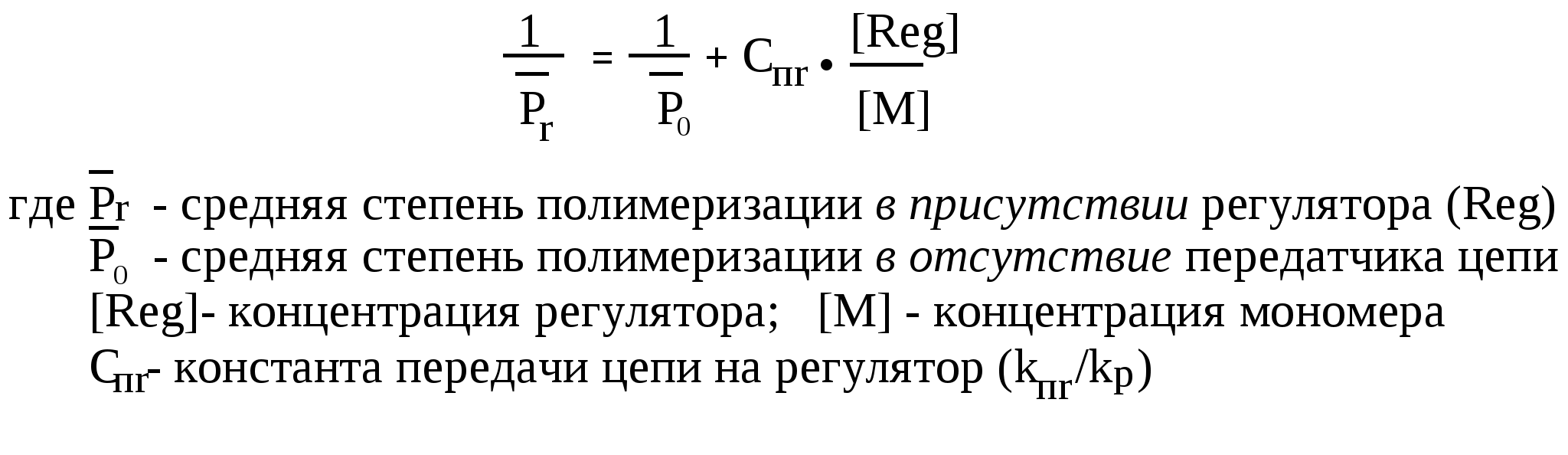 Регуляторы полимеризации не снижают скорости процесса, но уменьшают молекулярную массу его продукта ; естественно, при передаче цепи на регуляторы возникают активные радикалы, инициирующие рост новых цепей. Передача цепи на регулятор должна идти достаточно легко (kп ≡ kпr) не слишком мала); в этом случае она будет основным видом передачи и, дозируя количество регулятора, можно получать полимеры с рассчитанной молекулярной массой. Расчет производится по уравнению (вывод будет дан позже): В качестве регуляторов используют, в основном,: 1) меркаптаны и дисульфиды; 2) полигалогенпроизводные. Меркаптаны (и дисульфиды) используют для регулирования молекулярной массы высокомолекулярных соединений – например, при синтезе бутадиен-стирольных каучуков. Передача цепи идет по схеме:  Полигалогеналканы чаще используют для получения олигомеров. Наиболее известно использование тетрахлорметана СС14, который может применяться в качестве растворителя. Полимеризация при большой концентрации СС14 протекает по схеме: З  десь радикал, возникший из инициатора, вначале взаимодействует с СС14, а затем образовавшийся при этом радикал •СС13 инициирует рост полимерной цепи. Растущая цепь взаимодействует с СС14 с передачей цепи. При большой концентрации СС14 реакции передачи цепи проходят столь часто, что образуются олигомеры (n = 3 – 10). Такой вариант носит название теломеризации, а передатчики цепи (в данном случае СС14) называют телогенами. Варьируя количество телогена, можно регулировать степень полимеризации (n) олигомера. В частности, при теломеризации этилена (Х=Н) в присутствии СС14 можно получать тример (n=3) – 1,1,1,7-тетрахлоргептан (10), который далее превращают в ω-аминоэнантовую кислоту (11) – мономер для синтеза ценного полиамида (путем поликонденсации):  Ингибиторы полимеризации используются очень широко для предотвращения преждевременной полимеризации мономеров. Мономеры, способные полимеризоваться по радикальному механизму всегда хранятся с добавкой ингибитора и перед полимеризацией должны быть от него очищены. При передаче цепи на ингибиторы образуются неактивные радикалы, неспособные присоединяться к мономерам. В качестве ингибиторов обычно используют хиноны или пространственно затрудненные фенолы. Хиноны используются в практике очень широко; один из “стандартных” ингибиторов – гидрохинон; растворенный в мономере, он постепенно окисляется кислородом воздуха в бензохинон, который и является истинным ингибитором. Разумеется, можно прибавлять к мономеру и непосредственно хинон, например, тетрахлорбензохинон (хлоранил). Механизм ингибирования можно представить следующим образом:  Радикал (возникший из инициатора или уже начавшая расти цепь) присоединяется к молекуле хинона (схема 3, стр. 18) – либо по атому кислорода, либо к ядру; образуются малоактивные радикалы (12) или (13) (неспаренный электрон делокализован). 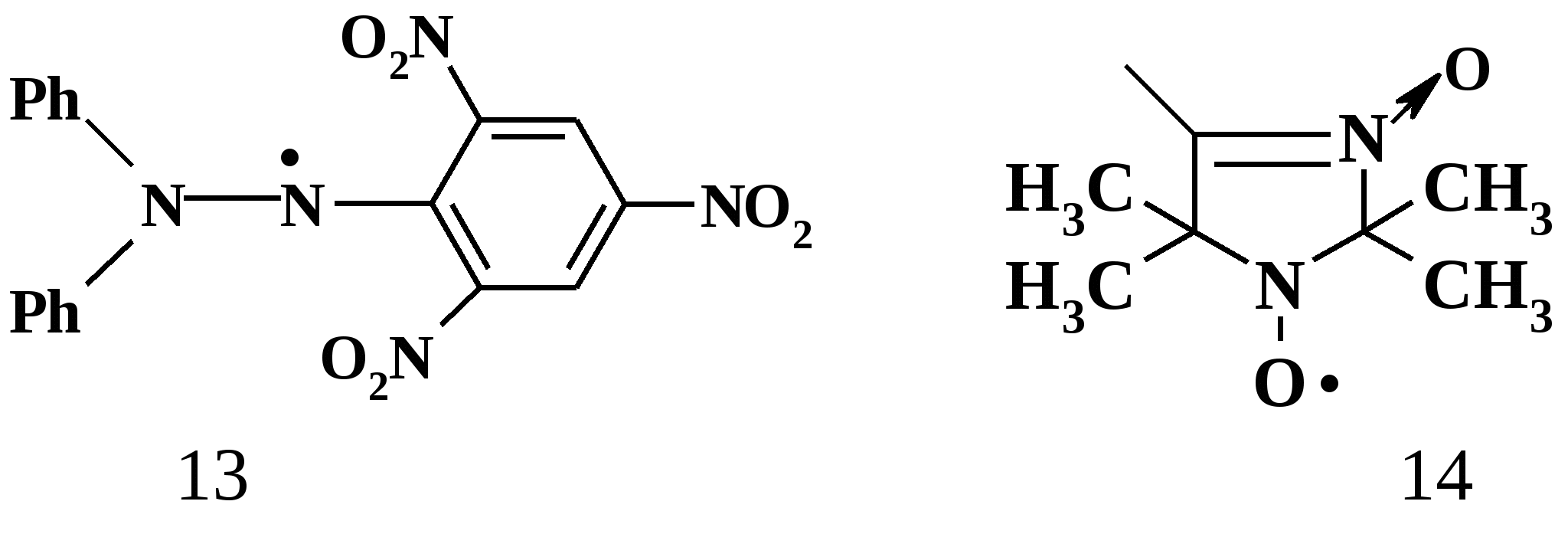 Специфический вариант ингибирования – использование в качестве ингибиторов долгоживущих радикалов, неспособных к рекомбинации друг с другом из-за пространственных затруднений. Эти радикалы, однако, могут рекомбинировать с радикалами небольшого объёма, которые и образуются при инициировании полимеризации и, таким образом, обрывать цепи. Такими ингибиторами, в частности, гидразилы [например, (14)] или нитроксилы [например, (14)]: 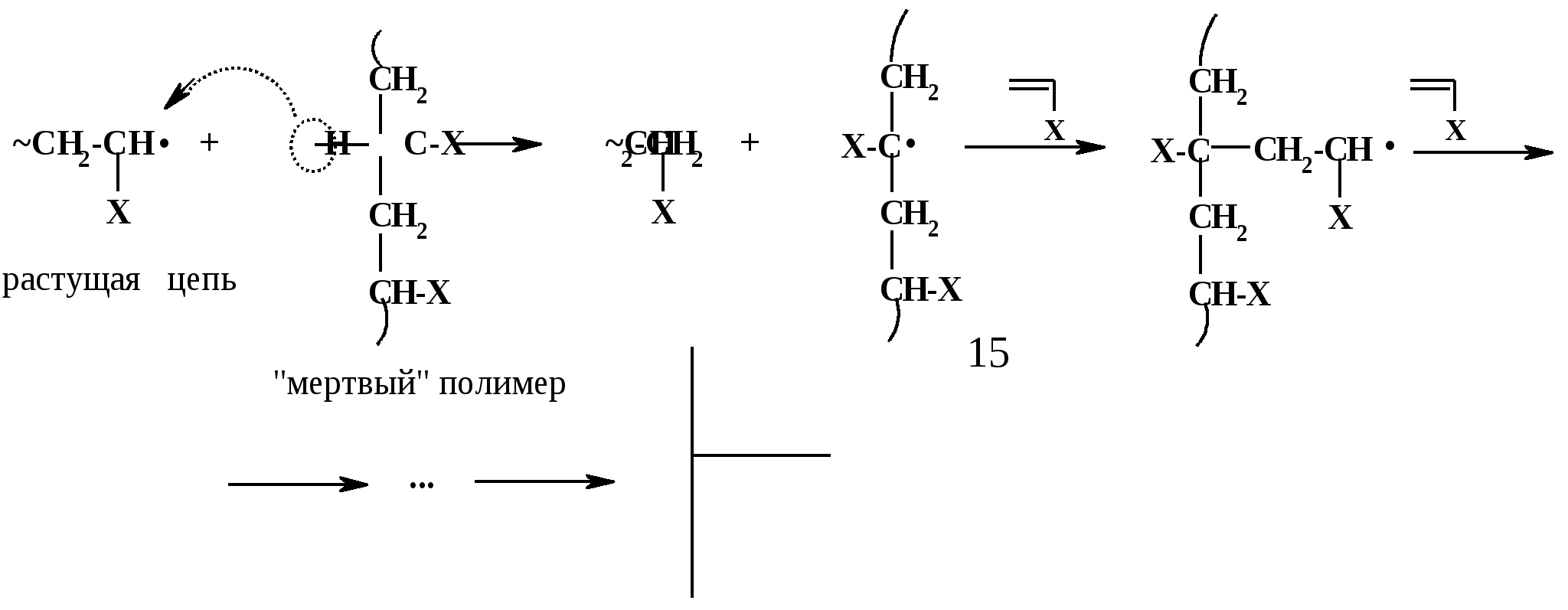 4) Передача цепи на полимер. В отличие от других видов передачи цепи, эта реакция начинает проявляться в заметной степени только при относительно больших глубинах полимеризации, когда становится заметной концентрация «мертвого» полимера, и возрастает вероятность его встречи с «живой» цепью. При такой встрече полимерный радикал может отрывать атом водорода от макромолекулы полимера: В результате такого отрыва макромолекула превращается в неконцевой макрорадикал (15) (отрыв атома водорода от неконцевого звена макромолекулы несоизмеримо более вероятен, чем от концевого). Этот радикал активен и присоединяется к молекуле мономера; инициируется рост новой цепи, боковой по отношению к исходной макромолекуле. Итогом такого роста цепи является образование разветвления (изображенного пиктограммой). Если бы реакции передачи цепи на полимер происходили часто, это приводило бы к образованию сильно разветвленного полимера, что значительно ухудшало бы его технические свойства. В этом случае реакцию вообще нельзя было бы проводить до сколько-нибудь заметных глубин полимеризации. Все же в общем случае они проходят не столь часто; отнюдь не каждое столкновение «живой» и «мертвой» цепей ведет к отрыву водорода: необходимое для передачи сближение радикального центра и атома водорода происходит лишь для малой доли столкновений (радикальный центр обычно «спрятан» в полимерном клубке «живой» цепи). Тем не менее, возможность передачи цепи на полимер обязательно необходимо учитывать при планировании процесса полимеризации. Легкость протекания передачи цепи на полимер зависит от природы полимера; передача протекает легче, если в молекуле полимера содержатся «подвижные» атомы водорода; в качестве примеров можно привести полистирол (Х= Ph) или полиакрилонитрил (X=CN). Напротив, для полимеров 1,1-дизамещенных этилена [например, для поли-α-метилстирола (-СН2-С(Me)Ph-)n], где таких атомов водорода нет, передача цепи на полимер протекает труднее. Реакции передачи на полимер могут специально использовать для получения привитых сополимеров (стр. 7). Для этого в мономере, допустим СН2=СНХ, растворяют полимер, полученный из другого мономера, допустим, [-CH2–CHY-]n, прибавляют инициатор и начинают полимеризацию мономера. В результате передачи цепи по схеме, приведенной выше, к цепи полимера [-CH2–CHY-]n «пристраиваются» боковые цепи [-CH2–CHХ-]m. Разумеется, процесс должен быть отрегулирован так, чтобы реакции передачи происходили достаточно редко и число разветвлений было малым. Реакции передачи на полимер играют также большую роль в процессах деструкции полимеров (Эти реакции, как и получение привитых сополимеров, будут описаны в разделе «Химические свойства ВМС»). Влияние различных факторов на ход и результаты радикальной полимеризации При оценке и прогнозировании протекания процесса получения любого полимера (неважно каким способом) необходимо в первую очередь оценить такие параметры: 1) скорость процесса; 2) молекулярную массу получаемого полимера (как правило, среднюю молекулярную массу или, что то же самое, среднюю степень полимеризации); 3) молекулярно-массовое распределение получаемого полимера; 4) регулярность строения образующихся макромолекул.Все эти параметры зависят как от природы молекул, принимающих участие в процессе, так и от условий его проведения. Один из наиболее важных подходов к оценке этих параметров – изучение кинетики процесса; она позволяет, прежде всего, оценить скорость процесса и молекулярную массу полимера. Далее рассмотрим в этом аспекте реакции радикальной полимеризации. |
