окс. Острый коронарный синдром Теоретические вопросы темы
 Скачать 282.41 Kb. Скачать 282.41 Kb.
|
|
Острый коронарный синдром Теоретические вопросы темы: Определение понятия,номенклатура. Этиология, патогенез. Клиническая картина в зависимости от варианта. Осложнения. Диагностика. Роль ЭКГ в выявлении нарушения ритма сердца, инфаркта миокарда и его разновидности, нестабильной стенокардии. Дифференцированное лечение в зависимости от клинических проявлений. Прогноз для жизни, выздоровления и трудоспособности. Первичная и вторичная профилактика. Содержание темы Понятием острый коронарный синдром (ОКС) эксперты ACC (American College of Cardiology)/AHA (American Heart Association) и ESC (European Society of Cardiology) обозначают «группу состояний, развивающихся при острой ишемии миокарда». ОКС обычно (но не всегда) причинно связан с атеросклеротическим поражением коронарных артерий, часто обусловлен процессом разрушения атеросклеротической бляшки с последующим каскадом патологических процессов, уменьшающих коронарный кровоток. Номенклатура ОКС. Пациенты с ОКС могут иметь элевацию сегмента ST на ЭКГ, либо не иметь ее. Большинство больных с ОКС с элевацией сегмента ST в последующем имеют инфаркт миокарда (ИМ) с зубцом Q (широкая стрелка), меньшая часть может иметь ИМ без зубца Q (узкая стрелка). Лица с ОКС без элевации ST могут иметь либо нестабильную стенокардию, либо ИМ без зубца Q (широкие стрелки), лишь небольшая часть из них имеет ИМ с зубцом Q (узкая стрелка) (адаптировано из АСС/АНА, 2007) (рис. 1). 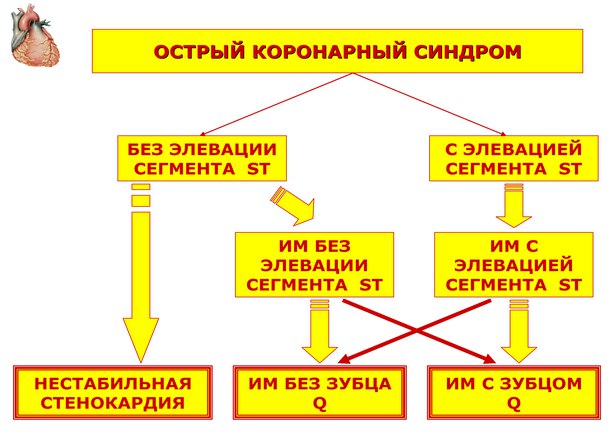 Рис. 1. Номенклатура ОКС. ОКС не является окончательным нозологическим диагнозом, он служит диагнозом первого контакта врача с пациентом, имеющим клиническую и ЭКГ-картину острой коронарной недостаточности. В связи с этим диагноз «ОКС» правомочен для врача скорой помощи, врача приемного отделения стационара и для врача отделения неотложной кардиологии в первые часы госпитализации. В дальнейшем по мере накопления информации (как клинической, так и лабораторно-инструментальной) диагноз «ОКС» должен трансформироваться в диагноз «нестабильная стенокардия» (НС), «ИМ без подъема сегмента ST», «ИМ с подъемом сегмента ST» или в какой-либо другой нозологический диагноз, отражающий имеющуюся сердечно-сосудистую патологию (рис. 1). Этиология и патогенез. Причиной возникновения ОКС служит атеротромбоз в коронарном бассейне вследствие разрыва, трещины или эрозии нестабильной атеросклеротической бляшки. Это повреждение атеросклеротической большинства больных в основе ОКС как с подъемом сегмента ST, так и без подъема сегмента ST лежат общие патофизиологические процессы, являющиеся проявлением атеротромбоза в коронарном бассейне вследствие разрыва, трещины или эрозии нестабильной атеросклеротической бляшки. Это повреждение атеросклеротической бляшки приводит к активации тромбоцитов и запускает каскад коагуляции, в результате чего в месте поврежденной атеромы образуется тромб, при этом размеры тромба могут быть различными. Четыре этапа интракоронарного тромбообразования. 1.Высвобождение тканевого фактора из места повреждения сосуда. 2.Каскадная активация факторов коагуляции (VII, VIIa, X, IX, Xa, IXa) образование тромбина из протромбина образование фибрина из фибриногена. Тромбин, кроме стимуляции образования фибрина, является мощным фактором активации, агрегации и адгезии тромбоцитов. 3.Адгезия, активация и агрегация тромбоцитов. Первичный тромбоцитарный тромб. Тромбоциты высвобождают биологически активные субстанции, в еще большей степени усиливающие активность тромбоцитов, препятствующие лизису тромба (ингибитор активатора плазминогена -- PAI-1), а также способствующие вазоконстрикции (тромбоксан А2). 4.Окончательное формирование фибриново-тромбоцитарного тромба. Дистальная эмболизация. Образующиеся под действием тромбина фибриновые нити формируют сетевидную структуру, укрепляющую исходно рыхлый первичный тромбоцитарный тромб. Фрагменты тромба и тромбоцитарные агрегаты могут отделяться от основной его структуры и эмболизировать. У больных с ОКС без подъема сегмента ST (ОКС ST(-)) тромб носит характер пристеночного, не окклюзирующего полностью просвет коронарной артерии и состоящий преимущественно из тромбоцитов, связанных между собою нитями фибрина, так называемый «белый тромб». Поэтому при возникновении ОКС ST(-) развивается ишемия в основном субэндокардиальных зон миокарда левого желудочка, что отражается на ЭКГ в виде депрессии сегмента ST. В последующем в этих зонах субэндокардиальной ишемии миокарда может развиваться некроз, что отражается на ЭКГ формированием характерного негативного равнобедренного зубца Т (так называемого «коронарного»), т. е. формируется ИМ без зубца Q. У больных с ОКС и с подъемом сегмента ST (ОКС ST(+)) тромб полностью окклюзирует просвет коронарной артерии, при этом в состав тромба входит большое количество эритроцитов, так называемый «красный тромб». Вследствие этого при возникновении ОКС ST(+), развивается трансмуральная ишемия обширных зон миокарда левого желудочка, что отражается на ЭКГ в виде подъема сегмента ST. В дальнейшем в этих зонах развивается необратимое повреждение кардиомиоцитов (некроз), что проявляется на ЭКГ появлением патологических зубцов Q или QS, т. е. формируется ИМ с зубцом Q. Клиническая картина в зависимости от варианта. ОКС без подъема сегмента ST(ОКС ST(-)) включает две нозологические формы: 1.Нестабильную стенокардию (НС); 2.ИМ без подъема сегмента ST (ИМ ST(-)). НС -- это одна из клинических форм ИБС, характеризующаяся развитием острой ишемии миокарда, тяжесть и продолжительность которой недостаточна для возникновения некроза миокарда. Нестабильная стенокардия проявляется типичными болями в грудной клетке, во время которых на ЭКГ отмечают признаки ишемии миокарда в виде стойкой либо преходящей депрессии сегмента ST, инверсии, сглаженности или псевдонормализации зубца Т, однако в плазме крови отсутствует повышение уровня биохимических маркеров некроза миокарда (сердечных тропонинов I или Т либо МВ-КФК). Необходимо подчеркнуть, что вне приступа болей ЭКГ может быть нормальной. Основной жалобой больных с НС являются типичные ангинозные боли в грудной клетке, локализующиеся чаще всего в области сердца. В соответствии с клинической картиной нестабильной стенокардии, выделяют следующие ее клинические варианты: 1. Впервые возникшая стенокардия напряжения. Под этим термином понимают стенокардию напряжения, возникшую в течение последнего 1 месяца и имеющую тяжесть не ниже III ФК по классификации Канадского сердечно-сосудистого общества. 2. Прогрессирующая стенокардия напряжения, т. е. прогрессирование ранее существовавшей стабильной стенокардии напряжения как минимум на 1 класс (по классификации Канадского сердечно-сосудистого общества) с достижением как минимум III ФК. Ангинозные боли становятся более частыми, более продолжительными, возникают при более низких физических нагрузках. 3. Стенокардия покоя, возникшая в течение последних 7 дней, с длительностью приступов до 20-30 мин., в том числе и стенокардия покоя, трансформировавшаяся из стенокардии напряжения. 4. Ранняя постинфарктная стенокардия. Стенокардия напряжения или покоя, возникшая в ближайшие дни после перенесенного ИМ, особенно после успешной тромболитической терапии у больных с ИМ с подъемом сегмента ST. ИМ ST(-), так же как и НС, проявляется типичными болями в грудной клетке, во время которых на ЭКГ могут отмечаться признаки ишемии субэндокардиальных слоев миокарда в виде стойкой либо преходящей депрессии сегмента ST, инверсии, сглаженности или псевдонормализации зубца Т. Однако, в отличие от больных с НС, у больных с ИМ без подъема сегмента ST в плазме крови выявляют повышение уровня биохимических маркеров некроза миокарда (тропонинов I или Т либо МВ-КФК), что свидетельствует о возникновении ИМ. Обычно это повреждение (некроз) миокарда локализуется в тех же субэндокардиальных зонах, которые подвергались ишемии. Развитие некроза миокарда отражается на ЭКГ формированием характерного негативного равнобедренного (так называемого «коронарного») зубца Т, т. е. образуется ИМ без зубца Q (ранее он носил название субэндокардиального, мелкоочагового ИМ). ОКС с подъемом сегмента ST(ОКС ST(+)) характеризуется типичными болями в грудной клетке, во время которых на ЭКГ регистрируют стойкий (более 20 мин) подъем сегмента ST (либо вновь возникшая полная блокада левой ножки пучка Гиса). Стойкий подъем сегмента ST на ЭКГ отражает возникновение обширной трансмуральной ишемии миокарда левого желудочка, обусловленной полной тромботической окклюзией крупной эпикардиально расположенной коронарной артерии. Как правило, в дальнейшем в этих зонах ишемии развивается обширный (часто трансмуральный) некроз миокарда, т. е. ОКС ST(+) трансформируется в ИМ с подъемом сегмента ST (ИМ ST(+)). На ЭКГ это проявляется появлением патологических зубцов Q, или QS, т. е. формируется ИМ с зубцом Q. Ранее такой ИМ носил называние крупноочагового (зубец Q на ЭКГ) либо трансмурального (зубец QS на ЭКГ) ИМ. Клиническая картина ИМ ST(+) определяется вариантом его начала, характером течения и развитием тех или иных осложнений. 1. Классический (типичный) или ангинозный вариант начала ИМ ST(+) наблюдается примерно в 70-80% случаев. Клиническая картина характеризуется типичным интенсивным ангинозным болевым синдромом с локализацией боли за грудиной (реже -- в области сердца), часто иррадиирующей в левую руку, плечо, лопатку, нижнюю челюсть и т. д. Боли по характеру обычно носят давящий, сжимающий, жгущий характер. В отличие от стенокардии, боль длительная, более 20 мин., не купируется нитроглицерином, сопровождается холодным потом, страхом смерти. 2. Помимо типичной формы начала болезни, выделяют ряд других, атипичных вариантов начала ИМ ST(+): • астматический -- начало болезни проявляется одышкой, удушьем, приступами отека легких; болевой синдром отсутствует либо выражен не резко (этот вариант развивается обычно при повторном ИМ у пожилых больных на фоне уже существовавшей ранее хронической сердечной недостаточности); • абдоминальный (гастралгический) -- боли в животе, чаще в подложечной области, диспептические расстройства, чаще возникает при нижнем (диафрагмальном) ИМ; • аритмический -- заболевание проявляется нарушениями ритма или проводимости, чаще в виде АВ блокады III степени либо желудочковой тахикардией, при этом болевой синдром отсутствует либо выражен слабо; • церебральный (цереброваскулярный) -- проявляется неврологическими расстройствами: головокружением, обмороками, симптомами, напоминающими клиническую картину инсульта. Чаще встречается у пожилых больных, имеющих поражения интра- и экстракраниальных артерий, перенесших ранее нарушения мозгового кровообращения; • бессимптомный (безболевой) -- симптомы общего недомогания, немотивированной слабости, адинамии; особенно часто встречается у пожилых лиц, у больных сахарным диабетом, перенесших ранее нарушение мозгового кровообращения; часто диагноз ставится ретроспективно, после случайной регистрации ЭКГ. В зависимости от клинического течения выделяют: 1.Первичный ИМ -- это впервые развившийся ИМ. 2.Повторный ИМ -- возникновение нового ИМ в сроки, превышающие 29 дней от начала предыдущего. 3.Рецидивирующий ИМ -- новый ИМ возникает в первые 4 недели после развития предыдущего, т. е. до окончания основных процессов рубцевания. Для повторного некроза миокарда характерно повышение уровня сердечных тропонинов во втором анализе >20% по сравнению с предыдущим. В течении ИМ выделяют несколько периодов. 1. Острейший период (ишемическая стадия) -- от 30 минут до 2 часов. Болевой синдром: сильные давящие, сжимающие, интенсивные жгучие или «кинжальные» боли. Как правило, боль иррадиирует в левую кисть, может появляться ощущение сильной сжимающей боли в области запястий. Может отдавать в левое плечо, левую лопатку, шею, нижнюю челюсть, ухо. Характерна волнообразность боли. Она постепенно нарастает, становится интенсивной, а затем несколько снижается, но вскоре возобновляется с большей силой. Применение нитроглицерина в любых формах, под язык или в виде спрея, не купирует болевой синдром. Во время приступа боли люди испытывают чувство страха смерти, тоски, обреченности, иногда возбуждены и беспокойны, могут ощущать чувство нехватки воздуха. При осмотре: бледность, нередко повышенная влажность кожи, синюшность губ, носа, ушей, подногтевых пространств. При пальпации области сердца: у больных с обширным трансмуральным ИМ можно обнаружить пресистолическую пульсацию, синхронную с IV тоном. Также может обнаруживаться систолическая пульсация в III, IV, V межреберьях слева от грудины. Частота пульса при неосложненном течении заболевания нормальная, но пульс иногда аритмичен за счет экстрасистол. Артериальное давление (АД) может незначительно повыситься, но затем быстро нормализуется. Но при обширном ИМ наблюдается его снижение, преимущественно систолического. Границы сердца лишь иногда незначительно увеличиваются за счет левой. Увеличение размеров может быть связано с обширным ИМ. При аускультации: у больных не осложненным, но обширным ИМ определяется приглушенный 1 тон и негромкий систолический шум на верхушке. При обширном трансмуральном ИМ может выслушиваться ритм галопа. В некоторых случаях выслушивается систолическое «кошачье мурлыканье». 2. Острый период -- до 7 дней -- формируется очаг некроза и в нем происходит миомаляция. Боль исчезает. Определяется учащение пульса, тенденция к снижению АД, сохранятся приглушенность тонов и негромкий систолический шум на верхушке сердца. На 2-й, реже 3-й день отмечается подъем температуры тела до 37,1-37,9°C, в редких случаях превышает 38°C. Длится повышение температуры около 3-7 дней, возможно и до 10 дней. ОАК: повышается количество лейкоцитов уже на 2-4 день и сохраняется до 3-7 дня. Обычно их количество достигает 10-12 Г/л, при распространенном трансмуральном ИМ -- до 15 Г/л. Лейкоцитоз сопровождается сдвигом лейкоцитарной формулы влево. Отмечается также увеличение СОЭ со 2-3 дня заболевания, которое достигает максимума между 8-12 днем, а затем медленно снижается, нормализуясь через 3-4 недели. Биохимический анализ крови: возрастает содержание фибриногена, серомукоида, сиаловых кислот, -глобулина, С-реактивного белка. Определяются маркеры гибели кардиомиоцитов, такие, как АСТ, ЛДГ КФК, миоглобин, миозин (в настоящее время потеряли свое значение и практически не применяются), кардиотропонины Т и I, гликогенфосфорилаза. 3. Подострый период -- от 7 до 28 дней -- формируется и уплотняется рубец. В прогностическом плане этот период является более благоприятным, так как наиболее опасные для жизни больного осложнения чаще всего развиваются в первые дни от начала заболевания. При осмотре состояние удовлетворительное, болевой синдром отсутствует. Частота сердечных сокращений нормализовалась, систолический шум в области верхушки сердца не выслушивается. АД обычно нормальное, если до развития ИМ была артериальная гипертензия, то в этом периоде АД начинает снова повышаться. В подостром периоде температура тела нормализуется, изменения со стороны крови исчезают. 4. Постинфарктный период (постинфарктный кардиосклероз) -- с 29 дня -- период полной адаптации сердечно-сосудистой системы к новым условиям функционирования, т. е. выключению сократительной функции участка миокарда. Осложнения. В период острого ИМ ST(+): 1.Нарушения ритма и проводимости (желудочковая пароксизмальная тахикардия, фибрилляция желудочков, предсердно-желудочковые блокады, мерцание и трепетание предсердий и др.). 2.Острая левожелудочковая недостаточность -- сердечная астма, отек легких, шок (рефлекторный, кардиогенный или аритмический). 3.Острая аневризма сердца. 4.Эпистенокардитический перикардит. 5.Разрывы миокарда как внутренние, так и наружные (в том числе перфорация межжелудочковой перегородки и отрыв сосочковых мышц). 6.Тромбоэмболические осложнения (в большом и малом круге кровообращения). 7.Парез желудка и кишечника, эрозивный гастрит с желудочным кровотечением, панкреатит. В период заживающего (рубцующегося) ИМ ST(+): 1.Тромбоэндокардит с тромбоэмболическим синдромом (чаще - эмболия мелких сосудов большого круга кровообращения). 2.Пневмония. 3.Постинфарктный синдром (синдром Дресслера, синдром передней грудной стенки, синдром плеча) развивается обычно на 2-6-й нед. после ИМ, характеризуется перикардитом, плевритом, пневмонитом; иногда в воспалительный процесс вовлекаются синовиальные оболочки суставов (одновременно все симптомы встречаются редко, чаще наблюдается сочетание перикардита с плевритом или пневмонитом; иногда каждый из этих симптомов может встречаться изолированно, затрудняя диагностику постинфарктного синдрома). 4.Психические изменения (чаще неврозоподобные симптомы). 5.Хроническая левожелудочковая сердечная недостаточность. 6.Начало формирования хронической аневризмы сердца. 7.Правожелудочковая недостаточность развивается редко; при ее наличии следует думать о тромбоэмболии ветвей легочной артерии, разрыве межжелудочковой перегородки и крайне редко -- об инфаркте правого желудочка. В периоде зажившего ИМ ST(+): 1.Продолжается ремоделирование левого желудочка, может идти формирование хронической аневризмы. 2.Развитие симптомов хронической сердечной недостаточности. 3.Могут также возникнуть новые нарушения ритма сердца (мерцательная аритмия). В целом, для данного периода развитие тяжелых осложнений нехарактерно. Диагностика. Диагноз НС либо ИМ без зубца Q устанавливают в процессе наблюдения и обследования больного с ОКС ST(-) в течение первых 24-72 ч. госпитализации на основании как клинической картины заболевания, так и результатов лабораторно-инструментальных методов диагностики. Этапы диагностики. На первом этапе: 1. Заподозрить развитие ИМ. 2. Высказать предположения о клиническом варианте болезни. 3. Получить сведения о тех или иных осложнениях. При наличии длительного приступа нестерпимых болей за грудиной и в области сердца с характерной иррадиацией, не купирующихся нитроглицерином, следует, прежде всего, предположить развитие ИМ. Остро возникший приступ удушья, особенно у лиц пожилого возраста, прежде всего, наводит на мысль об астматическом варианте ИМ и требует обязательной регистрации ЭКГ. Наличие резких болей в эпигастральной области, особенно у больных с хронической ИБС, позволяет заподозрить абдоминальный (гастралгический) вариант ИМ и требует регистрации ЭКГ. Жалобы больного на приступы сердцебиений или резкого урежения ритма, появление аритмий, обмороков могут указывать на начало ИМ или его осложнений. Внезапное немотивированное развитие кардиогенного шока, когда больной заторможен, вял, сознание его спутано, также должно вызвать у врача подозрение в отношении ИМ. На втором этапе: 1. Сведения, косвенно указывающие на развитие ИМ (прямых признаков не существует). 2. Сведения, позволяющие выявить осложнения. При соответствующем анамнезе такие симптомы, как повышение температуры тела, тахикардия, артериальная гипотензия, особенно развившаяся на фоне предшествующей гипертензии, глухость тонов сердца и кратковременно выслушиваемый шум трения перикарда, позволяют высказаться в пользу диагноза ИМ. Физикальное обследование помогает выявить симптомы возможных осложнений. Для кардиогенного шока характерны: холодная кожа серо-бледного цвета, покрытая липким потом (нарушение периферической циркуляции); олигоанурия (уменьшение мочеобразования); нитевидный пульс; уменьшение пульсового давления (менее 20-30 мм рт.ст.); снижение систолического АД (ниже 80 мм рт.ст.). Могут наблюдаться симптомы острой левожелудочковой недостаточности: одышка, ортопноэ, влажные незвонкие мелкопузырчатые хрипы в легких. Увеличенная печень, периферические отеки -- симптомы недостаточности кровообращения в большом круге. При физикальном обследовании представляется возможным обнаружить бради-, тахикардию, экстрасистолию, мерцательную аритмию, пароксизмальную тахикардию. Большое диагностическое значение приобретает выявление острой аневризмы (патологическая пульсация в прекардиальной области в четвертом межреберье слева от грудины), разрыва межжелудочковой перегородки (интенсивный систолический шум в нижней трети грудины с симптомами быстро нарастающей недостаточности кровообращения в малом и большом круге), разрыва или отрыва сосочковой мышцы (дующий систолический шум на верхушке сердца, иногда определяемый пальпаторно, в сочетании с нарастающим застоем в малом круге кровообращения). На третьем этапе можно: 1. Поставить окончательный диагноз ИМ. 2. Уточнить его локализацию и распространенность (степень поражения миокарда). 3. Подтвердить или выявить нарушения ритма и проводимости. 4. Выявить новые осложнения (аневризма сердца, очаговое поражение почек при тромбоэмболии). Поставить окончательный диагноз ИМ можно на основании сочетания признаков резорбционно-некротического синдрома и данных ЭКГ. Резорбционно-некротический синдром выявляют по результатам общеклинического и биохимического исследований крови: лейкоцитоз со сдвигом лейкоцитарной формулы влево и анэозинофилия (не всегда) с первых часов заболевания; увеличение СОЭ с 3-5-го дня. В настоящее время самым информативными методом диагностики ИМ служит определение в плазме крови сердечных тропонинов Т или I. При возникновении некроза миокарда уровень сердечных тропонинов повышается до диагностически значимого уровня не ранее, чем через 3-4 ч, поэтому для диагностики ИМ рекомендуется двукратное определение сердечных тропонинов: при поступлении больного в стационар и повторно через 6-9 ч. Допустимо использование MB-КФК. Диагностически значимого уровня в плазме крови MB-КФК достигает через 6-9 ч после возникновения некроза миокарда, однако сохраняет повышенное значение только около 2-3 суток. Еще одним биохимическим маркером некроза миокарда, используемым для диагностики инфаркта, служит миоглобин. Его преимущество -- быстрое повышение концентрации в плазме крови, которая достигает диагностического значения уже через 2 ч после возникновения ангинозного приступа. Однако миоглобин имеет существенный недостаток -- при высокой чувствительности он обладает низкой специфичностью. ЭКГ. У больных с ОКС ST (+) и у больных с ИМ ST(+) в период развивающегося ИМ и в начальный период острого ИМ (первые 6-12 ч заболевания) отмечают подъем сегмента ST в так называемых «прямых» отведениях (в этих отведениях в последующем будет формироваться патологический зубец Q) и реципрокное снижение ST в отведениях, при этом изменений комплекса QRS и формирования патологических зубцов Q пока еще не будет. Диагностически значимым считают подъем сегмента ST в точке J в 2 последовательных отведениях и более 0,2 мм (0,2 мВ) для мужчин и более 0,15 мм (0,15 мВ) для женщин в отведениях V2-V3 и более 0,1 мм (0,1 мВ) в других отведениях. • В период острого ИМ в «прямых» отведениях ЭКГ резко снижается амплитуда зубца R и формируется патологический зубец Q, по амплитуде равный не менее 1/3 зубца R, а по длительности -- равный 0,04 с и более (ранее называвшийся «крупноочаговым» ИМ). Либо зубец R исчезает полностью и формируется патологический комплекс QS (ранее называвшийся трансмуральным ИМ; рис. 2). 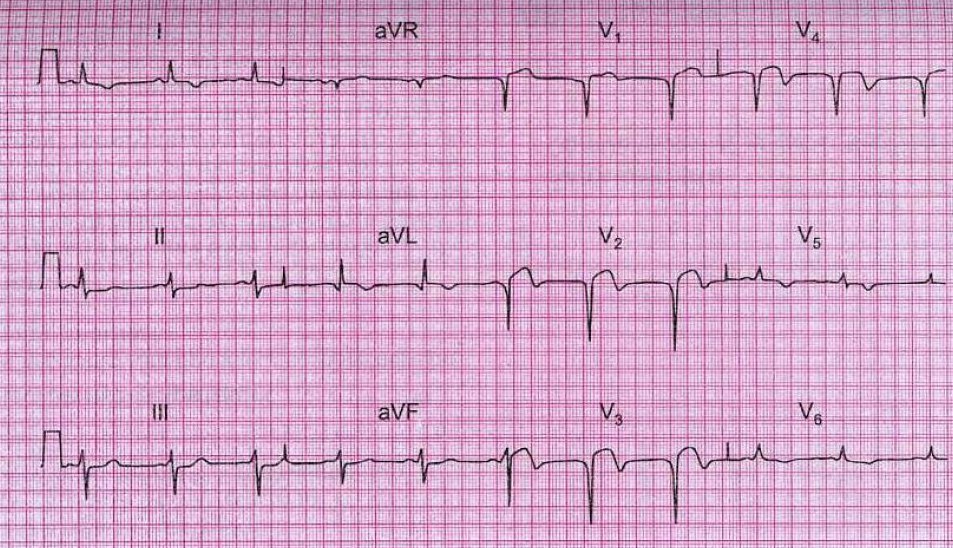 Рис. 2. Острый передний ИМ ST(+). • Последующая эволюция ЭКГ при ИМ ST(+) сводится к возвращению сегмента ST к изоэлектрической линии и формированию в «прямых» отведениях отрицательного («коронарного») зубца Т. • Для распространенного ИМ передней стенки левого желудочка, включая область верхушки, межжелудочковой перегородки и боковой стенки, характерны изменения ЭКГ в отведениях I, II, aVL и с V2 по V6; для инфаркта в области верхушки левого желудочка -- в отведениях V3-V4; при поражениях области межжелудочковой перегородки выявляют изменения в отведениях V1-V3; при инфаркте боковой стенки -- в отведениях I, aVL и V5, V6; для инфаркта нижней стенки характерны изменения -- в отведениях II, III и aVF. На ЭКГ могут выявлять самые разнообразные нарушения ритма, встречающиеся при ИМ. По ЭКГ можно узнать впервые о нарушениях предсердно-желудочковой проводимости и проводимости по ножкам пучка Гиса, определить характер блокады. Признаком, позволяющим предположить аневризму, является так называемая «застывшая» ЭКГ -- сохранение подъема сегмента ST в сочетании с комплексом QS в «прямых» отведениях, при этом может отмечаться «коронарный» зубец Т. Ультразвуковое исследование (УЗИ) сердца -- важный дополнительный метод исследования у больных с ИМ. УЗИ позволяет выявить участки нарушения локальной сократимости миокарда левого желудочка (гипокинезия, акинезия), соответствующие зоне поражения, а также состояние сосочковых мышц и межжелудочковой перегородки, которые также могут поражаться при ИМ. Велико значение УЗИ сердца в оценке глобальной сократимости левого желудочка (величина фракции выброса левого желудочка), в оценке его формы, размеров, в распознавании таких осложнений, как образование тромбов в полостях сердца, разрывов миокарда, возникновении перикардита. Рентгеноскопию органов грудной клетки рекомендуется проводить у всех больных с подозрением на ИМ либо с уже установленным диагнозом инфаркта. Рентгенография органов грудной клетки позволяет уточнить состояние легких, сердца. Особенно велико ее значение в диагностики начальных признаков застоя в малом круге кровообращения, которые еще не проявляются клинически. Специальные методы диагностики. 1. Визуализация ИМ с помощью радиоактивных изотопов. Этот метод применяют, если затруднена диагностика ИМ с помощью ЭКГ, а исследование активности ферментов сыворотки крови невозможно или малоинформативно. 2. Селективная коронарография в остром периоде ИМ применяется, если планируется выполнение первичной ангиопластики и стентирования коронарных артерий. Формулировка развернутого клинического диагноза ИМ должна отражать: 1. Характер течения (первичный, рецидивирующий, повторный). 2. Глубину некроза (ИМ с зубцом Q, или ИМ без зубца Q). 3. Локализацию ИМ. 4. Дату возникновения ИМ. 5. Осложнения (если они имелись): нарушения ритма и проводимости, острая сердечная недостаточность и др. 6. Фоновые заболевания -- атеросклероз коронарных артерий (если выполнялась коронароангиография, то указывается его тяжесть, распространенность и локализация), гипертоническая болезнь (при ее наличии) и ее стадия, сахарный диабет и др. Лечение. В начальном периоде ИМ ST(+) основные лечебные мероприятия направлены на обезболивание, скорейшее полноценное и стойкое восстановление коронарного кровотока в инфаркт-связанной артерии и лечение осложнений, если они возникают. 1. Купирование болевого синдрома. При неэффективности 1-2-кратного приема 0,4 мг нитроглицерина в виде таблеток или спрея, используют внутривенное введение наркотических анальгетиков, среди которых наиболее эффективен 1% раствор морфина (морфина гидрохлорида). Вместо морфина могут быть использованы и другие наркотические анальгетики (промедол, фентанил) как в сочетании с транквилизаторами или нейролептиками, так и без них. 2. Оксигенотерапия должна использоваться у лиц с сатурацией кислорода <94%, респираторным дистрессом, а также иными клиническими проявлениями гипоксемии. 3. Восстановление коронарного кровотока и перфузии миокарда. Существует две возможности восстановления коронарного кровотока: тромболитическая терапия, т. е. реперфузия с помощью тромболитических препаратов (стрептокиназа, тканевые активаторы плазминогена), и чрескожное коронарное вмешательство (ЧКВ), т. е. реперфузия с помощью механического разрушения тромботических масс, окклюзирующих коронарную артерию (баллонная ангиопластика и стентирование коронарных артерий). Попытка восстановления коронарного кровотока с помощью того или другого метода должна быть предпринята у всех больных с ИМ ST(+) в первые 12 ч заболевания (при отсутствии противопоказаний). Реперфузионные вмешательства оправданы и после 12 ч от начала заболевания, если имеются клинические и ЭКГ-признаки продолжающейся ишемии миокарда. Абсолютные противопоказания к проведению тромболитической терапии (адаптировано из Рекомендаций экспертов США, 2013): Перенесенные ранее интракраниальные геморрагии. Наличие структурных цереброваскулярных поражений (например, артериовенозной мальформации). Интракраниальные злокачественные новообразования (первичные или метастазы). Ишемический инсульт в течение последних 3 месяцев (исключая острый ишемический инсульт в течение ближайших 4,5 часов). Подозрение на расслоение аорты. Активное кровотечение / кровоточивость (кроме менструации). Значимая закрытая травма головы или травма лица в течение последних 3 месяцев. Хирургическое вмешательство -- интракраниальное или на позвоночнике -- в течение последних 2 месяцев. Тяжелая неконтролируемая артериальная гипертензия (которая не отвечает на экстренную антигипертензивную терапию). Для стрептокиназы -- ее использование в течение ближайших 6 месяцев. Относительные противопоказания к проведению тромболитической терапии (адаптировано из Рекомендаций экспертов США, 2013): Хроническая тяжелая и плохо контролируемая артериальная гипертензия в анамнезе. Значимая артериальная гипертензия при осмотре (систолическое артериальное давление > 180 мм рт. ст. или диастолическое > 110 мм рт. ст.). Ишемический инсульт в анамнезе давностью более 3 месяцев. Деменция. Интракраниальные нарушения, не упоминавшиеся в абсолютных противопоказаниях. Травматичная или длившаяся >10 минут сердечно-легочная реанимация. Большие хирургические вмешательства давностью менее 3 недель. Недавние (в течение 2-4 недель) внутренние кровотечения. Сосудистый доступ, который не может быть подвергнут компрессии. Беременность. Острая пептическая язва. Прием пероральных антикоагулянтов. 4. Учитывая чрезвычайно важную роль тромбоцитов в патогенезе ОКС ST(+), подавление адгезии, активации и агрегации тромбоцитов служит одним из ключевых моментов в лечении этой категории больных. Ацетилсалициловую кислоту (аспирин) в качестве антиагреганта назначают больному как можно раньше. Еще более эффективным является добавление к тромболитической терапии комбинации аспирина и клопидогрела. 5. Целесообразность применения антикоагулянтов (нефракционированный гепарин, низкомолекулярный гепарин, ингибиторы Ха-фактора) связана с необходимостью сохранения проходимости и предупреждения повторного тромбоза инфарктсвязанной коронарной артерии после успешного системного тромболизиса; профилактикой формирования пристеночных тромбов в левом желудочке и последующих системных артериальных эмболий, а также профилактикой возможных тромбозов вен нижних конечностей и тромбоэмболий ветвей легочной артерии. 5. Органические нитраты -- препараты, уменьшающие ишемию миокарда. Однако убедительных данных в пользу применения нитратов при неосложненном течении ИМ ST(+) нет, поэтому их рутинное применение в таких случаях не показано. Внутривенное введение нитратов может применяться в течение первых 1-2 сут. ИМ ST(+) при клинических признаках сохраняющейся ишемии миокарда, при высокой артериальной гипертензии, при сердечной недостаточности. 6. Применение β-адреноблокаторов на раннем этапе лечения больных с ИМ ST(+) (за счет снижения потребности миокарда в кислороде) способствует уменьшению ишемии миокарда, ограничению зоны некроза и вероятности возникновения жизнеугрожающих нарушений ритма, в том числе фибрилляции желудочков. У «стабильных» больных, не имеющих нарушений гемодинамики (артериальной гипотензии, острой левожелудочковой недостаточности), нарушений проводимости сердца, бронхиальной астмы, в первые часы ИМ ST(+) возможно внутривенное введение β-адреноблокаторов с последующим переходом на поддерживающий прием внутрь. 7. Ингибиторы ангиотензинпревращающего фермента (АПФ) (каптоприл, эналаприл, рамиприл, периндоприл, зофеноприл, трандолаприл и др.) следует назначать с первых суток ИМ ST(+), если нет противопоказаний. Учитывая нестабильность гемодинамики в первые сутки ИМ ST(+), возможность одновременного применения β-адреноблокаторов и нитратов, первоначальные дозы ингибиторов АПФ должны быть небольшими с последующим их увеличением под контролем АД, уровня калия и креатинина плазмы крови до максимально переносимых доз либо до достижения их целевых значений. Если больной не переносит ингибиторы АПФ, можно использовать блокаторы рецепторов ангиотензина II (валсартан, лозартан, телмисартан и др). Особенно эффективны ингибиторы АПФ у больных ИМ ST(+), у которых в ранней фазе заболевания имелось снижение фракции выброса или были признаки сердечной недостаточности. В зависимости от клинической картины и тяжести, острая сердечная недостаточность (ОСН) у больных ИМ подразделяется на четыре класса (классификация Killip). I класс: умеренная одышка, синусовая тахикардия при отсутствии застойных хрипов в легких. II класс: влажные незвонкие мелкопузырчатые хрипы в нижних отделах легких не выше лопаток, захватывающие менее 50% поверхности легких (интерстициальный отек легких). III класс: влажные незвонкие мелкопузырчатые хрипы, захватывающие более 50% поверхности легких (альвеолярный отек легких). IV класс: кардиогенный шок. Для лечения ОСН I-II класса по Killip используют: 1. Ингаляцию кислорода через лицевую маску либо через носовые катетеры под контролем насыщения крови кислородом. 2. Внутривенное введение петлевых диуретиков (фуросемид) в дозе 20-40 мг с интервалом 1-4 ч в зависимости от необходимости. 3. Внутривенную инфузию нитратов (нитроглицерин, изосорбида динитрат) в начальной дозе 3-5 мг/ч при отсутствии артериальной гипотензии. 4. Ингибиторы АПФ внутрь при отсутствии артериальной гипотензии, гиповолемии и почечной недостаточности. Лечение больных с ОСН III класса по Killip: 1. Оксигенотерапия, мониторирование насыщения крови кислородом и величины рН. 2. При снижении рО2 ниже 50% -- неинвазивная (лицевая маска, CIPAP, BiPAP) либо инвазивная (интубация трахеи) вспомогательная вентиляция легких. 3. Мониторный контроль показателей центральной гемодинамики с помощью плавающего баллонного катетера Swan-Ganz. 4. Внутривенное введение петлевых диуретиков (фуросемид) в дозе 60-80 мг и больше с интервалом 1-4 ч в зависимости от диуреза. 5. Наркотические анальгетики: внутривенно морфин (морфина гидрохлорид) 1% по 1,0 мл на 20,0 мл изотонического раствора натрия хлорида. 6. При отсутствии артериальной гипотензии (АД выше 100 мм рт. ст.) внутривенная инфузия периферических вазодилататоров (нитроглицерина либо изосорбида динитрата в стартовой дозе 3-5 мг/ч с последующей коррекцией) под контролем АД и показателей центральной гемодинамики. 7. При наличии артериальной гипотензии (АД ниже 90 мм рт. ст.) внутривенная инфузия инотропных препаратов -- добутамина, допамина (начальная доза 2,5 мкг/кг в 1 мин с последующей коррекцией) под контролем АД и показателей центральной гемодинамики. 8. Скорейшая реваскуляризация миокарда (ЧКВ или коронарное шунтирование). Лечение больных с ОСН IV класса по Killip: 1. Оксигенотерапия, мониторирование насыщения крови кислородом и величины рН. 2. При снижении рО2 ниже 50% -- неинвазивная (лицевая маска, CIPAP, BiPAP) либо инвазивная (интубация трахеи) вспомогательная вентиляция легких. 3. Мониторный контроль показателей центральной гемодинамики с помощью плавающего баллонного катетера Swan-Ganz. 4. Внутривенная инфузия инотропных препаратов -- добутамина, допамина (начальная доза 2,5 мкг/кг в 1 мин с последующей коррекцией) под контролем АД и показателей центральной гемодинамики. 5. Внутриаортальная баллонная контрпульсация. 6. Скорейшая реваскуляризация миокарда (ЧКВ или коронарное шунтирование). Лечение нарушений ритма, если они имеются (см. раздел «Нарушения ритма»). Ведение пациента в постинфарктном периоде. Как и для пациентов, перенесших ИМ ST(-), так и лица после перенесенного ИМ ST(+) при отсутствии противопоказаний должны длительно (неопределенно долго) получать терапию антитромботическими средствами (аспирином, во многих случаях также клопидогрелем), β-адреноблокаторами, ингибиторами АПФ/сартанами, статинами. У части пациентов для улучшения сердечно-сосудистого прогноза могут быть также использованы антагонисты альдостерона (эплеренон), ω3-полиненасыщенные жирные кислоты, при наличии стенокардии -- ивабрадин. Для этих пациентов крайне важной является коррекция факторов сердечно-сосудистого риска. Прогноз. Прогноз заболевания серьезный, возможно развитие повторного ИМ. С развитием осложнений (при сохранении артериальной гипертензии, хронической сердечной недостаточности) прогноз ухудшается. Профилактика. Устраняют так называемые факторы риска ИБС, особенно у лиц, в семьях которых есть случаи раннего атеросклероза. Немедикаментозная и медикаментозная терапия по существу представляют собой вторичную профилактику ИМ. Рекомендовано категорическое запрещение курения, соблюдение диеты с низким содержанием насыщенных жиров, обогащенной фруктами и овощами. Вторичная профилактика ИМ заключается в постоянном приеме антиангинальных препаратов, при измененном липидном спектре -- гиполипидемических препаратов, при наличии артериальной гипертензии -- антигипертензивных препаратов. |
