физика. Отсчета
 Скачать 2.35 Mb. Скачать 2.35 Mb.
|
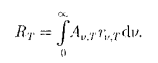 . смещения Вина, . смещения Вина, 95. Формулы Рэлея-Джинса и Планка. Формула Рэлея —Джинса для спектральной плотности эпергетической светимости черного тела имеет вид. 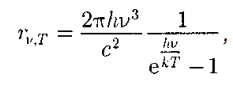 96. Законы внешнего фотоэффекта. 1-й закон внешнего фотоэффекта (закон Столетова): При фиксированной частоте падающего света фототок насыщения пропорционален падающему световому потоку. 2- й закон фотоэффекта: максимальная начальная скорость Vmax фотоэлектронов не зависит от интенсивности падающего света (от Ф), а определяется только его частотой ν .3- й закон фотоэффекта: для каждого вещества существует "красная граница'' фотоэффекта, то есть минимальная частота νкp, зависящая от химической природы вещества и состояния его поверхности, при которой ещё возможен внешний фотоэффект. 97. Модель атома Резерфорда. Постулаты Бора Маленькое очень массивное положительно заряженное ядро, от которого как раз и отскакивали альфа-частица в описанных опытах, расположено в центре атома Резерфорда. Вокруг ядра вращаются легкие отрицательно заряженные электроны. Большую часть пространства внутри атома заполняет пустота. В целом модель очень похожа на нашу Солнечную систему. К великому сожалению Резерфорда, статья была встречена молчанием. Резерфорд, конечно понимал почему. Его атом был недолговечен. Электрон, вращаясь вокруг ядра, должен излучать электромагнитные волны и терять вследствие этого энергию. При этом скорость его должна была бы замедлиться, и он должен был бы упасть на ядро. Однако опыт свидетельствует, что практически все атомы в природе устойчивы. Первый постулат Бора (постулат стационарных состояний): в атоме существуют стационарные (не изменяющиеся со временем) состояния, в которых он не излучает энергии; эти состояния характеризуются определенными дискретными значениями энергии. Второй постулат Бора (правило частот): при переходе электрона с одной стационарной орбиты на другую излучается (поглощается) один фотон с энергией. 98. Линейчатый спектр излучения атома водорода. Во всех случаях реакция атомов состоит в испускании частиц и электромагнитного излучения. Количественной характеристикой процесса электромагнитного излучения является спектр излучения - распределение интенсивности излучения тела по частотам этого излучения. Опытное изучение спектров излучения показало, что все атомные спектры линейчаты или дискретны: распределение по частотам интенсивности излучения представляет собой набор острых пиков интенсивности, между которых интенсивность очень мала. Пики интенсивности называются спектральными линиями. Часто говорят о расположении спектральных линий в спектре. Расположение линий определяется частотой на которую данный пик приходится. Расположение линий спектров разных элементов различно. Самым изученным является спектр наиболее простого атома - атома водорода. Швейцарский ученый Бальмер (1825-1898) подобрал эмпирическую формулу, описывающую все известные в то время спектральные линии атома водорода в видимой области спектра. Длина волны λ любой из спектральных линий этой серии удовлетворяет соотношению где k = 3, 4, 5... , R -постоянная Ридберга 99. Состав атомного ядра. Атомное ядро состоит из элементарных частиц – протонов и нейтронов. Массы протона mp и нейтрона mn близки друг к другу. Протон электрически заряжен. Его заряд положителен и по абсолютной величине равен заряду электрона. Дефект масс. 1  00. Под радиоактивным распадом, или просто распадом, понимают естественное радиоактивное прсвращение ядер, происходящее самопроизвольно. Атомное ядро, испытывающее радиоактивный распад, называется материнским, возникающее ядро — дочерним. Теория радиоактивного распада строится на предположении о том, что радиоактивный распад является спонтанным процессом, подчиняющимся статистическим законам. Так как отдельные радиоактивные ядра распадаются независимо друг от друга, то можно считать, что число ядер d/V, распавшихся в среднем за интервал времени от t до i + dt, пропорционально промежутку времени dt и числу N иераспавшихся ядер к моменту времени i: 00. Под радиоактивным распадом, или просто распадом, понимают естественное радиоактивное прсвращение ядер, происходящее самопроизвольно. Атомное ядро, испытывающее радиоактивный распад, называется материнским, возникающее ядро — дочерним. Теория радиоактивного распада строится на предположении о том, что радиоактивный распад является спонтанным процессом, подчиняющимся статистическим законам. Так как отдельные радиоактивные ядра распадаются независимо друг от друга, то можно считать, что число ядер d/V, распавшихся в среднем за интервал времени от t до i + dt, пропорционально промежутку времени dt и числу N иераспавшихся ядер к моменту времени i:  |
