Бюджетное профессиональное образовательное учреждение Омской Обл. СРС Низин. подготовка ответов на контрольные вопросы
 Скачать 36.6 Kb. Скачать 36.6 Kb.
|
|
БЮДЖЕТНОЕ ПРОФЕССИОНАЛЬНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ОМСКОЙ ОБЛАСТИ «Омский авиационный колледж имени Н.Е. Жуковского» СРС по учебной дисциплине: ОП.04 Материаловедение на тему: «подготовка ответов на контрольные вопросы» Выполнил студент I курса: Группы РД-111 Низин Игорь Владимирович Проверил преподаватель: С.Ю. Гайдук Омск, 2022г. Содержание 1.Сталь 45 1.1. Состав 1.2.Режимы термической обработки 1.3.Свойства стали при термической обработке 1.4.Описать сущность происходящих превращений после термической обработки 1.5.Заключение 2.ХВ5 2.1.Состав 2.2.Термическая обработка 2.3.Структура материала после термической обработки 2.4.Свойства материала после термической обработки 2.5.Заключение 3.Нержавеющая сталь 3.1.Термическая обработка 3.2.Описание микроструктуры стали 3.4.Заключение 4.Л80 4.1.Состав и структура 4.2.Режим термической обработки 4.3.Заключение 5.Список использованной литературы(8стр.) Основная часть Сталь 45 Закалка доэвтектоидной стали заключается в нагреве стали до температуры выше критической (Ас3), в выдержке и последующем охлаждении со скоростью, превышающей критическую. Доэвтектоидные стали для закалки следует нагревать до температуры на 30-50°С выше Ас3. Температура точки Ас3 для стали 45 составляет 755°С, а Ас1 равна 730°С. Структура доэвтектоидной стали при нагреве её до критической точки Ас1 состоит из зерен перлита и феррита. В точке Ас1 происходит превращение перлита в мелкозернистый аустенит. При дальнейшем нагреве от точки Ас1 до Ас3 избыточный феррит растворяется в аустените и при достижении Ас3 (линия GS) превращения заканчиваются. Температура нагрева стали под закалку, таким образом, составляет 800-820°С. Структура стали 45 при температуре нагрева под закалку – аустенит, после охлаждения со скоростью выше критической – мартенсит. Высокий отпуск проводится при температуре 580-600?С. В результате получаем структуру – сорбит отпуска. Высокий отпуск создает наилучшее соотношение прочности и вязкости. Закалка с высоким отпуском (по сравнению с нормализацией или отжигом) повышает временное сопротивление, предел текучести, относительное сужение и особенно ударную вязкость. Высокие отпуск почти полностью снимает остаточные напряжения, возникшие при закалке. Свойства стали 45 после улучшения: ?В = 870 МПа; ?т= 700 МПа; ?= 13%; ? = 65%; KCU = 1,3 МДж/м2; НВ = 255. ХВ5 Химический состав стали ХВ5: 1,25 … 1,45 % C, 4,0 … 5,0 % W, 0,40 … 0,70 % Cr, 0,15 … 0,30 % V, остальное – Fe. По структуре ХВ5 относится к заэвтектоидным сталям перлитного класса. Её подвергают неполной закалке от температуры несколько выше точки A1 и низкому отпуску. Температура закалки 800 … 820 °C, температура отпуска 100 … 140 °C. Структура мартенсит + избыточные карбиды (легированный цементит) обеспечивает высокую твёрдость и износостойкость. Дополнительное повышение твёрдости (до 69 HRC) и износостойкости обеспечивается присутствием карбидов вольфрама, которые практически не растворяются при температуре закалки. Из-за высокой твёрдости сталь ХВ5 называют «алмазной» и применяют для чистовой обработки твёрдых материалов. ХВ5 меньше склонна к перегреву, чем углеродистые стали, и позволяют изготавливать инструменты бОльших размеров и более сложной формы. При этом, однако, сталь обладает низкой теплостойкостью и применяется для инструментов, работающих при небольших скоростях резания, не превышающих 250 °C. Закалка предназначена для обеспечения требуемых показателей твёрдости, износостойкости, теплостойкости и прочности инструмента. Эти требованиям удовлетворяет структура мартенсита – твёрдого раствора углерода в α – железе. Назначение вольфрама и ванадия – главным образом тормозить рост зерна аустенита при нагреве стали для закалки. Влияние хрома обусловлено тем, что он вместе в вольфрамом и железом образует сложные карбиды. Ниже приводится рисунок, показывающий влияние легирующих элементов на температуру AC1. 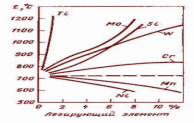 Нержавеющая сталь Разрушение металлов и сплавов в результате химического или электрохимического воздействия на их поверхность внешней агрессивной среды называется коррозией. Коррозия, как правило, сопровождается: образованием на поверхности металла продуктов коррозионного разрушения. Так, например, на поверхности сплавов железа в результате коррозии образуется ржавчина, имеющая бурый цвет. В некоторых же отдельных случаях коррозия металлов не сопровождается образованием таких заметных продуктов разрушения и тогда ее появление обнаружить довольно сложно. Коррозионное разрушение является результатом взаимодействия металла с внешней средой и интенсивность его развития зависит от свойств самого металла, а также от природы окружающей среды. Большинство металлов, будучи стойкими в одних средах, довольно легко разрушается при взаимодействии с другими средами. Например, медные сплавы устойчивы во влажной атмосфере, но сильно подвергаются коррозии, если в атмосфере присутствует даже незначительное количество аммиака; тантал и титан при комнатных температурах весьма стойки по многих агрессивных средах, но приобретают высокую химическую активность при нагреве их выше 600° С. Различают несколько видов коррозии: сплошную или равномерную, когда коррозии подвергается вся поверхность изделия; точечную или местную, если коррозия развивается на отдельных небольших участках; межкристаллитную коррозию (МКК), когда коррозия распространяется в глубь изделия по границам зерен; коррозия под напряжением—возникновение коррозионных трещин вследствие одновременного воздействия на металл растягивающих напряжений и агрессивной среды. Наибольшее количество металла разрушается в результате электрохимической коррозии. Электрохимической коррозией назвают разрушение металлов и сплавов пр воздействии на них электролитов.. Наиболее часто встречающимися на практике электролитами являются водные растворы солей, кислот и щелочей. Таким образом, к электрохимической коррозии относится корродирование металлических емкостей, трубопроводов, деталей машин и частей стационарных сооружений под действием кислот, морской, речной, грунтовой и других вод. Наиболее распространенной является атмосферная коррозия. Если в электролите находятся два металла с различными электродными потенциалами, то металл с более отрицательным электродным потенциалом (анод) непрерывно отдает ноны в раствор (растворяется), а образующиеся избыточные электроны непрерывно перетекают в металл с менее отрицательным электродным потенциалом (катод). Катод в контактной паре не разрушается, электроны из него непрерывно удаляются во внешнюю среду. В технических металлах и сплавах, являющихся телами поликристаллическими, микроструктура состоит из зерен одной или нескольких фаз, неметаллических включений и т. п. Эти различные структурные составляющие, имеющие разные физико-химические свойства, при контакте с электролитом приобретают неодинаковые по величине и знаку электродные потенциалы и одни из них станут анодами, а другие—катодами. Таким образом, технические металлы и сплавы при воздействии на них электролитов можно рассматривать как многоэлектродные элементы, состоящие из огромного числа микроскопически малых коррозионных гальванических пар — микротальванопар. Чем сильнее отличаются электродные потенциалы фаз, находящихся в сплаве, тем быстрее происходит его коррозионное разрушение (в частности, дендритная ликвация именно поэтому снижает стойкость против электрохимической коррозии). Отсюда следует, что высокую коррозионную устойчивость могут иметь либо очень чистые металлы, либо сплавы, имеющие однородную (гомогенную) структуру твердого раствора. Коррозионная стойкость стали может быть повышена, если во-первых, содержание углерода снизить до минимально возможного количества, во-вторых, ввести легирующий элемент, образующий с железом твердые растворы, в таком количестве, при котором скачкообразно повысится электродный потенциал сплава. Сталь, стойкую против атмосферной коррозии, называют нержавеющей. Сталь или сплав, имеющие высокую стойкость при коррозионном воздействии кислот, солей, щелочей и других агрессивных сред, называют кислотостойкими. Основным легирующим элементом всех марок нержавеющих сталей является хром. От коррозии сталь предохраняет прочная тонкая плотная пленка окислов хрома Cr2О3, которая образуется на поверхности деталей. Хрома должно быть не менее 12 – 13 %, в противном случае пленка не будет сплошной. Наибольшее распространение имеют хромистые и хромоникелевые нержавеющие стали. Л80 Латунь марки Л80 – это полутомпак, простой двойной сплав 80% меди и цинка, содержание которого не превышает 20%. В сплаве присутствуют добавки: сурьма, фосфор, свинец, железо, суммарное количество которых достигает 0,3%. Латунь Л80 изготавливается в соответствии с ГОСТ 15527-2004. Цинк выступает легирующим элементом, улучшающим свойства меди: повышает коррозионную стойкость и прочность сплава. Сплав меди с цинком называют латунью. Различают двухкомпонентные (простые) латуни, состоящие только из меди, цинка и некоторых примесей, и многокомпонентные (специальные) латуни, в которые вводят еще один или несколько легирующих элементов (свинец, кремний, олово) для придания сплаву тех или иных свойств. Двухкомпонентныелатуни в зависимости от способа обработки подразделяют на деформируемые и литейные. деформируемые двухкомпонентные латуни (Л96, Л90, Л80, Л63 и др. ) обладают высокой пластичностью и хорошо обрабатываются давлением, их используют для изготовления листов, ленты, полос, труб, проволоки и прутков разного профиля. Литейные латуни применяют для отливки фасонных деталей. В процессе холодной обработки давлением двухкомпонентные латуни, как и медь, получают наклеп, вследствие которого возрастает прочность и падает пластичность. Поэтому такие латуни подвергают термической обработке — рекристаллизационному отжигу по режиму: нагрев до 450—650° С, со скоростью 180—200° С/ч, выдержка 1,5—2,0 ч и охлаждение на спокойном воздухе. Прочность латуни после отжига σΒ = 240-320 МПа, относительное удлинение δ = 49-52%· Латунные изделия с большим внутренним напряжением в металле подвержены растрескиванию. При длительном хранении на воздухе на них образуются продольные и поперечные трещины. Чтобы избежать этого, изделия перед длительным хранением подвергают низкотемпературному отжигу при 250—300° С. Наличие в многокомпонентных (специальных) латунях легирующих элементов (марганца, олова, никеля, свинца и кремния) придает им повышенную прочность, твердость и высокую коррозионную стойкость в атмосферных условиях и морской воде. Наиболее высокой устойчивостью в морской воде обладают латуни, легированные оловом, например ЛО70-1, ЛА77-2 и ЛАН59-3-2, получившие название морской латуни, их применяют в основном для изготовления деталей морских судов. По способу обработки специальные латуни подразделяют на деформируемые и литейные. Деформируемые латуни используют для получения полуфабрикатов (листов, труб, ленты) , пружин, деталей часов и приборов. Литейные многокомпонентные латуни применяют для изготовления полуфабрикатов и фасонных деталей методом литья (гребные винты, лопасти, детали арматуры и т. п.) . Требуемые механические свойства специальной латуни обеспечивают термической обработкой их, режимы которой приведены в таблице. Для получения мелкого зерна перед глубокой вытяжкой деформируемые латуни для листов, лент, полос подвергают отжигу при температуре 450—500° С. Список литературы http://www.markmet.ru/kniga-po-metallurgii/meditsinskie-instrumenty http://www.instrumentalchik.ru/stali/3-instrumentalnye-stali.html http://www.mashb.ru/book_view.jsp?idn=019876&page=339&format=html http://www.studarhiv.ru/dir/cat40/subj145/file394/view394/page8.html http://www.menc.ru/book_view.jsp?idn=005581&page=451&format=html http://www.mtomd.info/archives/1651 |
