Понятие о патогенности и вирулентности бактерий. Факторы патоген. Понятие о патогенности и вирулентности бактерий. Факторы патогенности
 Скачать 217.11 Kb. Скачать 217.11 Kb.
|
АнтифагиТретья группа включает в себя бактерии, содержащие по верхностные структуры, обладающие антифагоцитарным действием. К ним относятся А-протеин золотистого стафилококка, М-протеин пи огенного стрептококка, vi-антиген сальмонелл, липиды корд-фактора микобактерий туберкулеза и др. Механизм антифагоцитарного дейст вия этих микробов объясняют не токсигенностью, а способностью бло кировать антитела (опсонины) или отдельные фракции комплемента (например, С3), способствующие фагоцитозу. Бациллы сибирской язвы, пневмококки могут синтезировать выраженную капсулу, хорошо заметную в мазках-отпечатках, приготовленных из свежего патологического материала или из культур, выращенных на сывороточных средах. Доказано, что капсульное вещество – полисахарида у пневмококков, полипептид d-глутаминовой кислоты у сибиреязвенной бациллы – не простая механическая преграда для бактерицидных соков организма, хи мических, лекарственных веществ, антибиотиков; капсула и ее вещество защищают бактерии от переваривания. Капсула подавляет фагоцитоз бактерий, обеспечивает их устойчивость к антителам и усиливает их инвазионные свойства. Например, капсулообразующие сибиреязвенные бациллы не подвергаются фагоцитозу, в то время как бескапсульные варианты легко фагоцитируются. Данный фактор патогенности сибиреязвенного микроба настоль ко важен, что его используют в качестве критерия для оценки степени вирулентности возбудителя сибирской язвы, а в медицин ской и ветеринарной практике успешно используют вакцины (СТИ и ВГНКИ) против этой болезни, представляющие собой взвесь жизнеспособных спор бескапсульных штаммов сибиреязвенных бацилл. К этой же группе факторов патогенности можно отнести нетоксичные неантигенные капсульные структуры некоторых стрептококков (например, группы А), построенные из гиалуроновой кислоты. Ввиду общности с межклеточным веществом макроорга низма они, вероятно, не распознаются хозяином и остаются нефагоцитированными. ТоксиныЧетвертая группа включает в себя токсины. Представления о природе микробных токсинов получены благодаря исследованиям патогенных бактерий.К 1890 г. были обнаружены первые токсины двух патогенных микроорганизмов: Corynebacterium diphtheriae и Clostridium tetani. В обоих случаях были поставлены одинаковые опыты: бактерию выращивали в культуральной среде in vitro, и стерильный фильтрат, приготовленный из выросшей культуры, вводили опытным животным. Последние погибали, а при их вскрытии обнаруживали изменения органов, характерные для соответствующей естественной инфекции. Эти токсические вещества оказались белками. Поскольку они представляли продукты обмена бактерий и не были связаны с бактериальными клетками, их назвали экзотоксинами. Экзотоксины образуют ряд других патогенных бактерий (возбудитель ботулизма, инфекционной энтеротоксемии, дизентерии и др.), в основном грамположительных. Однако фильтраты, приготовленные из культур многих других патогенных микроорганизмов, не были токсичны. Кипячением бактериальных культур доказано, что клетки почти всех грамотрицательных патогенных бактерий токсичны сами по себе. Более того, такое же токсическое действие оказывают и убитые нагреванием клетки многих патогенных грамотрицательных бактерий. Устойчивые к нагреванию токсины, связанные с клеточной оболочкой грамотрицательных бактерий, назвали эндотоксинами. Однако для многих патогенных бактерий, в том числе для возбудителя сибирской язвы, эти подходы не позволили обнаружить никаких сколько – нибудь токсичных продуктов. Условия культивирования в лаборатории всегда отличаются от условий в организме зараженного животного. Осознание этого очевидного факта заставило предпринять поиски бактериальных токсинов, образуемых непосредственно в организме инфицированного животного. Эта работа привела к обнаружению специфического экзотоксина у Bacillus anthracis. Токсичность – способность патогенного микроба вырабатывать и выделять ядовитые вещества, вредно действующие на организм. Микробы, способные образовывать токсины, получили название токсигенных. Токсины бывают двух видов – экзотоксины и эндотоксины. Экзотоксины – высокоактивные яды, выделяемые микроорганизмом на протяжении его жизни в качестве продуктов обмена в окружающую среду (организм животного, пробирка с культурой микроба). Обнаруживаются в высоких концентрациях в жидких средах, содержащих компоненты клеточной стенки грамотрицательных бактерий, освобождающиеся при их дезинтеграции полипептиды, ОММ 10000–100000. Липополисахаридные комплексы, липид А, очевидно, ответственен за токсичность. Эндотоксины – менее ядовитые по сравнению с экзотоксинами вещества, образующиеся в результате распада микробной клетки. Следовательно, эндотоксины представ ляют собой фрагменты или отдельные химические компоненты микробных клеток. Экзотоксины в основном образуют грамположительные микроорганизмы (возбудители ботулизма, столбняка, газовой инфекции и др.), а эндотоксины образуют клетки грамотрицательных мик робов (сальмонеллы, кишечная палочка, протей и др.). Сравнительная характеристика экзотоксинов и эндотоксинов следующая:
Химическая природаТоксические вещества, синтезируемые бактериями, по своей химической природе относятся к белкам и липополисахаридам. Однако белковые токсины предназначены не только для поражения клеток, тканей и органов животного и человека. Возможно также их участие в метаболических реакциях самих бактерий-продуцентов. Липополисахариды (ЛПС) - эндотоксины - локализуются в клеточной стенке бактерий и освобождаются только после их разрушения. Наряду с ЛПС токсическими свойствами обладают пептидогликан, тейхоевые кислоты, белки клеточной стенки грамположительных бактерий (например, протеин А стафилококка). Белковые токсины. В настоящее время описано свыше 80 бактериальных токсинов, которые отличаются друг от друга по молекулярной массе, химической структуре, клеточным «мишеням» макроорганизма и биологической активности. Одни из них являются термолабильными, другие термостабильными. Так, например, термолабильный дифтерийный гистоксин разрушается при 60°С в течение 1 ч, а столбнячный - в течение 20 мин. Термостабильные токсины клостридий ботулизма С. botulinum, кишечной палочки, стафилококков могут переносить кратковременное кипячение. Независимо от сложности строения токсины имеют два центра. Один из них фиксирует молекулу токсина на соответствующем клеточном рецепторе, второй - токсический фрагмент - проникает внутрь клетки, где блокирует жизненно важные метаболические реакции. Клеточные рецепторы для разных токсинов неодинаковы. Так, на холинсодержащих рецепторах фиксируются тетанолизин, О-стрептолизин, пневмолизин и др., на ганглиозидах определенного типа - тетаноспазин, холероген, энтеротоксины кишечных бактерий и др. Биологическая активность белковых токсинов проявляется в специфичности токсического действия, антигенных и иммуногенных свойствах. Специфичность токсического действия определяется избирательной фиксацией токсина на рецепторах клеток-«мишеней» определенных тканей (эпителиальной, нервной и др.) организма человека и животных. Различия в механизме действия данных токсинов позволили классифицировать четыре типа, каждый из которых состоит из нескольких групп. Токсины, отнесенные к типу «цитотоксины», блокируют синтез белка на субклеточном уровне. Например, группа антиэлонга-торов, включающая дифтерийный гистотоксин, токсин синегнойной палочки и др., выводят из строя фермент трансферазу II, ответственную за элонгацию (наращивание) полипептидной цепи на рибосоме. Наряду с ними к данному типу принадлежат токсины с энтеропатогенной активностью и дермонекротоксины, поражающие соответствующие ткани и органы. Второй тип - «мембранотоксины» - повышают проницаемость поверхностной мембраны эритроцитов (гемолизины) и лейкоцитов (лейкоцидины), вызывая гемолиз первых и разрушение вторых. Это связано с тем, что мембранотоксины, встраиваясь в мембрану клетки, образуют в ней канал, который гидрофилен внутри и гидрофобен снаружи. В результате происходит нарушение саморегуляции клетки, погибающей от осмотического шока. Гемолuзuны. Некоторые микроорганизмы (стрептококки, стафи лококки) продуцируют экзотоксины (гемолизины), растворяющие эритроциты крови. Бактерийные гемолизины следует отличать от иммуногемолизинов, которые возникают в организме и обнаруживаются в сыворотке крови животных при иммунизации последних эритроцитами. Различают альфа-, бета- и дельта- бактерийные гемолизины. Альфа-гемолизины вызывают гематометаморфоз железа эритроци тов (переход гемоглобина в метгемоглобин). В результате этого образуются зеленые продукты, которые окрашивают кровяной агар вокруг колонии растущего микроба в зеленый или грязно-зеленый цвет. Этим свойством обладает зеленящий стрептококк. Бета-гемолизины целиком растворяют эритроциты крови; они нарушают адсорбционную связь между гемоглобином и стромой эритроцитов. Поэтому кровь гемолизируется, становится прозрач ной, лаковой. К микроорганизмам, вырабатывающим гемолизины, относятся возбудители листериоза, гемолитические стрептококки, стафилококки, которые формируют на кровяном агаре вокруг колоний бесцветную прозрачную гемолитическую зону, иногда значительно превышающую диаметр колоний. Дельта-гемолизин разрушает эритроциты человека и некоторых животных. Вырабатывается патогенными стафилококками. Отличие бактерийных гемолизинов заключается в неодинаковом механизме повреждающего действия. Лейкоцuдuн. Установлено, что некоторые грамположительныс кокки (стафилококки, стрептококки) могут вырабатывать особый вид экзотоксина - лейкоцидин, парализующий активность лейкоци тов и разрушающий их. Третий тип - «функциональные блокаторы» - включают термолабильные (ТЛ) и термостабильные (ТС) энтеротоксины. Энтеротоксины – белки, вызывающие расстройства желудочно-кишечного тракта у животных вследствии активизирования клеточной аденилатциклазы, что приводит к повышению проницаемости сосудов стенки тонкой кишки и выходу жидкости, ионов натрия и хлоридов кальция в просвет кишечника. Это вызывает нарушение обменных процессов и развитие диарей. Этот тип включает, например, холероген, термолабильные энтеротоксины Е. coli и других энтеро-бактерий. Энтеротоксины (экзотоксины) обнаружены у эшерихий, стафилококков и других микроорганизмов. К функциональным блокаторам принадлежат токсикоблокаторы (к ним относятся сибиреязвенный и чумной, «мышиный», токсины, которые в отличие от ТЛ- и ТС-энтеротоксинов инактивируют аденилатциклазу, являясь антагонистами данного фермента) и нейротоксины. Нейротоксины обладают выраженной тропностью: к цен тральной нервной ткани (тетанолизин - токсин столбнячного микроба); к периферической ткани (ботулинические нейротокси ны); к отдельным звеньям симпатической нервной системы, ней рогуморальной системе и др. Возбудитель столбняка (Clostridium tetani) продуцирует токсин, который путем ретроградного движения по аксонам проникает в ЦНС, где происходит его фиксация ганглиозидами. Токсин усиливает рефлекторную возбудимость в нейронах спинного мозга, подавляя освобождение ингибиторного медиатора в синапсах нейронов. Он также нарушает синаптическую передачу в нервно–мышечном соединении; в результате этих процессов возникают мышечные спазмы. Токсин возбудителя ботулизма (Clostridium botulinum) блокирует освобождение ацетилхолина в синапсах и нервно–мышечных соединениях, вызывая дисфагию, паралич дыхательной мускулатуры, а также двигательные параличи. К четвертому типу относятся эксфолиатины и эритрогенины, образуемые некоторыми штаммами золотистого стафилококка и скарлатинозным стрептококком. Они влияют на процесс взаимодействия клеток между собой и с межклеточными веществами. Высокую токсичность белковых токсинов можно объяснить особенностью строения участков их молекул, имитирующих структуру субъединиц гормонов, ферментов и нейромедиаторов макроорганизма. Это делает их антиметаболитами вышеупомянутых жизненно важных соединений, блокирующих функциональную активность последних. Токсичность измеряется в тех же единицах, в которых оценивается вирулентность, - DLM и LD50. Иммуногенные свойства белковых токсинов проявляются в способности вызывать иммунный ответ со стороны макроорганизма, в частности индуцировать синтез специфических антител - антитоксинов, нейтрализующих гомологичный токсин. Следующей особенностью ряда белковых токсинов, например столбнячного, дифтерийного и некоторых других, является их способность под действием формалина утрачивать свою ядовитость, сохраняя при этом иммуногенные свойства. Такие токсины получили название анатоксинов. Они применяются в качестве вакцин для профилактики одноименных заболеваний. Многие бактерии образуют не один, а несколько белковых токсинов, обладающих разным действием: летальным, дермонекротическим, цитотоксическим, нейротоксическим, гемолитическим. Липополисахариды. К ним относятся эндотоксины. Липополисахариды (ЛПС) содержатся в клеточной стенке грамотрицательных бактерий. Токсические свойства эндотоксина определяются всей молекулой ЛПС, а не отдельными ее частями: полисахаридами или липидом А. Хорошо изучены эндотоксины энтеробактерий (эшерихии, шигеллы и сальмонеллы, бруцеллы, туляремийные бактерии). ЛПС (эндотоксины) в отличие от токсинов белковой природы (экзотоксинов) более устойчивы к повышенной температуре, менее ядовиты и малоспецифичны. Различные ЛПС при введении в организм подопытных животных вызывают более или менее однотипную реакцию, независимую от того, из каких грамотрицательных бактерий они выделены. При введении больших доз у животных наблюдаются угнетение фагоцитоза, явления выраженного токсикоза, сопровождающегося слабостью, одышкой, расстройством кишечника (диарея), падением сердечной деятельности и понижением температуры тела. При введении небольших доз отмечается обратный эффект: стимуляция фагоцитоза, менее выраженный токсикоз, повышение температуры тела. Некротоксин(гистотоксин) приводит ткань к омертвению, тормо зит теплорегуляцию, понижая температуру тела. Это полисахаридо липоидные комплексы, вырабатываемые сальмонеллами, коринс бактериями, кокками, анаэробами, нередко изменяют содержание са хара в крови, изъязвляют слизистую оболочку тонких кишок, что обусловливает появление кровавых диарей. Гистотоксины при внут рикожном введении приводят к деструкции клеток системы мононук леарных фагоцитов или активации протеолитических ферментов. ЛПС - сравнительно слабый иммуноген. Сыворотка крови животных, иммунизированных чистым эндотоксином, не обладает высокой антитоксической активностью и не способна полностью нейтрализовать его ядовитые свойства. Как уже было сказано выше, к эндотоксинам можно отнести пептидогликан, тейхоевые и липотейхоевые кислоты, содержащиеся в клеточной стенке. Все эндотоксины, кроме пептидогликана, оказывают опосредованное действие через изменение активности клеток организма. ДНК бактерий не являются в этом случае иссечением. Непосредственным эффектором ДНК является динуклеотид цитозин-гуанин. В организме человека такие пары метилированы, а у бактерий они свободны и легко проникают в клетку, где распознаются иммунной системой, в результате чего происхо-дит выброс цитокинов, контролирующих воспаление. Пептидоглиан оказывает прямое токсическое действие. Так, например, пептидогликан клеточной стенки гонококков непосредственно поражает эпителий уретры. Некоторые бактерии одновременно образуют как белковые токсины, так и эндотоксины, например кишечная палочка, холерный вибрион и др. Токсины Bacillus anthracis представляют собой комплекс из двух или более веществ. Само по себе каждое из них нетоксично, но в результате их взаимодействия в организме возникает токсический эффект. Для понимания патогенеза недостаточно выделить токсичное вещество из патогенной бактерии. Чтобы выяснить, обусловливает ли такое вещество вирулентность, следует показать, что оно вызывает один или несколько симптомов болезни. Кроме того, место действия и эффективная концентрация вещества должны соответствовать таковым при инфекции, возникающей в естественных условиях. Эти требования, имеющие экологическое значение, очень трудно удовлетворить, и полностью они были выполнены лишь в немногих случаях. Часто используют еще два критерия: корреляцию между образованием токсина и вирулентностью у различных штаммов патогенного вида и способность соответствующей антитоксичной сыворотки защищать животных от заболевания. Гены, определяющие синтез бактериальных экзотоксинов, во многих случаях локализованы в плазмидах или профагах, которые несет бактерия, а не в бактериальной хромосоме. К настоящему времени установлено, что эритрогенный токсин Streptococcus pyogenes, энтеротоксин, a–токсин Staphylococcus aureus и токсин Clostridium botulinum детерминируются генами профага, а ряд токсинов, продуцируемых Escherichia coli,– плазмидными генами. Во всех случаях утрата профага или плазмиды делает клетку нетоксигенной, а при введении профага или плазмиды в клетку образование токсина восстанавливается. Химический состав
Роль эндотоксина в повышении устойчивости к заражению неспецифична, и механизм этого явления не известен. Такая устойчивость может играть весьма важную роль в природе, поскольку все млекопитающие постоянно подвергаются действию эндотоксинов кишечных бактерий. В клинических и экспериментальных условиях при введении эндотоксина кишечных бактерий отмечают следующие наиболее выраженные изменения: лихорадка, лейкопения, гипогликемия, гипотония и шок, нарушение кровоснабжения жизненно важных органов, активизация СЗ (компонент комплемента), внутрисосудистый тромбоз и смерть. Механизм действияТоксин в целом нарушает постоянство внутренней среды организма путем изменения его метаболических функций. Действие экзотоксинов проявляется в разрушении определенных субклеточных структур или в нарушении определенных клеточных функций: в ряде случаев удалось продемонстрировать действие очищенных токсинов на органоиды чувствительных клеток. Экзотоксины обладают цитотоксическим, пирогенным, антикомплементарным, ингибирующим дыхательную функцию митохондрии действием. Они лизируют эритроциты (род Streptococcus), гидролизуют лейкоциты (Cl.perfringens), вызывают поражения центральной и вегетативной нервных систем (Staphylococcus aureus), нарушают функции органов пищеварения (род Staphylococcus). Истинные энтеротоксины связываются со специфическими рецепторами мембран чувствительных клеток. Связанный токсин активизирует мембранную аденилатциклазу, что вызывает резкое увеличение концентрации циклического АМФ в клетке. Это, в свою очередь, нарушает регуляторные процессы в клетке и вызывает анормальное повышение скорости переноса электролитов, их утечку из тканей. Вместе с электролитами уходит вода; потеря тканевой жидкости приводит к ацидозу и шоку. Если не восполнить потери жидкости и электролитов, циркулирующих в организме, может наступить смерть. Экзотоксины вызывают глубокие изменения обмена веществ, что сопровождается интоксикацией. В отличие от химических ядов действие токсинов проявляется после определенного инкубационного периода. Эндотоксины состоят из трех фрагментов, и по разному действию их можно разделить на липополисахаридную, обладающую пирогенной активностью и токсичностью, и белковую фракции. Последняя не обладает ни той, ни другой активностью, но сообщает всему комплексу антигенные свойства. Очищенные эндотоксины как вирулентных, так и авирулентных энтеробактерий при введении животным вызывают многие патологические явления. Они также вызывают воспаление, которое увеличивает проницаемость капилляров и разрушает клетки. Из разрушенных клеток в свою очередь выделяются воспалительные агенты, которые усугубляют поражения. Эндотоксины, не действуя непосредственно на терморегуляторные центры головного мозга, вызывают освобождение эндогенного пирогенного вещества из полиморфно–ядерных лейкоцитов. Это вещество, химическая природа которого до сих пор неизвестна, вызывает повышение температуры. У животных и людей поступление эндотоксинов в кровяное русло приводит к лихорадке в результате их действия и на клетки крови (гранулоциты, моноциты), из которых выделяются эндогенные пирогены. Начало лихорадки совпадает с ранней лейкопенией, которая сменяется вторичным лейкоцитозом. В результате усиления гликолиза в клетках разных типов может возникнуть гипогликемия. При эндотоксинемии имеют место гипотония в результате поступления в кровь повышенного количества серотонина и кининов, а также нарушение кровоснабжения органов и ацидоз. ЛПС активирует фракцию СЗ комплемента по альтернативному пути, что приводит к снижению его уровня в сыворотке крови и накоплению биологически активных фракций (СЗа, СЗb, С5а и др.). Большие количества поступившего в кровь эндотоксина приводят к токсико-септическому шоку. Эндотоксины повышают порозность мелких кровеносных сосудов, выход из капилляров и разрушение лейкоцитов с образованием новых пирогенов. Липополисахарид ингибирует дыхательную функцию митохондрий клеток печени и сердца. Антикомплементарное действие эндотоксинов снижает в организме концентрацию основных хемотаксических и опсонирующих факторов. Эндотоксины продуцируют бруцеллы, сальмонеллы, возбудители туберкулеза, сапа и многие другие в основном грамотрицательные бактерии. Особенно характерны эти яды для семейства кишечных бактерий. Термостабильные токсические вещества, нарушающие обмен веществ в восприимчивых клетках, обнаружены и у некоторых вирусов. Эндотоксины энтеробактерий при введении их животным в небольших дозах вызывают временные изменения неспецифической устойчивости к инфекции. Рис. 2 Совокупность факторов патогенности бактерии и их влияние на макроорганизм 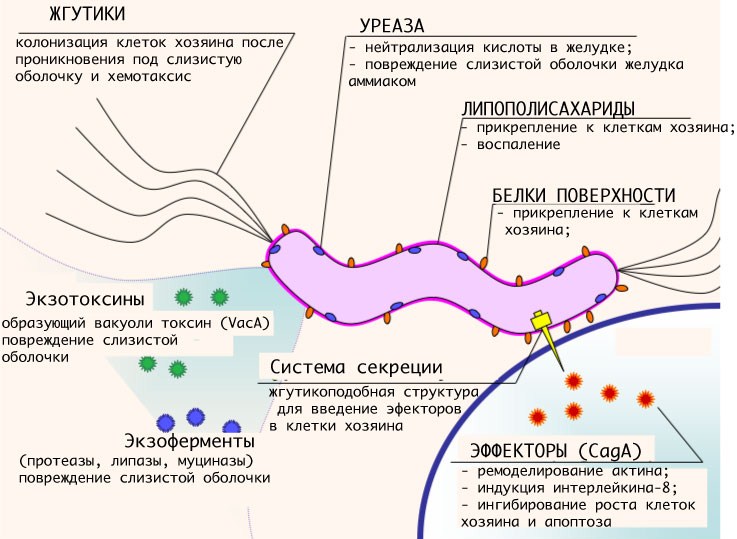 ЗаключениеМногие микроорганизмы способны вызывать патологические изменения в организме животного, что приводит к различным заболеваниям. Однако эта способность неодинакова у разных микробов. Это объясняется патогенностью и вирулентностью каждого отдельного микроорганизма, а так же совокупностью факторов макроорганизма и условий внешней среды. Обзор факторов патогенности позволяет составить общее представление, каким образом микроб может наносить тот или иной вред организму. При этом один вид патогенных микроорганизмов, как правило, образует несколько токсинов. Большое количество различных токсинов образуют клостридии, патогенные кокки, энтеробактерии и др. Различия в химической структуре этих факторов и в механизме действия затрудняют их систематизацию. Однако в микробиологии ферментативная активность бактерий уже давно служит приемом дифференциальной диагностики отдельных видов микроорганизмов. Таким образом, факторы вирулентности приводят основные системы организма к дисфункции, в силу чего последний погибает. Однако нельзя думать, что каждый вирулентный штамм патогенных микроорганизмов обладает всей суммой указанных факторов виру лентности: одного-двух из них иногда бывает достаточно, чтобы ослабить реактивность животного и вызвать его гибель. Список литературы
|
