Электрогенез в клетках. Потенциал покоя
 Скачать 1.16 Mb. Скачать 1.16 Mb.
|
|
Потенциал покоя Экспериментально установлено, что между поверхностями биомембраны невозбужденной клетки существует разность потенциалов, часто называемая для краткости потенциалом покоя: 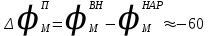 ÷ ÷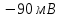 Однако до начала XX века этот вопрос (как и вообще природа электричества в живом организме) был предметом спора, суть которого можно коротко выразить тезисом: непонятно, возникает ли электричество, например, в мышце только в момент ее повреждения или существует и до него. Э. Бернштейну удалось понять, что электрические свойства мышц и нервов обусловлены не особенностями их устройства как целого, а свойствами и особенностями мембран составляющих их клеток. Этот ученый по праву считается основателем мембранной теории биопотенциалов Разберем, что такое потенциал покоя и как он возникает. Представим себе, что внутри клетки имеется много свободных ионов какого-нибудь элемента (рис. 1.) и клеточная мембрана пропускает только эти ионы. Естественно, они начнут двигаться наружу, и вместе с ними наружу будет выноситься положительный заряд. В результате между внутренней и наружной поверхностями мембраны возникает разность потенциалов (рис. 2). Потенциал наружной поверхности будет больше, чем потенциал внутренней (при этом разность концентраций ионов внутри и снаружи будет к этому моменту еще довольно значительной). Эта разность потенциалов будет тормозить движение наружу новых положительных ионов, и увеличивать их поток внутри клетки. В конце концов, эти потоки станут равными по величине (установится динамическое равновесие), а суммарный поток будет равным нулю. Установившаяся при этом между поверхностями биомембраны разность электрических потенциалов и есть потенциал покоя. Его величину можно вычислить из условия равенства электрохимических потенциалов внутри и снаружи клетки 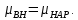 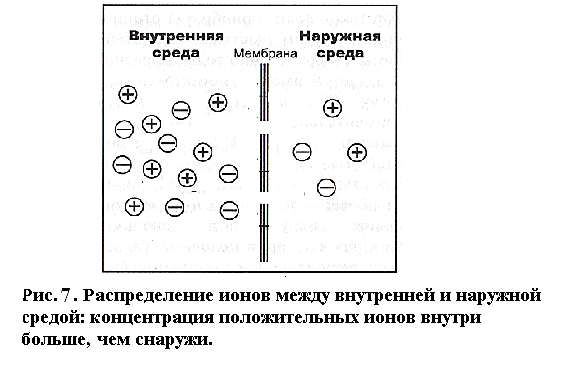 Рис. 1. Распределение ионов между внутренней и наружной средой: концентрация положительных ионов внутри больше, чем снаружи 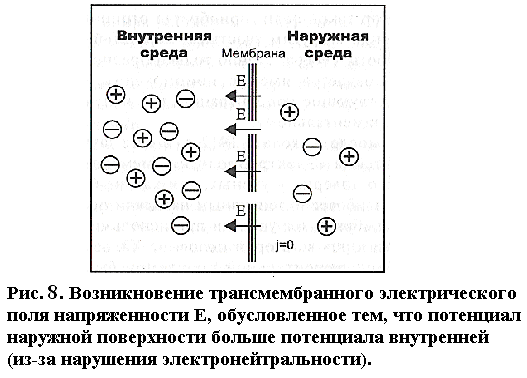 Рис. 2. Возникновение трансмембранного электрического поля напряженности Е0, обусловленное тем, что потенциал наружной поверхности больше потенциала внутренней Рис. 2. Возникновение трансмембранного электрического поля напряженности Е0, обусловленное тем, что потенциал наружной поверхности больше потенциала внутреннейИспользуя формулу для нахождения электрохимического потенциала, получим: 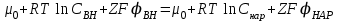 После несложных преобразований получим: 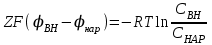 Разность 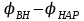 и есть обсуждаемый нами потенциал покоя: и есть обсуждаемый нами потенциал покоя: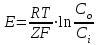 уравнение Нернста. уравнение Нернста.Очень слабым местом мембранной гипотезы в то время было отсутствие данных о том, концентрацию каких ионов следует подставлять в полученную формулу, чтобы получить значение 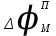 близкое к наблюдаемому в эксперименте. Стоило только предположить, что потенциал покоя создается именно ионом калия и подставить в формулу соответствующие концентрации, как получался результат, близкий к экспериментальному. близкое к наблюдаемому в эксперименте. Стоило только предположить, что потенциал покоя создается именно ионом калия и подставить в формулу соответствующие концентрации, как получался результат, близкий к экспериментальному.Еще одной экспериментальной проблемой было определение ионного состава внутренней среды. Кроме того, сторонникам мембранной теории надо было показать не просто присутствие калия внутри клеток, а присутствие именно свободных, несвязанных ионов калия. В 1936 г. английский специалист по головоногим моллюскам Дж. Юнг обнаружил у кальмаров нервное волокно, диаметр которого доходит до 1 мм, т.е. гигантское по клеточным масштабам, хотя сам моллюск вовсе не был гигантом. Такое волокно, выделенное из организма и помещенное в морскую воду, не погибало. В 1939 г. английский ученый А. Ходжкин и его ученик А. Хаксли впервые измерили разность потенциалов на мембране животной клетки. Удалось также доказать, что внутри этого волокна действительно много ионов калия и эти ионы представляют собой «ионный газ», т.е. могут участвовать в создании мембранного потенциала. Расчетное значение потенциала покоя неплохо совпадало с непосредственно измеренным (около 60 мВ). Использование ионочувствительных электродов в сочетании с методом меченых атомов и другими методами позволило определить и ионный состав внутриклеточного содержимого. Оказалось, что, как и предсказывала мембранная теория, внутри клеток концентрация ионов калия в 30-40 раз выше, чем в наружной среде. В 1961 г. А. Ходжкин, Бейкер и Шоу поставили интересный опыт: они брали гигантский аксон кальмара, выдавливали из него протоплазму и получали пустую трубку из одной мембраны. Появилась возможность работать на мембране нервного волокна, произвольно меняя концентрацию вещества и внутри, и снаружи. Оказалось, что при заполнении аксона раствором, содержащим такую же концентрацию калия, как и в протоплазме, в аксоне возникал потенциал покоя 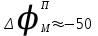 ÷ ÷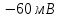 Если концентрация калия внутри и снаружи волокна была одинаковой, то потенциал покоя в полном соответствии с формулой Нернста не возникал. Если внутрь волокна накачивали морскую воду, а в наружную среду – раствор с высокой концентрацией калия, знак потенциала покоя менялся, а его величина соответствовала формуле Нернста. Это стало важным подтверждением теории Бернштейна. Если концентрация калия внутри и снаружи волокна была одинаковой, то потенциал покоя в полном соответствии с формулой Нернста не возникал. Если внутрь волокна накачивали морскую воду, а в наружную среду – раствор с высокой концентрацией калия, знак потенциала покоя менялся, а его величина соответствовала формуле Нернста. Это стало важным подтверждением теории Бернштейна. Когда методы измерения потенциала покоя достигли высокой точности, обнаружилось, что на самом деле измеряемый потенциал покоя всегда ниже, чем теоретически вычисленный по формуле Нернста. Ясно, что существует какой-то возмущающий фактор, не учтенный теорией Бернштейна. Найти причину расхождения эксперимента и теории помог опять - таки кальмар. Работая с гигантским аксоном, А. Ходжкин и Б. Катц установили, что потенциал покоя, измеряемый в опыте, оказывается ближе всего к теоретическому в одном особом случае: если из наружной среды исключен натрий. Оказалось, что для совпадения экспериментальных данных с расчетными приходится принять, что сопротивление, которое «преодолевают» ионы натрия, в 25 раз больше, чем для калия. Это означает, что проницаемость мембраны для ионов натрия хотя и в 25 раз меньше, чем для калия, но все же не равна нулю. Вскоре предположение, что ионы натрия могут проходить через мембрану гигантского аксона, было прямо доказано в опытах с радиоактивным изотопом натрия. Учтя влияние на величину потенциала покоя и ионов натрия и хлора, в 1949г. Гольдман, Ходжкин и Катц вывели для величины потенциала покоя уравнение (оно называется уравнением Гольдмана): 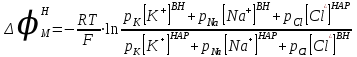 Оно было получено из того предположения, что в невозбужденном состоянии через поверхность мембраны проходят потоки ионов калия, натрия и хлора, алгебраическая сумма которых должна быть равна нулю: 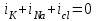 Очевидно, если в этом уравнении вновь пренебречь проницаемостью мембраны для ионов натрия и хлора по сравнению с проницаемостью для иона калия, оно автоматически станет уравнением Нернста. Потенциал действия Потенциалы действия (нервные импульсы) могут возникать только в возбудимых клетках. К ним относятся клетки нервной системы, клетки скелетной мускулатуры, кардиомиоциты и ряд других. Посредством потенциалов действия в живом организме передается информация от рецепторов к нейронам мозга и от нейронов мозга к мышцам. Потенциалом действия называется электрический импульс, возникающий между внутренней и наружной сторонами мембраны и обусловленный изменением ионной проницаемости мембраны. 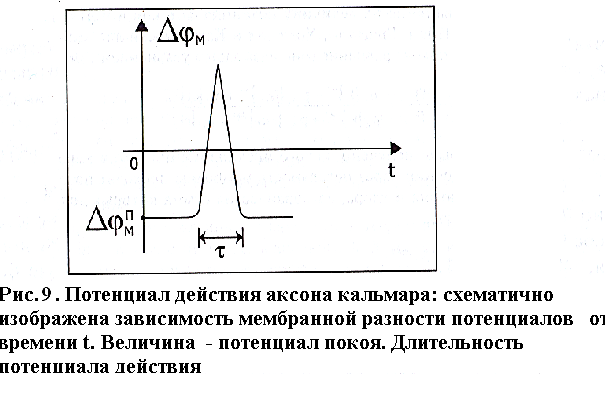 Э. Бернштейн, изучая процесс возбуждения клеточной мембраны, предсказал изменение ее проницаемости для различных ионов. В 1939 г. Коул и Кертис (США) и Ходжкин и Хаксли (Великобритания) измеряли потенциалы невозбужденной и возбужденной клеток на гигантском аксоне кальмара: оказалось, что в состоянии покоя разность потенциалов была примерно равна - 80 мВ (отрицательная), а максимальная разность потенциалов при возбуждении + 40мВ (положительная). Далее Ходжкин и Хаксли сформулировали гипотезу о том, что при возбуждении меняется характер проницаемости мембраны для разного типа ионов: из проницаемой главным образом для калия она превращается в проницаемую для натрия и, следовательно, поток ионов натрия внутрь клетки увеличивается. Разносность потенциалов между поверхностями мембраны поднимается до нуля, а затем становится положительной – наступает деполяризация мембраны. Далее процесс развивается в обратном направлении: поток ионов натрия внутрь клетки постепенно уменьшается и возвращается к невозбужденному» значению; разность потенциалов также возвращается к значению Э. Бернштейн, изучая процесс возбуждения клеточной мембраны, предсказал изменение ее проницаемости для различных ионов. В 1939 г. Коул и Кертис (США) и Ходжкин и Хаксли (Великобритания) измеряли потенциалы невозбужденной и возбужденной клеток на гигантском аксоне кальмара: оказалось, что в состоянии покоя разность потенциалов была примерно равна - 80 мВ (отрицательная), а максимальная разность потенциалов при возбуждении + 40мВ (положительная). Далее Ходжкин и Хаксли сформулировали гипотезу о том, что при возбуждении меняется характер проницаемости мембраны для разного типа ионов: из проницаемой главным образом для калия она превращается в проницаемую для натрия и, следовательно, поток ионов натрия внутрь клетки увеличивается. Разносность потенциалов между поверхностями мембраны поднимается до нуля, а затем становится положительной – наступает деполяризация мембраны. Далее процесс развивается в обратном направлении: поток ионов натрия внутрь клетки постепенно уменьшается и возвращается к невозбужденному» значению; разность потенциалов также возвращается к значению 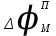 . .Рис. 3. Потенциал действия Такой импульс (рис. 3) называют потенциалом действия. Термин деполяризация означает исчезновение поляризации, а реполяризация – ее последующее восстановление. В состоянии покоя мембрана поляризована, т.е. потенциал цитоплазмы отрицателен по отношению к внеклеточной среде. При возбуждении происходит деполяризация мембраны, и после снятия возбуждения происходит реполяризация мембраны (рис. 4). После снятия возбуждения еще в течении 1-2 мс в мембране наблюдаются остаточные явления, во время которых мембрана остается рефрактерной, т. е. невозбудимой. 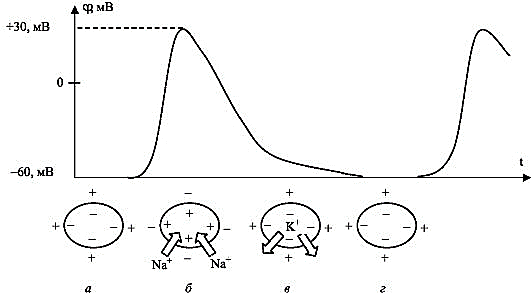 Рис. 4. Возникновение потенциала действия и деполяризация мембраны В дальнейшем Ходжкин и Хаксли предложили математическую модель, которая описывала изменения проводимостей, а, следовательно, и токов ионов натрия и калия через мембрану в процессе возбуждения. Эксперименты подтвердили: первая фаза потенциала действия связана с потоком ионов натрия внутрь клетки, а вторая – с потоком ионов калия наружу в процессе возбуждения изменяются проводимости, следовательно, и токи ионов натрия и калия через мембрану в мембране существуют отдельные каналы для переноса ионов натрия и калия. Математическая модель Ходжкина – Хаксли хорошо позволяет теоретически объяснить наблюдаемые в эксперименте свойства потенциала действия: 1. ПД - это короткий импульс длительностью 2-3 мс 2. наличие порогового значения деполяризующего потенциала; 3. закон «все или ничего»: если деполяризующий потенциал больше порогового, то развивается потенциал действия, амплитуда которого не зависит от амплитуды возбуждающего импульса; если амплитуда деполяризующего потенциала меньше пороговой, то потенциала действия не возникает; 4. наличие периода рефрактерности (невозбудимости) мембраны во время развития потенциала действия и остаточных явлений после снятия возбуждения. Ионные канала и ионные насосы Ионные каналы — порообразующие белки (одиночные либо целые комплексы), поддерживающие разность потенциалов, которая существует между внешней и внутренней сторонами клеточной мембраны всех живых клеток. Относятся к транспортным белкам.  Рис. 5. Схема ионного канала Ионные каналы мембраны представляют собой интегральные белки мембраны, которые образуют отверстия в мембране, заполненные водой. • В плазматической мембране обнаружен ряд ионных каналов, которые характеризуются высокой специфичностью, допускающей перемещение только одного вида ионов. Существуют натриевые, калиевые, кальциевые и хлорные каналы. • Каждый из них имеет так называемый селективный фильтр, который способен пропускать только определённые ионы. Проницаемость ионных каналов может изменяться благодаря наличию ворот - определенных групп атомов в составе белков, формирующих канал. • Конформационные изменения ворот переводят канал из открытого состояния в закрытое и наоборот. Механизмы регуляции положения ворот могут отличаться в различных каналах. • Некоторые из них открываются при изменениях электрического потенциала мембраны. • Другие открываются под действием специфических химических веществ, выполняющих сигнальные функции. К 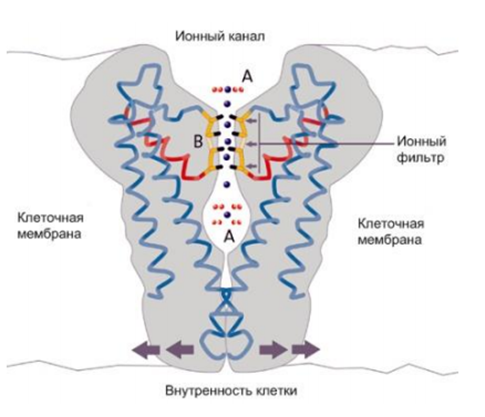 лассификация ионных каналов по их функциям: лассификация ионных каналов по их функциям:1) по количеству ионов, для которых канал проницаем, каналы делят на селективные (проницаемы только для одного вида ионов) и неселективные (проницаемы для нескольких видов ионов); 2) по характеру ионов, которые они пропускают на Na+, Ca++, Cl-, K+-каналы; 3) по способу регуляции делятся на потенциалзависимые и потенциалнезависимые. Потенциалзависимые каналы реагируют на изменение потенциала мембраны клетки, и при достижении потенциалом определенной величины, канал переходит в активное состояние, начиная пропускать ионы по их градиенту концентрации. Так, натриевые и быстрые кальциевые каналы являются потенциалзависимыми, их активация происходит при снижении мембранного потенциала до 50-60 мВ, при этом ток ионов Na+ и Ca++ в клетку вызывает падение потенциала и генерацию ПД. Калиевые потенциалзависимые каналы активируются при развитии ПД и, обеспечивая ток ионов К+ из клетки, вызывают реполяризацию мембраны. Потенциалнезависимые каналы (хемоуправляемые) реагируют не на изменение мембранного потенциала, а на взаимодействие рецепторов, с которыми они взаимосвязаны, и их лигандов (лиганд — это химическое соединение, которое образует комплекс определенной биомолекулой (чаще всего белком, например клеточным рецептором) и производит, вследствие такого связывания, определенные биохимические, физиологические или фармакологические эффекты. Эти каналы открываются, когда медиатор, связываясь с их наружными рецепторными участками, меняет их конформацию. Открываясь, они впускают ионы, изменяя этим мембранный потенциал. Лиганд-зависимые каналы почти нечувствительны к изменению мембранного потенциала. Они генерируют электрический потенциал, сила которого зависит от количества медиатора, поступающего в синаптическую щель и времени, которое он там находится Неуправляемые (независимые) ионные каналы. Эти каналы обычно находятся в открытом состоянии и постоянно пропускают через себя ионы за счёт диффузии по градиенту их концентрации и/или по электрическому градиенту зарядов по обе стороны мембраны. Некоторые неуправляемые каналы различают вещества и пропускают через себя по градиенту концентрации все молекулы меньше определённой величины, их называют «неселективные каналы» или «поры». Существуют также «селективные каналы», которые благодаря своему диаметру и строению внутренней поверхности переносят только определённые ионы. Примеры: калиевые каналы, участвующие в формировании мембранного потенциала покоя, хлоридные каналы. Стимул-управляемые (механочувствительные, механосенситивные, активируемые растяжением (stretch) липидного бислоя, протон-активируемые, температурно-чувствительные). Совместно-управляемые. Они открываются одновременно как лигандами, так и определённым электрическим потенциалом мембраны. Можно сказать, что у них двойное управление. Инактивация — это способность ионного канала через некоторое время после своего открытия автоматически понижать свою проницаемость даже в том случае, когда открывший их активирующий фактор продолжает действовать. Блокировка — это способность ионного канала под действием веществ-блокаторов фиксировать какое-то одно своё состояние и не реагировать на обычные управляющие воздействия. Блокировку вызывают вещества-блокаторы, которые могут называться антагонистами, блокаторами или литиками. Пластичность — это способность ионного канала изменять свои свойства, свои характеристики. Для исследования тока из одного отдельного канала был разработан метод локальной фиксации потенциала. Микроэлектрод подводится к мембране так чтобы он располагался только в одном канале. Рис.7. показывает: а-установление с помощью специальной схемы фиксированной разности потенциалов на мембране; б – зависимость тока от времени. Расположение графика в отрицательной области свидетельствует о том, что ток ионов натрия направлен внутрь клетки. По абсолютной величине он сначала возрастает, а затем вновь убывает; в – зависимость тока от времени. Расположение кривой в положительной области свидетельствует о том, что ток ионов калия направлен наружу. Возрастание начинается несколько позже установления фиксированной разности потенциалов, когда уже инактивируется; г – суммарный ток через мембрану. В момент времени, соответствующий пересечению кривой оси абсцисс, он равен нулю, а затем меняет направление. Несмотря на то, что сила тока через каждый одиночный канал меняется скачком, зависимость суммарного тока от времени есть плавная кривая, это обусловлено огромным числом одновременно функционирующих каналов 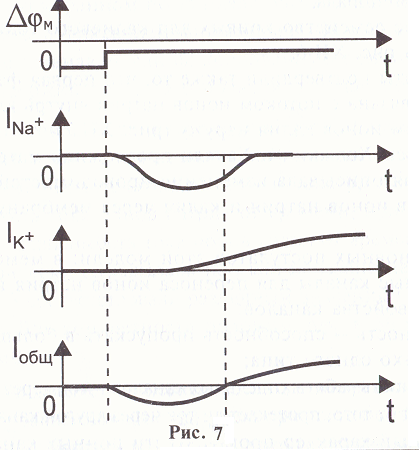 (например, подсчитано, что на аксоне кальмара длиной 1 см и диаметром 1 мм примерно 1010 каналов). На рис. 8. представлена связь между токами в одиночных натриевых каналах и суммарным натриевым током; (например, подсчитано, что на аксоне кальмара длиной 1 см и диаметром 1 мм примерно 1010 каналов). На рис. 8. представлена связь между токами в одиночных натриевых каналах и суммарным натриевым током;- зависимость параметров канала от мембранного потенциала. Это проявляется в том, что после начала деполяризации мембраны соответствующие токи начинают изменяться с той или иной кинетикой. Исходя из гипотезы об ионных каналах, этот процесс происходит следующим образом. Ионоселективный канал имеет так называемый сенсор – элемент конструкции, чувствительной к действию электрического поля. При изменении мембранного потенциала меняется величина действующей на него силы, в результате эта часть ионного канала перемещается и меняет вероятность открывания или закрывания ворот – своеобразных заслонок, действующих по закону «все или ничего». Примерно в 1952 г. Хаксли, исходя из разработанной математической модели, рассчитал, как меняется мембранная разность потенциалов со временем. Результаты этого расчета с большой точностью совпали с потенциалом действия, зарегистрированным экспериментально.  Из проведенных исследований было получено, что канал за время деполяризующего сдвиг мембранного потенциала открывается лишь один раз на некоторое время – это время открытого состояния одиночного канала. Время в течении которого вероятность открывания Na+-каналов велика называется временем активации натриевых каналов. По прошествии времени активации каналов вероятность их открывания падает до 0 и этот процесс называется инактивацией Na+-каналов. Суммарный ток является результатом сложения дискретных токов большого количества отдельных натриевых каналов. Основные свойства каналов: Селективность – способность пропускать в большинстве случаев ионы только одного типа; Независимость работы отдельных каналов – ток через тот или иной канал не зависит от того, протекает ли ток через другой канал или нет. Влияние каналов друг на друга происходит опосредовано: изменение проницаемости каналов (например натриевых) меняет мембранный потенциал, а он уже влияет на проводимости других ионных каналов. Дискретный характер проводимости ионных каналов: в первом приближении можно утверждать, что ионный канал может находиться в двух состояниях – открытом или закрытом, переходы между этими состояниями происходят в случайные моменты времени и подчиняются статистическим закономерностям Несмотря на то, что сила тока через каждый одиночный канал меняется скачком, зависимость суммарного тока от времени есть плавная кривая, это обусловлено огромным числом одновременно функционирующих каналов (например, подсчитано, что на аксоне кальмара длиной 1 см и диаметром 1 мм примерно 1010 каналов). Исходя из гипотезы об ионных каналах, этот процесс происходит следующим образом. Ионоселективный канал имеет так называемый сенсор – элемент конструкции, чувствительный к действию электрического поля. При изменении мембранного потенциала меняется величина действующей на него силы, в результате эта часть ионного канала перемещается и меняет вероятность открывания или закрывания ворот – своеобразных заслонок, действующих по закону «все или ничего». Ворота ионного канала управляются мембранным потенциалом. Под действием электрического поля увеличивается вероятность открытого состояния, ворота открываются. Все каналы независимо от их строения, назначения и выполняемых функций пропускают через себя только пассивные потоки ионов.  Как показано выше, потенциал покоя создается в основном в результате разности концентраций ионов калия внутри и снаружи клетки. Однако после нескольких потенциалов действия, сопровождающихся потоком ионов натрия внутрь на первой фазе и ионов калия наружу на второй, разности концентраций этих ионов внутри и снаружи клетки должны меняться. Однако этого не происходит. Видимо, существует какой-то механизм, поддерживающий разность концентраций. С помощью такого механизма ионы калия должны закачиваться внутрь клетки (где их концентрация и так больше), а ионы натрия – откачиваться наружу, где их концентрация также больше, чем внутри. Что же это за механизм? Выше уже шла речь о том, что в клеточную мембрану встроены различные белковые молекулы. Оказывается, что некоторые из них играют роль своеобразных насосов, закачивающих ионы калия внутрь, а ионы натрия – наружу (пример активного ионного транспорта). Известно также, за счет энергии какого источника происходит работа насосов. В случае калий – натриевого насоса опыты с радиоактивными изотопами показали, что для закачивания внутрь клетки 2 ионов калия и выкачивания наружу 3 ионов натрия (один цикл работы насоса) достаточно энергии распада одной молекулы АТФ (рис. 6). Рис. 6. Калий-натриевый насос Как показано выше, потенциал покоя создается в основном в результате разности концентраций ионов калия внутри и снаружи клетки. Однако после нескольких потенциалов действия, сопровождающихся потоком ионов натрия внутрь на первой фазе и ионов калия наружу на второй, разности концентраций этих ионов внутри и снаружи клетки должны меняться. Однако этого не происходит. Видимо, существует какой-то механизм, поддерживающий разность концентраций. С помощью такого механизма ионы калия должны закачиваться внутрь клетки (где их концентрация и так больше), а ионы натрия – откачиваться наружу, где их концентрация также больше, чем внутри. Что же это за механизм? Выше уже шла речь о том, что в клеточную мембрану встроены различные белковые молекулы. Оказывается, что некоторые из них играют роль своеобразных насосов, закачивающих ионы калия внутрь, а ионы натрия – наружу (пример активного ионного транспорта). Известно также, за счет энергии какого источника происходит работа насосов. В случае калий – натриевого насоса опыты с радиоактивными изотопами показали, что для закачивания внутрь клетки 2 ионов калия и выкачивания наружу 3 ионов натрия (один цикл работы насоса) достаточно энергии распада одной молекулы АТФ (рис. 6). Рис. 6. Калий-натриевый насосОказалось, что работа ионных насосов управляется концентрацией ионов внутри и вне клетки. Работа насоса ускоряется избытком ионов калия снаружи клетки и избытком ионов натрия внутри. Важнейшую роль в осуществлении различных клеточных функций играет ион кальция. Так, для мышечного сокращения необходимо много ионов кальция и его необходимо доставлять к каждой из белковых фибрилл, пронизывающих тело клетки, а затем также быстро убирать от фибрилл, чтобы мышца могла расслабиться. Если бы каждый ион кальция поступал и удалялся через наружную мембрану клетки, то его быстрое перемещение было бы невозможным. Внутри мышечных клеток имеется разветвленная система полостей и трубочек, образованных специальной внутренней мембраной, в которых хранится кальций, туда же он убирается после расслабления мышцы. Вся эта мембрана «покрыта» кальциевыми насосами. Источником активного транспорта кальция является также гидролиз АТФ .  |
