ПРАКТИКУМ АГРОПОЧВОВЕДЕНИЕ. Практикум по агропочвоведению Учебное пособие
 Скачать 17.78 Mb. Скачать 17.78 Mb.
|
Происхождение, состав и свойства почвенных коллоидовПроисхождение почвенных коллоидовВыделяют два основных пути происхождения коллоидов:
Первый путь проявляется при дроблении более крупных частиц в процессе выветривания и почвообразования. Второй, при укрупнении частиц, в результате химических реакций между продуктами выветривания. Состав почвенных коллоидовПо вещественному составу коллоиды почвы бывают минеральные, органические и органо-минеральные. В большинстве своем минеральные коллоиды представлены вторичными минералами. Часть из них находится в кристаллическом состоянии. Это, прежде всего, глинистые минералы: монтмориллонит, каолинит, вермикулит, гидрослюды. Кроме них в коллоидной фракции всегда присутствует небольшая примесь тонкодисперсных первичных минералов, главным образом кварца и слюд, не проявляющих коллоидные свойства. Органические коллоиды состоят преимущественно из гумусовых веществ и белков. В коллоидно-дисперсном состоянии могут находиться полисахариды, лигнин, клетки наиболее мелких бактерий, диаметр которых соответствует диаметру коллоидных частиц. Органо-минеральные коллоиды представлены соединениями гумусовых веществ с глинистыми минералами и полуторными оксидами в осажденной форме. В почвах присутствуют и многочисленные комплексные минеральные и органо-минеральные соединения коллоидной природы, образующиеся при совместном осаждении двух или нескольких веществ. Сюда относят кремнеалюминевые и кремнежелезистые образования, железисто-марганцевые, органо-железисто-марганцевые соединения. В большинстве почв преобладают минеральные коллоиды, составляющие 85-90 % их общей массы. Свойства почвенных коллоидовВажнейшее свойство почвенных коллоидов – способность обменивать ионы, находящиеся в компенсирующем слое, на ионы того же знака, находящиеся в дисперсионной среде. Ионы диффузного слоя обмениваются легко, гораздо труднее обмениваются ионы неподвижного слоя. В почвах почти все коллоиды имеют отрицательный заряд. Это ацидоиды, в диффузном слое которых сосредоточены катионы. К ацидоидам относятся: коллоидно-дисперсные системы кремнезема, глинистых минералов, гидраты окиси марганца, гумусовые кислоты, а также органо-минеральные коллоиды, представляющие собой глинистые минералы, покрытые пленками органических веществ. Коллоиды с положительным зарядом называются базоидами. У них в компенсирующем слое противоионов концентрируются анионы. Типичных базоидов в почве нет. Но в почвах могут встречаться амфолитоиды – коллоиды с переменным знаком заряда. К амфолитоидам относятся гидраты окиси железа, алюминия, а также протеиновые вещества гумуса. В кислой среде они заряжены положительно, в щелочной – отрицательно. Количество амфолитоидов в почвах крайне незначительно. Наряду с поглощением ионов коллоиды способны притягивать к себе молекулы воды, или гидратироваться, что обусловлено проявлением поляризационных сил. При приближении молекулы воды к заряженной коллоидной частице ее электронейтральная оболочка деформируется. Хотя молекула воды остается в целом нейтральной, она принимает форму диполя. Попадая в сферу электрического поля заряженной частицы, диполи строго ориентируются, обращаясь к ней концами, несущими заряд, противоположный заряду частицы. Вокруг коллоида образуется связанная с ним пленка воды, мощность которой зависит от природы коллоида и величины заряда частицы. В зависимости от количества воды, которое удерживают коллоиды, их разделяют на гидрофильные и гидрофобные. Коллоиды, способные сильно гидратироваться, т.е. удерживать мощные водные пленки, называют гидрофильными. Это аморфная кремниевая кислота, минералы группы монтмориллонита, гумусовые кислоты. Коллоиды, слабо гидратирующиеся, называют гидрофобными. К ним относят гидроксиды железа и алюминия, минералы группы каолинита. На способность к гидратации влияет не только природа коллоида, но и состав ионов компенсирующего слоя, которые сами способны притягивать молекулы воды с помощью электростатических сил. Важнейшее свойство почвенных коллоидов – их агрегативная устойчивость, т.е. способность коллоидной системы сохранять степень дисперсности неизменной. Наличие заряда обусловливает электрокинетические свойства почвенных коллоидов. К ним относят коагуляцию и пептизацию коллоидной системы. В зависимости от наличия и отсутствия заряда почве коллоиды могут находиться в состоянии золя (во взвешенном состоянии) или геля. Золь – коллоидный раствор. Обусловлен наличием заряда в коллоидной системе; представляет состояние коллоидно-раздробленного вещества, рассеянного в дисперсионной среде. Электрический заряд способствует взаимному отталкиванию коллоидных частиц, а гидратная оболочка препятствует их слипанию при столкновении друг с другом. В силу различных причин заряд коллоидов снижается, гидратная оболочка уменьшается, коллоиды начинают взаимодействовать между собой, что ведет к слипанию частиц и выпадению их в осадок в виде геля. Это явление называют коагуляцией. Гель – коллоидный осадок. При отсутствии заряда в коллоидной системе дисперсная фаза укрупняется и отделяется от дисперсионной среды. 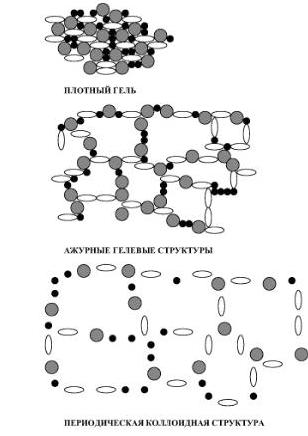 Рисунок 16 - Схемы гелевых структур способных существовать в почвах (Шеин, 2007) Можно предположить, что в почвах возможно существование следующих типов гелевых структур (рис. 16): 1. Плотные пленки-гели, в которых коллоидные частицы органической и неорганической природы с адсорбированными на них органическими молекулами контактируют между собой, плотно заполняя пространство. 2. Ажурные гелевые структуры, возникающие при непосредственном контакте коллоидных частиц и включающие в свой состав почвенный раствор. 3. Периодические коллоидные структуры, возникающие за счет дальней агрегации коллоидных частиц и тоже включающие в свой состав большие количества почвенного раствора. Коагуляция – переход коллоида из состояния золя в состояние геля. Коагуляцию вызывают периодическое высушивание, нагревание, промораживание почвы, что приводит к дегидратации частиц и потере ими водной оболочки Коагуляция способствует образованию почвенной структуры, уменьшению связности тяжелых по гранулометрическому составу почв, сохранению от вымывания коллоидов, обусловливающих важнейшие агрономические свойства почвы. Некоторые коллоиды способны переходить обратно из геля в золь. Это явление называется пептизацией. Она связана с восстановлением заряда коллоидной системы, повышением дзета-потенциалом, обусловленным главным образом действием растворов щелочей и гидролитически щелочных солей. При пептизации разрушается почвенная структура, коллоиды распыляются и приобретают способность к передвижению по почвенному профилю. Строение коллоидной мицеллы. Физико-химическая поглотительная способность (обменная). Закономерности поглощенияСтроение коллоидовОснову коллоидной частицы, называемой коллоидной мицеллой, составляет ее ядро. Ядро в химическом отношении представляет сложное соединение и имеет аморфное или кристаллическое строение. У минеральных коллоидов ядро состоит из алюмо-магниевых и других силикатов, иногда кремнезема, окислов железа и алюминия. У органических коллоидов ядро состоит из гуминовых и фульвокислот, протеина, клетчатки и других сложных веществ. У органо-минеральных коллоидов ядро образуется в результате взаимодействия органических и минеральных компонентов. На поверхности ядра расположен прочно удерживаемый слой ионов, несущий заряд – слой потенциалопределяющих ионов (рис. 17). Ядро мицеллы вместе со слоем потенциалопределяющих ионов называется гранулой. Между гранулой и раствором, окружающим коллоид, возникает термодинамический потенциал, под влиянием которого из раствора притягиваются ионы противоположного знака (компенсирующие ионы). Так, вокруг ядра коллоидной мицеллы образуется двойной электрический слой, состоящий из слоя потенциалопределяющих и слоя компенсирующих ионов. Компенсирующие ионы в почвоведении называются обменными или поглощенными, а сумма этих катионов составляет емкость катионного обмена. 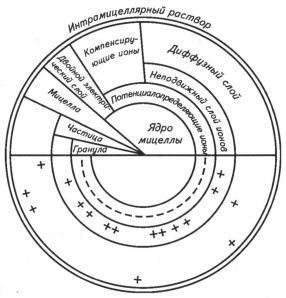 Рисунок 17 - Строение коллоидной мицеллы (по Н.И. Горбунову) Компенсирующие ионы. В свою очередь, располагаются вокруг гранулы двумя слоями. Один – неподвижный слой, прочно удерживаемый электростатическими силами потенциалопределяющих ионов. Гранула вместе с неподвижным слоем компенсирующих ионов называется коллоидной частицей. Между коллоидной частицей и окружающим раствором возникает электрокинетический потенциал (дзете-потенциал), под влиянием которого находится второй (диффузный) слой компенсирующих ионов. Физико-химическая (обменная) поглотительная способность – способность почвы поглощать преимущественно катионы в результате эквивалентного обмена катионов, находящихся в почвенном растворе, на катионы диффузного слоя коллоидов. Поглощение преимущественно катионов обусловлено тем, что у большинства почв в поглощающем комплексе преобладают ацидоиды (заряженные коллоиды), в диффузном слое которых в качестве противоионов находятся катионы, способные к эквивалентному обмену. Физико-химическое поглощение имеет ряд закономерностей:
Li+
Виды поглотительной способности почвК.К. Гедройц выделил пять видов поглотительной способности – четыре абиотических вида: механическая, физическая, физико-химическая (обменная), химическая и пятый вид – биологическая поглотительная способность. С физической точки зрения, ППК (почвенный поглощающий комплекс) представляет собой совокупность веществ в тонкодисперсном состоянии (коллоиды). В химическом отношении это нерастворимые в воде солеобразные алюмосиликатные, органические и органо-минеральные соединения. Механическая поглотительная способность – это свойство почвы задерживать твердые частицы, взмученные в фильтрующейся воде, размеры которых превышают размеры почвенных пор. Поэтому почва способна механическим путем задерживать не только крупные взвешенные частицы, но также илистые и коллоидные. По мере заполнения каналов тонкодисперсными частицами механическая поглотительная способность возрастает. Механическая поглотительная способность зависит от гранулометрического и агрегатного состава почвы, а также от плотности сложения. Плотные глинистые почвы практически полностью задерживают взмученные тонкодисперсные частицы. В легких по гранулометрическому составу и рыхлых почвах с крупными агрегатами низкая механическая поглотительная способность. Явление механического поглощения используют для очистки питьевых и сточных вод путем их фильтрации через почву, для заиливания (кольматирования) дна и стенок каналов, водохранилищ в целях уменьшения потерь воды на фильтрацию. Физическая поглотительная способность – это способность почвы изменять (увеличивать или уменьшать) концентрацию молекул различных веществ у поверхности соприкосновения тонкодисперсных частиц с почвенным раствором. Явление физического поглощения связано с наличием свободной поверхностной энергии. Влажную почву можно рассматривать как дисперсную систему, у которой дисперсионная среда представлена почвенным раствором, а дисперсная фаза минеральными, органическими и органо-минеральными частицами. На границе раздела фаз имеется свободная поверхностная энергия, равная произведению поверхностного натяжения раствора и суммарной величины поверхности частиц. Чем выше степень дисперсности почвенных частиц, тем больше их поверхностная энергия вследствие увеличения общей удельной поверхности. Химическая поглотительная способность – способность почвы удерживать некоторые ионы путем образования в результате химических реакций нерастворимые или труднорастворимые соединения, т.е. переводить анионы и катионы почвенного раствора в труднорастворимые соединения. Из катионов, находящихся в почвах, чаще всего нерастворимые соединения образуют катионы Ca2+, Mg2+, Al3+, Fe3+, а среди анионов – CO32-, PO43-, SO42-. Так, при внесении фосфорных удобрений образующиеся малорастворимые соли осаждаются и переходят из почвенного раствора в твердую фазу почвы. Процессы такого типа называют химическим поглощением: на черноземных почвах: Ca(HCO3)2 + Ca(H2PO4)2 → CaHPO4 + H2CO3 → Ca3(PO4)2 ↓; на почвах элювиального ряда: Al(OH)3 + Ca(H2PO4)2 → AlPO4 +H2O. Образование осадков возможно и на поверхностности почвенных частиц при взаимодействии ионов, способных к взаимному осаждению. Такая сорбция получила название осадочной. К химическому поглощению относится и комплексообразовательная сорбция. В этом случае за счет образования координационной связи происходит связывание поливалентных ионов почвенного раствора органическим веществом, сорбированным твердой фазой почвы. Хемосорбция играет большую роль во взаимодействии гумусовых веществ с глинистыми минералами и в образовании сорбционного глиногумусового комплекса. При этом осуществляется и адгезионное взаимодействие минеральных и органических компонентов. Химическая поглотительная способность – важнейший фактор аккумуляции в почвенном профиле органического вещества, анионов фосфорной кислоты, многих катионов, в том числе и микроэлементов. Благодаря ей почва способна предотвращать появление соды в почвенном растворе. В результате хемосорбции в почвах накапливаются гипс, карбонаты и другие соединения. Состав обменных катионов и анионов в различных почвах и их влияние на свойства почвПочвы существенно различаются между собой составом обменных катионов. Эти различия обусловлены типом почвообразования, спецификой почвообразующих пород, водным и солевым режимами почв. Заметно влияют на этот показатель химические мелиорации. Содержание обменных катионов в почве выражается как в абсолютных величинах (мг. экв/100 г почвы), так и в относительных (% от емкости обмена). Основные обменные катионы в почве:Ca2+, Mg2+, Na+, K+, NH4+, H+, Al3+, Fe2+, Mn2+ Основные обменные анионы в почве:PO43-, HPO42-, H2PO4-, SiO32-, NO3-, CI- Практически все почвы в составе обменных катионов содержат кальций и магний, причем в большинстве случаев Ca2+ преобладает над Mg2+. Так же среди обменных катионов всегда содержатся K+ и NH4+, но их доля в ППК не велика. Так, количество обменного калия чаще всего не превышает 2…5% от емкости обмена, содержание аммония еще меньше. В географическом аспекте содержание обменных катионов почв варьирует в широких пределах и подчиняется определенным закономерностям. Примерный состав обменных катионов в почвах:Подзолистые – Ca2+, Mg2+, NH4+, H+, Al3+ Серые лесные – Ca2+, Mg2+, K+, NH4+, H+ Чернозем обыкновенный, южный – Ca2+, Mg2+, K+, NH4+, Na+ Чернозем выщелоченный, оподзоленный – Ca2+, Mg2+, K+, NH4+, H+ Солонец – Ca2+, Mg2+, Na+ Каштановые – Ca2+, Mg2+, Na+, K+ Почвы полярной зоны - Ca2+, Mg2+, K+, Na+ Отдельные поглощенные катионы неравнозначны по результативной сущности в многообразных явлениях природы почв. Об экологической значимости отдельных обменных катионов дает представление следующая информация: Ca2+ – считается катионом хранителем плодородия в связи с его многогранной значимостью. Он присутствует во всех без исключения почвах, но в разных количествах и в разных соотношениях с другими катионами. Оптимум его содержания – 80-90% от ЕКО. Это величина характерна для черноземов. Присутствие кальция в таких количествах обеспечивает 99,9%-ную коагуляцию коллоидных систем, а, следовательно, создается необходимая предпосылка для высокого структурообразования при активной деятельности корневых систем травянистой растительности и достаточного содержания гумусовых веществ. Однако, повышенные количества кальция в почвах, содержащих монтмориллонит и другие, набухающие интенсивно глинистые минералы, могут вызвать слитогенетические явления, противоположные зернистому и комковатому структурообразованию даже при оптимальном содержании ионов кальция. Кальций способен к ионообменному поглощению корнями растений. Однако этот способ питания растений, как правило, не принимается во внимание, так как кальций всегда присутствует в почвенных растворах и не является в биосфере дефицитным. Mg2+ – магний всегда сопровождает кальций. Типичное соотношение Ca2+: Mg2+ = 5:1. В таких количествах его действие аналогично действию кальция. Экологическая дисгармония почвенной среды может возникать в щелочных почвах при повышении количества магния в ППК за счет снижения содержания Ca2+, т.е. при изменении соотношения Ca :Mg в сторону магния. В этом случае сам магний вызывает повышение щелочности в связи с присутствием в почвенной среде карбонатов и бикарбонатов магния. Присутствие магния в ППК поддерживает свойства солонцеватости почв и даже приводит в отдельных случаях к образованию особых почв – магниевых солонцов. При высоком содержании обменного магния возрастает растворимость гумусовых веществ и ухудшается структура почвы, снижается водопроницаемость, что отрицательно сказывается на водном режиме. При повышенном содержании обменного магния усиливается отрицательное действие обменного натрия при невысоком содержании последнего в почве. Na+ – натрий в количествах менее 3% от ЕКО – необходимый компонент оптимального для биоценозов функционирования почвенной системы. В этом случае натрий обеспечивает дисперсность коллоидов на уровне около 0,1%, что важно для подвижности, динамичности и первоочередной резервности для минерализации гумусовых веществ и обеспечения почвенных растворов биологически необходимыми компонентами. Однако следует признать, что эта роль натрия в почвоведении и агрохимии изучена недостаточно. Натрий как обменный катион является активным пептизатором коллоидов при концентрации его в почвенном растворе ниже порога коагуляции. При этом в состояние золя переходят все коллоидные системы, почва приобретает свойства солонцеватости, становясь текучей, вязкой, бесструктурной. В растворах появляются щелочные соли, рН может достигать 9,5-10,0. Образуются особые соли – солонцы. K+ – в питании растений – основной источник доступного калия. Отмечена тенденция необменного поглощения калия из слоя компенсирующих противоионов в кристаллическую решетку минералов. Избыток калия может вызвать солонцеватость почв. NH4+ – ион аммония: единственная возможная аккумуляция доступного растениям азота. Поглощается коллоидами в процессе аммонификации. Легко используется корневыми системами растений. Не накапливается в количествах, превышающих 3% от ЕКО. Физическая и физико-химическая значимость не изучена. Повышенное содержание свидетельствует о недостатке азота. H+ – обменный водород – источник почвенной кислотности. Его присутствие фиксируется всегда в бескарбонатных почвах, т.е. в почвах, не содержащих CaCO3. В нейтральных почвах при рН от 6,5 до 7,2 водород присутствует в ППК в количествах менее 5% от ЕКО. В этих условиях обменный водород экологически нейтрален. В количествах более 5% от ЕКО начинают проявляться кислотные свойства почв. При этом кислотные свойства проявляются сильнее при повышении количества H+ в коллоидно-поглощенном состоянии. Максимум кислотности почвенной среды наступает когда среди обменных катионов водорода становится более 40-50%, рН почвы при этом становится кислой и сильнокислой (рН 3-5). Максимальное количество водорода в ППК может достигать 80% от ЕКО. Al3+ – алюминий в обменном состоянии – интенсивный коагулятор коллоидов. Является объектом пристального внимания в кислых почвах. При переходе в почвенный раствор образует гидролитически кислые соли, способствующие повышенной пептизации Al3+ в почвенной среде, поэтому учитывается при определении кислотности почв, наравне с ионом водорода. Алюминий изучается как физиологически токсичный катион. Fe3+ – интенсивный коагулятор коллоидов, как и алюминий во влажных тропических почвах. Участвует в создании структурных микроагрегатов. Принимая во внимание огромную роль обменных катионов в жизни растений, неоднократно предпринимались попытки обосновать их оптимальное содержание в почве. Так, Байер (1945) предложил модель почвы с «идеальным» соотношением обменных катионов: Ca2+ - 65%, Mg2+ - 10%, K+ - 5%, H+ - 20%. Такие модели, несомненно, представляют интерес, но следует учитывать, что оптимальный состав обменных катионов может существенно меняться в зависимости от различных факторов – требований культуры, минералогического и гранулометрического составов почв и т.д. В почвах со слабокислой, нейтральной и слабощелочной реакцией среды состав обменных катионов, как правило, благоприятен для большинства сельскохозяйственных культур. При высоком содержании в почвах обменных H+ и Al3+ или Mg2+ и Na+ состав обменных катионов регулируют с помощью химической мелиорации. Показатели, оценивающие поглотительную способность почвКоличественно поглотительную способность почвы характеризуют следующие показатели: Емкость катионного обмена (ЕКО, мг•экв на 100 г почвы) – общее количество катионов, удерживаемых почвой в обменном состоянии и способных к замещению на катионы раствора, взаимодействующего с почвой; выражают в мг*экв на 100 г почвы. Величина ЕКО зависит от гранулометрического и минералогического составов почвы, содержания и качественного состава органического вещества, реакции среды. ЕКО = сумма всех катионов способных к обмену (S), в т.ч. водорода и алюминия (Нг); ЕКО = S + НгВклад того или иного компонента в ЕКО почвы зависит от его содержания и характера взаимодействия с другими веществами. Часто это взаимодействие сопровождается снижением величины ЕКО, свойственной индивидуальным компонентам. Например, ЕКО гумуса почвы в целом намного меньше, чем собственно гуминовых или фульвокислот. Это связано с тем, что часть функциональных групп гумусовых веществ взаимодействует с поверхностью глинистых минералов и не принимает участия в реакциях обмена. Тесная взаимосвязь наблюдается между ЕКО и размером почвенных частиц. Крупные фракции механических элементов, состоящие в основном из первичных минералов, практически не участвуют в обменных реакциях. С уменьшением размера механических элементов и увеличением в их составе количества глинистых минералов ЕКО существенно возрастает. В то же время необходимо учитывать, что тонкодисперсные частицы, особенно в гумусовых горизонтах, всегда обогащены органическим веществом, имеющим высокую ЕКО. На величину ЕКО почвы существенно влияет реакция среды. С увеличением pH возрастает ионизация функциональных групп глинистых минералов, в реакции обмена помимо карбоксильных групп гумусовых веществ дополнительно включаются их спиртовые и фенольные гидроксилы. В щелочной среде происходит перезарядка амфотерных коллоидов, и они приобретают способность к обменному поглощению катионов. Все это способствует увеличению ЕКО почвы по мере возрастания pH. В зависимости от типа почвы емкость катионного обмена может варьировать в следующих пределах (табл. 8). Таблица 8. Емкость катионного обмена в почвах 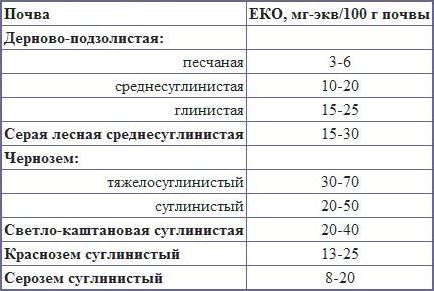 Уровень поглотительной способности можно оценить по следующей шкале (табл. 9): Таблица 9. Оценка уровня поглотительной способности почв 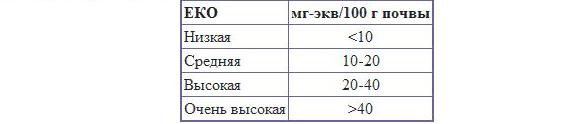 Сумма обменных оснований (S, мг•экв на 100 г почвы) – суммарное содержание обменных оснований (преимущественно Ca2+ и Mg2+) в некарбонатных незасоленных, преимущественно кислых почвах, вытесненных ионом водорода соляной кислоты. Ионы H+ и Al3+ не учитываются (не суммируются). Исходя из этого, все почвы разделяют на две большие группы:
Первые не содержат в ППК ионы H+ и Al3+. Обменные катионы в них представлены только обменными основаниями Ca2+, Mg2+, K+, NH4+, Na+, количество которых соответствует реальной емкости обмена. Вторые всегда содержат некоторое количество обменных H+ и Al3+, поэтому сумма обменных оснований у них меньше ЕКО. Степень насыщенности почв основаниями (V, %) – доля суммы обменных оснований от емкости катионного обмена, выраженная в процентах. V = (S/ЕКО) ×100, %, по другому можно записать V = S / (S + Нг) ×100, % Сорбционная способность почвы – максимальное количество вещества, которое может быть сорбировано почвой. Как сорбент почва полифункциональна, поэтому ее сорбционная емкость по отношению к различным веществам неодинакова. Например, Zn2+ может поглощаться обменным и необменным путем, а также за счет комплексообразовательной и осадочной сорбции, Na+ – преимущественно обменно, K+ – по обменному и необменному типу. В связи с этим сорбционная емкость поглощения разных веществ одной и той же почвой существенно варьирует. Буферность почв Под буферностью почвы понимают ее способность как полифункциональной системы противостоять изменению концентрации почвенного раствора, особенно ее щелочно-кислотного и окислительно-восстановительного состояния. Буферные свойства почвы связаны с процессами физико-химического (обменного) поглощения ионов, перехода различных соединений в ионные и молекулярные формы, с нейтрализацией и выпадением в осадок вновь образующихся соединений. В основном буферность почвы определяется качеством ее твердой фазы, однако, механизм работы буферных систем почвы весьма разнообразен и может обходиться без вовлечения элементов твердой фазы. Изменение концентрации почвенного раствора проявляется при внесении в почву в виде удобрений водорастворимых солей, которые локально могут создавать токсичные для растений концентрации. Благодаря буферности почв это отрицательное свойство высоких концентраций блокируется. В целом, чем большей емкостью поглощения обладает почва, тем выше ее буферная способность. Наименьшая буферность свойственна песчаным почвам и пескам. Величина буферности почв зависит от содержания почвенных коллоидов (чем больше коллоидов, тем выше буферность), их качества (чем больше гумусовых веществ, глин группы монтмориллонита, минеральных коллоидов с широким отношением кремнезема к глинозему, тем буферность выше), состава обменно-поглощенных катионов (наличия в ППК катионов кальция, магния, калия, натрия препятствует подкислению почв, а катионов водорода, алюминия – подщелачивания). Контрольные вопросы
Содержание работы Решите следующие задачи самостоятельно и представьте преподавателю для проверки. Вариант 1
Вариант 2
Вариант 3
Вариант 4
Вариант 5
Вариант 6
Вариант 7
Вариант 8
Вариант 9
Вариант 10
Вариант 11
Вариант 12
Вариант 13
Вариант 14
Вариант 15
Вариант 16
Вариант 17
6. Общие физические и водно-физические свойства почв (практическая работа № 6) Основные теоретические положенияАгрофизика. Структура почвыАгрофизика – наука о физических основах формирования урожая, изучающая физические, физико-химические и биологические процессы в системе “почва – растение – деятельный слой атмосферы”, основные закономерности продукционного процесса, разрабатывающие научные основы, методы, технические, математические средства и агроприемы рационального использования природных ресурсов, повышения эффективности и устойчивости агроэкосистем, земледелия и растениеводства в полевых и регулируемых условиях. Почва, ее физические свойства – это одно из центральных понятий продукционного процесса. Почва обеспечивает растения питательными веществами и водой, она преобразует солнечную радиацию в тепло, хранит это тепло, являясь теплым “одеялом” для семян растений, она впитывает осадки, сохраняет воду, избавляясь от ее избытков и предоставляя воздуху свободно циркулировать в поровом пространстве. Почва обладает свойствами аккумулировать и выделять, проводить и трансформировать вещества и энергию. Структура почвыВ почвах механические элементы находятся в раздельно-частичном состоянии или соединяются под действием разнообразных сил в комки разной формы и размера, которые называют почвенными агрегатами. Почвенный агрегат (структурная отдельность) – представляет собой определенной количество механических элементов, объединенных в единое целое в результате слипания и склеивания под влиянием абиотических и биотических факторов. Совокупность агрегатов различного размера, формы и качественного состава называют почвенной структурой, а способность почвы распадаться на агрегаты при механическом воздействии – структурностью. Милановский Е.Ю. и Шеин Е.В. подмечают, что если из комочка чернозема сделать тонкий срез и рассмотреть его в микроскоп, то можно увидеть соединенные друг с другом частички с просвечивающей между ними пустотой – поровым пространством. В нем как раз и сохраняются вода и питательные вещества, живет и функционирует почвенная биота. Крупные отдельные частицы – это кусочки минералов и горных пород (песчинки, пылинки и др.). Они когда-то составляли геологическую породу, на которой и образовалась почва с характерной структурой. Теперь эти минеральные частицы соединены между собой прочной, но пластичной связью, которая не рвется даже при проникновении воды. В то же время при насыщении агрегата водой возникают очень большие силы, стремящиеся отодвинуть частицы друг от друга. Физико-химический характер этих сил можно пояснить на схеме (рис. 18). На поверхности минеральных частиц, расположенных рядом и омывающихся водой, образуется некоторый, как правило, отрицательный электрический заряд. К таким частицам обязательно подойдут из раствора положительно заряженные катионы. Они окружат их, формируя поверхностный слой. Но вот что интересно: в межчастичном пространстве количество катионов окажется значительно больше, чем в окружающей воде. 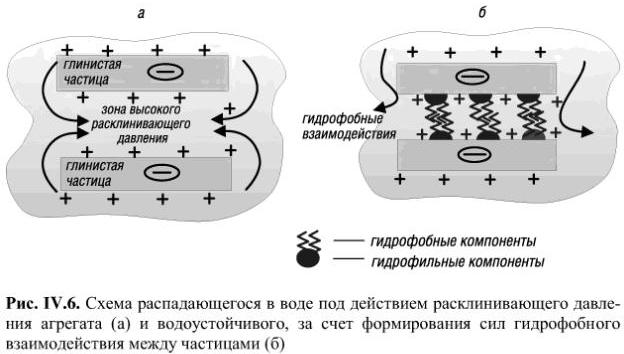 Рисунок 18 - Схема распадающегося в воде под действием расклинивающего давления агрегата (а) и водоустойчивого, за счет формирования сил гидрофобного взаимодействия между частицами (б). В настоящее время (Т.А.Зубкова, Л.О.Карпачевский), считают: структура почвы определяется как способ упаковки разных по минералогическому составу, размеру и химическим свойствам почвенных частиц (рис. 19). 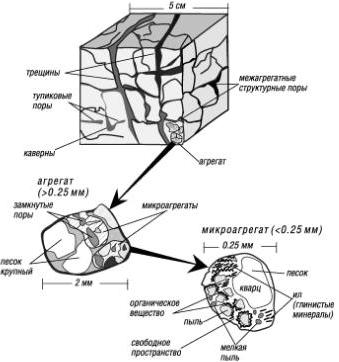 Рисунок 19 - Схема агрегатного строения почв (по Е.В. Шеину с соавт., 2007) По мнению этих авторов, склеивание механических элементов происходит под действием следующих условий:
Кроме размера агрономическая ценность структуры характеризуется связностью (механическая прочность), водопрочность и пористостью агрегатов. Под связностью понимают способность агрегатов не разрушаться при механическом воздействии. Связность возрастает с увеличением количества илистых и коллоидных частиц, участвующих в формировании агрегатов. Высокую механическую прочность имеют агрегаты глинистых и тяжелосуглинистых по гранулометрическому составу иллювиальных горизонтов. В сухом состоянии они разрушаются с большим трудом, однако в воде легко распадаются на механические элементы. Агрономически ценная структура должна отличаться не только механической прочностью, но и водопрочностью. Водопрочность – это способность агрегатов длительное время противостоять размывающему действию воды. Она зависит от качества материала, склеивающего механические элементы. Свойство почвы образовывать устойчивые агрегаты – это свойство почвенной структуры, пожалуй, самое важное структурное и функциональное свойство почвы. Агрегат характеризуется тем, что связи внутри него, между отдельными частицами (в микроагрегате) или микроагрегатами (в макроагрегате) выражены сильнее, чем между агрегатами. Поэтому в почве и выделяются отдельные агрегаты, что свидетельствует о том, что почвенная структура представлена рассыпчатым, зерноподобным, агрегированным веществом, а не единой монолитной массой. Чем лучше выражена эта структура, чем устойчивее к воздействию воды и механических нагрузок почвенные агрегаты, тем лучше функционирует почва, тем выше и устойчивее ее продуктивность. Хорошая структура определяет и хорошее проникновение влаги, за счет пониженной плотности повышается ее порозность, и почва способна вместить и удержать большое количество воды, питательных веществ, в ней лучше движутся газы, активнее газообмен. Почва должна сохранять свою уникальную комковато-зернистую структуру после обильных осадков и последующего легко подсушивания, когда образуется не плотная непроницаемая для газов и воды корка, а вновь хорошо различимые почвенные комочки и агрегаты. Во всех теориях структурообразования отсутствует главный действующий “герой” практически всех почвенных процессов – вода. Без нее все события в формировании почвенной структуры кажутся разобщенными, не связанными друг с другом. В последнее время родилась идея, что основную роль в природном клее должно играть органическое вещество почвы, которое затрудняет быстрое поступление воды в межчастичное пространство, препятствует возникновению высоких расклинивающих давлений и разрыву агрегата (рис. 20). 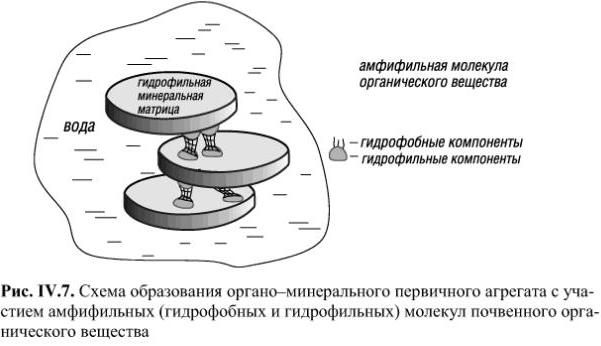 Рисунок 20 - Схема образования органо-минерального первичного агрегата с участием амфифильных (гидрофобных и гидрофильных) молекул почвенного органического вещества К общим физическим свойствам почв относят:
|
