Практикум по бх. Практикум по биологической химии Для студентов лечебного и педиатрического
 Скачать 5.3 Mb. Скачать 5.3 Mb.
|
Классификация и номенклатура ферментовВ 1961 г. в Москве Комиссия по ферментам Международного биохимического союза (IUBМВ) приняла современную систематическую классификацию ферментов. В соответствии с систематической классификацией учитывается реакционная и субстратная специфичность ферментов. Ферменты делятся:
Выделяют 6 классов ферментов: I. Оксидоредуктазы II. Трансферазы III. Гидролазы IV. Лиазы V. Изомеразы
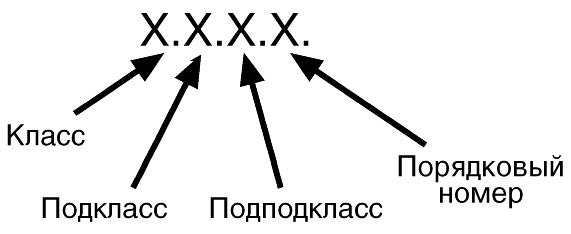
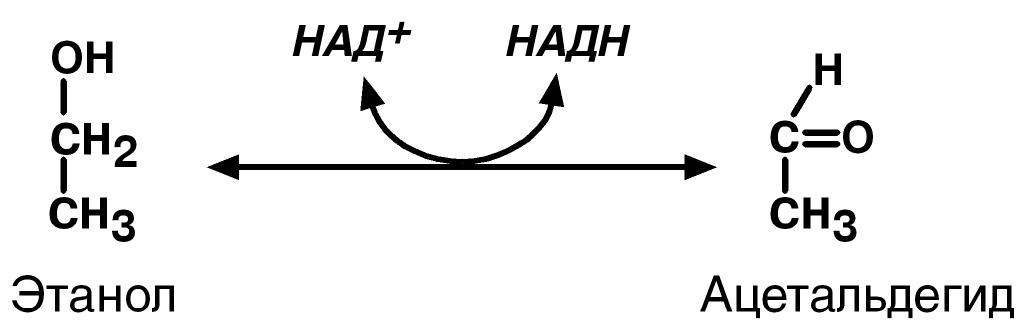
Каждому ферменту присваивается четырехзначный классификационный номер. Например, алкогольдегидрогеназа имеет номер КФ 1.1.1.1. – это оксидоредуктаза, действует на ОН-группу донора с НАД+ в качестве акцептора с первым порядковым номером в своем подподклассе; лактатдегидрогеназа – КФ 1.1.1.27. Ферменты могут иметь тривиальное или систематическое название: 1. Систематическое название – согласно современной классификации (http://www.chem.qmul.ac.uk/iubmb/enzyme/). Зачастую такое название сложно для использования, тогда оно упрощается и вводится рабочее название фермента. 2. Тривиальное название – название, сложившееся исторически, которое более употребимо, например, пепсин, трипсин. Иногда к названию субстрата добавляется окончание "-аза" – уреаза, амилаза, липаза. Тем не менее, у всех таких ферментов есть и систематическое название. I класс. ОксидоредуктазыФерменты катализируют окислительно-восстановительные реакции, лежащие в основе биологического окисления. Класс насчитывает 22 подкласса. Коферментами этого класса являются НАД+, НАДФ+, ФАД, ФМН, убихинон, глутатион, липоевая кислота. В подклассы выделяются группы ферментов, действующие на: 1.1. CH-OH группу доноров; 1.2. альдегидную или кетонную группу доноров; 1.3. CH-СH группу доноров; 1.4. CH-NH2 группу доноров; 1.5. CH-NН группу доноров; 1.6. НАДH или НАДФН в качестве доноров; 1.8. содержащие серу группы доноров; 1.9. гем-содержащие доноры; 1.10. дифенолы в качестве доноров; 1.11. пероксид водорода в качестве акцептора; 1.11. водород в качестве донора; 1.13. один донор с включением молекулярного кислорода; 1.14. два донора с включением молекулярного кислорода; 1.15. супероксидные радикалы в качестве акцептора; 1.17. СН2 группу доноров; 1.18. ферредоксин в качестве донора. На подподклассы деление производится в зависимости от акцептора – НАД+ или НАДФ+ (1.1.1., 1.2.1., 1.3.1., 1.4.1.), дисульфиды (1.2.4.), кислород (1.3.3.). Наиболее распространенные рабочие названия оксидоредуктаз следующие: 1. Дегидрогеназы – оксидоредуктазы, катализирующие дегидрирование субстрата с использованием в качестве акцептора водорода любых молекул, кроме кислорода. 2. Если перенос водорода от молекулы донора трудно доказуем, то такие оксидоредуктазы называют редуктазами. 3. Оксидазы – оксидоредуктазы, катализирующие окисление субстратов с молекулярным кислородом в качестве акцептора электронов без включения кислорода в молекулу субстрата. 4. Монооксигеназы – оксидоредуктазы, катализирующие внедрение одного атома кислорода в молекулу субстрата с молекулярным кислородом в качестве донора кислорода. 5. Диоксигеназы – оксидоредуктазы, катализирующие внедрение двух атомов кислорода в молекулу субстрата с молекулярным кислородом в качестве донора кислорода. 6. Пероксидазы – оксидоредуктазы, катализирующие реакции с пероксидом водорода в качестве акцептора электронов. Систематическое название оксидоредуктаз образуется следующим образом: Донор электронов : акцептор электронов – оксидоредуктаза Пример 1
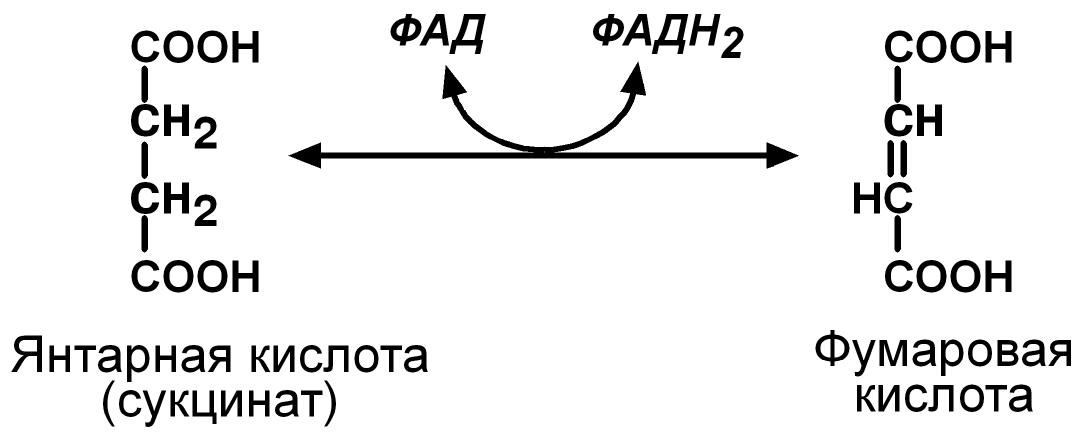
Пример 2
Пример 3
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||