Большой практикум. Практикум по почвоведению с основами геологии красноярск 2006 удк ббк рецензенты Ю. Н. Трубников
 Скачать 13.42 Mb. Скачать 13.42 Mb.
|
|
Разложение органических соединений в почве Разложение – сложный процесс, который расчленяется на 2 звена: минерализацию и гумификацию. Минерализация – процесс полного распада органического вещества до СО2, Н2О, NН3 и др. Гумификация – сложный биофизикохимический процесс трансформации промежуточных высокомолекулярных продуктов разложения органических остатков в гумусовые кислоты. В разложении участвуют: - беспозвоночные, например, дождевые черви. Они измельчают растительные остатки, смешивают с почвой, перемешивают в профиле, повышают микробиологическую деятельность, ускоряют разложение в 1,5-2 раза. Дождевые черви в среднем ежегодно перерабатывают до 1 т/га органических остатков. В лесной зоне обнаруживается до 5 млн шт/га, а масса выбросов достигает 35-40 т/га: - бактерии активно участвуют в трансформации органических веществ, используя белок, простые сахара, органические кислоты; - актиномицеты еще активнее используют углеводы, разрушают длинные цепи жирных кислот и углеводородов; - грибы с меньшей скоростью совершают многие процессы трансформации органического вещества, хотя разложение ароматических соединений ведут активнее, чем бактерии. Расщепляют лигнин; - ферменты – это структурированные белки, несущие множество функциональных групп, осуществляющих катализ (синтез). Главное свойство ферментов заключается в специфичности реакций. Почвенные ферменты активно участвуют в процессах трансформации органических остатков как в процессе жизни, так и после отмирания создавших их организмов. Например, целлюлозу могут разлагать около 5% микроорганизмов, синтезирующих ферменты – целлюлазы. На скорость разложения влияют следующие факторы:
Механизм гумификации рассматривается в 3-х гипотезах: Конденсационная гипотеза, которую описала М.М. Кононова, исходя из теоретических построений И.В. Тюрина. Суть ее состоит в следующем. Процесс гумификации растительных остатков идет параллельно процессу минерализации. Все компонеты растительных тканей могут быть первоисточниками структурных единиц в формах: а) продуктов распада растительных остатков (фенольные соединения из лигнина, танина и др. соединений), б) продуктов метаболизма (фенольные соединения – метаболиты, образующиеся при использовании углеводов микроорганизмами), в) продуктов распада и ресинтеза (аминокислоты и пептиды при разложении белков, продукты метаболизма микроорганизмов). Ответственным звеном процесса формирования гумусовых веществ является реакция конденсации структурных единиц, которая проходит путем окисления фенолов до хинонов и взаимодействие последних с аминокислотами и пептидами. Таким образом, специфической реакцией гумификации является конденсация фенольных соединений и хинонов с аминокислотами и пептидами. Эта реакция дает темноокрашенные гумусовые вещества. Гипотеза окислительного кислотообразования (или деградации биополимеров), по Л.Н. Александровой, основана на 3-х этапах: а) новообразование гумусовых веществ, б) их дальнейшая гумификация и консервация, в) постепенное медленное разрушение гумуса. Окисление происходит с участием оксидаз, в реакциях участвуют высокомолекулярные соединения, входящие в состав растительных остатков. Поэтому уже на первых этапах разложения образуются высокомолекулярные кислоты с различными молекулярными массами. Формирование азотистой части молекулы гумусовых кислот происходит по мере гумификации, когда снижается доля гидролизуемых форм соединений азота и нарастает относительное содержание более устойчивых, негидролизуемых компонентов, в т.ч. азота гетероциклических соединений. Оба пути гумификации реально существуют. Преобладание того или иного зависит от факторов почвообразования. В подзолистых, горных почвах, где ослаблена микробиологическая деятельность, путь трансформации промежуточных высокомолекулярных продуктов распада протекает по Л.Н. Александровой. В почвах с высокой биохимической активностью вполне вероятно более глубокое и более быстрое ферментативное расщепление высокомолекулярных соединений до мономеров. Поэтому гумус черноземов сформирован по схеме М.М. Кононовой. Гипотеза фрагментарного обновления гумуса принадлежит А.Д. Фокину. Суть состоит в том, что продукты разложения не формируют целиком гумусовую молекулу, а в результате конденсации сначала включаются в периферические фрагменты уже сформированных молекул, затем образуют более устойчивые циклические структуры. Поэтому атомный и фрагментарный состав почвенного гумуса постоянно обновляется за счет новых поступлений органического материала. При этом, периферические фрагменты гуминовых кислот обновляются в несколько раз быстрее, чем ядерные. Гипотеза фрагментарного обновления гумуса хорошо объясняет роль свежего растительного вещества (зеленые удобрения) и органических удобрений (навоз, компосты) в повышении запасов гумуса в почве. Исходя из представлений о различной биотермодинамической устойчивости органических соединений, Д.С. Орлов сформулировал кинетическую теорию гумификации. Известно, что от устойчивости соединений зависит скорость их распада или трансформация. Гумусовые вещества более устойчивы к биодеградации, чем органические соединения попадающих в почву растительных остатков. Поэтому гумусообразование можно рассматривать как процесс «отбора», при котором непрочные вещества растительных остатков и продуктов их трансформации разлагаются за короткий промежуток времени, а гуминовые кислоты как наиболее устойчивые соединения подвергаются непрерывным превращениям. Иначе говоря, процесс гумификации всегда имеет одно направление – отбор устойчивых продуктов, независимо от факторов почвообразования и типа почвы. Отсюда гумификация – глобальное явление, а гумусовые вещества всех почв имеют общий принцип строения. Глубина гумификации – это степень преобразования органических остатков в гумусовые вещества. Она увеличивается по мере накопления гуминовых кислот и нарастания их «зрелости». Скорость преобразования органических остатков в гумусовые вещества зависит от скорости отдельных стадий процесса и условий среды: концентрации реагирующих компонентов, влажности, температуры, реакции почвенного раствора, окислительно-восстановительного потенциала и т.п. Д.С. Орлов считает, что зависимость скорости гумификации и ее стадий от перечисленных параметров характеризует кинетику реакции (отсюда название теории). Глубину гумификации можно оценить количественно с помощью содержания гуминовых кислот в составе гумуса, отношения ГК:ФК, оптической плотности гумусовых веществ. Глубину гумификации можно связать также с длительностью периода биологической активности почв (ПБА). ПБА, по О.Н. Бирюковой – отрезок времени, в течение которого создаются благоприятные условия (температура воздуха устойчиво превышает 100С, а запас продуктивной влаги составляет не менее 1-2%) для нормальной вегетации растений, активной микробиологической деятельности. В зональном ряду почв величина отношения ГК:ФК непосредственно следует за величиной длительности ПБА. Как правило, нарастание биологической деятельности и длительности этого периода в зональном ряду почв способствует формированию гуматного гумуса. К этим условиям ближе всего отвечают черноземы, в которых отбор устойчивых продуктов гумификации («зрелые» гуминовые кислоты, наиболее богатые бензольными циклами, с наибольшей оптической плотностью) происходит активно. Неспецифические органические вещества, фульвокислоты, периферическая часть гуминовых кислот в черноземах минерализуются и вовлекаются в реакции трансформации быстрее, чем в других почвах. В подзолистых почвах при сравнительно холодной погоде летом и в каштановых почвах за счет летнего иссушения длительно сохраняются слабо гумифицированные компоненты и неспецифические соединения. Поэтому в таких почвах преобладают фульвокислоты и неспецифические соединения (липиды, углеводы), а гуминовые кислоты отличаются слабой обуглероженностью, но повышенным содержанием азота и высокой долей периферических алифатических цепей. Количество углерода, гумифицировавшееся из общего количества углерода в растительных (органических) остатках, означает коэффициент гумификации (Кг). Кг различных разлагающихся растительных остатков варьирует от 0,07 до 0,35. На скорость и характер гумификации влияют:
Гумусовые вещества представляют собой гетерогенную полидисперсную систему высокомолекулярных азотсодержащих соединений кислотной природы. Они подразделяются на гуминовые кислоты, фульвокислоты и гумины. Гуминовые кислоты (ГК)хорошо растворяются в щелочных растворах, слабо в воде и не растворяются в кислотах. Препараты ГК имеют темно-коричневую или черную окраску со средней плотностью 1,6 г/см3. Они содержат 50-62% С, 31-40% О, 3-7% Н, 2-6% N. Молекула ГК характеризуется сложным строением (рис. 16). На рисунке показан фрагмент молекулы – структурная ячейка. В молекуле находится 40-45 таких ячеек. Ядро молекулы составляют бензолполикарбоновые кислоты, ароматические и гетероциклические кольца типа бензола, пиридина, индола. Эти ароматические компоненты соединены непосредственно через С или мостиками –О-N-Н, -СН2- в рыхлую сетку. Периферическую часть молекулы ГК составляют цепи боковых радикалов (углеводные, аминокислотные и углеводородные) и функциональные группы (карбоксильные, фенолгидроксильные, метоксильные, амидные). Ароматические и гетероциклические компоненты занимают 50-60%, углеводные – 25-30%, функциональные группы – 10-15%. Рыхлое, «губчатое» строение молекулы ГК обусловливает их способность к набуханию и адсорбции. Кислотные свойства ГК определяются наличием функциональных групп. 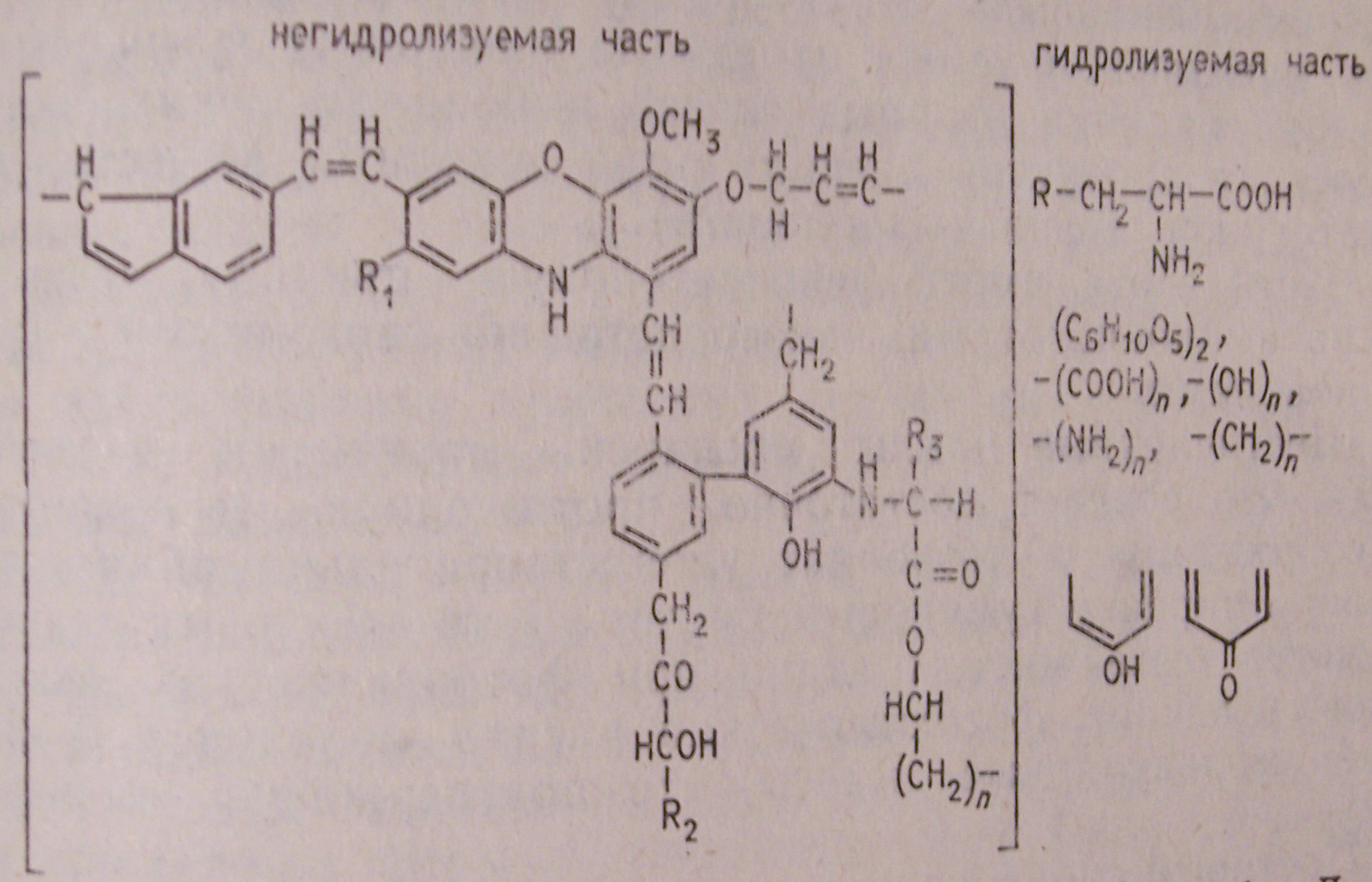 Рис. 16. Формула структурной ячейки гуминовой кислоты (по Д.С. Орлову) Фульвокислоты (ФК) отличаются светлой окраской, растворимостью в воде, щелочах и кислотах. Содержат 41-46% С, 45-53% О, 4-5% Н, 3-4% N. Строение молекулы ФК однотипно ГК. Но в отличие от ГК в молекуле ФК доминирует гидролизуемая, периферическая (60-75%) часть. Это определяет хорошую гидрофильность и реактивную способность ФК по сравнению с ГК. Гетерогенность и полидисперсность ГК и ФК означает, что эти кислоты можно разделить на ряд фракций различной молекулярной массы, элементного и компонентного состава. Гумины – совокупность КГ и ФК, прочно связанных с минеральной частью почвы. Особенности группового состава гумуса в различных почвах иллюстрируются данными табл. 26. Таблица 26. Состав гумуса в различных почвах, % к Сгумуса (по данным Д.С. Орлова)
О запасах гумуса в почвенном покрове природных зон Евразии можно судить по данным табл. 27. Они основаны на массовых анализах содержания гумуса и плотности почвенной толщи до глубины 200 см, полученных многими исследователями и обобщенными М.А. Глазовской (1997). Таблица 27. Запасы гумуса в слое 0-200 см современных почв Евразии (М.А. Глазовская, 1997)
Запасы гумуса в слое 0-200 см колеблются от100 до 816 т/га. Они наименьшие в подзолистых почвах, самые высокие – в типичных черноземах и лугово-черноземных почвах. В почвах сухих степей – светло-каштановых, лугово-каштановых – запасы гумуса составляют лишь 152-214 т/га, а в такыровидных почвах пустынь снижаются до 109 т/га. Основные запасы гумуса во всех почвах сосредоточены в слое 0-100 см. Эти данные согласуются с «правилом» Тюрина, гласившем о том, что максимальные запасы гумуса и гуматный тип гумуса характерны для черноземов. К югу и северу от зоны распространения черноземов запасы гумуса постепенно снижаются, а тип гумуса переходит в фульватно-гуматный и гуматно-фульватный. Запасы гумуса в пахотных почвах Красноярского края следующие (табл. 28). Как видим, запасы гумуса в почвах лесостепных регионов земледельческой территории Красноярского края убывают в ряду: чернозем оподзоленный > чернозем выщелоченный > чернозем обыкновенный > чернозем южный > темно-серая > серая. Таблица 28. Запасы гумуса в основных почвах земледельческой территории Красноярского края, т/га в слое 0-20 см (В.В. Чупрова, 1997)
Гумусное состояние почв – совокупность морфологических признаков, общих запасов, свойств органического вещества и процессов его создания, трансформации и миграции в почвенном профиле. Гумусное состояние служит показателем плодородия почв и их устойчивости к различным воздействиям. Отдельные его параметры являются объектом мониторинга окружающей среды. Система показателей гумусного состояния почв предложена Л.А. Гришиной и Д.С. Орловым. Приведем основные из них (табл. 29) Таблица 29. Показатели гумусного состояния
Примечание: в числителе – запасы гумуса в слое 0-20 см, в знаменателе – в слое 0-100 см. Эта оценочная шкала используется при выполнении контрольных заданий и курсовой работы.
Многочисленные материалы свидетельствуют о значительных потерях гумуса из почв. Главные причины:
Одним из способов контроля почв является определение баланса гумуса. Баланс гумуса представляет собой разность между статьями его прихода (гумификация растительных остатков) и расхода (минерализация при возделывании полевых культур и паровании почвы). Известно, что среднегодовой баланс гумуса в черноземах Украины равен 0,45-0,55 т/га, Краснодарского края – 0,5 т/га, Центральных черноземных областей – 0,47 т/га, Красноярского края – 0, 23 т/га. Таким образом, дефицит гумуса в нашем регионе ниже, чем в почвах европейского региона. Это связано с более медленными темпами минерализации органического вещества в условиях Сибири. Способами регулирования гумусного состояния почв следует назвать следующие: - внесение навоза, различных компостов и нетрадиционных органо-минеральных удобрений, полученных на основе отходов деревообрабатывающей промышленности (кора, опилки) и минерального сырья (фосфориты, цеолиты, вермикулит и др.). Например, расчетная норма навоза для поддержания бездефицитного баланса гумуса в черноземах составляет 5,4 т/га пашни. При такой норме навоза в пашню края объем внесения необходимо увеличить до 22 млн т. Что касается торфа, то он во многом противоположен навозу. Достаточно сказать, что торф подавляет микробиологическую активность почв, слабо ассимилируется почвенной массой и, оставаясь долго в не разложенном состоянии, создает вредную иллюзию увеличения содержания гумуса в пахотных почва. Месторождения торфа обнаружены более чем в 30 районах Красноярского края. Прогнозный запас торфа около 25 млрд м3, торф низинного типа с нейтральным рН, средней степенью разложения и зольностью, равной 35%. Поэтому необходимы исследования по разработке использования торфа в качестве органических удобрений; - введение в структуру пашни полей многолетних трав, которые оставляют после себя большие запасы растительных остатков; - увеличение высоты стерневых остатков полевых культур во время уборки; - запашка соломы в паровые поля; - применение зеленых удобрений. Установлено (Чупрова, 1997), что положительный баланс гумуса и азота в черноземах устанавливается при запашке в почву 8 т/га пожнивно-корневых остатков люцерны и 12 т/га зеленого (донникового) удобрения. Вопросы для семинара
Задачи и упражнения В тетради для самостоятельной работы дайте ответы на вопросы и решите следующие задачи и упражнения: 1. Принцип метода определения гумуса по Тюрину. 2. Химизм метода определения гумуса по Тюрину. 3.Специфика подготовки почвенного образца для анализа на содержание гумуса. Почему из почвенного образца выбираются растительные остатки? 4.От чего зависит навеска почвы для определения гумуса? 5. Что произошло, если при окислении суспензия приобрела зеленый цвет? Как поступить дальше? 6. Для чего проводится «холостое» титрование? 7.Как перевести содержание услерода в гумус? 8. Показатели гумусного состояния почв. 9. Как определить запасы гумуса в почве? 10. Определите и оцените запасы гумуса в почве: 0-20 см слоя при содержании гумуса 5,5% и плотности сложения 0,98 г/см3; 0-20 см слоя при содержании гумуса 1,7% и плотности сложения 1,23 г/см3; 0-20 см при содержании гумуса 8,2% и плотности сложения 1,10 г/см3; 0-20 см слоя при содержании гумуса 6,8% и плотности сложения 1,30 г/см3; 0-100 см слоя при содержании гумуса 5% в первом 0-20 см слое и снижении его глубже через каждые 20 см на 1%. Плотность почвы в первом 0-20 см слое равна 1,01 г/см3, глубже увеличивается через каждые 20 см на 0,03 г/см3; 0-100 см слоя при содержании гумуса 7% в первом 0-20 см слое и снижении его содержания глубже через каждые 20 см на 1,5%. Плотность почвы в первом 0-20 см слое равна 1,15 г/см3, глубже увеличивается через каждые 20 см на 0,02 г/см3. 11. Оцените гумусное состояние почв в слое 0-20 см: запасы гумуса 200 т/га, степень гумификации 40%, ГК:ФК = 1,7; запасы гумуса 60 т/га, ГК:ФК = 0,6, степень гумификации 10%; содержание гумуса 6%, запасы гумуса 170 т/га, ГК:ФК = 1,1, степень гумификации 32%; содержание гумуса 10%, запасы гумуса 200 т/га, ГК:ФК = 1,2, С:N =13,4; содержание гумуса 7%, запасы гумуса 188 т/га, С:N = 11,1, ГК:ФК = 2,6; в слое 0-100 см: содержание гумуса 8%, запасы гумуса 465 т/га, ГК:ФК = 1,2; содержание гумуса 7%, запасы гумуса 658 т/га, ГК:ФК = 1,7.
Бактерий и многолетних злаковых трав; Водорослей и многолетних бобовых трав; Древесных хвойных и лиственных пород; Навоза и соломы пшеницы; Бобового и злакового сидерата (зеленого удобрения).
тундровой зоны; таежно-лесной зоны; лесостепно зоны; степной зоны; пустынной зоны; агроценозов.
Тесты
а) населяющие почву организмы, непосредственно участвующие в процессах почвообразования; б) почвенная фауна, микроорганизмы, живые корни растений; в) почвенная фауна, влияющая на процессы и режимы в почвах. 2. Органическое вещество почвы – это: а) масса растительных остатков и гумуса; б) совокупность живой биомассы и мертвых остатков растений, животных, микроорганизмов, продуктов их метаболизма и гумусовых веществ: в) совокупность мортмассы и гумусовых веществ. 3. Гумус почвы – это: а) гуминовые кислоты и их производные; б) органический материал, оказавшийся в почве после отмирания живых организмов; в) совокупность специфических и неспецифических органических веществ. 4. Источники почвенного гумуса: а) корни, микробобиомасса, удобрения, стерня; б) опад зеленых растений, биомасса микроорганизмов и беспозвоночных, органические удобрения; в) корни, фауна, органические удобрения, пожнивные остатки. 5. Процесс разложения – это: а) процесс полного распада органических веществ; б) процесс образования гумуса; в) совокупность минерализации и гумификации. 6. Основные гипотезы гумификации: а) конденсационная, окислительного кислотообразования, обновления, кинетическая теория; б) биофизико-химическая, деградации биополимеров; в) окисления, дезаминирования. 7. Две наиболее важные группы гумусовых веществ специфической природы: а) гуминовые кислоты и гумины; б) гумины и фульвокислоты; в) фульвокислоты и гуминовые кислоты. 8. Самые подвижные группы гумусовых веществ: а) фульвокислоты; б) гуминовые кислоты; в) гумины. 9. Элементный состав ГК и ФК: а) С,N, Р, Са; б) С, О, Н, N; в) С, О, Н, N2. 10. Среднее содержание углерода в гумусе: а) 10; б) 90; в) 56. 11. Почва, содержащая 8% гумуса: а) каштановая; б) подзолистая; в) чернозем. 12. Почва с фульватным типом гумуса: а) серая лесная; б) подзолистая; в) каштановая. 13. Почва с запасами гумуса в пахотном слое > 200 т/га: а) чернозем; б) темно-каштановая; в) серозем. 14. Процесс, сопровождающийся потерями гумуса в пахотных почвах: а) минерализация; б) нитрификация; в) аммонификация. 15. Главная причина потерь гумуса в пахотных почвах: а) усиление минерализации; б) уменьшение массы растительных остатков, поступающих в почву; в) эрозия и дефляция.
Материалы и оборудование: весы технические; колбы на 250 мл; воронки; фильтры; цилиндр на 100 мл; пипетка на 25 мл; бюретка для титрования; 0,05 н. раствор NaOH; 0,05 н. раствор HCl; индикатор - фенолфталеин. Содержание работы: Сумма обменных оснований (S) – это сумма всех катионов за исключением H+ и Al3+, выраженная в мг. экв/100 г почвы. Как правило, чем выше сумма обменных оснований, тем почва плодороднее. Принцип и химизм метода основан на вытеснении обменных оснований из почвенного поглощающего комплекса ионом водорода соляной кислоты, по следующей схеме: [ППК]Ca++ Mg++ + 4HCl ↔ [ППК] 2H+ 2H+ + CaCl2 + MgCl2 Количество перешедших в раствор обменных оснований определяют по разности между содержанием ионов H+ в растворе до и после взаимодействия кислоты с почвой, поскольку обмен ионов проходит в строго эквивалентном количестве. Однако при однократной обработке почвы кислотой в раствор переходят не все обменные основания, к тому же часть кислоты расходуется на побочные реакции, поэтому в подзолистых и дерново-подзолистых почвах показатели этого метода будут завышены, а в черноземах – занижены. Следовательно, данный метод дает только приблизительное представление о сумме обменных оснований в почве и его используют лишь в практических целях для выяснения степени насыщенности почв основаниями. Ход определения. На технических весах отвешивается навеска 5 г воздушно-сухой почвы, пропущенной через сито с диаметром ячеек 1 мм. Навеску помещается в колбу на 250 мл, куда приливается из мерного цилиндра 100 мл 0,05 н. раствора HCl. Суспензия встряхивается 15 минут, затем фильтруется через бумажный фильтр, перенося всю почву на воронку. Первые порции фильтрата отбрасывают. Из полученного фильтрата отбирается пипеткой 25 мл в коническую колбу на 250 мл, прибавляется 2-3 капли индикатора фенолфталеина. Остаток кислоты в фильтрате титруют 0,05 н. раствором NaOH до слабо-розовой окраски, не исчезающей в течение 1 минуты. Одновременно проводится опыт с холостым определением. Для этого 25 мл 0,05 н. раствора HCl титруют 0,05 н. раствором NaOH до слабо-розовой окраски. Титрование иногда осложняется тем, что выпадает осадок полуторных оксидов переходят в раствор в результате разрушающего действия соляной кислоты на алюмосиликатную часть ППК. В этом случае дают осадку осесть на дно и проверяют окраску прозрачной жидкости над осадком. Сумму обменных оснований (S) вычисляют по формуле: S (мг-экв/ 100 г почвы) = (a-b) · 100 · 0.05 ·100 5·25 где: а – количество 0,05 н. NaOH, пошедшего на титрование холостой пробы, мл; b – количество 0,05 н. NaOH, пошедшего на титрование рабочего фильтрата, мл; 100 – количество HCl, мл; 0,05 – нормальность HCl; 5 – навеска почвы, г; 25 – количество фильтрата, мл; 100 – коэффициент пересчета на 100 г почвы. Обсуждение результатов: Результаты определения заносятся в сводную таблицу по данным химического анализа почвы (табл. 22). Обсуждение ведется по следующим вопросам: 1. По данным таблицы постройте график распределения суммы обменных оснований по профилю почвы, проанализируйте результаты, сопоставляя распределение суммы обменных оснований с:
и сделайте выводы. 2. Дайте оценку суммы обменных оснований для данной почвы, используя оценочную шкалу, мг.экв/100 г почвы: <10 низкая 10-20 средняя 20-40 высокая >40 очень высокая.
Материалы и оборудование: весы технические; колбы на 100 мл; дистиллированная вода; 1 н раствор KCl; стаканчики на 50 мл; стандартные буферные растворы с рН от 1,68 до 9,22; иономер; вспомогательный хлорсеребряный электрод; стеклянный электрод, предварительно выдержанный в 0,1 н растворе НСl. Содержание работы: определение реакции почв относится к числу наиболее распространенных анализов, как при теоретических, так и при прикладных исследованиях почв. Реакция почвенного раствора имеет большое значение для произрастания растений и жизнедеятельности микроорганизмов, может определять развитие и направление химических и биохимических процессов, то есть влиять на трансформацию минеральной и органической части почвы, растворение, миграцию соединений и т.д. Реакция почвенного раствора определяется концентрацией водородных ионов, но эта концентрация часто бывает очень малой, поэтому для удобства, в практических целях используется обратный десятичный логарифм активности этих ионов (ан+), который условно обозначается символом рН. рН = -lg ан+ Таким образом, рН - это обратный десятичный логарифм активности или концентрации ионов водорода в растворе. Символ рН позволяет выразить активность водородных ионов (ан+) в кислой и в щелочной среде, то есть представить ан+ в пределах 100 – 10-14. С увеличением концентрации водородных ионов (подкисление раствора) активность ионов водорода так же повышается, значение рН понижается; при подщелачивании раствора происходит обратное. Например, при активности ан+ равной 10-3, отрицательный логарифм 10-3=3 и рН=3; если ан+=10-9, то –lg 10-9=9 и рН=9. В зависимости от величины рН реакция почв может изменяться от сильнокислой до сильнощелочной (табл. 30). | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
