Лекция 4 (2). Предупредительные мероприятия внутриаптечного контроля лф
 Скачать 109.02 Kb. Скачать 109.02 Kb.
|
|
ТЕМА: ПРЕДУПРЕДИТЕЛЬНЫЕ МЕРОПРИЯТИЯ ВНУТРИАПТЕЧНОГО КОНТРОЛЯ ЛФ. ВИДЫ ВНУТРИАПТЕЧНОГО КОНТРОЛЯ. Внутриаптечный контроль (ВАК) качества лекарственных средств, включает не только аналитический контроль, но и систему мероприятий, которые обеспечивают правильное хранение, приготовление и отпуск их. ВАК основан, на строгом соблюдении фармацевтического и санитарного режима в аптеке. Особенно внимательно необходимо соблюдать правила хранения медикаментов и технологию их приготовления. В аптеках должны быть аналитические кабинеты или аналитические столы, оснащенные необходимыми приборами, реактивами, справочной и специальной литературой. ВАК проводят провизоры-аналитики, входящие в штат крупных аптек. Провизоры-технологи, в обязанности которых также входит проверка качества лекарств, имеют оборудованное рабочее место на ассистентском столе или рядом с ним. Заведующий аптекой и его заместители руководят работой по контролю качества лекарств. Они должны владеть всеми видами ВАК, а в небольших аптеках сами выполнять функции провизора-технолога Внутриаптечному контролю подвергаются все изготовляемые в аптеке лекарственные формы. Существуют несколько видов контроля, которые условно подразделяются на обязательные и выборочные. Все эти виды контроля регламентируются приказом от 26 октября 2015 г. N 751Н Об утверждении правил изготовления и отпуска лекарственных препаратов для медицинского применения аптечными организациями, индивидуальными предпринимателями, имеющими лицензию на фармацевтическую деятельность. 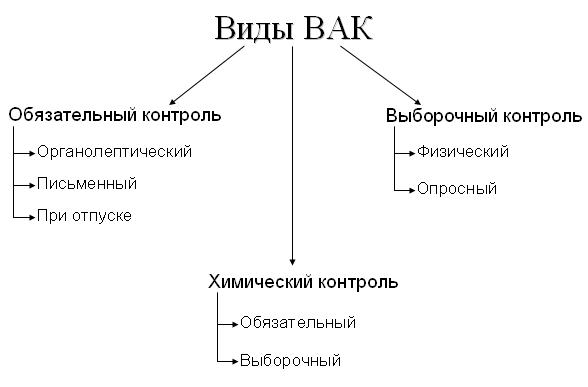 Показатели качества, по которым можно установить неудовлетворительность изготовленных лекарственных средств регламентируются приказом от 26 октября 2015 г. N 751Н. Основной задачей предупредительных мероприятий является предотвращение проникновения в аптеку и из нее не качественных ЛП, медицинской техники и изделий медицинского назначения. Приемочный контроль: упаковка; маркировка; описание; сопроводительные документы. Предупредительные мероприятия: санрежим (Приказ № 309); получение и хранения H2O; метрологическое обеспечение (весы, приборы); контроль рецептов, требований ЛПО; фармацевтическая технология; условия и сроки хранения, заполнение штангласов; номенклатура концентратов, полуфабрикатов, внутриаптечной заготовки, фасовки. Предупредительные мероприятия, обеспечивающее высокое качество изготовленных в аптеке ЛС и безопасность их применения заключаются в выполнении следующих требований: 1. Соблюдение санитарных норм и правил противоэпидемического режима, а также правил асептики и фармацевтического порядка в соответствии с действующими НД; 2. Соблюдение правил получения, сбора и хранения воды очищенной и воды для инъекций, своевременная санитарная обработка трубопровода, контроль за своевременным изъятием стерильных растворов, вода очищенная и вода для инъекций для испытания на стерильность в соответствии с действующими требованиями. Сборники для воды очищенной и воды для инъекций должна иметь четкую надпись вода очищенная, вода для инъекций. На сборнике воды прикрепляется бирка с указанием даты её получения, номера анализа и подписи проверившего. При одновременном испытании нескольких сборников они должны быть пронумерованы; 3. Обеспечение исправности и точности приборов, аппаратов, весов и регулярность их проверки; 4. Тщательный просмотр поступающих в аптеку рецептов и требований с целью проверки правильности их выписывания, совместимости веществ, входящие в состав ЛС. Соответствие прописанных доз возрасту больного и наличие указаний о способах применения лекарств; 5. Соблюдение технологии ЛС в соответствии с требованиями действующей ГФ и др. НД. Изготовление ЛС по индивидуальным прописям в виде внутриаптечной заготовки, а также концентратов и полуфабрикатов считается законченным только после оценки качества их изготовления и правильности оформления; 6. Обеспечение в аптеке условий и средств хранения ЛВ в соответствии с их физико-химическими свойствами и требованиями действующей ГФ, приказов и инструкций. Предупредительные мероприятия включают проведение приёмочного контроля, который проводиться с целью предупреждения поступления в аптеку некачественных лекарственных средств. Приёмочный контроль заключается в проверке лекарственных средств по показателям: «Описание», «Упаковка», «Маркировка»; в проверке правильности оформления расчётных документов (счетов), а также наличия сертификатов качества. Контроль по показателю «Описание» включает проверку внешнего вида, запаха. При проверке по показателю «Упаковка» особое внимание обращается на её целостность и соответствие физико-химическим свойствам лекарственных средств. При контроле по показателю «Маркировка» обращается внимание на оформление лекарственных средств. На этикетках должно быть указано: предприятие-изготовитель; наименование лекарственного средства; масса или объём; концентрация или состав; номер серии; номер анализа; срок годности; дата фасовки. В случае сомнения в качестве лекарственных средств образцы направляются в территориальную контрольно-аналитическую лабораторию. Такие лекарственные средства с обозначением: «Забраковано при приёмочном контроле» хранятся в аптеке изолированно от других лекарственных средств до решения вопроса о его качестве. Письменный контроль осуществляется при изготовлении лекарственных форм по индивидуальным прописям и требованиям ЛПУ. При этом заполняются паспорта письменного контроля. В паспорте указывается: дата, номер рецепта (требования), взятые лекарственные вещества и их количество, число доз, ставятся подписи изготовившего, расфасовавшего и проверившего лекарство. В случае изготовления лекарственной формы практикантом ставятся подписи практиканта и лица, ответственного за производственную практику. Паспорта письменного контроля сохраняются в аптеках в течение 2-х месяцев. Изготовленные лекарственные формы, рецепты и заполненные паспорта передаются на проверку провизору-технологу или лицу, выполняющему его функции. Контроль заключается в проверке соответствия записей в паспорте письменного контроля прописи в рецепте, правильности произведенных расчетов. Если провизором-аналитиком проведен полный химический контроль лекарственной формы, то на паспорте ставится номер анализа и подпись провизора-аналитика. Опросный контроль применяется выборочно. Проводится после приготовления фармацевтом не более пяти лекарственных форм. При проведении опросного контроля провизор-технолог называет первый входящий в лекарственную форму ингредиент, а в лекарственных формах сложного состава указывает так же его количество, после чего фармацевт называет все взятые им ингредиенты и их количество. При использовании полуфабрикатов (концентратов) фармацевт называет их состав и концентрацию. Органолептический контроль заключается в проверке внешнего вида лекарственной формы, его цвета, запаха, однородности смешения, отсутствия механических включений в жидких лекарственных формах. На вкус проверяются выборочно лекарственные формы, предназначенные для детей. Результаты органолептического контроля лекарственных форм регистрируются в журнале. Физический контроль заключается в проверке общей массы или объема лекарственной формы, количества и массы отдельных доз, входящих в данную лекарственную форму (но не менее 3 доз) 1) Проверяются: - каждая серия фасовки и внутриаптечной заготовки в количестве не менее трёх упаковок. - лекарственные формы, изготовленные по индивидуальным рецептам (требованиям) выборочно в течение рабочего дня с учетом всех видов лекарственных форм, но не менее 3% от количества лекарственных форм, изготовленных за день. - лекарственные формы, требующие стерилизации, после расфасовки до их стерилизации, не менее 5 флаконов (бутылок). 2) Результаты физического контроля регистрируются в журнале 3) При проверке лекарственных форм контролируется так же качество укупорки. Химический контроль заключается в определении подлинности (качественный анализ) и количественного содержания лекарственных веществ, входящих в состав лекарственной формы. I. Качественному анализу подвергаются обязательно: 1) Вода очищенная ежедневно (из каждого баллона, а при подаче воды по трубопроводу на каждом рабочем месте) на отсутствие хлоридов, сульфатов, солей кальция. Вода, предназначенная для изготовления растворов для инъекций, новорожденных и глазных капель, кроме указанных выше испытаний, должна быть проверена на отсутствие восстанавливающих веществ, солей аммония и диоксида углерода в соответствии с требованиями Государственной Фармакопеи. Ежеквартально вода очищенная направляется в контрольно-аналитическую лабораторию для полного химического анализа. 2) Все лекарственные средства, в том числе концентраты и полуфабрикаты, поступающие из помещений хранения в ассистентскую, а в случае сомнения – лекарственные средства, поступающие в аптеку со склада. 3) Концентраты, полуфабрикаты и жидкие лекарственные средства в бюреточной установке и в штанглассах с пипеткой в ассистентской комнате при заполнении. 4) Лекарственные средства, расфасованные в аптеке, и внутриаптечная заготовка (каждая серия). II. Качественному анализу подвергаются выборочно: 1) Лекарственные формы, изготовленные по индивидуальным рецептам и требованиям ЛПУ, выборочно у каждого фармацевта в течение рабочего дня, не менее 10 % от общего количества изготовленных лекарственных форм. Проверке должны подвергаться различные виды лекарственных форм. Особое внимание обращается на лекарственные формы для детей (особенно новорожденных), применяемые в глазной практике; содержащие наркотические и ядовитые вещества; гомеопатические лекарственные форма четвёртого десятичного разведения. Результаты качественного анализа регистрируются в журнал 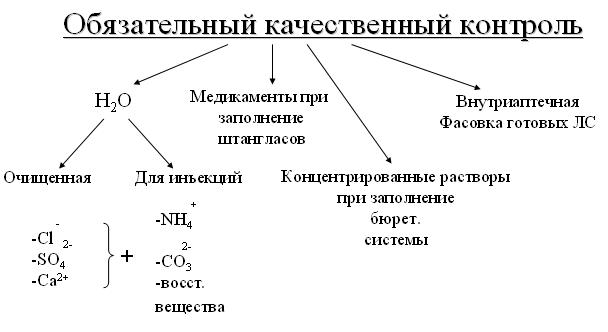 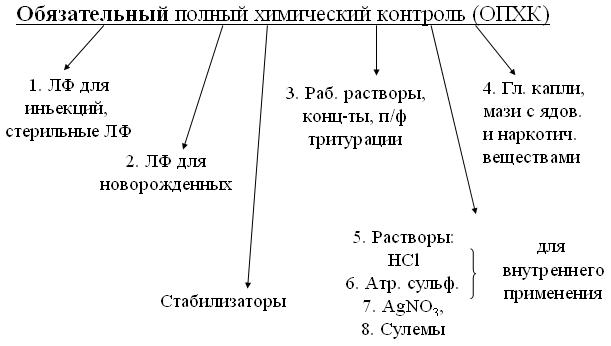 III. Качественному и количественному анализу (полный химический контроль) подвергаются обязательно: 1) Все растворы для инъекций до и после стерилизации, включая определение pH, изотонирующих и стабилизирующих веществ. 2) Стерильные растворы для наружного применения (офтальмологические растворы для орошений, растворы для лечения ожоговых поверхностей и открытых ран, для интравагинального введения и других) 3) Глазные капли и мази, содержащие наркотические и ядовитые вещества. При анализе глазных капель содержание в них изо тонирующих и стабилизирующих веществ определяется до стерилизации. 4) Все лекарственные формы для новорожденных детей. (При отсутствии методик количественного анализа лекарственных форм, они должны быть проверены качественным анализом. Как исключение, изготовление лекарственных форм для детей – новорожденных сложных по составу, не имеющих методик качественного и количественного анализа производится в присутствии провизора–аналитика или провизора-технолога «под наблюдением»). 5) Растворы кислоты хлористоводородной (для внутреннего употребления), атропина сульфата, ртути дихлорида и серебра нитрата. 6) Все концентраты и полуфабрикаты (в том числе тритурации). 7) Вся внутриаптечная заготовка лекарственных средств (каждая серия) 8) Стабилизаторы, применяемые при изготовлении растворов для инъекций и буферные растворы, применяемые при изготовлении глазных капель. 9) Концентрация этилового спирта путем определения плотности (спиртометром) при разведении в аптеке, а в случае необходимости – при приеме со склада. IV. Качественному и количественному анализу (полный химический контроль) подвергаются выборочно: 1) Лекарственные формы, изготовленные в аптеке по индивидуальным рецептам или требованиям ЛПУ, в количестве не менее трех при работе в одну смену с учетом всех видов лекарственных форм. Особое внимание следует обращать на контроль лекарственных форм для детей; применяемых в глазной практике; содержащих наркотические и ядовитые вещества; растворы для лечебных клизм. Результаты полного химического контроля регистрируются в журнале. В журнал заносятся также случаи неудовлетворительного изготовления лекарственных средств, обнаруженные при контроле качества. Контролю при отпуске подвергаются все изготовленные в аптеках лекарственные средства при их отпуске. При этом проверяется соответствие: - упаковки лекарственных средств физико-химическим свойствам, входящих в них ингредиентов; - оформления лекарственных средств действующим требованиям; - указанных доз лекарственных средств списка А или Б возрасту больного; - номера на рецепте и номера на этикетке, фамилии больного на квитанции, фамилии на этикетке, фамилии больного на рецепте или его копии; - копий рецептов прописям рецептов; При отпуске особое внимание обращается на оформление соответствующими предупредительными надписями лекарственных форм: на растворах для лечебных клизм должна быть надпись «Для клизм»; на растворах для дезинфекции - надписи «Для дезинфекции», «Обращаться с осторожностью». На все лекарственные средства, отпускаемые в детские отделения лечебных учреждений, - надпись «Детское». Лицо, отпустившее лекарственное средство, обязано поставить свою подпись на обратной стороне рецепта (требования). |
