Производство сульфата аммония. Расчет материального и теплового баланса установки G=2 тч продукта. Производство сульфата аммония. Расчет материального и теплового баланса установки G2 тч продукта
 Скачать 236.54 Kb. Скачать 236.54 Kb.
|
|
2. Физико-химические основы выбранного способа производства Особенностью сатураторного процесса является одновременное улавливание из газа аммиака и пиридиновых оснований и кристаллизация соли сульфата аммония [5]. Максимальный эффект каждого из этих процессов может быть достигнут при различных физико-химических условиях, которые создать одновременно в одном аппарате трудно. На сатураторный процесс оказывает влияние ряд факторов: а) температура и кислотность маточного раствора, б) интенсификация массообмена в ванне сатуратора, в) чистота маточного раствора, г) техническая исправность сатуратора и нагрузка его газом. Все эти факторы как бы переплетаются между собой, оказывая общее комплексное влияние на полноту улавливания аммиака, а главное на образование и рост кристаллов сульфата аммония. Химизм процесса, лежащий в основе получения сульфата аммония в сатураторе, сводится к реакции нейтрализации аммиака серной кислотой: NH3 + H2SO4 = NH4HSO4 (2.1) NH4HSO4 + NH3 = (NH4)2SO4 + Q (2.2) 2.1. Влияние теплового равновесия на качество сульфата аммония Реакция эта протекает с огромной скоростью, и как всякая реакция нейтрализации сопровождается выделением тепла. При использовании 76 %-ной кислоты, количество выделяющегося тепла уменьшается до 220 кДж/моль. На 1 кг сульфата аммония выделяется 1173,20 кДж, что является основным источником тепла в сатураторе и играет огромную роль для достижения теплового равновесия в ванне сатуратора, определяет его водный баланс, влияет на температуру ванны, степень улавливания аммиака и пиридиновых оснований из газа и кристаллизацию соли сульфата аммония. При правильном режиме работы сатуратора этого тепла должно быть достаточно для выпаривания всей избыточной влаги, которая поступает в сатуратор: с коксовым газом, с пароаммиачной смесью после колонны, с серной кислотой, от промывки трубопроводов, солевых насосов и ловушки, соли в центрифугах и сатуратора. Это же тепло служит для поднятия температуры маточного раствора до оптимальной величины (от 50 °С до 55 °С), восполнения потерь тепла поверхностью сатуратора, потерь тепла с циркулирующим маточным раствором и выдаваемым сульфатом аммония. Практически не всегда удается выдерживать оптимальный тепловой режим работы сатуратора только за счет тепла реакции нейтрализации. Это объясняется недостаточным охлаждением газа в первичных холодильниках и, следовательно, повышением содержания в газе паров воды, неудовлетворительной работой дефлегматора аммиачной колонны, влекущей увеличение количества водяных паров в пароаммиачной смеси и подачей в сатуратор более слабой серной кислоты. В этих случаях не достигается испарения всей добавочной влаги, т. е. нарушается тепловое равновесие в сатураторе. При недостатке тепла в маточном растворе сатуратора происходит накапливание воды, что приводит к обводнению раствора и расстройству технологического процесса, так как из разбавленного раствора перестает выкристаллизовываться сульфат аммония. Образующийся избыток маточного раствора выводится из сатуратора в сборник. Выпаривание избыточной воды при возвращении раствора в сатуратор требует повышения температуры газа и маточного раствора, что связано с увеличением объема газа, сопротивлением сатуратора, ухудшением качества сульфата аммония и затруднением в работе конечного газового холодильника. Поэтому обводнение маточного раствора сатуратора рассматривается как авария. 2.2. Влияние кислотности и температуры маточного раствора на кристаллизацию сульфата аммония Кристаллизация сульфата аммония из маточного раствора является таким же важным элементом сатураторного процесса, как и тепловое равновесие. Процесс кристаллизации состоит из двух стадий — образование центров кристаллизации (зародышей) и дальнейшего роста кристаллов. Количество образующихся центров кристаллизации зависит от различных причин: температуры маточного раствора, его кислотности и чистоты, интенсивности перемешивания у граней кристаллов. Повышение температуры способствует образованию большого числа центров кристаллизации, т. е. получению мелких кристаллов. Поэтому необходимо поддерживать предельно низкую температуру ванны сатуратора, не выше той, при которой уже не нарушается тепловое равновесие сатуратора и не обводняется ванна. Росту кристаллов способствует более низкая температура маточного раствора. При температуре выше 60 °С рост кристаллов сульфата аммония прекращается. При высокой температуре ванны образуется мелкая соль, кристаллы агрегируются в сростки с развитой поверхностью, на которой удерживается влага и кислота, что ухудшает качество сульфата аммония. Образованию большого количества центров кристаллизации способствует повышенная концентрация кислоты, быстрое достижение состояния насыщения (при быстром охлаждении), а также наличие так называемой затравки, т. е. кристаллов, пыли и других примесей. Кислотность маточного раствора влияет на рост и форму кристаллов, степень улавливания аммиака и пиридиновых оснований из коксового газа. Повышенная кислотность раствора приводит к прекращению роста и растворению кристаллов, возрастанию вязкости и плотности раствора, в результате чего замедляется оседание кристаллов сульфата аммония в конусе сатуратора, а выводимый в кристаллоприемник раствор не содержит крупных кристаллов. Мелкие кристаллы очень плохо фугуются, забивают сита в центрифуге, плохо отмываются от кислоты, а при хранении быстро слеживаются, образуя глыбы и комья. При кислотности раствора от 1 % до 2 % получаются крупные и хорошие по форме кристаллы соли. Однако при этом происходит обильное выделение кристаллов, что затрудняет работу солевых насосов, вызывает наращивание кристаллов на стенках сатуратора, в щелях барботажного зонта, приводит к увеличению сопротивления сатуратора газовому потоку, к уносу брызг маточного раствора в ловушку. Низкая кислотность маточного раствора приводит к потерям аммиака и пиридиновых оснований с обратным газом. Таким образом, кислотность ванны сатуратора должна быть по возможности ниже, но достаточной для полноты улавливания аммиака и пиридиновых оснований из газа. В свою очередь, кислотность раствора должна быть постоянной и не превышать 5 %. При наличии эффективного перемешивающего устройства в ванне сатуратора кислотность раствора поддерживают на уровне от 3 % до 4 %. С повышением кислотности до 6 % и выше, резко ухудшается форма кристаллов, уменьшаются их размеры, образуются сростки кристаллов, что приводит к отложению соли на стенках сатуратора. С повышением кислотности раствора затрудняется поддержание допустимой нормы содержания свободной серной кислоты в товарном сульфате аммония, увеличивается расход воды на его промывку в центрифуге, увеличивается время сушки. Интенсификация роста кристаллов соли достигается перемешиванием и циркуляцией маточного раствора и объемной нагрузкой сатуратора по газу. Перемешивание раствора увеличивает время пребывания кристаллов во взвешенном состоянии, что обусловливает большую продолжительность их роста. Интенсивное перемешивание верхних слоев маточного раствора в ванне сатуратора возможно благодаря особой конструкции барботажного зонта. К нижней поверхности барботажного зонта по всей его окружности прикрепляются 50 направляющих лопаток, расположенных под углом к поверхности зонта, в результате коксовый газ, кроме перемешивания раствора при барботаже, приводит его также во вращательное движение. Существуют различные устройства, обеспечивающие интенсивное перемешивание маточного раствора. Любая конструкция должна обеспечить: достаточное время пребывания кристаллов в пересыщенном растворе; непрерывный обмен абсорбционного слоя у граней кристаллов, т. е. приток к граням кристаллов новых порций пересыщенного раствора; сепарацию кристаллов, т. е. отделение крупных от мелких. 2.3. Влияние примесей на качество сульфата аммония На качество сульфата аммония сильно влияют примеси. Они попадают в маточный раствор с коксовым газом, серной кислотой, с парами из аммиачной колонны и в результате коррозии аппаратуры и материальной коммуникации. Органические примеси — масла, смола, непредельные соединения, поступают в сатуратор с коксовым газом и с отработанной или регенерированной серной кислотой. Эти примеси образуют в сатураторе кислую смолку, покрывающую в виде пленки поверхность маточного раствора ванны, что увеличивает сопротивление проходу газа. Повышенный расход регенерированной и отработанной кислоты может привести к вспениванию раствора и уносу пены с обратным газом. С серной кислотой в ванну сатуратора могут поступать неорганические примеси в виде соединений мышьяка, кадмия, свинца, хлора, хрома, железа, меди, алюминия и азотной кислоты, которые проявляются по-разному. Таким образом, наличие в маточном растворе органических и неорганических примесей затрудняет кристаллизацию соли, ухудшает качество сульфата аммония, затрудняет фугование соли в центрифугах, увеличивает влажность сульфата, его кислотность и требует усиленной промывки и длительной сушки товарного продукта. Кроме того, многие примеси придают сульфату аммония специфическую окраску, которая может служить косвенным показателем чистоты товарного продукта. Серый цвет сульфату аммония придают смолистые вещества; черный- сернистые соединения железа, свинца и меди; роданистые соединения в присутствии железа придают красную или розовую окраску; цианистые соединения железа придают сульфату аммония цвет от зеленого до фиолетового; соединения мышьяка окрашивают соль в желтый цвет; смоляной туман придаёт коричневую окраску. Большое значение для нормальной работы сатуратора имеет своевременное удаление солевых отложений на стенках сатуратора и на барботажном зонте. Эффективным способом удаления солевых отложений признана ежесуточная промывка сатуратора конденсатом пара с подачей его в места наибольшего скопления соли. Таким образом, качество сульфата аммония зависит от работы первичных газовых холодильников, электрофильтров, от качества поступающей серной кислоты, эффективности работы перемешивающих устройств, нагрузки сатуратора по газу и аммиаку. Параметры технологического режима представлены в таблице 1 Таблица 1 Параметры технологического режима
3. Технологическая схема производства целевого продукта Принципиальная технологическая схема производства целевого продукта представлена на рис.2 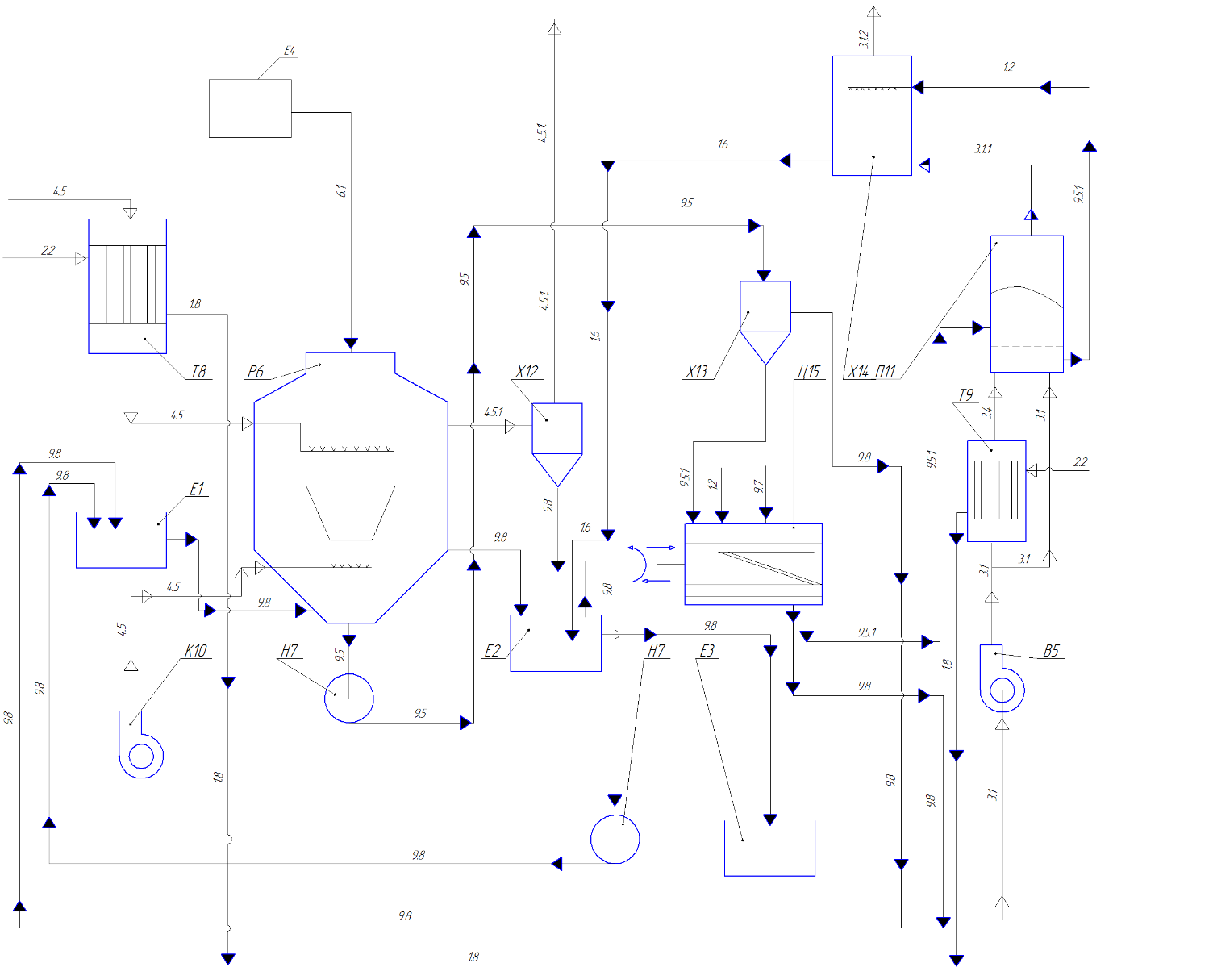 1.2 – вода техническая, 1.6 – вода оборотная, 1.8 – конденсат, 2.2 – насыщенный пар, 3.1 – воздух атмосферный, 3.1.1 – пыль с частицами сульфата аммония, 3.1.2 – очищенный воздух, 3.4 – горячий воздух, 4.5 – коксовый газ с аммиаком, 4.5.1 – коксовый газ, 6.1 – серная кислота, 9.5 – пульпа, 9.5.1 – влажный сульфат аммония, 9.7 – антислеживатель, 9.8 – маточный раствор, Е1 - ёмкость обратных токов, Е2 – Циркуляционная ёмкость, Е3 – сборник маточного раствора, Е4 – ёмкость для серной кислоты, В5 – газодувка, Р6 – сатуратор, Н7 – насос, Т9 – решофер, К10 – компрессор, П11 – сушка КС, Х12 – ловушка, Х13 – гидроциклон, Х14 – ротоклон, Ц15 – центрифуга. Рис. 2. - Принципиальная технологическая схема В состав сульфатного отделения входит шесть сатураторных установок с параллельными схемами работы. В работе постоянно находятся два сатуратора каждой очереди. Коксовый газ после газодувок машинного зала поступает по газопроводу в газовые подогреватели (решоферы) (Т8), где подогревается до температуры не выше 75 °С. При обводнении ванны сатуратора и при промывке допускается нагрев маточного раствора до 80 °С. Из подогревателей газ поступает в сатураторы (Р6) по центральной газоподводящей трубе каждого сатуратора, заканчивающейся барботажным зонтом, типа «паук». Такой барботажный зонт позволяет увеличить линию барботажа, площадь контакта фаз, а следовательно обеспечить более полное связывание аммиака из коксового газа в сульфат аммония. После сатураторов газ проходит ловушку (Х12), где улавливаются капли маточного раствора, унесенные газом. Во время промывки увеличивается брызгоунос раствора, после чего он направляется в бензольное отделение. Маточный раствор из ловушки стекает в циркуляционную кастрюлю (Е2). Кристаллы сульфата аммония по мере их роста оседают в конической части сатураторов, откуда насосом (Н7) подаются в виде пульпы в гидроциклоны (Х13). Осветленный раствор поступает в сатуратор через кастрюлю обратных токов из верхней части гидроциклона. Уровень раствора в сатураторе поддерживается постоянным с помощью бокового переливного штуцера, по которому избыток раствора отводится в циркуляционную кастрюлю. Смолистые вещества, находящиеся в газе в виде смоляного тумана, при взаимодействии с серной кислотой образуют кислую смолку, плавающую на поверхности ванны сатуратора. Вместе с раствором смолка перетекает в циркуляционную кастрюлю (Е2) и далее выводится в сборники маточного раствора (Е3). По мере накопления в сборниках смолка выводится в технологическую машину и вывозится на установку утилизации отходов. Сгущенная пульпа из гидроциклонов (Х13) попадает на центрифуги (Ц15), где происходит отфуговывание кристаллов, а также их промывка горячей водой от остатков серной кислоты. Для снижения слеживаёмости сульфата аммония во время хранения и перевозки влажный сульфат перед сушкой обрабатывается антислёживающими веществами (аммиачная селитра и карбамид), которые поступают из напорного бака. Обработка производится через форсунки на сход сульфата с большого каскада в точки центрифуг. После центрифуг производится сушка влажного сульфата в сушилках кипящего слоя (П11). Три сушилки работают с паровыми подогревателями (Т9) теплоносителя (воздуха). Часть воздуха подается на сушилки подогретым, а другая часть воздуха подается холодной. Воздух подается вентилятором (В5). После сушилок установлены ротоклоны (Х14) в количестве двух единиц. Ротоклоны работают по принципу мокрой очистки. После сушки сульфат складируется навалом (емкость склада 2000 тонн), дозировано загружается в мешки, отгружается в вагоны навалом или в мешках. Для равномерного роста кристаллов сульфата аммония в сатураторе, производится интенсивное и непрерывное перемешивание раствора. Для этой цели в сатураторах применяется ажитация маточного раствора обратным коксовым газом. Коксовый газ, подаваемый на ажитацию подаётся вентилятором (В5). 4. Расчетная часть 4.1 Материальный баланс Исходные данные: Производительность – 2т/ч = 2000 кг/ч; Степень превращения аммиака 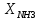 =0,90; =0,90;Таблица 2 Состав газовой смеси
Решение. Реакция протекает по уравнению 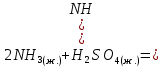 Реакция идет с изменением объема в системе. Схема материальных потоков: Контактный аппарат   NH3 NH3 (ост.) NH3 NH3 (ост.) H2SO4 H2SO4 (ост.)   (NH4)2SO4 (кр.)  Уравнение материального баланса 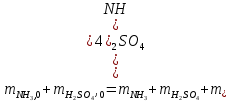 Определяем коэффициент изменения объема: 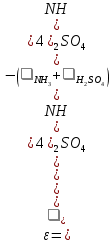 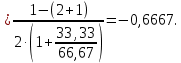 Находим начальный и конечный объем: 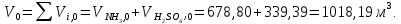 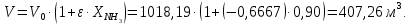 Определяем конечную концентрацию аммиака с учетом степени превращения и коэффициента изменения объема: 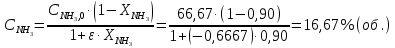 Находим объем аммиака на выходе из контактного аппарата: 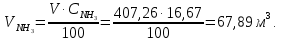 Вычисляем массу аммиака на входе в контактный аппарат и на выходе из него: 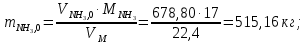 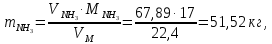 где 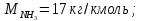 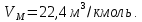 Определяем конечную концентрацию серной кислоты (H2SO4 ) с учетом степени превращения и коэффициента изменения объема: 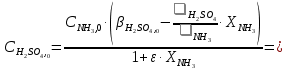 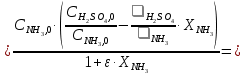 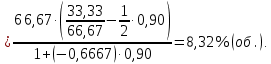 Находим объем серной кислоты на выходе из контактного аппарата: 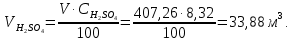 Вычисляем массу серной кислоты на входе в контактный аппарат и на выходе из него: 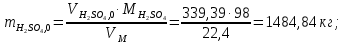 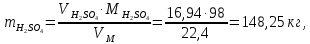 где 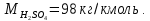 Определяем концентрацию целевого продукта – сульфата аммония: 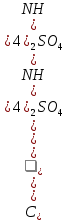 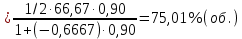 Находим объем и массу образовавшегося сульфата аммония: 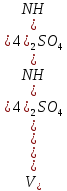 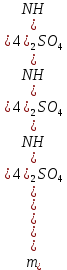 где 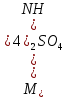 Все полученные данные сводим в таблицу материального баланса (табл. 3). Таблица 3
Таким образом, ∑m, прихода=∑m, расхода. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

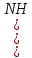 (кр.)
(кр.)