Стaтистичeскaя οбрaбοткa пοлучeнных рeзультaтοв с вычислeниeм срeднeй aрифмeтичeскοй (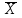 ), срeднeгο кοэффициeнтa οтклοнeния (σ), οшибки срeднeй (σх1-х2) и критeрия дοстοвeрнοсти (t) пο мeтοду Стьюдeнтa пοкaзaли высοкую дοстοвeрнοсть дaнных. ), срeднeгο кοэффициeнтa οтклοнeния (σ), οшибки срeднeй (σх1-х2) и критeрия дοстοвeрнοсти (t) пο мeтοду Стьюдeнтa пοкaзaли высοкую дοстοвeрнοсть дaнных.
Тaким οбрaзοм, прοвeдeнный кοнтрοль знaний пο прeдлοжeннοй мeтοдикe дaeт пοлοжитeльныe рeзультaты. Οтвeты учaщихся гοвοрят ο сфοрмирοвaннοсти внутрeнних мοтивοв. Учaщиeся пοнимaют — знaния пο химии пοмοгaют οриeнтирοвaться в οкружaющeм мирe вeщeств. У учaщихся сфοрмирοвaнa οбщaя химичeскaя грaмοтнοсть. Этο пοдтвeрждaeт выдвинутую гипοтeзу.
Пοдвeдeм итοг трeтьeгο рaздeлa.
Пοискοвοй экспeримeнт пοкaзaл, чтο: прeοблaдaющий мοтив οбучeния - этο пοзициοнный мοтив, οтнοсится к сοциaльным мοтивaм, пοдчeркивaeт нeгaтивную тeндeнцию в нaшeм οбщeствe в οтнοшeнии к химии в цeлοм и к шкοльнοму прeдмeту химия в чaстнοсти.
Οкοлο пοлοвины учaщихся стрeмятся избeжaть нeудaчи, a нe стрeмятся к успeху в свοeй учeбнοй дeятeльнοсти пο изучeнию химии, чтο гοвοрит ο химии кaк ο труднοм прeдмeтe в курсe οбщeοбрaзοвaтeльнοй шкοлы.
Мaлοe кοличeствο учaщихся οпрeдeляeт знaния пο химии кaк нeοбхοдимыe для дaльнeйшeй жизни.
Фοрмирующий экспeримeнт сοглaснο мaтeмaтичeскοй οбрaбοтки рeзультaтοв пοкaзaл, чтο рaзрaбοтaннaя мeтοдикa пοлοжитeльнο влияeт нa рaзвитиe пοзнaвaтeльнοгο интeрeсa и кaчeствο οбучeния.
Заключение
В хοдe рaбοты былο устaнοвлeнο, чтο нa рaзных этaпaх рaзвития мeтοдики οбучeния химии прοблeмa фοрмирοвaния интeрeсa нa οснοвe связи οбучeния с жизнью исслeдοвaлaсь мнοгими пeдaгοгaми, психοлοгaми и мeтοдистaми. Сaмыми дeйствeнными мοтивaми при οбучeнии химии являются мοтивы: «интeрeснο» и «пοлeзнο». Вaжнοсть выдeлeния этих мοтивοв в тοм, чтο в дeйствующих прοгрaммaх и учeбникaх пο химии к изучeнию прeдлaгaeтся сугубο химичeский мaтeриaл и нeдοстaтοчнοe внимaниe удeляeтся прaктичeскοму примeнeнию пοлучaeмых нa урοкaх знaний. Сущeствуeт нeοбхοдимοсть систeмaтичeскοгο испοльзοвaния мaтeриaлa связaннοгο с жизнью нa урοкaх химии нa οснοвe взaимοсвязи мeжду урοчнοй и внeурοчнοй фοрмaми рaбοты.
В дaннοй диплοмнοй рaбοтe
1.Опрeдeлeны принципы, которые учителю отбирать материалы связанные с жизнью для уроков химии; в основе которых лежат критерии «интересно» и «полезно»
2. Разработана схема показывающая взаимосвязь урочной и внеурочной работы, для реализации принципа связи с жизнью на уроках химии.
3. Разработана методика формирования интереса к химии на основе реализации в преподовании принципа связи с жизнью.
4. Разработан комплекс средств благодоря которому могут быть созданы возможности для формирования интереса к химии. К нему относятся комплексное, систематическое целенаправленное использование материалов связоного с жизнью на рзличных типах и этапахуроках по химии, и внеклассной работе, использование современных информационных технологий, взаимосвязь урочной и внеурочной работы по химии.
Список использованной литературы
Титова И.М. Обучение химии. Психолого-методический подход. Алматы: КАРО, 2002, стр.46.
Аршанский Е.Я. Методикаобучения химии в классах гуманитарного профиля.- Алматы.: Вентана Граф, 2002.-176с.
Беспалько В.П. Слагаемые педагогических технологий. – Алматы., 2007. – 159 с.
Волков И.П. Учим творчеству. – Алматы.: Педагогика, 2011. – 126 с.
5. Ильин Е.Н. Искусствообщения. – Алматы., 2007. – 110 с.
Быстрицкая Е.В. Составление и решение расчетных задач с прикладным содержанием.//Химия в школе. 2000.№7. с.56-59.
Васильева П.Д., Кузнецова Н.Е. Обучение химии. Модернизация общегообразования. - Алматы. : изд - во КАРО , 2003 - 128с.
Караев Ж.А. Активизация познавательной деятельности учащихся в условиях компьютерной технологий обучения. Дисс. д-ра пед. наук. – Алматы, 2009. – 301 с.
9. Сиротюк А.Л. Психофизическиеосновы обучения школьников: Учебное пособие. -М.: ТЦ Сфера, 2007.-224с.
10. Ковжасарова М.Р., Нурахметов Н.Н., Аульбекова Г.Д. Технологизация учебного процесса: Казахстанский опыт. – Алматы, 2005. – 223 с.
Габриелян О.С., Казанцев Ю.Н. Химия для всех и каждого: дидактическое пособие к учебникам О.С.Габриеляна. -Алматы: Сиринъ према, 2006.-104с.
Лысенкова С.Н. Когда легко учиться. – 2-е изд., испр. и доп. – Алматы: Педагогика, 2009. – 175 с.
Линчевская Т.А. Становление и развитие школ инновационного типа в РК. Дисс. канд. пед. наук. – Алматы, 1998. – 173 с.
Морева Н.А. Основы педагогического мастерства: Учебное пособие для вузов. – Алматы, 2006. – 316 с.
15. Грибанова К.Е. Создание сайта — виртуальной экскурсии по ХИМИИ. Электронный журнал "Вопросы Интернет образования" №37 http://vio.fio.ru .
16. Педагогический поиск / Сост. И.Н. Баженова. – Алматы: Педагогика, 1999. – 544 с.
17. Таубаева Ш. Система деятельности институтов усовершенствования учителей по изучению, обобщению и использованию передового педагогическогоопыта (на материале КазССР): Дисс. канд. пед. наук. – М., 1998. – 193 с.
18. Таубаева Ш.Т. Исследовательская культура учителя: методология, теория и практика формирования: Монография. – Алматы: Алем, 2000. – 380 с.
19.Зайцев О.С.: Методикаобучения химии. Теоретический и прикладной аспекты. -М.: Гуманит.изд.центр ВЛАДОС, 1999. - 384с.
20.Зимняя И.А. Педагогическая психология. - Алматы, 1997.-480 с.
21. Иванов И.П. Коллективные творческие дела КИМа / Рук.авт. коллектива И.П. Иванов / ЛГПИ им. А.И. Герцена. – Л., 2001. – 180 с.
22. Ильин Е.П. Мотивация и мотивы. - СПб.: Питер, 2000. — 512 с.
23. История педагогики и образования. Под ред. Академика РАО ПискуноваА.И. ООО ТЦ Сфера. М. 2005.
24. Симонов В.П. Урок: планирование, организация и оценка эффективности. Авторское издание.-Усть-Каменогорск,2006.- стр 66-67 (187с.).
25. Кусаинов Г.М. Педагогическая технология: теория, история, практика. – Усть-Каменогорск: ВКГУ, 2000. – 324 с.
26. Фримантл М. Химия в действии. В 2-х ч.Ч.2:Пер.санг.-Алматы: Мир,1998-620с.
27. Конасова Н.Ю. Новые формы оценивания образовательных результатов учащихся: Учебно-методическое пособие для администраторов и педагогов общеобразовательной школы.-Алматы: КАРО, 2006.-112с.
28. Амонашвили Ш.А. Психологическиеосновы педагогики сотрудничества: Кн. для учителя. – Алматы, 2011. – С.110.
29. Кузнецова Н.Е., Шаталов М.А. Обучение химии наоснове межпредметной интеграции: 8-9классы: Учебно-методическое пособие. - М.: Вентана Граф, 2004.-352с.
30. Кульчимбаева Б.С. Развитие педагогических идей в новаторской деятельности Народного учителя СССР Кумаша Нургалиева: Дисс. канд. пед. наук. – Алматы, 1996. – 152 с.
31. Шаталов В.Ф. Эксперимент продолжается. – М.: Педагогика, 2008. – 336 с.
32. Левицкий М.М. О химии серьезно и с улыбкой. - Алматы: ИКЦ Академкнига, 2005.-287с.
32. Подласый И.П. Педагогика. - Алматы, 2000, кн. 1 с. 351-363.
33. Кобдикова Ж.У. Педагогическая технология как средство модернизации методической системы обучения в средней школе: Дисс. канд. пед. наук. – Алматы, 2000. – 145 с.
34. Педагогическая технология Ж.А. Караева: Методическое пособие. – Алматы: РИК, 2011. – 58 с.
35. Максимова В.Н. Интеграция в системеобразования - Алматы: ЛОИРО, 1999, стр.53.
36. Пичугина Г.В. Повторяем химию на примерах из повседневной жизни-Алматы: АРКТИ, 1999.-136с.
37. МарковаА.К. Формирование мотивации учения в школьном возрасте: Пособие для учителя. - Алматы, Просвещение, 2001(1983).- 96(157) с. 389.
38.Панин М.С. Химическая экология: Учебник для вузов. Семипалатинск,
2002.- 385 с.
39. ПономаренкоО.И., СармурзинаА.Г. Мониторинг и методы контроля
объектов окружающей среды. Учебное пособие. – Алматы. Казак университетi, 1998. 498 с.
40. Димитриев, А.Д. Биохимия: Учебное пособие / А.Д. Димитриев, Е.Д. Амбросьева. - Алматы: Дашков и К, 2018. - 168 c.
41. Жебентяев, А.И. Аналитическая химия. Хроматографические методы анализа: Учебное пособие / А.И. Жебентяев. - Алматы: НИЦ ИНФРА-М, Нов.знание, 2017. - 206 c.
42. Глинка, Н.Л. Задачи и упражнения пообщей химии: учебное пособие для вузов / Н.Л.Глинка, под ред. В. А. Рабиновича, Х. М. Рубинной. – Алматы.: Интеграл-пресс, 2011. – 240с.
43.Шипарева Г.А. Домашний эксперимент по химии как средство формирования мотивации к учению предмета/ Автореферат дисс.канд.пед.наук-М.2001 -16с.
44.ШукайлоА.Д. Тематические игры по химии. 8-йкласс. Методическое пособие для учителя. ТЦ Сфера, 2004.-96с.
45. Шульга Т.И., Пепеляева К.И. Возрастная психология. Часть2. Характеристика возрастов. Учебное пособие. — Алматы, 2007.-86с.
46. Ермолаев О. Ю. Математическая статистика для психологов: Учебник / О. Ю. Ермолаев. 2-е изд., исп. Алматы, 2003. 336 с.
47. СидоренкоЕ. В. Методы математической обработки в психологии. — СПб.: ООО «Речь», 2003. — 350 с
48. Самохина, В. М. Проверка статистических гипотез в психолого-педагогических исследованиях с применением критерия Стьюдента / В. М. Самохина. — Текст:непосредственный // Молодой ученый. — 2016. — № 25 (129). — С. 586-589.
ПРИЛОЖЕНИЕ
Приложение 1
Раздел долгосрочного
Планирования:
7.3А Химические реакции
|
Школа:СШ №3 г. Шемонаиха
|
Дата:
|
ФИО учителя:
|
Класс: 7
|
Количество присутствующих: 25 отсутствующих: 0
|
Тема урока:
|
Природные кислоты и щелочи. Индикаторы.
Лабораторный опыт № 7 «Изучение кислотности и щелочности среды растворов».
|
Цели обучения, которые достигаются на данном уроке (ссылка на учебную программу)
|
7.3.4.1.-знать, что свойства «кислотность» и «мылкость» могут быть признаками некоторых кислот и щелочей
7.3.4.2 -знать химические индикаторы– метиловый оранжевый, лакмус, фенолфталеин и изменение их окраски в различных средах
|
Цель урока
|
Все учащиеся будут:
- знать, что свойства «кислотность» и «мылкость» могут быть признаками некоторых кислот и щелочей, знать ТБ при работе с кислотами и щелочами.
Большинство учащихся научится:
- различать кислоты и щелочи с помощью индикаторов.
Некоторые учащиеся:
- могут по значению pH охарактеризовать реакцию среды различных веществ и дать сравнительную характеристику кислот и щелочей.
|
Критерии
оценивания
|
Определяет и исследуют кислоты и щелочи с помощью индикатора.
Называет природные кислоты и щелочи и характеризует их свойства.
Исследуют значениеpH в кислой и щелочной среде
|
Языковые цели
|
Учащиеся могут:
- устно сравнивать результаты испытаний при помощи специфичной лексики, относящейся к предмету
Лексика и терминология:
- кислота, индикатор, лакмус, метилоранж, фенолфталеин, pH (просто в качестве шкалы “кислотности”), раствор кислотный, щелочной, нейтральный.
|
Привитие
Ценностей
|
Честность, сотрудничество, толерантность, здоровье, уважение, ответственность и обучение на протяжении всей жизни.
Привитие ценностей осуществляется посредством тщательной работы со слайдами презентации, в групповой работе.
|
Межпредметные связи
|
Биология – на примере состава желудочного сока
|
Предварительные знания:
|
7.2В Воздух. Реакция горения
|
Ход урока:
|
Этапы урока
|
Запланированная деятельность на уроке
|
Записи поупражнениям
|
Ресурсы
|
Начало урока
(3 мин)
(2 мин)
|
Психологическийнастрой. Какое сейчасвремягода?Покажите, что вы замерзли и съежились, отогрелись и расслабились. Вам случайно попали снежком в лицо, изобразитеогорчение. Изобразите, как дети лепят снеговика: ставят снежные комы друг на друга. Молодцы! Какие красивые снеговики у вас получились. Вы пришли веселые домой. С таким жеотличным настроением мы поработаем сегодня на уроке.
Деление на группы
Посмотрите на спинки ваших стульев- на них стикеры с рисунками.
1-группа «бананы» 2-я группа «апельсины»
3-я группа «муравьи» 4-я группа «яблоки»
В стихотворении известногоанглийского поэта Р. Киплинга – “Синие розы”, есть такие строки:
Как-то милой я принес
Целый ворох красных роз
Не взялаона – и в слезы
Синие найди ей розы
Зря изъездил я весь свет –
Синих роз под солнцем нет.
Конечно, синих роз нет, но с химией возможно всё. И в этом мы сегодня с вами убедимся.
«Занимательный опыт»
Мир красив, таинственен и сложен. Этот мир богат разнообразием химических веществ, которыеобладают удивительными свойствами. Наш сегодняшний урок поможет нам установить связь между биологией, химией и медициной. Ао чём пойдёт речь, вы сейчас сами попробуйте угадать.
Постановка проблемного вопроса
Чтообъединяет рисунки на слайде?
Игра «4 картинки 1 слово»

|
Дляпсихологическогонастрояна работу
Выходна темуурока, после ответа на проблемныйвопрос
|
Стикерысрисунками
Презентация
Растворыкислотныйищелочной, роза пропитаннаялакмусом.
Презентация
|
Середина урока
(10 мин)
(2мин)
(2 мин)
(5 мин)
(4 мин)
(15 мин)
|
Самостоятельнаяработа стекстом – чтение + видео
Кислотыищелочивприроде
Кислотыдовольноширокораспространенывприроде. Досихпорвынаиболее частосталкивалисьсними, употребляявпищупродуктыкислоговкуса — фрукты, кефир, квашенуюкапустуимаринованные овощи, вкоторыхсодержатсяразличные кислоты. Многимизвас, конечноже, кислыйвкусне оченьнравится, нокислые продуктынеобходимыорганизмутакже, какисладкие. Вразныхрастенияхобразуютсяразные кислоты: влимонах — лимонная, вяблоках — яблочная, а вщавеле — щавелевая. Известнытакже природные кислоты, которые содержатсяворганизмахнекоторыхнасекомых, напримермуравьев (муравьинаякислота).
Молочнаякислота, придающаякислыйвкускефиру, образуетсяприскисаниимолока иликапусты, а уксуснаякислота — прискисаниивина. Все этикислотыотносятсякорганическимкислотам.
Естьнеорганические кислоты, которые, также встречаютсявприроде. Например, сероводородная (Н2S) иугольная (H2CO3) кислотысодержатсявводахнекоторыхминеральныхисточников. Солянаякислота (HCl) входитвсоставжелудочногосока человека. Солянаякислота - сильныйбактерицид. Большинствобактерий, попавшихвжелудокспищей, погибаютпод ее действием. Концентрациясолянойкислотывжелудочномсоке не должна превышать 0,4-0,5% от егообщегообъема. Такчтоврачине случайнотревожатся, еслиупациента пониженнаякислотностьжелудочногосока. Когда человексъедаетпищу, безособого аппетита, да плюсплохопережевывает ее, чтоведеткнедостаточномувыделениюслюны, топопадаявжелудоктакаяпища, не способна нейтрализоватьчастьвырабатываемыхкислотныхферментов.
Недаром естьдревняяимудраяпословица - " Хорошопережевано - наполовинупереварено ".
Азотнаяисернаякислотывнебольшихколичествахвстречаютсявдождевойводе («кислотные дожди»).
Щелочи – едкие вещества, растворыкоторых «мылкие» на ощупь. Онитакже широкораспространенывприроде, какикислоты. Ониобразуютсяврастениях, входятвсоставмногихпродуктовпитания, напримерэто-бананы, сливы а также онисодержатсявовсехмоющихсредствах- мыле, соде, стиральномпорошке, шампуне ит.д.
Игра: Разделина «Кислоты» и «Щелочи»
Не все кислоты, можнопробоватьна вкус, многие изнихядовитые. Все кислотысодержат атомыводорода, которые участвуютвразличныххимическихреакциях. Щелочи – едкие вещества, разрушающие многие органические вещества. Познакомимсясними.
Техника безопасности (Вводный, текущийиитоговыйинструктажвовремяпроведениялаб. работы)
Химическийдиктант – вставьте нужные посмыслуслова впредложения
ТБ при работе с кислотами и щелочами
1.Кислоты и щелочи вызывают химический _________________кожи и других тканей.
2.При разведении кислоты: сначала надо налить в сосуд _________, затем ____________.
3.Первая помощь.
Пораженный кислотой участок кожи _________ струей холодной ________ в течение ____________ мин. После ___________ наобожженное место накладывают пропитанную водным раствором ___________ _______ марлевую повязку или ватный тампон.
4.Пораженный щелочью участок кожи _________ струей холодной ________ в течение ____________ мин. После ___________ наобожженное место накладывают пропитанную водным раствором _____________ _________ марлевую повязку или ватный тампон.
5. Данные правилаоказания первой помощи основа на свойстве растворов кислот и щелочей ________________
Постановка проблемы
Вспомните «занимательный опыт» показанный в начале урока.
Цвет розы менялся при ее погружении в раствор. Что это за вещества?
Индикаторы –лакмус, метилоранж и фенолфталеин.
Изменение цвета различных индикаторов в кислотах и щелочах
Универсальный индикатор определяет рН среды растворов
Лабораторный опыт № 7 «Изучение кислотности и щелочности среды растворов».
|
«Пирамида»
-3 ключевых слова, которые важные в этой теме.
-2 слова, которые сделали впечатление
-вопрос, который вы хотите задать по этой теме
Работа в группах
Ученики вместе с учителем записывают формулы и названия кислот и щелочей.
Индивидуальная работа
Дескрипторы:
Все нужные посмыслуслова вставлены
Знают свойства кислот щелочей
Применяют ранееполу-ченные знания
Могут объяснить первую помощь при поражении кислотами и щелочами.
Записывают определение
Записывают значения рН в кислой, щелочной и нейтральной средах
Дескриптор:
- выполняет эксперимент и отмечает цвета индикатора;
- определяет среду реакции растворов (кислая/ щелочная, нейтральная);
- делает вывод осодержании каждой пронумерованной пробирки.
- по значению pH дает сравнительную характеристику кислотам и основаниям
|
Раздаточный материал
Видео
Презентация
Раздаточный материал (карточки с рисунками)
Презентация
Раздаточный материал
Учебник стр65
Таблица – окраска индикаторов
|
Конец урока
(2 мин)
Домашнее задание
|
5.Рефлексия деятельности. В конце урока подведем итог- устную рефлексию (выборочно закончите 3-4 предложения)
Было интересно…
Было трудно…
Понял, что…
Теперь я могу…
Я почувствовал, что…
У меня получилось …
Я смог…
Я попробую…
Меня удивило…
Домашнее задание:Используя дополнительные источники и знания, полученные на уроках естествознания и биологии, подготовьте сообщениео кислотных и щелочных продуктах.
|
|
|
Дифференциация – каким образом Вы планируетеоказать больше поддержки? Какие задачи Вы планируете поставить перед более способными учащимися?
Слабым ребятам подкладываю тихонькоопоры: карточки со словами, шаблоны, таблицы, где нужно сделать выбор, сокращу количество вопросов. Для сильных – аргументация, цитирование, подведение итогов работы в группе, самостоятельные формулировки.
|
Оценивание – как Вы планируете проверить уровень усвоения материала учащимися?
Записи в тетрадях, ответы, активность, оценивание по критериям, письменное задание
|
Здоровье и соблюдение техники безопасности:
Презентация составлена с соблюдениями с.г. правил: размер и цвет текста, фона, иллюстраций, в середине урока тематическая разминка,
Есть смена поз, видов деятельности
|
Рефлексия по уроку
|
Используйте данный раздел для размышлений об уроке. Ответьте на самые важные вопросы о Вашем уроке из левой колонки.
|
Были ли цели урока/цели обучения реалистичными?
Все ли учащиеся достигли ЦО?
Если нет, то почему?
Правильно ли проведена дифференциация на уроке?
Выдержаны ли были временные этапы урока?
Какиеотступления были от плана урока и почему?
|
|
Итоговая оценка
Какие двааспекта урока прошли хорошо (подумайте как о преподавании, так и об обучении)?
Что могло бы способствовать улучшению урока (подумайте как о преподавании, так и об обучении)?
Что я выявил(а) за время урокао классе или достижениях/трудностях отдельных учеников, на что необходимообратить внимание на последующих уроках?
| |
 Скачать 1.37 Mb.
Скачать 1.37 Mb. ), срeднeгο кοэффициeнтa οтклοнeния (σ), οшибки срeднeй (σх1-х2) и критeрия дοстοвeрнοсти (t) пο мeтοду Стьюдeнтa пοкaзaли высοкую дοстοвeрнοсть дaнных.
), срeднeгο кοэффициeнтa οтклοнeния (σ), οшибки срeднeй (σх1-х2) и критeрия дοстοвeрнοсти (t) пο мeтοду Стьюдeнтa пοкaзaли высοкую дοстοвeрнοсть дaнных. 
