Тонкослойная хроматография. Реферат по дисциплине Аналитическая химия
 Скачать 140.2 Kb. Скачать 140.2 Kb.
|
|
Липецкий государственный технический университет Металлургический институт Кафедра химии РЕФЕРАТ по дисциплине «Аналитическая химия» «Тонкослойная хроматография» С  тудент Платонова Е.С. тудент Платонова Е.С.Группа – ХТ–п–18–1 Р  уководитель Дергунова Е.С. уководитель Дергунова Е.С.к.х.н., доцент Липецк, 2021 СодержаниеВведение 3 1 Методика тонкослойной хроматографии 4 2 Сорбенты в тонкослойной хроматографии 7 3 Подвижные фазы в тонкослойной хроматографии 10 3.1 Идентификация компонентов 13 3.2 Методы количественной оценки содержания вещества в хроматографических зонах 14 4 Достоинства и недостатки тонкослойной хроматографии 16 5 Применение тонкослойной хроматографии 18 Список использованной литературы 21 Введение Тонкослойная хроматография (ТСХ) является одним из вариантов планарной хроматографии. Планарная хроматография – способ анализа, в котором процессы разделения смеси веществ осуществляются в плоском слое сорбента (неподвижной фазе) [1]. Тонкослойная хроматография занимает одно из ведущих мест в качественном и полуколичественном анализе сложных природных, фармацевтических, медикобиологических и химических объектов. Тонкослойная хроматография может использоваться для отслеживания хода реакции, идентификации соединений, присутствующих в данной смеси, и определения чистоты вещества. Конкретные примеры этих приложений включают: анализ церамидов и жирных кислот, обнаружение пестицидов или инсектицидов в продуктах питания и воде, анализ красителя. состав волокон в судебной медицине, анализ радиофармпрепаратов или идентификация лекарственных растений и их компонентов [2]. Можно внести ряд улучшений к исходному методу для автоматизации различных этапов, увеличения разрешения, достигаемого с помощью ТСХ, и обеспечения более точного количественного анализа. Этот метод упоминается как HPTLC или «высокопроизводительная TLC». В ВЭТСХ обычно используются более тонкие слои неподвижной фазы и меньшие объемы образца, что снижает потерю разрешения из-за диффузии [3]. 1 Методика тонкослойной хроматографии Хроматографический процесс, протекающий при движении подвижной фазы в тонком слое сорбента, нанесенном на инертную твердую подложку (пластинку) из соответствующего материала – стекла, металла или полимера, называется тонкослойной хроматографией или хроматографией в тонком слое сорбента. Тонкослойная хроматография (ТСХ) может использоваться для анализа как однокомпонентных, так и многокомпонентных лекарственных средств. В последнем случае подбираются условия хроматографирования, обеспечивающие разделение компонентов смеси [4]. Разделение может осуществляться по различным механизмам: адсорбционному, распределительному, ионообменному или какой-либо их комбинации. Классическая, наиболее простая и широко используемая методика тонкослойной хроматографии включает проведение следующих основных операций: нанесение анализируемой пробы на слой сорбента; разделение компонентов пробы на отдельные зоны в потоке подвижной фазы; обнаружение зон на слое сорбента (часто реагентом, образующим с разделенными веществами окрашенные соединения); количественная оценка полученного разделения, включая определение величины удерживания и определение содержания вещества в зонах на хроматограмме [5]. Положение зоны вещества на хроматограмме характеризуется величиной Rf, которая равна отношению расстояния от стартовой линии до центра зоны вещества к расстоянию от стартовой линии до линии фронта. Значение Rf – величина постоянная для данного соединения в данной системе и зависит от ряда условий: способа элюирования, качества и активности сорбента, толщины слоя, качества растворителей, количества нанесенного вещества, длины пробега растворителей, положения стартовой линии и почти не зависит от температуры. По этой величине проводят идентификацию компонентов в смеси. На качество разделения компонентов смеси в планарной хроматографии влияет большое число факторов: тип разделительной камеры; предварительное насыщение камеры и слоя сорбента парами подвижной фазы; стартовый размер пятна; расстояние от старта до нижнего края пластинки; относительная влажность воздуха лабораторного помещения; средний диаметр частиц и их форма; толщина и равномерность нанесения слоя сорбента; наличие микроповреждений слоя; тип вещества, связывающего сорбент; скорость элюирования; объем растворителя в камере; наличие примесей в элюенте; конвекция в газовой фазе внутри камеры. Для разделения смесей веществ в тонком слое сорбента применяют адсорбционную, распределительную и ионообменную хроматографию, отличающиеся, прежде всего характером взаимодействий между растворенными веществами и твердой или жидкой фазами, с которыми они соприкасаются. На практике эти взаимодействия почти никогда не протекают изолированно, и разделение веществ обусловлено несколькими взаимодействиями. При выборе подходящего варианта хроматографии в первую очередь следует обратить внимание на строение разделяемых веществ. При помощи адсорбционной и распределительной хроматографии разделяются вещества, строение которых различается природой, числом и характером полярных и неполярных заместителей. При хроматографировании в тонком слое сорбента чаще всего применяют адсорбционную хроматографию, которая проще по выполнению, более эффективна, а результаты анализа более воспроизводимы [6]. 2 Сорбенты в тонкослойной хроматографии В качестве сорбентов в ТСХ применяют материалы, которые отвечают следующим требованиям: образуют химически и физически стабильные слои; не образуют ковалентных связей с разделяемыми веществами; не растворяются в подвижной фазе или перемещаются вместе с ней по пластинке; не содержат компонентов, мешающих разделению или детектированию; не имеют собственной окраски; не набухают и не сжимаются под действием подвижной фазы. В качестве подложки для сорбента используется стекло, алюминевая фольга, полимерные пленки (полиэтилентерефталат). Для приданаия стабильности слоя сорбента на подложке используются различные связующие вещества: гипс (5–10%), силиказоль, силикаты щелочных металлов, полиакриламид, полиакриловый эфир, крахмал. К адсорбенту часто добавляют флуоресцентный индикатор для детектирования веществ, поглощающих в УФ – области спектра. С этой целью используют: смесь силикатов цинка и магния; смесь сульфидов цинка и кадмия; вольфраматы щелочноземельных элементов. Большое значение, особенно для эффективности разделения, имеют такие характеристики сорбентов, как диаметр частиц, среднее распределение частиц по размерам и размер пор. В классической тонкослойной хроматографии для производства пластинок используются частицы с размером 5 – 20 мкм. Для высокоэффективной тонкослойной хроматографии (ВЭТСХ) необходим сорбент, диаметр частиц которого составляет 5 – 7 мкм. Сравнение характеристик пластинок для ТСХ и ВЭТСХ приведено в таблице 1. Монолитные сорбенты представляют собой новое поколение стационарных фаз, которые могут быть использованы и в планарной хроматографии. Их получают прямой сополимеризацией метакриловых полимеров, например, сополимера глицинметакрилата и этилендиметакрилата. Монолитные стационарные фазы не содержат частиц, а роль разделительного пространства выполняют поверхность и объем проточных каналов (пор). Макропористая структура монолитных сорбентов содержит как минимум два вида пор: макро– и мезо–поры. Преимущества таких носителей заключаются в заметном повышении скорости и эффективности разделения, так как для них отсутствуют обычные диффузионные ограничения межфазного массообмена [7]. Таблица 1 – Сравнение характеристик пластинок для классической (ТСХ) и высокоэффективной (ВЭТСХ) тонкослойной хроматографии
Основные типы сорбентов, используемых в ТСХ, описаны ниже. Силикагель – полярный адсорбент, содержит активные силанольные и силоксановые группы, его применяют для разделения соединений различной полярности. Оксид алюминия – полярный адсорбент с гетерогенной поверхностью, содержит активные ОН-группы, обладает заметно выраженными протоноакцепторными свойствами. Его применяют для разделения ароматических углеводородов, алкалоидов, хлоруглеводородов, стероидов. Флоросил – основной силикат магния, занимает промежуточное положение между оксидом алюминия и силикагелем. Удобен для разделения флаваноидов, стероидов и ацетилированных углеводородов. Полиамиды – группа полярных сорбентов со смешанным механизмом разделения: карбоксамидная группа ответственна за адсорбционный механизм, метиленовые звенья – за распределительный механизм. Эти сорбенты применяют для разделения пищевых красителей, флаваноидов, танинов, нитрофенолов, спиртов, кислот. Модифицированные силикагели с привитыми группами (амино, циано, диол–, С2–,С8–, С18–), отличными по полярности [8]. Важной характеристикой сорбента является его активность, она зависит от содержания воды и понижается при увеличении содержания воды в сорбенте. Для успешного разделения смесей веществ большое значение имеет выбор сорбента. В первую очередь нужно исходить из свойств разделяемых соединений: их растворимости (гидрофильности, гидрофобности), содержания и характера функциональных групп. Насыщенные углеводороды адсорбируются слабо или совсем не адсорбируются на силикагелях и оксиде алюминия. Введение двойных связей, особенно сопряженных, увеличивает адсорбционную способность соединений. Функциональные группы в еще большей степени усиливают способность веществ к адсорбции [9]. 3 Подвижные фазы в тонкослойной хроматографии Растворители, применяемые в тонкослойной хроматографии, должны быть чистыми и осушенными. Смеси веществ могут разделяться с помощью одного растворителя, однако обычно применяют системы, состоящие из двух, трех и даже четырех растворителей. Выбор растворителей определяется их элюирующей способностью, которая зависит от полярности растворителя, а также его протонодонорных и протоноакцепторных свойств. Характеристика элюирующей способности наиболее важных для ТСХ растворителей приведена в таблице 2 и 3. Для каждой новой пластинки систему растворителей следует готовить заново, так как в ней соотношение компонентов после хроматографирования изменяется. Таблица 2 – Значения силы растворителя для неполярных неподвижных фаз
Существенную роль при разделении веществ с помощью тонкослойной хроматографии играет количество наносимой смеси, оно влияет и на величину Rf и на разрешение пятен. Пробы испытуемых веществ массой от 0,1 до 50 мкг, наносят на пластинку в виде растворов в эфире, хлороформе или другом летучем растворителе [10]. Природа растворителя может влиять на размер пятна наносимой пробы. При нанесении пробы необходимо, чтобы: растворитель легко удалялся со стартовой зоны, и растворимость анализируемых веществ была бы не менее 0,01 г/мл. Таблица 3 – Значения силы растворителя Si для полярных неподвижных фаз
Пробы наносят в виде точки или полоски длиной 5–7 мм при помощи капилляра, пипетки на 0,1 мл или микрошприца, предварительно отметив стартовую линию на расстоянии 1,5 см от края пластинки. Расстояние между отдельными пробами должно быть не менее 1 см. После этого ждут, когда растворитель испарится, затем пластинку опускают в разделительную камеру с выбранной подвижной фазой. В зависимости от того, в каком направлении поступает растворитель на пластинку, различают методы восходящей, нисходящей и горизонтальной хроматографии. На рисунке 1 показаны различные методы элюирования в планарной хроматографии. Применение многоступенчатого и двумерного элюирования позволяет повысить селективность разделения за счет изменения элюирующей способности подвижной фазы [11]. 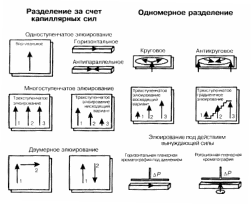 Рисунок 1 – Варианты элюирования компонентов в тонкослойной хроматографии Однако во всех указанных способах не удается исправить существенный недостаток ТСХ – низкую эффективность разделения, поскольку движение элюента осуществляется за счет капиллярных сил. Вариант планарной хроматографии с принудительным движением элюента (под давлением) позволяет существенно улучшить эффективность разделения. Это наглядно подтверждает пример разделения лекарственных веществ на адсорбенте – силикагель 60 при элюировании смесью н–бутанол– хлороформ–метилэтилкетон–уксусная кислота (25 : 17 : 8 : 6), показанный на рисунке 2 [12]. 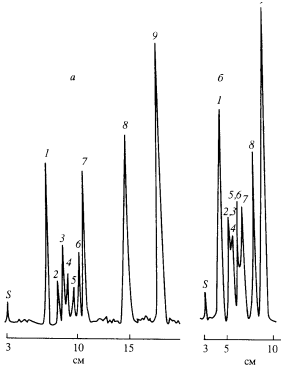 1 – стрихнин; 2 – эфедрин; 3 – метамфетамин; 4 – фенметразин; 5 – метилфенидат; 6 – амфетамин; 7 – дезопинон; 8 – корамин; 9 – кофеин; S – старт.,а – под давлением, б – при использовании обычной тонкослойной хроматографии Рисунок 2 – Хроматограмма смеси 3.1 Идентификация компонентов После разделения веществ необходимо обнаружить их на хроматограмме. Для обнаружения бесцветных веществ, в первую очередь, следует воспользоваться физическими методами, основанными на поглощении света и флуоресценции. Для обнаружения веществ, поглощающих в УФ-области 120 спектра, часто применяют пластинки со слоем сорбента, содержащим флуоресцирующее вещество или опрыскивают хроматограмму после разделения смеси раствором флуоресцирующего вещества. При облучении пластинки УФ–излучением вещества, поглощающие в этой области спектра, обнаруживаются в виде темных зон (пятен). Флуоресцировать в УФ–свете способно значительное количество веществ, полученные пятна имеют при этом различный оттенок. Для обнаружения флуоресцирующих веществ или веществ, поглощающих в УФ–области спектра, используют источники света с максимумами излучения в области 254 и 365 мкм. Помимо оптических методов обнаружения веществ, применяют химические методы проявления хроматограмм. К химическим методам относится использование «универсальных реагентов» и реагентов, избирательно реагирующих с определенными функциональными группами определяемых соединений [13]. 3.2 Методы количественной оценки содержания вещества в хроматографических зонах [14] Для количественной оценки содержания вещества в хроматографических зонах используют различные методы: 1. Определение с удалением хроматографической зоны с пластинки можно проводить двояким образом: переносом хроматографической зоны вместе с сорбентом либо экстрагированием хроматографической зоны со слоя сорбента. 2. Определение соединений непосредственно на пластинке методом визуального сравнения размеров площадей пятен и их окраски с соответствующими параметрами пятен стандартных образцов 3. Метод денситометрии, повышающий точность результатов определения, основан на сканировании хроматограмм в видимом и УФсвете с помощью «хроматографических спектрофотометров» – денситометров. Денситометры позволяют измерять поглощение света веществом на хроматограмме в режиме пропускания или отражения, а также флуоресценцию и ее тушение. Режим пропускания доступен, если только исследуемое вещество имеет полосу поглощения в видимой области спектра. В УФ–области регистрацию в режиме пропускания осуществить нельзя из–за собственного поглощения силикагеля и подложки хроматограммы. 4. Метод видеоденситометрии – сравнительно новый метод для количественной обработки хроматограмм. Принцип метода заключается во введении изображения хроматограммы в компьютер с помощью видеокамеры или цифровой камеры с последующим сравнением интенсивностей пятен стандартных и определяемых соединений. 5. Денситометрия с планшетным сканером с программным обеспечением для обработки хроматограмм практически не отличающимся от стандартных программ, применяемых для видеоденситометров, но существенно меньшей стоимости. При этом сканирование дает более четкое изображение хроматографических зон, что можно объяснить пониженным влиянием неравномерности освещения анализируемых объектов, чем в случае видеоденситометра. 4 Достоинства и недостатки тонкослойной хроматографии Среди других хроматографических методов ТХ отличают следующие достоинства и особенности: – это единственный хроматографический метод, позволяющий проводить полный анализ неизвестной смеси, поскольку исследователь имеет возможность проверить, не остались ли на старте неэлюированные компоненты; – по производительности превосходит газовую и высокоэффективную жидкостную хроматографию, по крайней мере, на порядок; использует более простое и дешевое оборудование; – обладает высокой селективностью, которую легко варьировать, подбирая состав подвижной фазы; в отличие от ВЭЖХ нет ограничений в выборе растворителей; – дает возможность одновременного разделения нескольких образцов; использования однократного или многократного элюирования (при различных условиях), а также одновременного разделения компонентов одного и того же образца с помощью различных элюентов; – возможна оптимизация разрешающей способности хроматографической системы при разделении сложной смеси только для интересующих компонентов, что позволяет экономить время; – возможно детектирование соединений с высокой чувствительностью и селективностью, которые легко варьировать подбором проявляющего реагента; полученные результаты разделения легко оценить визуально; – можно сохранять хроматограммы для последующего детектирования и осуществлять спектральную идентификацию хроматографических зон после разделения в любом диапазоне длин волн, включая ИК [15]. У ТХ есть и некоторые недостатки: – ограниченная разделяющая способность из-за сравнительно небольшой длины разделяющей зоны (3–10 см); – чувствительность ниже, чем в случае ВЭЖХ; – зависимость результатов анализа от окружающей среды: относительной влажности, температуры, а также наличия загрязняющих веществ в воздухе; – трудности в работе с образцами, имеющими высокую летучесть, а также с веществами, чувствительными к действию кислорода воздуха или света [16]. 5 Применение тонкослойной хроматографии Применение ТСХ особенно эффективно для предварительного разделения (по классам, группам, видам веществ) компонентов сложных смесей органических загрязнителей воды, почвы и воздуха. Индивидуальная идентификация с помощью одной лишь ТСХ затруднена из–за отсутствия выокочувствительных и селективных детекторов, кроме того, определение целевых компонентов менее точно, чем в случае ГХ и ВЭЖХ. Часто ТСХ применяют на первом этапе анализа для разделения сложных и многокомпонентных смесей органических соединений на отдельные более простые группы, и уж потом проводят более детальное исследование этих групп «более тонкими» методами (ГХ, ВЭЖХ, ЯМР, ИК или масс–спектрометрией) [17]. Использование ТСХ при анализе загрязненной пресной и морской воды открывает широкие возможности для препаративного разделения, предшествующего другим методам, разделения искомых примесей и дополнительной идентификации. ТСХ используют для обнаружения и полуколичественного определения веществ разной природы: поверхностно-активных веществ, углеводородов, ПАУ, фенолов, пестицидов [18]. Для определения неионных ПАВ в сточных и речных водах используют пластинки со слоем силикагеля или Кизельгеля G. На пластинку наносят хлороформенный экстракт ПАВ и разделяют их при использовании в качестве подвижной фазы смесей этилацетат : вода : уксусная кислота. Обнаруживают пятна при опрыскивании смесью: реактив Бургера : фосфорная кислота : этанол : 5% раствор BaCl2*2H2O (10:1:10:5). ПАВ проявляют в виде розовых пятен. Метод позволяет определить в воде от 0,1 до 1,0 мг/л неионогенных ПАВ. Из сточных вод в этих условиях экстрагируются ионные ПАВ, но они движутся вместе с фронтом растворителя и не проявляются [19]. Предложено много методик определения фенолов. Хлорфенолы разделяют на пластинках с оксидом алюминия при многократном элюировании бензолом или на силикагелевых пластинках при элюировании смесью бензола и петролейного эфира (1:1). Определяют фенолы проявлением 2% раствором 4–аминоантипирина (предел 125 обнаружения 0,5 мкг/л) или по флуоресценции при 254 нм (до 0,5 мкг фенолов). Второй вариант определения фенолов – разделение в виде: антипириновых, 4–аминоантипириновых производных или с п–нитрофенилазокрасителями. Часто ТСХ определяют в водах пестициды: хлорфеноксиуксусные кислоты, хлорсодержащие пестициды, триазиновые гербициды, гербициды на основе мочевины, карбаматы и фенилмочевины и фосфорорганические пестициды. Условия определения пестицидов в водах представлены на рисунке 3 [20]. 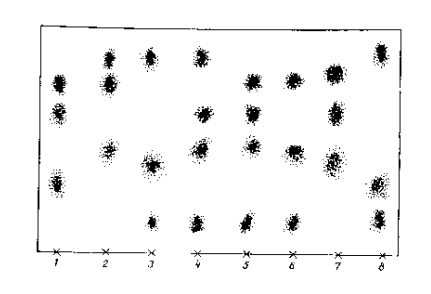 1 – прометон, атразин, промазин; 2 – симетрин, пропазин, прометрин; 3 – атратон, симазин, прометрин; 4 – атратон, десметрин, атразин, прометрин; 5 – атратон, симетрин, атразин, промазин; 6 – атратон, десметрин, промазин; 7 – симазин, атразин, промазин; 8 – атратон, прометон, прометрин Рисунок 3 – Хроматограмма разделения гербицидов (зоны сверху вниз) ТСХ является недорогим и эффективным методом разделения, идентификации и полуколичественного определения пестицидов в почвах. В органических почвенных вытяжках определяют также ПАУ, разделяя их на силикагеле или целлюлозе, идентификацию проводят флуоресцентным методом [21]. Для определения загрязнителей в воздухе его предварительно аспирируют через различные фильтры, уловленные вещества экстрагируют подходящим растворителем, и полученный экстракт анализируют ТСХ [22]. ТСХ позволяет определять в воздухе ароматические углеводороды, ароматические карбонильные соединения, ароматические амины и имины, фенолы, металлорганические соединения, сложные эфиры фталевой кислоты. Сканирование хроматограмм с использованием спектроскопических методов, особенно флуоресценции, позволяет идентифицировать весь спектр токсичных соединений [23]. Таким образом, примеры использования ТСХ для определения токсичных соединений в различных водах, почвах и воздухе подчеркивают важность этого метода для экологического контроля, особенно, с учетом современного аппаратурного оформления метода [24]. Список использованной литературы Хроматография в тонком слое сорбента [Электронный ресурс]. –URL: https://pharmacopoeia.ru/ofs-1-2-1-2-0003-15-tonkoslojnaya-hromat(дата обращения: 10.04.2021) Основы аналитической химии. В 2 кн. Ю.А. Золотов, Е.Н. Дорохова, В.И. Фадеева и др.; Под ред. Ю.А. Золотова. –М.: Высш. шк., 1996. Алесковский В.Б., Бардин В.В., Булатов М.И. Физико–химические методы анализа. Практическое руководство. – Л.: Химия, 1988. Валиахметов Д.Р. Хроматографический метод анализа / Д.Р. Валиахметов, Т. Ф. Дехтярь // Наука и инновации в современных условиях : сб. ст. междунар. науч. –практ. конф. – Казань, 2017. - 17-19 с. Ф. Гейсс, Основы тонкослойной хроматографии. Москва, Т. I и II, 1999, 405 и 348 с. Высокоэффективная тонкослойная хроматография (под. ред. А. Златкиса и Р. Кайзера), М.: Мир, 1979, 265 с. Б. Дамаскин, О. Петрий. Введение в электрохимическую кинетику. М.: «Высшая школа 1983 г. Ю. Кирхнер. Тонкослойная хроматография, т.1. М.: «Мир», 1981, 523 с.бб.Э.Шталь. Хроматография в тонких слоях. М.: «Мир», 1965, 508 с. Сумина Е.Г., Штыков С.Н., Тюрина Н.В. Тонкослойная хроматография. Теоретические основы и практическое применение. Саратов: Изд-во Саратовского университета, 2002. 106 с. Березкин В.Г., Бочков А.С. Количественная тонкослойная хроматография. М.: Наука, 1980. 184 с. Кибардин С.А., Макаров К.А. Тонкослойная хроматография в органической химии.М.: Химия, 1978. 126 с. Волынец М.П. Тонкослойная хроматография в неорганическом анализе. М.: Наука, 1974, 152 с. Кирхнер Ю. Тонкослойная хроматография. М.: Мир, 1981, т.2, –494 с. Дорохова Е.Н., Прохорова Г.В. Аналитическая химия. Физико-химические методы анализа. – М.: Высшая школа, 1991. – 256 с. Тонкослойная хроматография (ТСХ) [Электронный ресурс]. –URL: http://orgchemlab.com/chromatography/thin-layer-chromatography.html (дата обращения: 10.04.2021) Современная тонкослойная хроматография [Электронный ресурс]. –URL: http://elibrary.sgu.ru/uch_lit/590.pdf (дата обращения: 10.04.2021) А. А. Ахрем, А. И. Кузнецова, “Тонкослойная хроматография”, –М: Наука, 1964. – 175 с. Хроматография в тонких слоях. /Под ред. Э. Шталя – М: Мир, 1965. – 508 с. Тонкослойная хроматография в современном виде [Электронный ресурс]. –URL: https://wikichi.ru/wiki/Thin-layer_chromatography (дата обращения: 10.04.2021) Экспресс метод анализа химических соединений [Электронный ресурс]. –URL: https://petrolaser.ru/literature/tsh_ecpress-analiz-him-soed/(дата обращения: 10.04.2021) Справочник по аналитической химии по ТСХ [Электронный ресурс]. –URL: https://dic.academic.ru/dic.nsf/enc_chemistry/4573/ (дата обращения: 10.04.2021) Информация их википедии по ТСХ и ВЭСХ [Электронный ресурс]. –URL: https://ru.wikipedia.org/wiki/ (дата обращения: 10.04.2021) Тонкослойная хроматография – Студопедия [Электронный ресурс]. –URL: https://studopedia.ru/2_119831_tonkosloynaya-hromatografiya.html (дата обращения: 10.04.2021) Методические указания для лабораторных [Электронный ресурс]. –URL: http://window.edu.ru/resource/458/64458/files/0052.pdf (дата обращения: 10.04.2021) |
