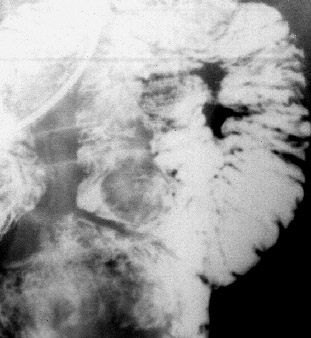
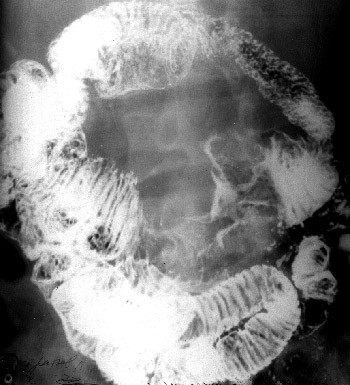
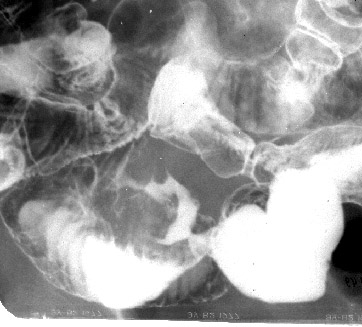
Лучевая диагноститка заболеваний кишечника. Реферат по теме Лучевая диагностика опухолей кишечника
 Скачать 0.84 Mb. Скачать 0.84 Mb.
|
|
Московский Государственный Медико-Стоматологический Университет Стоматологический факультет, дневное отделение Кафедра лучевой диагностики Заведующий кафедрой: д.м.н., профессор Васильев А.Ю. Преподаватель: к.м.н., доцент Лежнев Д.А. Реферат по теме: «Лучевая диагностика опухолей кишечника» Работу выполнил Мартынов Дмитрий Викторович Москва, 2007 год Опухоли кишечникаД 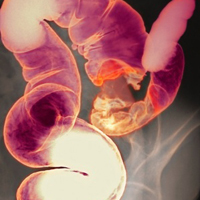 иагностика опухолей кишечника является одновременно трудной и необходимой. Часто опухоли дают синдром интоксикации, диарейный синдром, анемический, то есть дают сходную симптоматику с другими заболеваниями. Опухоли тонкой кишки встречаются довольно редко, в основном доброкачественные (аденома, липома, шванома и др.). В 50% всех опухолей составляет рак тонкой кишки и саркомы. Злокачественные опухоли двенадцатиперстной кишки встречаются еще реже. К ним относятся опухоли Фатерова соска, карциноиды. Кроме того, встречаются рак, саркомы. Нередко встречается лимфогранулематоз тонкой кишки, который часто приходится дифференцировать с раком. Опухоли толстой кишки обычно злокачественные- это чаще рак и саркомы. Доброкачественные опухоли как правило полипы - по типу цветной капусты, нашлепки и др. Чаще доброкачественные опухоли - фибромы, липомы, гемангиомы, лейомиом. Опухоли прямой кишки чаще встречаются чаще после 40 лет. Рак прямой кишки имеет довольно широкое распространение. Является ведущим злокачественным поражением кишки. К предраковым заболеваниям относят анальные лейкоплакии, полипы. Диагностика - эндоскопическая, инструментальная, включая конечно биопсию, для того чтобы доказать наличие опухоли гистологически. Рак толстого кишечника - это опухоль, которая не поддается лучевой терапии, поэтому лечение только оперативное. Рак толстой и прямой кишок имеет много общих черт, поэтому его объединяют общим названием "колоректальный рак". Рак может возникнуть в любом отделе толстой кишки или в прямой кишке. Опухоли во всех указанных отделах толстой кишки могут вызывать различные симптомы. Одни методы обследования позволяют лучше выявлять рак правой половины толстой кишки, другие - левой половины или прямой кишки. Колоректальный рак развивается медленно, в течение нескольких лет. В настоящее время известно, что большинство этих опухолей начинается с полипа, известного под названием аденома. В течение многих лет (обычно 5-10) такие полипы постепенно перерождаются в рак. Полип представляет собой кусочек ткани, растущей в просвет кишки. Некоторые виды полипов, например, воспалительные полипы, не являются предопухолевыми заболеваниями. Однако наличие аденоматозных полипов увеличивает риск развития рака, особенно, если полипов много и они больших размеров. Как только из полипов формируется рак, он продолжает расти в просвет толстой или прямой кишок. Затем по кровеносным или лимфатическим сосудам опухолевые клетки могут распространяться по всему организму, образуя метастазы опухоли. По данным Всемирной Организации Здравоохранения в мире ежегодно регистрируется более 500 тыс. случаев колоректального рака. Наибольшая заболеваемость отмечается в США, Канаде, странах Западной Европы и России. Менее выражен рост заболеваемости в странах Азии и Африки На сегодняшний день статистические данные свидетельствуют о том, что в России колоректальный рак занимает одну из ведущих позиций. За последние 20 лет рак толстой кишки переместился в структуре онкологической заболеваемости населения Российской Федерации с 6-го на 3-е место. В России среди заболевших злокачественными новообразованиями мужчин колоректальный рак составляет 8.7%, прочно занимая 3-е место после рака легкого (26.5%) и желудка (14.2%). Среди заболевших женщин соответственно 11.1% вслед за раком молочной железы (18.3%) и кожи (13.7%). Более того, все чаще отмечается, что заболеваемость этой формой рака выходит на второе место после рака легких у мужчин и после рака молочной железы у женщин. Мужчины заболевают раком прямой кишки в 1.5 раза чаще, чем женщины. Наибольший удельный вес рака обеих локализаций отмечено в возрасте старше 60 лет у мужчин (6.4% и 5.8%) и женщин (9.8% и 7.0%). В структуре смертности от злокачественных новообразований на долю рака ободочной кишки приходится 4.3% у мужчин и 7.9% у женщин, прямой кишки — 4.2% и 6.1% соответственно. 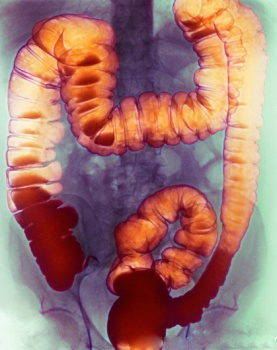 Тревожным является тот факт, что на 100 новых больных раком ободочной и прямой кишки приходится более 70 умерших, из них на 1-м году с момента установления диагноза около 40%. Данное обстоятельство обусловлено тем, что при первичном обращении пациентов к врачу запущенные формы рака (III-IV стадии) диагностируются у 71,4% больных раком ободочной кишки и у 62,4% в случаях заболевания раком прямой кишки Приведенные статистические данные свидетельствуют о том, что в России колоректальный рак является чрезвычайно насущной проблемой и требует своевременной диагностики. Комплексное обследование больных позволяет уточнить степень распространения опухоли, избрать оптимальный метод лечения, определить объем операции и оценить прогноз. ДиагностикаПри подозрении на рак толстой или тонкой кишок после осмотра назначаются специальные исследования, которые позволят подтвердить или исключить это заболевания, а в случае подтверждения рака, уточнить стадию (степень распространения) заболевания. Может быть назначен один или несколько методов диагностики в зависимости от того, насколько подозрительны симптомы в отношении колоректального рака. Наиболее старыми и распространенными являются рентгенологические методы исследования ЖКТ. Сюда относятся рентгеноскопия и рентгенография, томография, экскреторные методы, т. е. введение контрастов и рентгенологическое наблюдение за выведением этих контрастов, и, наконец, ангиография. В качестве контрастного вещества вводится барий, различный по консистенции (густой или жидкий) в зависимости от того, как плотно мы хотим наполнить обследуемый орган. Безконтрастное исследование делается в двух случаях: если надо определить инородное тело или в случае кишечной непроходимости. При кишечной непроходимости на обзорной рентгенограмме мы видим уровни жидкости в кишечнике Основные методы искусственного контрастирования органов и систем
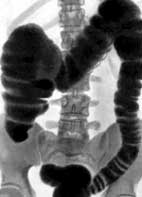
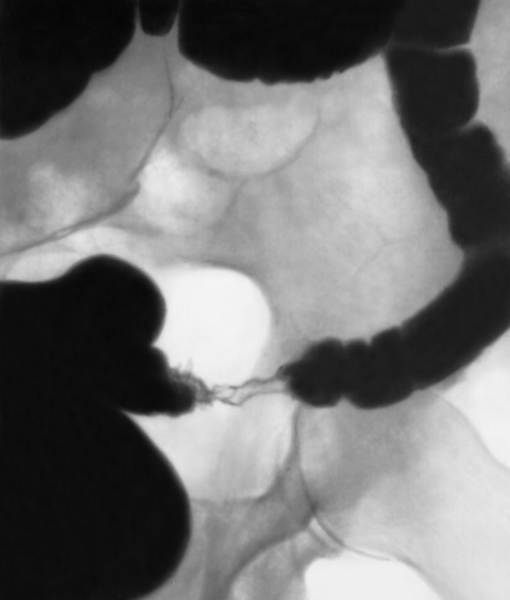
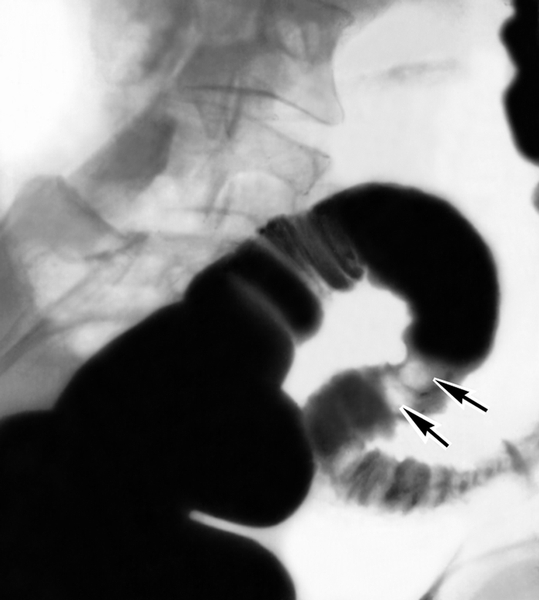
ИрригоскопияПозволяет получить информацию о локализации новообразования, оценить протяженность опухоли по длиннику, форму роста выявить крупные полипы, дивертикулы, в известной степени судить о прорастании в окружающие ткани. При выполнении ирригоскопии возможно также выявить синхронные опухоли толстой кишки. Последнее обстоятельство является важным еще и потому, что при стенозирующем характере роста новообразования эндоскопическое исследование не позволяет до операции оценить состояние вышележащих отделов толстой кишки. Рентгенологическая картина рака опухолей кишечника разнообразна и диагноз можно установить только на основании нескольких рентгенологических признаков при соблюдении правильной методики исследования. Например, в случае рака прямой кишки к ним относят: дефект наполнения, ригидность, нечеткость и неровность контуров стенки кишки, сужение просвета, тень внутрипросветного образования, стойкое депо бариевой взвеси, деформацию кишки, локальные изменения рельефа слизистой оболочки. О прорастании рака прямой кишки в окружающие ткани можно предположить при выявлении отчетливого увеличения пресакрального пространства, если оно сочетается с оттеснением кишки в области опухоли. 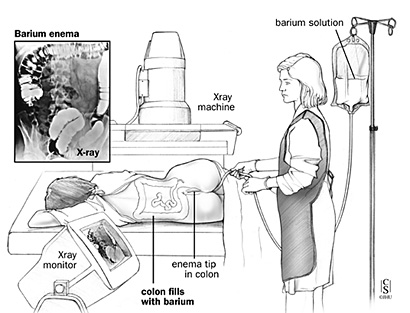 Ирригоскопия — рентгенологическое исследование толстой кишки при ретроградном заполнении ее рентгеноконтрастной взвесью. Противопоказания Ирригоскопия противопоказана при тяжелом состоянии больного и при перфорации стенки толстой кишки. Подготовка к ирригоскопии За 2—3 дня до исследования больному назначают бесшлаковую диету, 1 сут. — 30 г касторового масла внутрь. Вечером накануне ирригоскопии делают 1—2 очистительные клизмы. Ужин не разрешается. Утром в день исследования допускается легкий завтрак и вновь делают 1—2 очистительные клизмы. В качестве рентгеноконтрастного вещества используют водную взвесь сульфата бария из расчета 400 г сухого порошка на 1600—2000 мл воды с добавлением не более 2 г танина. Рентгеноконтрастную взвесь подогревают до 33—35° и вводят в толстую кишку с помощью аппарата Боброва через резиновую трубку без жесткого наконечника. Безшлаковая диета в течении суток. Рекомендуется: белый хлеб, отварное мясо, рыбу, сливочное масло, сыр, макаронные изделия. Следует исключить: молочные продукты (молоко, кефир, простокваша,) ,овощи, (горох, фасоль, капуста, картофель, яблоки) , черный хлеб , острые приправы , кофе, шоколад. В день исследования рекомендуется легкий завтрак: 1 стакан чая, бутерброд с белым хлебом, сыр. Техника выполнения Под рентгенологическим контролем постепенно заполняют рентгеноконтрастной взвесью толстую кишку и производят обзорные и прицельные снимки всех ее отделов в разных положениях больного. На следующем этапе, после удаления из толстой кишки рентгеноконтрастной взвеси, исследуют рельеф слизистой оболочки кишки.
На заключительном этапе ирригоскопии, особенно при подозрении на опухоль толстой кишки, исследование проводят при дозированном заполнении кишки воздухом, используя аппарат Боброва (двойное контрастирование). Осложнения Ирригоскопия не вызывает серьезных осложнений. При перерастяжении кишки и передозировке танина могут отмечаться боль в животе и болезненные позывы.
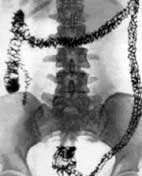
Двухэтапная зондовая энтерографияДо настоящего времени основным методом визуализации тонкой кишки является метод рентгенодиагностики. Однако, рентгенологи недостаточно часто применяют его в своей практической работе, особенно метод зондовой энтерографии, что связано с известными трудностями методического характера, отсутствием необходимого технического оснащения и высококачественного контрастного вещества. Первые сообщения о способе контрастирования тонкой кишки через зонд появились в зарубежной литературе в 1911 году [8]. В России метод зондовой энтерографии впервые был описан в 1953 году. В последующем эта методика достаточно подробно была разработана отечественными авторами [3,4,5]. Несомненным преимуществом метода явилось сокращение времени исследования и снижение лучевой нагрузки на медицинский персонал и больного. Но из исследования исключался верхний отдел желудочно-кишечного тракта, что по тем временам, при отсутствии гастроскопии, было достаточно серьезным отрицательным моментом методики. Кроме того, сложной была сама процедура исследования, в частности, зондирование зондом с оливой и введение контрастного вещества в просвет кишки шприцем Жане или аппаратом Боброва. Все это ограничивало применение метода в практике. Между тем в 70-е годы в зарубежной практике активно разрабатывались и применялись более совершенные методы рентгеноконтрастного исследования тонкой кишки, такие как энтероклизма с введением в просвет кишки большого количества малоконтрастной бариевой взвеси и зондовая энтерография с двойным контрастированием. В качестве второго контрастного вещества авторы использовали воду, раствор метилцеллюлозы, воздух. При этом исследователями была доказана целесообразность использования дуоденальных зондов без оливы с управляемыми металлическими проводниками, разработан новый состав контрастного вещества, предложено несколько вариантов введения его в кишку с помощью специальных приспособлений. Дальнейшее развитие метода зондовой энтерографии в условиях двойного контрастирования получило в работах отечественных исследователей. Подготовка к исследованию Накануне исследования рекомендуется прием жидкой пищи и обильное питье. Из рациона питания необходимо исключить продукты, вызывающие газообразование. Последний прием пищи должен быть не менее, чем за 12 часов до исследования. Вечером накануне исследования и утром за два часа до него назначаются очистительные клизмы с водой комнатной температуры в объеме 1,0 л-1,5 л. Эмоциональным больным, больным с сопутствующим заболеванием сердечно-сосудистой системы, а также ослабленным больным следует назначать вечером перед исследованием седативные препараты. В день процедуры запрещается прием лекарственных препаратов, воды, курение. Исследование проводится натощак. Зондирование За 15 минут до исследования больному подкожно вводят 2,0 мл церукала или перинорма. Препараты, являясь прокинетиками, усиливают перистальтическую активность пищевода, желудка, тонкой кишки, что значительно сокращает время исследования. Зондирование осуществляется полихлорвиниловым дуоденальным зондом с внешним диаметром 4 мм длиной 125 см (отечественного производства или производства польско-французской фирмы "Balton") с металлическим проводником внутри. При отсутствии возможности приобретения специального импортного управляемого проводника можно с успехом использовать отечественные сосудистые проводники. Сосудистый проводник также придает упругость зонду, облегчает процедуру зондирования, уменьшает вероятность закручивания его в области свода желудка и в препилорическом отделе желудка. Сосудистый проводник вводится в зонд до начала зондирования и не извлекается из него до конца исследования. Перед зондированием проводится местная анестезия носо- и ротоглотки 2% раствором лидокаина через нижний носовой ход с помощью пипетки или шприца. При этом больной должен делать глотательные движения во избежание аспирации лидокаина в дыхательные пути. Зондирование предпочтительно осуществлять через нос. В этом случае несколько снижается вероятность возникновения таких осложнений, как рвота, кашель, тошнота. У ослабленных больных и у больных с сопутствующими заболеваниями сердечно-сосудистой системы во время зондирования может возникнуть приступ тахикардии, сердцебиения. Исследование начинают в положении пациента сидя, позвоночник выпрямлен, голова откинута назад. Зонд, смазанный вазелиновым маслом, через нижний носовой ход вводят в пищевод. В момент прохождения его рото- и гортаноглотки больной должен делать глотательные движения. После того, как зонд установлен в дистальном отделе пищевода, пациента помещают на универсальный штатив рентгенодиагностического аппарата. Продвижение зонда через желудок и привратник осуществляют в вертикальном положении больного под контролем рентгеноскопии. После выхода зонда из желудка штатив рентгенодиагностического аппарата переводят в горизонтальное положение и зондирование продолжают в положении пациента на спине. Дистальный конец зонда по возможности следует завести дистальнее связки Треица и установить в начальном сегменте тощей кишки. При нормотоничном желудке в форме крючка зонд при выходе из желудка делает характерный изгиб в области верхнего колена двенадцатиперстной кишки, повторяет форму "дуоденального окна", образует полузамкнутую или замкнутую фигуру восьмерки (рис.1) за счет пересечения тени зонда в просвете желудка с тенью зонда в просвете восходящей ветви двенадцатиперстной кишки. Рентгеноконтрастная масса Обязательным условием успешного проведения методики зондовой энтерографии в условиях двойного контрастирования является использование высококачественной бариевой взвеси. Контрастная масса должна быть повышенной плотности, мелкодисперсной, гомогенной, устойчивой к флоккуляции в тонкой кишке, обладать хорошей адгезивной способностью и низкой вязкостью. Всем этим качествам соответствуют рентгеноконтрастные средства для исследования тонкой кишки известных иностранных фирм Nicolas (Австрия), EZEM (США). В меньшей степени для исследования тонкой кишки подходит отечественная продукция фирмы "ВИПС-МЕД" (БАР-ВИПС). В своей работе мы использовали разработанное нами контрастное вещество на основе сульфата бария с добавлением веществ-стабилизаторов. Предложенная бариевая взвесь с нашей точки зрения отвечает всем требованиям, необходимым для зондовой энтерографии. Она свободно, с заданной скоростью поступает через узкий дуоденальный зонд в просвет тонкой кишки, устойчива к воздействию органических компонентов кишечного сока, равномерно, стойко и тонким слоем покрывает слизистую оболочку, создавая после введения воздуха эффект двойного контрастирования. Состав контрастной массы: 0,3% раствор натрий - карбоксиметилцеллюлозы (натрий-КМЦ) - 100,0 мл, сульфат бария - 200,0 мг, цитрат натрия - 2,5 г, эмульсия эспумизана (пеногаситель) -5 мл. 0,3% раствор пищевой натрий-КМЦ повышает агрегативную устойчивость бариевой взвеси в содержимом тонкой кишки и улучшает прилипание ее к слизистой оболочке. Повышенная плотность сульфата бария (66,6 весовых %) обеспечивает высокую контрастность изображения рельефа слизистой и контура кишки при двойном контрастировании. Цитрат натрия уменьшает вязкость контрастного вещества, повышает его пластические свойства, что позволяет получить тонкий слой контрастного покрова слизистой оболочки. Эмульсия эспумизана уменьшает пенообразование в просвете кишки при введении воздуха. Методика двухэтапной зондовой энтерографии позволяет в большинстве случаев получить оптимальное изображение всей тонкой кишки в фазу рельефа и в фазу двойного контрастирования. Рентгеноскопия и серия рентгенограмм дают полную информацию о расположении, подвижности кишки, о состоянии ее просвета и эластичности стенок, характере рельефа слизистой оболочки в условиях традиционного и двойного контрастирования. Применение специальной бариевой взвеси улучшает визуализацию рельефа слизистой оболочки и обеспечивает равномерное, высококонтрастное покрытие внутренней поверхности кишки в условиях двойного контрастирования. Двойное контрастирование позволяет дифференцированно изучить состояние петель тонкой кишки даже при суперпозиции их. Особую ценность приобретает методика при исследовании тазовых сегментов подвздошной кишки, для которых, как известно, традиционный метод исследования малоинформативен. Кроме того, сочетание зондовой энтерографии в условиях двойного контрастирования с ретроградным введением воздуха в правую половину толстой кишки позволяет получить исчерпывающую информацию о состоянии такого сложного и для рентгенологического, и для эндоскопического исследования отдела кишечника, как илеоцекальный.
Определение степени распространения опухолевого процессаПрограмма обследования больного до операции, кроме традиционных общепринятых методов, включает в себя специальные рентгенологические, радиоизотопные методы, методики радионуклеидной диагностики, а также радиоиммуновизуализацию первичной опухоли и ее метастазов. В основе гематогенного метастазирования рака лежит процесс эмболизации раковыми клетками венозных путей оттока из органов, пораженных опухолевым процессом. Проникновение опухолевых клеток в венозные сосуды происходит, в основном, в результате инвазии и разрушения опухолью стенки сосуда. В связи с тем, что основная масса венозной крови по системе нижней и верхней брыжеечных вен поступает в воротную вену, основной локализацией отдаленных метастазов у больных колоректальным раком является печень. Ультразвуковое исследованиеДо недавнего времени считалось, что осмотреть органы, содержащие газ, нельзя, поскольку они полностью отражают ультразвуковые волны. Однако с развитием ультразвуковой техники и разработкой новых методик исследования появилась возможность визуализации толстой кишки. В настоящее время существует две методики УЗИ ободочной и прямой кишки: • УЗИ через переднюю брюшную стенку: – ободочной кишки без подготовки; – ободочной кишки с наполнением (ультразвуковая ирригоскопия); – прямой кишки при хорошо наполненном мочевом пузыре. • Внутриполостное исследование: – толстой кишки с помощью ультразвукового колоноскопа; – прямой кишки с использованием ректального (эндоректальная ультрасонография), а в отдельных случаях – вагинального датчика. Подготовка к УЗИ зависит от применяемой методики. Обследование ободочной кишки через переднюю брюшную стенку проводится натощак, без предварительной подготовки, при исследовании прямой кишки требуется хорошее наполнение мочевого пузыря. Для проведения внутриполостного исследования необходимо хорошее очищение толстой кишки, а при ультразвуковой ирригоскопии – дополнительное введение 2 л физиологического раствора. Эндоректальную ультрасонографию рекомендуется выполнять только после пальцевого исследования прямой кишки и ректороманоскопии. УЗИ нашло широкое распространение для оценки степени распространения опухолевого процесса. Оно основано на принципе регистрации отраженной ультразвуковой волны от границ раздела тканей отличающихся по плотности и строению. Обладая высокой разрешающей способностью и информативностью, ультразвуковое исследование является практически безвредным диагностическим методом, позволяющим визуализировать опухолевые узлы размерами 0,5–2,0 см. Метод позволяет выполнить прицельную тонкоигольчатую чрезкожную пункцию очагового образования. Кроме того, может быть использован интраоперационно, что значительно увеличивает информативность. 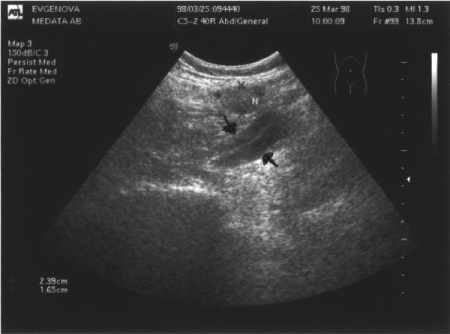 Ультрасонограмма метастаза рака прямой кишки в подвздошные лимфоузлы слева. Между стрелками общие подвздошные сосуды; N – увеличенный лимфоузел размером 1,6х2,4 см При раке ободочной кишки выявляется локальный участок с неравномерно утолщенной до 0,8 – 3,0 см стенкой, представленный сигналами пониженной и средней интенсивности. При сопоставлении данных УЗИ и патогистологического исследования операционного препарата какой-либо зависимости между толщиной стенки, полученной при ультрасонографии, и глубиной инфильтрации стенки установить не удается из-за экзофитного роста опухоли. Исключением является сигмовидная кишка; при раке сигмовидной кишки с толщиной стенки 10 – 17 мм опухоль инфильтрирует все слои стенки кишки, а при толщине более 17 мм прорастает в окружающую клетчатку. С большой достоверностью можно говорить о прорастании рака в паранефральную клетчатку и о связи опухоли с близлежащими органами (петли тонкой кишки, печень, селезенка) при локализации образования в восходящем и нисходящем отделах ободочной кишки. При ячеистой структуре опухоли следует думать о перифокальном воспалении. Однако опухоль ободочной кишки может остаться недиагностированной, если имеет небольшие размеры (1 – 4 см в диаметре) и неглубоко инфильтрирует кишечную стенку (до мышечного слоя). Метастазы рака ободочной кишки в брыжеечные ЛУ данная методика выявить не позволяет, однако определяются отдаленные метастазы в печень и парааортальную зону. Ультрасонографическая картина рака прямой кишки характеризуется изменениями толщины, структуры и наружного контура стенки. У всех больных отмечается локальное утолщение стенки кишки, соответствующее протяженности опухоли, от 10 мм и более в зависимости от степени инфильтрации кишечной стенки опухолевым процессом. При сопоставлении данных патогистологического исследования и ультрасонографии установлено, что при толщине стенки 10 – 11 мм опухоль инфильтрирует мышечный слой, 13 – 14 мм – прорастает все слои кишечной стенки, а при толщине более 15 мм врастает в окружающую клетчатку. Структура стенки прямой кишки при раковом поражении нарушается, исчезает ее двухслойность, она представлена сигналами средней интенсивности. Наружный контур стенки кишки неровный за счет неравномерного прорастания опухоли в окружающую клетчатку. На месте расположения новообразования просвет кишки не выявляется. Точность дооперационной диагностики глубины прорастания опухолью кишечной стенки составляет 82 %. При прорастании рака прямой кишки в близлежащие органы имеет место истинное прилежание опухоли к пораженному участку, т.е. отсутствует граница между ними. Следует отметить, что при инфильтрации опухолью стенки мочевого пузыря при опорожнении его ультразвуковая картина не меняется. Прорастание опухоли в мочевой пузырь или влагалище проявляется утолщением стенки органа. Однако, как показывает наш опыт, в отдельных случаях утолщение стенки мочевого пузыря возможно не только за счет инвазии, но и вследствие перифокального воспаления. Точность диагностики прорастания опухолью соседних органов составляет 90,5 %. У всех больных раком прямой кишки, осложненным перифокальным воспалением, при УЗИ отмечается утолщение стенки от 17 мм и более. Структура опухоли при этом изменяется по двум типам: I тип – структура опухоли однородная, представлена сигналами пониженной интенсивности – выявлен у 21,7% больных; II тип – структура опухоли неоднородная, мозаичная, могут наблюдаться единичные полостные образования – выявлен у 69,6 %; у 8,7 % больных изменений структуры новообразования не обнаружено. Отмечается понижение плотности опухоли по данным гистограмм по сравнению с контрольной группой до 12,8 ± 0,9 ед. (р < 0,001), плотность опухоли в контрольной группе составляет 25,2 ± 1,5 ед. В связи с анатомо-топографическим строением и расположением печени, хорошее распространение в ней ультразвука обусловливает высокую информативность исследования. Важным является тот факт, что эхотомография помогает определить не только характер патологических изменений в печени, но и установить локализацию и глубину залегания очаговых изменений. При выполнении ультразвуковой томографии представляется возможность получить послойное изображение внутренней структуры печени без предварительного ее контрастирования и выявить патологические объемные образования или диффузные изменения. Для оценки результатов лечения и сравнения данных ультразвуковой томографии в процессе терапевтического воздействия важным является тот факт, что исследование возможно повторять довольно часто без ущерба для организма больного. Подготовка для УЗИ органов брюшной полости: За 2-3 дня до исследования необходимо исключить из рациона пищевые продукты, способствующие газообразованию (сырые фрукты и овощи, черный хлеб, молоко, газированная вода и др.). При склонности к метеоризму ("вздутию живота") желателен прием энтеросорбентов. Исследование проводится натощак (обычно в утренние часы после ночного голодания). Недопустимо проведение УЗИ после гастроскопии или колоноскопии. Подготовка для УЗИ органов малого таза: Для качественного исследования органов малого таза необходимо наполнить мочевой пузырь (обычно нужно выпить 1 л негазированной жидкости за 1 час до исследования). Для проведения ТВУЗИ (трансвагинального исследования) подготовки не требуется. Трансректальное УЗИТрансректальное ультразвуковое исследование является одним из самых информативных методов определения глубины опухолевой инвазии стенки кишки и поражения регионарных лимфатических узлов. Ультразвуковая томография, как неинвазивный метод интроскопии давно привлекал внимание исследователей. Традиционная трансабдоминальная методика ультразвуковой томографии нашло широкое применение как метод диагностики рецидива рака прямой кишки после экстирпации органа. Однако первичная диагностика заболевания трансабдоминальным способом затруднена по целому ряду объективных причин. В первую очередь это связано с тем, что при трансабдоминальном сканировании прямая кишка визуализируется только в 85% случаев. Область анального канала практически недоступна для трансабдоминального способа исследования из-за артефактов вызванных большой глубиной расположения и наложения акустической тени от лонной кости. К тому же проведение трансабдоминального исследования требует хорошего наполнения мочевого пузыря. Все вышесказанное не позволяет использовать трансабдоминальный способ ультразвуковой томографии для диагностики и оценки степени местного распространения рака прямой кишки. Проведение исследования Во время исследования пациент располагается лежа на левом боку, с приведенными к животу коленями. Постепенно перемещая датчик, осматривают анальный канал и ампулярный отдел прямой кишки. Специальные деления, нанесенные на тубусе аппарата, позволяют четко контролировать глубину введения датчика в полость органа. На ультразвуковых томограммах стенка анального канала имеет трехслойную структуру. Эпителий и подэпителиальная соединительная ткань формируют первый слой представленный отражениями средней интенсивности. Второй, достаточно выраженный слой с отражениями низкой интенсивности, представляет собой внутренний сфинктер. Наружный слой представляющий собой перианальную жировую клетчатку формируют отражения высокой интенсивности. Стенка прямой кишки на трансректальных ультразвуковых томограммах представлена пятью слоями. Первый слой интенсивно отражающий ультразвуковые волны является границей между поверхностью датчика и слизистой. Слизистая оболочка имеет вид гипоэхогенного слоя, в толще которого, в виде прерывистой, хорошо отражающей ультразвуковые волны линии прослеживается собственная мышечная пластинка. Третий, гиперэхогенный слой разделяет слизистый и мышечный слои, который имеет отражения низкой интенсивности. Пятый слой, который формируют отражения высокой интенсивности отображает параректальную жировую клетчатку или серозную оболочку (для экстраперитонеальных отделов кишки). Основным критерием инвазивного роста опухоли является нарушение пятислойного строения стенки кишки. Так как во время исследования рабочий, дистальный конец аппарата полностью обтурирует просвет кишки, прямым ультразвуковым признаком опухоли является утолщение стенки органа. При выходе процесса за пределы стенки кишки, нарушается четкость наружного контура органа. Внутренний контур стенки (и опухоли в том числе), остается четким и ровным за счет сдавления поверхностью датчика. При специфической инфильтрации параректальной клетчатки, опухолевый инфильтрат, как правило, формируют отражения низкой интенсивности. Диагностическая эффективность эндоректальной ультразвуковой томографии особенно высока на ранних стадиях опухолевого процесса (Т1-Т2). В этих случаях опухоль визуализируется как образование с отражениями низкой интенсивности, занимающее часть окружности кишки. При этом четко определяются наружные границы опухоли и степень инфильтрации различных слоев стенки кишки. Установлено, что эндоректальное ультразвуковое исследование позволяет дифференцировать опухоли локализующиеся в пределах слизистого и подслизистого слоев от новообразований инфильтрирующих мышечный слой стенки кишки. При выходе процесса за пределы стенки кишки, нарушается четкость наружного контура органа. Внутренний контур стенки (и опухоли в том числе), остается четким и ровным за счет сдавления поверхностью датчика. При специфической инфильтрации параректальной клетчатки, опухолевый инфильтрат, как правило, формируют отражения низкой интенсивности. Чувствительность метода при дифференциальной диагностике локализованных и местнораспространенных новообразований составляет 91%, специфичность 89%. В некоторых публикациях отмечаются трудности в дифференциации различных стадий опухолевого роста при местнораспространенном раке прямой кишки. Наибольшие трудности встречаются при определении начальных признаков инвазии параректальной жировой клетчатки, выявляющихся микроскопически. Однако до настоящего времени нет четких данных о необходимости разграничения между пациентами, у которых опухолевый процесс распространяется на всю глубину кишечной стенки, от пациентов с микроскопически определяемой инвазией параректальной клетчатки. При прорастании всей толщи кишечной трубки всегда (или в большей степени вероятности) имеются начальные признаки инвазии параректальной клетчатки. Эти больные, по мнению ряда исследователей, могут быть объединены в одну группу, и выбор метода комбинированного лечения в этих случаях зависит от наличия метастазов в параректальных лимфатических узлах. При метастатическом поражении параректальных лимфатических узлов в параректальной клетчатке определяются округлые образования с отражениями пониженной эхогенности размером от 0.3см. Однако необходимо учитывать, что в ряде случаев, при развитии перифокального воспалительного процесса ультразвуковая томография регистрирует реактивные изменения в параректальных лимфатических узлах, которые имеет сходную с метастазами структуру. Безусловно, трансректальная ультразвуковая томография не может являться методом первичной диагностики рака прямой кишки. Однако этот вид интроскопии позволяет решить важнейшие диагностические задачи: 1) оценить протяженность опухолевого процесса; 2) определить степень поражения стенки кишки; 3) определить глубину инфильтрации параректальных тканей; 4) выявить метастатическое поражение параректальных лимфатических узлов; 5) выявить распространение опухолевого процесса на расположенные рядом органы; 6) оценить эффективность предоперационной лучевой терапии. Для выявления метастазов в легких выполняется рентгенография грудной клетки в двух проекциях, при необходимости рентгеновская томография, компьютерная томография. Компьютерная томографияОдним из наиболее информативных из доступных методов выявления отдаленных метастазов в печени и забрюшинных лимфоузлах является компьютерная томография. С ее помощью выявляют метастазы в печени, воротах печени размерами более 1 см, портальных, парааортальных лимфатических узлах Патологические изменения могут проявляться участками с высоким коэффициентом абсорбции (опухоли) и низким, наиболее характерным для кист, полостей. Компьютерная семиотика и дополнительное контрастирование позволяет отличить опухолевое поражение от других очаговых заболеваний печени. Кроме этого метод также позволяет выполнить прицельную тонкоигольчатую чрезкожную пункцию очагового образования и получить материал для цитологического исследования. Компьютерная томография обладает следующими важными преимуществами перед другими методами обследования:
В  ыявление микрометастазов в регионарных и отдаленных лимфатических узлах, определение субклинических метастазов в печени имеют огромное значение как в тактическом, так и в прогностическом плане. Однако возможности дооперационной диагностики микрометастазов существенно ограничены. Одним из наиболее чувствительных и информативных методов выявления "маленьких" опухолей, рецидивов, микрометастазов является протонно-эмиссионная томография (PET). Протонно-эмиссионная томография позволяет дифференцировать метастатическое поражение лимфатических узлов от лимфаденопатий другой природы, что невозможно сделать при использовании компьютерной томографии, а также может успешно применяться для определения распространенности первичной опухоли. Изучается также возможность использования PET с FDG для оценки операбельности больных с метастазами в печени. Метод представляет собой разновидность сканирования с использованием меченного радиоактивным изотопом производного глюкозы. Эмиссионное сканирование проводится через 45 мин после внутривенного введения 325 МБк ('"F) флюоро-деоксиглюкозы (FDG). Полученные данные подвергаются обработке с использованием стандартной компьютерной техники. Готовые томограммы выводятся на дисплей в трансаксиальной, фронтальной и сагиттальной проекциях с конечной толщиной слоя около 4 мм. PET имеет ряд преимуществ перед другими визуализирующими методами. Основанный на метаболической активности, метод позволяет дифференцировать жизнеспособную опухолевую ткань от участков фиброза, некроза или рубцовых изменений. Кроме того, он позволяет выявлять опухолевую ткань максимально рано, поскольку метаболическая активность может быть установлена раньше, чем появятся определяемые различными методами структурные изменения. Магнитно-резонансная томография (МРТ)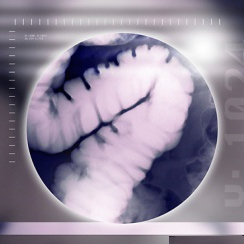 Магнитно-резонансная томография (ядерно-магнитная резонансная томография, МРТ, ЯМРТ, NMR, MRI) - нерентгенологический метод исследования внутренних органов и тканей человека. Здесь не используются Х-лучи, что делает данный метод безопасным для большинства людей. Технология МРТ достаточно сложна: используется эффект резонансного поглощения атомами электромагнитных волн. Человека помещают в магнитное поле, которое создает аппарат. Молекулы в организме при этом разворачиваются согласно направлению магнитного поля. После этого радиоволной проводят сканирование. Изменение состояния молекул фиксируется на специальной матрице и передается в компьютер, где проводится обработка полученных данных. В отличие от компьютерной томографии МРТ позволяет получить изображение патологического процесса в разных плоскостях. Метод особенно эффективен для изучения динамических процессов (например, состояния кровотока и результатов его нарушения) в органах и тканях. МРТ лучше визуализирует некоторые структуры головного и спинного мозга, а также другие нервные структуры. В связи с этим она чаще используется для диагностики повреждений, опухолевых образований нервной системы, а также в онкологии, когда необходимо определить наличие и распространенность опухолевого процесса. Список заболеваний, которые можно обнаружить с помощью МРТ, внушителен: воспалительные, дистрофические и опухолевые поражения сосудов и сердца, органов грудной и брюшной полости, поражение лимфатических узлов, паразитарные процессы и другие патологии. АнгиографияПосле введения контрастного вещества в кровеносный сосуд выполняется серия снимков. Это позволяет выявить расположение сосудов по отношению к метастазам опухоли для того, чтобы избежать серьезных кровотечений во время операции. Используемая литература1. Медицинская Энциклопедия 2003 2. Яицкий, Н.А.; Седов, В.М. «Опухоли кишечника» Издательство: СПб: АНТ-М, 1995 г. 3. Клиническая рентгенорадиология, под ред. Г.А. Зедгенидзе, т. 3, М., 1983 4. Иванова Е.М. К методике рентгенологического исследования тонкой кишки введением бария через дуоденальный зонд. //Вестн. ренгенол. 1963. № 1. С. 30-32. 5. Колерова Н.В. Рентгенологическое исследование всего кишеч-ника при помощи энтероклизмы в предельно короткий срок. /Материалы расширенного пленума Всерос. науч. об-ва рентген. и радиол. Ростов - на Дону. М., 1963. С. 95-97. 6. http://www.colorectalcancer.ru 7. Интернет. 8. Cole L.G. Artificial Dilation of the duodenum for radiographie eхamination. //Аmer. J. Roentgenol.1911.V. 3. P. 204. | |||||||||||||||||||||||||||||||