Пробиотки:классификация, методы выделения и очистки пробиотиков. Реферат мобав. Реферат Пробиотки классификация, методы выделения и очистки пробиотиков Дисциплина Методы очистки бав студентка
 Скачать 184.05 Kb. Скачать 184.05 Kb.
|
|
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ федеральное государственное бюджетное образовательное учреждение высшего образования «Пермская государственная фармацевтическая академия» Министерства здравоохранения Российской Федерации Факультет очного обучения Кафедра промышленной технологии лекарств с курсом биотехнологии Реферат Пробиотки:классификация, методы выделения и очистки пробиотиков Дисциплина: Методы очистки БАВ Выполнила: студентка Верещагина Е.В. Приняли: Хволис Е.А. Пермь 2020 ОглавлениеВведение 4 Общая характеристика и биологическая роль пробиотиков 5 Классификация пробиотиков 8 Методы получения и очистки 10 Список литературы 15 ВведениеПроблема неуклонного ухудшения здоровья населения всё больше волнует медицинскую общественность. Несмотря на бурное развитие фармацевтической промышленности, насыщающей медицину огромным количеством лекарственных препаратов, тенденция к увеличению заболеваемости не снижается. Это явилось одной из причин возросшего в последние десятилетия интереса учёных к роли микроорганизмов, обитающих в организме человека, в поддержании его здоровья. Достижения зародившейся на рубеже ХХ - ХХI столетий и интенсивно развивающейся современной медицинской науки - микробной экологии человека - способствовали появлению принципиально новых «микробных» лечебно-профилактических препаратов, получивших название пробиотики. Общая характеристика и биологическая роль пробиотиковПробиотики - препараты, содержащие живые микроорганизмы, относящиеся к нормальной, физиологически и эволюционно обоснованной флоре кишечного тракта. Они положительно влияют на организм хозяина, способствуют восстановлению пищеварения, биологического статуса, иммунного ответа, повышают эффективность вакцинаций. При их применении снижаются заболеваемость, количество фармакологических обработок и связанные с ними материальные издержки. К числу наиболее известных пробиотиков относятся молочно-кислые бактерии, бифидобактерии, стрептококки. Многие из предлагаемых в настоящее время на ветеринарном рынке препаратов рекламируют как пробиотики. Они различны по составу, качеству, фармакологической направленности действия, показаниям к применению. Пребиотики - субстраты, стимулирующие естественную микрофлору, которые в норме поступают в организм животных и птицы в составе рациона. Они не перевариваются и не всасываются в желудке и тонком отделе кишечника, а, попадая в толстый отдел кишечника, используются в качестве питательной среды для нормальной микрофлоры. Синбиотики - рациональная комбинация пробиотика и пребиотика. Следует отметить, что многие авторы относят к пробиотикам препараты, состоящие из отдельных структур клеток микробного происхождения, а также метаболиты, органические кислоты и соединения любой природы, способствующие качественному и количественному восстановлению нормальной микрофлоры. Поэтому, выбирая для использования тот или иной пробиотик, необходимо анализировать его состав. Он определяет основные показания к применению и фармакологические свойства. Пробиотические препараты можно разделить на несколько основных групп: Дрожжи и продукты их жизнедеятельности являются источником легкоусвояемого полноценного по составу микробного белка, витаминов. Фармакологическое действие заключается в повышении уровня перевариваемого белка и витаминов группы В в составе рациона, стимуляции роста и продуктивности животных. Они не восстанавливают нормальную микрофлору желудочно-кишечного тракта, не устраняют дисбактериозы. Пробиотики, включающие споровые микроорганизмы, чаще В. subtilis. Штаммы в составе пробиотических препаратов отбирают по выраженности антагонистических свойств к патогенной микрофлоре. Они продуцируют большое количество антибиотических и других веществ, подавляющих многие микроорганизмы. Препараты улучшают переваримость корма, имеют выраженные ферментативные и протеолитические свойства. Их часто рекомендуют вместо антибиотиков для вытеснения патогенных микроорганизмов, что не всегда фармакологически корректно. Если нет глубокого нарушения микробиоценоза и слизистой кишечника, то нормальная микрофлора может восстановиться самопроизвольно после курса использования пробиотиков, содержащих В. subtilis. В некоторых случаях, иногда при длительном применении такие препараты могут провоцировать развитие дисбактериозов, привыкание и селекцию устойчивых патогенных штаммов, поражающих как кишечник, так и другие органы. Фармакологическое действие ●заселяют с первых дней жизни организма животных и птиц нормальной микрофлорой (стимуляция пищеварения, иммунитета, профилактика колибактериоза, сальмонеллеза, других инфекций, вызываемых патогенной и условно-патогенной микрофлорой); ●восстанавливают микробиоценоз и пристеночное пищеварение при инфекционных заболеваниях. Можно использовать одновременно с антибиотиками, если пробиотики включают устойчивые к антибиотикам штаммы (например, лактобифадол). Если штаммы, входящие в препарат, не устойчивы к антибиотикам, то его применяют после антибиотикотерапии для восстановления нормальной микрофлоры.; ●нормализуют пищеварение при дисбактериозах различной природы, после кормовых отравлений, использования фармакологических препаратов (антибиотиков, антгельминтиков, кокцидиостатиков и др.); ●способствуют повышению иммунитета. Классификация пробиотиковТаблица № 1 Классификация пробиотиков (Г.Г. Онищенко, 2002)
• I поколение - классические монокомпонентные препараты, содержащие один штамм бактерий: бифидумбактерин, лактобактерин, колибактерин; • II поколение - самоэлиминирующиеся антагонисты: бактисубтил, биоспорин, споробактерин и др.; • III поколение - комбинированные препараты, состоящие из нескольких штаммов бактерий (поликомпонентные) или включающие добавки, усиливающие их действие: аципол, ацилакт, линекс, бифилиз, бифи-форм; • IV - поколение иммобилизованные на сорбенте живые бактерии, представители нормофлоры. В настоящее время к ним относятся сорбированные бифидосодержащие пробиотики: бифидумбактерин форте и пробифор. Бифидумбактерин - лиофильно взвешенная взвесь живых бифидобактерий (B.bifidum). В одной дозе содержится не менее 100 млн. живых микробных клеток. Форма выпуска для энтерального применения - флаконы с сухой биомассой, пакеты с порошком и таблетки. Противопоказаний для препарата и побочных реакций на его прием нет. Показания: для лечения детей, особенно первого года жизни, перенесших острую кишечную инфекцию, страдающих длительной кишечной дисфункцией неустановленной этиологии, детей, находящихся с первых дней жизни на искусственном вскармливании, недоношенных; для применения через 3-5 дней после отмены антибиотиков, при назначении совместно с антибиотиками надо учитывать совместимость; при отягощенном фоне (рахит, гипотрофия, анемия); в комплексной терапии больных тяжелыми инфекционными заболеваниями, локальными гнойничковыми поражениями, при любых дисфункциях кишечника (метеоризм, изменение частоты и характера стула); больным с заболеваниями органов пищеварения (независимо от возраста); людям, страдающим ферментопатиями, наследственными заболеваниями обмена веществ; при длительной гормонотерапии; при облучении. Методы получения и очисткиСпецифика биотехнологических методов получения препаратов-пробиотиков состоит в том, что, штаммы микроорганизма симбионта должны быть совместимыми с организмом человека, т.е. выделяться, например, из кишечного содержимого здоровых детей и взрослых, как это было в случае со штаммом Enterococcus faecium, который был выделен из кишечника ребенка. Во-вторых, выделенные штаммы обязательно надо идентифицировать. Дело в том, что для получения пробиотиков разрешены штаммы только определенных видов микроорганизмов. Эти штаммы должны обладать следующими свойствами: • эффективной антагонистической активностью, обеспечиваемой в свою очередь синтезом органических кислот, которые штамм должен активно продуцировать. При выделении штаммов бифидобактерий важным антагонистическим началом продуктов метаболизма являются муравьиная и молочная кислоты. Желательно также, чтобы эти штаммы продуцировали пероксиды и антибиотикоподобные вещества; • эффективной способностью прикрепляться к эпителию кишечника, если речь идет о пристеночных микроорганизмах; • не гидролизовать кишечную слизь, которая обладает протективным действием. Некоторые микроорганизмы продуцируют мукополисахариды, которые разрушают (гидролизуют) эту слизь; • не повреждать клетки кишечного эпителия (холециты). Отобранные штаммы обязательно проверяют на патогенность и токсичность in vitro на культуре клеток холецитов, на чувствительных животных. Побочные эффекты у пробиотиков не должны проявляться даже при их избыточных дозах. Для проверки препарат вводят в организм чувствительных животных в больших количествах, иногда до нескольких граммов на килограмм веса. Штаммы должны быть технологичны, т.е. хорошо расти и размножаться на искусственных питательных средах. Их обрабатывают методом лиофилизации: замораживают до низких температур и затем высушивают при низком давлении. Соответственно, отобранные штаммы должны быть криорезистентны и выдерживать процедуру высушивания. Удовлетворяющие всем этим требованиям штаммы поступают в контрольный институт, откуда их передают в фармацевтическое производство с соответствующими документами, в которых отражены их характеристики. В заводских лабораториях штаммы высеивают на искусственные питательные среды, проверяют их соответствие паспортным данным (род, вид, биологические свойства). И только после этого используют для получения препаратов пробиотиков. В условиях промышленного производства эти штаммы рассеивают и получают отдельные колонии, которые затем пересевают на агаризованные или жидкие питательные среды (например, молочнокислые бактерии хорошо растут в обезжиренном молоке). И бифидобактерии, и лактобациллы, и энтерококки — это ауксотрофы, т.е. для своего роста они нуждаются в ряде питательных веществ и микроэлементов, не могут сами синтезировать аминокислоты, пуриновые и пиримидиновые основания, витамины: их должна содержать питательная среда. Для культивирования этих бактерий используют такое сырье, которое разрешено к применению в пищевой промышленности, так как препарат, выращенный на этих средах, впоследствии используется для внутреннего применения. Обычно молочнокислые бактерии культивируют от 8 до 16 ч (довольно короткая ферментация). Собирают штаммы в той фазе роста, при которой выживание клеток культуры будет наиболее длительным, что в свою очередь, при дальнейшем получении препарата, обеспечивает его длительное хранение. Все это определяется экспериментальным путем и часто является ноу-хау фирмы-производителя. Как правило, выбирают конец логарифмической фазы или начало стационарной, в зависимости от культуры (штамма). По завершении процесса культивирования получают бактериальную суспензию, содержащую в 1 мл 109 и более клеток. Эти клетки собирают, используя поточные центрифуги или сепараторы, в которых образуется похожая на сметану с кремовым оттенком масса со специфическим запахом кислого молока (напоминает прессованные дрожжи). Раствор криопротекторов (вещества белковой природы — обезжиренное молоко или желатин; углеводы — лактоза, сахароза) добавляют в проточную массу и получают густую суспензию клеток, которую разливают в ампулы. Затем их замораживают в жидком азоте и подвергают лиофильной сушке. Сухая масса приобретает пузырчатый вид. Ее измельчают и определяют титр, в соответствии с которым вносят во флаконы (стеклянные, пластмассовые) или 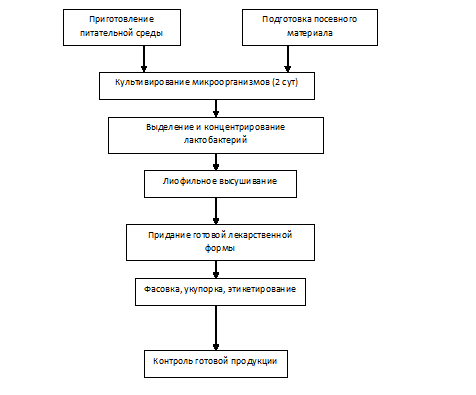 смешивают с культурой другого штамма. смешивают с культурой другого штамма.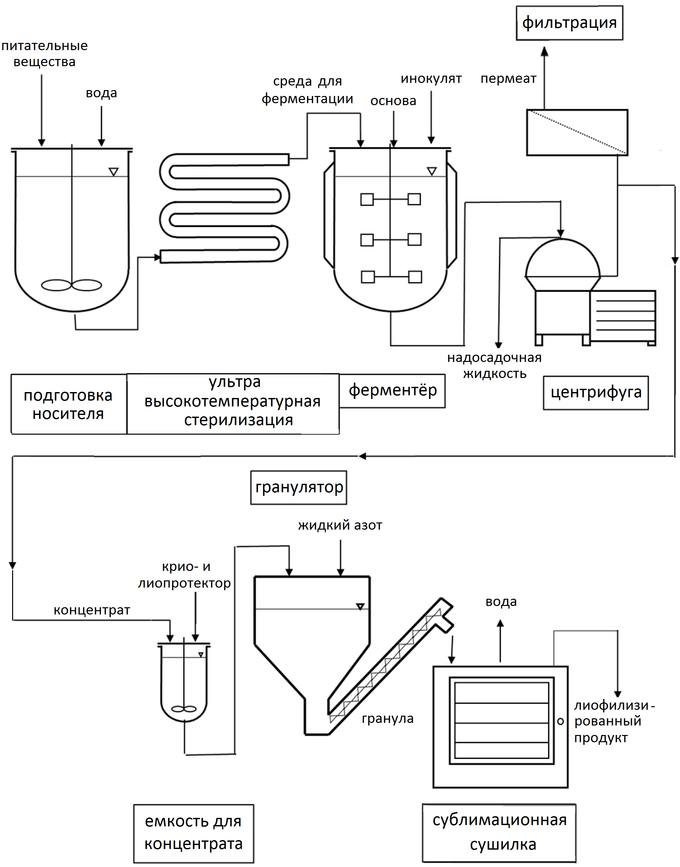 Схематическое изображение производства пробиотиков для пищевых добавок и штаммов молочных заквасок. Схематическое изображение производства пробиотиков для пищевых добавок и штаммов молочных заквасок.После удаления из сушилки лиофилизированный материал измельчают в порошок с определенным размером частиц и плотностью. Измельченный материал затем может быть использован для смешивания с наполнителями, дополнительными функциональными ингредиентами, если это необходимо, и вспомогательными средствами, в зависимости от потребностей клиента. Затем смесь используется для изготовления готовых форматов, таких как капсулы, саше или таблетки. Контроль качества проводится на образцах в процессе и на конечном продукте, чтобы убедиться, что конечный продукт имеет высокое качество и не содержит загрязнений. Вывод Велика защитная роль нормофлоры в обеспечении здоровья, поэтому нарушение равновесия между отдельными видами микроорганизмов в местах их постоянного обитания за счет более интенсивного размножения или гибели какого-либо вида может повлечь нарушение гомеостаза с соответствующими последствиями патологического характера. Дисбиотические состояния приводят к изменениям количественного и качественного состава нормофлоры человека. Нормальная микрофлора кишечника в процессе эволюции приобрела исключительно важную роль в формировании колонизационной резистентности организма. Одним из главных механизмов защиты от колонизации условно-патогенными и патогенными бактериями является присутствие в организме достаточного количества собственной полезной микрофлоры. Нормальная микрофлора кишечника играет важную роль в конверсии желчных пигментов м желчных кислот, абсорбции питательных веществ и продуктов их расщепления. Ее представители продуцируют аммиак и другие продукты, которые могут адсорбироваться и участвовать в развитии печеночной комы. Нормофлора кишечника выполняет и регулирует многие функции организма, которые можно уподобить работе лаборатории, осуществляющей многие сотни биохимических процессов. Поэтому очень важно поддерживать нормальную работу микрофлоры организма человека. Список литературыhttp://propionix.ru/proizvodstvo-i-postavka-probiotikov-obzor-praktiki Промышленная технология лекарств: В 2-х т. / Под. ред. В.И. Чуешова. – Харьков: НФАУ, МТК-книга, 2002, - Т.1. – 557с.; Т.2. – 714с. Кайрос, Наталия Пробиотики и ферменты — суперфуд XXI века / Наталия Кайрос. - М.: Питер, 2013. - 224 c. Чебаева, С.О. Пробиотики. Незаменимые помощники вашему организму / С.О. Чебаева. - М.: Рипол Классик, Дом. XXI век, 2013. - 589 c. | ||||||||||||||||
