РЕГУЛЯЦИЯ И НАРУШЕНИЕ КИСЛОТНО-ЩЕЛОЧНОГО БАЛАНСА В ЖИВЫХ ОРГАНИЗМАХ: АЦИДОЗ И АЛКАЛОЗ.. Реферат по химии. Регуляция и нарушение кислотнощелочного баланса в живых организмах ацидоз и алкалоз
 Скачать 216.78 Kb. Скачать 216.78 Kb.
|
|
Федеральное государственное бюджетное образовательное учреждение высшего образования «Новосибирский государственный медицинский университет» Министерства здравоохранения Российской Федерации (ФГБОУ ВО НГМУ Минздрава России) Кафедра медицинской химии Реферат по теме РЕГУЛЯЦИЯ И НАРУШЕНИЕ КИСЛОТНО-ЩЕЛОЧНОГО БАЛАНСА В ЖИВЫХ ОРГАНИЗМАХ: АЦИДОЗ И АЛКАЛОЗ. (обзор литературы) Выполнил(а): студентка 1 курса педиатрического факультета специальности «Педиатрия», 6 группы Палкина Юлия Владимировна Проверила: Доктор биолог.наук, доцент Гимаутдинова О.И Содержание Введение…………………………………………………………………………….3 1.Характеристика кислотно-щелочного баланса и механизмы его регуляции...5 2.Нарушение кислотно-щелочного баланса……………………………………...11 2.1 Ацидоз…………………………………………………………………11 2.2 Алкалоз………………………………………………………………...15 Заключение…………………………………………………………………………19 Список литературы………………………………………………………………...20 Введение Кислотно-щелочной баланс – индикатор здоровья. Человек — единая биологическая система. Ежеминутно, ежесекундно в нас рождаются и умирают миллиарды клеток, они постоянно обновляются. Все эти процессы абсолютно невозможны без кислорода, воды и водорода. Наш организм живет и правильно функционирует только в слабощелочной среде. Метаболическая активность организма обеспечивается четкой регуляцией кислотно-основного равновесия, отражением которого является рН внеклеточных жидкостей. Возбудимость мембран, активность ферментных систем, течение химических реакций зависят от баланса кислот и оснований. Организм человека располагает тонкими механизмами координации происходящих в не физиологических и биохимических процессов и поддержания постоянства внутренней среды (оптимальных значений рН и уровней содержания различных веществ в жидкостях организма, температуры, кровяного давления и т. д.). Эта координация названа, по предложению В. Кеннона (1929), гомеостазисом (от греч. "гомео" – подобный; "стазис" – постоянство, состояние). Она осуществляется путем гуморальной регуляции (от лат. "гумор" – жидкость), т. е. через кровь, тканевую жидкость, лимфу и т. д. с помощью биологически активных веществ (ферментов, гормонов и др.) при участии нервных регулирующих механизмов. Гуморальные и нервные компоненты тесно взаимосвязаны между собой, образуя единый комплекс нейро-гуморальной регуляции. Сохранение постоянства кислотности жидких сред имеет для жизнедеятельности человеческого организма первостепенное значение, потому что, во-первых, ионы Н+ оказывают каталитическое действие на многие биохимические превращения; во-вторых, ферменты и гормоны проявляют биологическую активность только в строго определенном интервале значений рН; в-третьих, даже небольшие изменения концентрации ионов водорода в крови и межтканевых жидкостях ощутимо влияют на величину осмотического давления в этих жидкостях. В данной работе рассматривается характеристика кислотно-щелочного баланса и механизмы его регуляции[1], нарушения кислотно-щелочного баланса в живых организмах: ацидоз и алкалоз.[2] 1.Характеристика кислотно-щелочного баланса и механизмы его регуляции Кислотно-щелочным балансом называется соотношение концентрации водородных и гидроксильных ионов в биологических средах. Ионы водорода создают кислую реакцию среды, а гидроксильные ионы и другие компоненты - щелочную. На сегодня чаще применяемым термином является кислотно-щелочной баланс, который по содержанию больше соответствует характеристике степени регуляции реакции среды, поскольку концентрация кислотных и основных компонентов в организме постоянно меняется. Все биологические процессы в организме происходят в водной среде при определенной концентрации водородных ионов. Вода является слабым электролитом и незначительно диссоциирует на ионы. Одним из условий жизнедеятельности организма является постоянство реакции внутренней среды. Эволюционно в организме животных сложились системы, которые способны поддерживать реакцию среды в достаточно узких пределах Основными буферными системами организма является гидрокарбонатная, фосфатная, белковая, гемоглобиновая и кислотная (образована органическими кислотами: уксусной, молочной и т.п. и их солями). Среди буферных систем плазмы крови важнейшую роль играет гидрокарбонатный буфер (Н2СО3: NaHCO3). Его буферная емкость, т.е. физиологическая способность противодействовать изменениям концентрации ионов водорода, составляет больше половины общей буферной емкости плазмы и 7,0-9,0% - крови. Механизм буферного действия этой системы состоит в том, что при поступлении в кровь большого количества кислых продуктов водородные ионы взаимодействуют с ионами гидрокарбоната, в результате чего образуется слабодиссоциированная угольная кислота, которая дегидратируется до углекислого газа, который выделяется дыхательной системой вследствие гипервентиляции легких. Таким образом, несмотря на снижение концентрации натрия гидрокарбоната в крови, соотношение H2CO3: NaHCO3 быстро восстанавливается, что обеспечивает поддержание величины рН в пределах нормы. При поступлении в организм щелочнореагирующих соединений ионы ОН - связываются свободной углекислотой с образованием бикарбоната: OH - + H2CO3 → HCO3 - + H2O. Сохранение нормального соотношения между концентрацией H2CO3 и натрия гидрокарбоната при компенсированном алкалозе обеспечивается, как и при компенсированном ацидозе, включением физиологических механизмов регуляции кислотно-щелочного равновесия: в плазме крови при этом задерживается некоторое количество CO2 вследствие гиповентиляции легких. Этот процесс осуществляется при участии нейрогуморальных механизмов, сочетание которых с чисто химическим и обеспечивает возможность сохранения рН крови и кислотно-щелочного баланса в пределах нормы. HCO3- Учитывая эти специфические свойства бикарбонатный буфер называют летучим, а его действие в организме можно описать уравнением: Это означает, что рН крови, парциальное давление углекислого газа (рСО2), а также концентрация гидрокарбонатных ионов [HCO3-] является главными параметрами, которые характеризуют кислотно-щелочное равновесие в организме. Чрезмерное количество NaHCO3 выводится почками. Отношение H2CO3: NaHCO3 в норме составляет 1: 20, т.е. щелочной компонент преобладает над кислым в 19 раз. До тех пор, пока соотношение не нарушается, гидрокарбонатная буферная система эффективно противодействует поступлению в кровь кислот и оснований. Действие летучего гидрокарбонатного буфера в организме дополняется действием нелетучих буферных систем. Важнейшим среди них является гемоглобиновый буфер HbO2: Hb, который составляет более 75% всей буферной емкости крови. Буферные свойства гемоглобина состоят в том, что кислые продукты обмена веществ взаимодействуют с калиевой солью гемоглобина с образованием эквивалентного количества их калиевых солей и свободного гемоглобина, который обладает свойствами слабой органической кислоты: K-Hb + HCl → KCl + H-Hb. Если в кровь попадает щелочь, она реагирует с H-Hb: H-Hb + NaOH → Na-Hb + H2O. Вследствие этой реакции, вместо сильной щелочи, образуется нейтральная соль гемоглобина и вода, а величина рН среды при этом изменяется незначительно. Кроме того, система оксигемоглобин-гемоглобин участвует еще в одном своеобразном механизме поддержания постоянной величины рН крови. Как известно, венозная кровь содержит значительное количество углекислоты в виде бикарбонатов, а также связанной с гемоглобином. Через легкие углекислота выделяется в воздух, но смещения рН крови в щелочную сторону не происходит, так как образующийся оксигемоглобин является более сильной кислотой, чем гемоглобин, и избыточный бикарбонат реагирует с буферной системой оксигемоглобина с образованием калийной соли (K-HbO2): KHCO3 + H-HbO2 → K-HbO2 + H2CO3. Нарушенное равновесие между углекислотой и бикарбонатом восстанавливается. В этом процессе роль основного буфера выполняет система оксигемоглобина. В тканях и в артериальных капиллярах под влиянием низкого парциального давления кислорода оксигемоглобин диссоциирует, и кислород диффундирует в ткани. Образованный при этом свободный гемоглобин (H-Hb) и калия гидрокарбонат не изменяют рН крови в щелочную сторону, поскольку в кровь из тканей поступает большое количество углекислоты и других кислореагирующих продуктов обмена веществ. Здесь основное значение имеет буферная система гемоглобина. 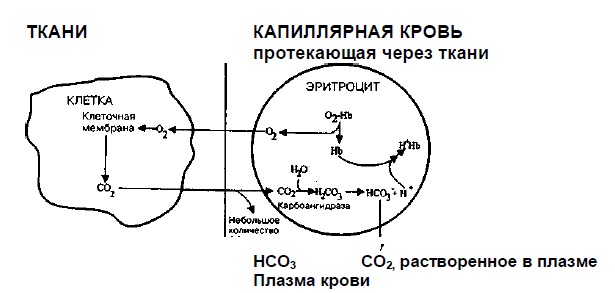 Рис.1 Доставка 02 к тканям и первые стадии элиминации CO2 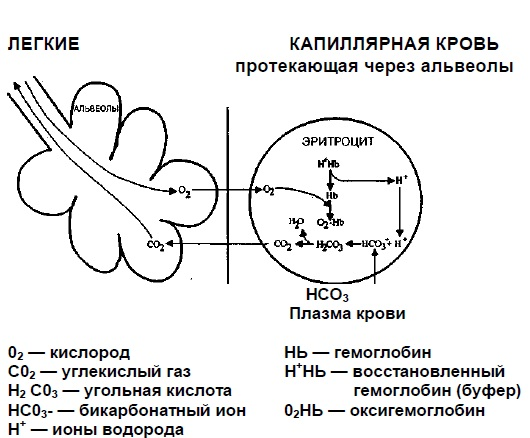 Рис.2 В легких бикарбонат снова превращается в С02 и выводится Фосфатная буферная система имеет важнейшее значение в тканях почек и таких биологических жидкостях, как моча и соки пищеварительных желез. Фосфатный буфер состоит из однозамещенной и двузамещенной солей ортофосфорной кислоты - МН2РО4 и М2НРО4, где M - металл. Первая имеет роль слабой кислоты, а вторая - щелочнореагирующей соли. В крови отношение MH2PO4: M2HPO4 составляет 1: 4. Восстановление фосфатного буфера происходит медленнее, чем гидрокарбонатного. Буферность белков обусловлена наличием в их структуре карбоксильной группы-СООН, которая придает им свойства слабодиссоциированной белок-кислоты (Pt-COOH) и ее соли с сильной щелочью (Pt-COONa). Механизм действия белкового буфера подобный механизму других буферов. Но белки обладают также амфотерными свойствами, поскольку в состав молекул белка входят группы - COOH и - NH2. Поэтому даже отдельная белковая молекула проявляет буферное действие, связывая кислоты и щелочи с образованием солей. То есть, при добавлении сильной кислоты образуется слабокислая соль белка, а при добавлении щелочи - слабощелочная соль белка. Буферные системы играют важную роль в регуляции кислотно-щелочного баланса, которая осуществляется как на клеточном, так и органном уровнях. Клетки является постоянным источником образования С02 и нелетучих кислот. Показателем, который в значительной мере отражает количество созданных или задержанных в организме нелетучих кислот, является анионный интервал (Al) плазмы крови. Величина AI рассчитывается как разница концентрации натрия и двух главных анионов - хлорида и карбоната: AI = [Na+] - { [Сl-] + [НС03-] }. Проявлением способности клеток использовать ионы водорода является изменение концентрации ионов калия в плазме. Проникновение ионов водорода в клетку сопровождается освобождением в ней эквивалентного количества ионов калия. Это означает, что ацидоз чаще сопровождается гиперкалиемией, а алкалоз - гипокалиемией. Большое количество CO2, а также нелетучих кислот, образующихся в организме, выделяется, и поэтому регуляция их выделения становится важнейшим элементом поддержания кислотно-щелочного баланса. Фактически только легкие и почки являются органами, которые отвечают за процесс выделения CO2 и нелетучих кислот. Другие органы могут существенно изменять кислотно-щелочной баланс, но не способны заменить выделительную функцию дыхательной системы и почек. Главная функция легких в поддержании кислотно-щелочного баланса в организме заключается в сохранении оптимальной концентрации угольной кислоты в крови, поскольку углекислый газ и вода образуются не только в результате реакции гидрокарбонатной буферной системы с более сильными кислотами, а также конечными продуктами обмена в организме, поэтому удаление избыточного углекислого газа имеет для организма важное физиологическое значение. CO2 является специфическим раздражителем дыхательного центра: при накоплении в организме угольной кислоты и повышении парциального давления углекислого газа возникает компенсаторная гипервентиляция. При этом избыток углекислого газа выделяется с выдыхаемым воздухом. При избыточном поступлении основных компонентов для их нейтрализации требуется повышенное количество углекислоты. При уменьшении содержания угольной кислоты снижается также концентрация углекислого газа и стимуляция дыхательной центра, вследствие чего возникает гиповентиляция, что приводит к сохранению СО2, восстановления запасов Н2СО3 в крови и выравнивания соотношения [H2CO3]: [HCO3-] = 1: 20. Дыхательный центр очень чувствителен к изменению рН, парциального давления CO2 и О2 в крови. Изменение рН в пределах ± 0,1 соответственно увеличивает или уменьшает вентиляцию в два раза. Повышение парциального давления CO2 на 10 мм рт. ст. (1,3 кПа) увеличивает вентиляцию в 4 раза, а при 70 мм рт. ст. (9,3 кПа) она увеличивается в 10 раз. По сравнению с почками, легкие выделяют за сутки примерно в 200 раз больше кислых продуктов в форме СО2, постоянно восстанавливая нарушенный баланс между гидрокарбонатом и угольной кислотой. Легкие, кроме регуляции выделения СО2, обеспечивают поставку кислорода. Поэтому функцию дыхательной системы характеризует не только парциальное давление СО2 (рС02), но и показатели кислородного равновесия: парциальное давление О2 (р02), насыщение гемоглобина кислородом, а также общее содержание кислорода в крови. Одной из основных функций почек является поставка в кровоток дополнительного количества бикарбонатных ионов, которые уравновешивают образование в организме ионов водорода. Эту функцию почки выполняют двумя путями: а) увеличением реабсорбции в проксимальных канальцах гидрокарбонатов из первичной мочи; б) секрецией и выделением ионов водорода с мочой. Существует несколько механизмов экскреции ионов H+: а) угольная кислота, которая образуется в эпителии канальцев, реагирует с Na2HPO4.[Na2HPO4 + H2CO3 = NaH2PO4 (выделяется с мочой) + NaHCO3 (возвращается в кровь и тем самым почки не только сохраняют натрий, но и восстанавливают щелочной резерв крови)]. Соотношение кислого и щелочного фосфата [NaH2PO4: Na2HРO4] в моче составляет 9: 1, иногда доходит до 50: 1, в то время как в первичной моче оно такое же, как и в плазме - 1: 4. При значительной концентрации Na2HРO4 в моче реакция ее становится кислой; б) значительное количество солей органических кислот, которые выделяются из организма, в почках замещают ионы Na+ и K+ на ион H+ и выводятся с мочой в виде кислот. При тяжелых формах ацидоза почки выводят в 10 раз больше ионов H+ и концентрация их в конечной моче может в 800 раз превышать концентрацию этих ионов в крови; в) в эпителии почечных канальцев постоянно происходит образование аммиака. Он связывается в просвете канальцев с ионами H+, образуя ионы аммония, который в дальнейшем выводится с мочой в виде аммонийных солей. Ионы аммония могут замещать ионы Na+ и K+ в солях неорганических кислот, которые выделяются с мочой, сохраняя натрий для поддержания кислотно-щелочного баланса. Кроме легких и почек, в регуляции кислотно-щелочного баланса значительная роль принадлежит также печени, костной ткани и пищеварительному каналу. Роль печени в сохранении кислотно-щелочного баланса состоит в том, что в ней: а) синтезируется значительное количество белков организма - сильных буферных систем плазмы крови; б) происходит окисление органических кислот до Н2O и CO2; в) происходит синтез гликогена из молочной кислоты; г) значительное количество кислых и щелочных продуктов обмена попадает в желчь и выделяется с ней. Кости скелета содержат значительное количество ионов Na+ и значительно меньше ионов K+, Ca2+, Mg2+, которые могут обмениваться на катионы внеклеточной жидкости и ионы Н+. Поглощение ионов водорода минеральными компонентами костей сопровождается высвобождением в плазму крови катионов. Поэтому при длительных ацидозах возможна декальцинация скелета. Пищеварительный канал поддерживает постоянство водно-электролитного баланса, регулируя тем самым кислотно-щелочной баланс. Поскольку в желудке образуется НСl, а в поджелудочной железе натрия гидрокарбонат, то пищеварительный канал является источником ионов H+ и НСОз-. 2.Нарушение кислотно-щелочного балансаНарушение кислотно-щелочного баланса может проявляться в форме ацидоза или алкалоза. Ацидозы характеризируются увеличением концентрации ионов водорода по сравнению с нормой. Величина рН при этом снижается. В случаях, когда концентрация ионов водорода снижается, и накапливаются щелочные компоненты, наблюдается состояние алкалоза. Значение рН при этом повышается. Предел, несовместимый с жизнью, наступает когда рН = 8. В зависимости от механизма развития расстройств, различают четыре типа нарушений кислотно-щелочного баланса, хотя чаще они являются смешанными: метаболический и респираторный ацидоз, метаболический и респираторный алкалоз (табл.1). По степени компенсации различают компенсированные, субкомпенсированные и некомпенсированные формы. Таблица 1 - Изменения кислотно-щелочного баланса и их происхождение
Компенсированный ацидоз или алкалоз характеризуются лишь изменением концентрации НСОз--, CO2 и H+, которые направлены на нормализацию pll и протекают без изменений величины рН крови: она составляет соответственно 7,40-7,35 (компенсированный ацидоз) и 7,40-7.45 (компенсированный алкалоз). Однако, когда в тканях животных продолжают накапливаться кислые или щелочные продукты обмена веществ, степень повышения или понижения в них CO2 становится такой, что компенсация этих изменений становится невозможной. Тогда в организме животных развивается субкомпенсирований ацидоз (рН крови при этом составляет 7,34-7,25) или алкалоз (pН находится в пределах 7,46-7,55), т.е. изменение величины рН еще является незначительным (табл.2). Углубление патологии вызывает необратимые изменения показателей кислотно-щелочного баланса. Развивается некомпенсированный ацидоз (рН крови ниже 7,25) или алкалоз (рН больше 7,55). Таблица 2 - Ориентировочные показатели разных степеней ацидоза и алкалоза
Метаболический ацидоз относится к наиболее частым и тяжелым нарушениям кислотно-щелочного баланса, в основе которого лежит первичное повышение содержания в организме нелетучих кислот или потеря щелочей. Он развивается вследствие нарушений промежуточного обмена веществ в тканях и накопления в них органических кислот. Метаболический ацидоз является следствием многих патологий - сердечно-сосудистой недостаточности, гипоксии, вызванной болезнями легких и анемиями, поражения почек, диабете. Метаболический ацидоз характеризуется снижением величины рН крови, бикарбоната и буферных оснований крови, парциального давления углекислоты, значительным дефицитом буферных оснований. При метаболическом ацидозе снижается сродство гемоглобина к кислороду. Это означает, что образование оксигемоглобина в легких утрудняется, но при умеренном ацидозе гемоглобин легче отдает кислород тканям. Под воздействием кислых продуктов обмена веществ подавляется функция миокарда и нарушается сердечный ритм (при рН <7,25). Сосуды миокарда сужаются, что приводит к уменьшению в них кровообращения. Вследствие снижения АД уменьшается кровоснабжение головного мозга и почек, нарушается выделительная функция почек, и в организме накапливаются токсические продукты обмена веществ, в частности аммиак. При метаболическом ацидозе наблюдаются признаки нарушения водно-солевого обмена. Вследствие удержания воды в межклеточной среде и нарушения гемодинамики, ткани становятся гидрофильными. Одновременно в клетке происходит электролитическая переориентация, при которой в плазме крови увеличивается содержание H+, K+, Na+, Сl-, органических кислот и уменьшается - НСОз--. Ацидоз рефлекторно усиливает функцию надпочечников. В крови растет уровень катехоламинов, в частности адреналина, который обеспечивает поддержания кровяного давления в пределах нормы. Респираторный ацидоз развивается при избытке в организме CO2 и повышении рСО2 (гиперкапнии) вследствие снижения легочной вентиляции. Гиповентиляция легких и гиперкапния наблюдаются при бронхитах и пневмониях, отеке легких, злокачественных опухолях, сердечно-сосудистой недостаточности, снижении возбудимости дыхательного центра при травмах мозга, кровоизлиянии в мозг, увеличении внутричерепного давления, передозировке анальгетических, седативных препаратов и анестетиков; вдыхании воздуха с высокой концентрацией CO2 и при длительной нехватке O2. Гиперкапния приводит развитие гипоксии, что вызывает недостаточное окисление продуктов промежуточного обмена в тканях и накопление кислых метаболитов, то есть к респираторному ацидозу присоединяется метаболический и развивается смешанный ацидоз. Респираторный ацидоз приводит прежде всего к нарушениям функций нервной системы и кровообращения. Повышение концентрации CO2 обуславливает развитие ацидоза в мозговой ткани, расширение сосудов и увеличение тока крови. Поставка крови к мозгу увеличивается лишь до определенного предела, а дальнейший рост рС02 и расширение сосудов вызывает просачивание плазмы через стенку сосудов и увеличение жидкости, которая отделяет клетки мозга от сосудистого русла. При этом нарушается диффузия кислорода из крови в клетки, вследствие чего развивается гипоксия нервной ткани. Гипоксемия стимулирует гликолиз, поэтому увеличивается образование молочной кислоты, что осложняет ацидоз мозговой ткани и еще больше расширяет сосуды мозга. Диффузия плазмы возрастает, усиливает гипоксию, и таким образом образуется замкнутый круг. Ацидоз тормозит сократительную способность сердечной мышцы вследствие непосредственного воздействия повышенной концентрации H+, он вызывает также спазм венозных сосудов, в результате чего объем циркулирующей крови увеличивается, что приводит к увеличению объема и давления в сосудистом русле легких, перегрузке правого желудочка и может вызвать отек легких. Рост рСО2 приводит к сужению артериол легких и увеличение сопротивления в них, что также перегружает правый желудочек и может привести к его недостаточности, особенно у больных, у которых уже развился синдром "легочного сердца". Компенсация респираторного ацидоза осуществляется почками так же, как и при метаболическом ацидозе: Na2HPO4 + Н2СО3 →NaН2PO4 +NaHCО3. Кроме того, вследствие накопления CO2 происходит возбуждение дыхательного центра, что приводит к гипервептиляции легких за счет тахипноэ. Иногда за счет этого удается достичь максимальной элиминации CO2 из крови через легкие. Для нейтрализации CO2 до H2CO3 используются также основные компоненты буферных систем, прежде всего гидрокарбонатной. Развитие процесса компенсации является быстрым, но заметить признаки повышения HCO3 - можно только через 2-3 дня с момента появления ацидоза. Поэтому лечебные процедуры при респираторном ацидозе должны быть направлены на улучшение альвеолярной вентиляции. Метаболический алкалоз развивается при накоплении в организме щелочей, усиленной потере нелетучих кислот, избыточном выведении почками H+. Алкалоз характеризуется увеличением величины рН крови, буферных оснований, аниона угольной кислоты (НСО3--). Респираторный алкалоз развивается при избыточном выведении из организма СО2 (гипокапния), возникающая вследствие гипервентиляции легких, которая наблюдается при непосредственном воздействии на дыхательный центр различных токсических продуктов (в том числе аммиака), на начальных стадиях пневмонии. Парциальное давление СО2 снижается, поэтому величина рН крови увеличивается. Компенсируется алкалоз почками, которые выводят ионы НСОз - и задерживают ионы H+. Реакция мочи становится щелочной. Основным следствием респираторного и метаболического алкалоза является снижение тонуса гладких мышц сосудов мозга, сердца, легких, при этом снижается артериальное давление и уменьшается ток крови через эти органы. Механизмы устранения алкалоза заключаются в использовании кислотных компонентов буферных систем, но они значительно слабее по сравнению с механизмами устранения ацидоза. 2.Нарушение кислотно-щелочного балансаНарушение кислотно-щелочного баланса может проявляться в форме ацидоза или алкалоза. Ацидозы характеризируются увеличением концентрации ионов водорода по сравнению с нормой. Величина рН при этом снижается. В случаях, когда концентрация ионов водорода снижается, и накапливаются щелочные компоненты, наблюдается состояние алкалоза. Значение рН при этом повышается. Предел, несовместимый с жизнью, наступает когда рН = 8. В зависимости от механизма развития расстройств, различают четыре типа нарушений кислотно-щелочного баланса, хотя чаще они являются смешанными: метаболический и респираторный ацидоз, метаболический и респираторный алкалоз (табл.1). По степени компенсации различают компенсированные, субкомпенсированные и некомпенсированные формы.
Компенсированный ацидоз или алкалоз характеризуются лишь изменением концентрации НСОз--, CO2 и H+, которые направлены на нормализацию pll и протекают без изменений величины рН крови: она составляет соответственно 7,40-7,35 (компенсированный ацидоз) и 7,40-7.45 (компенсированный алкалоз). Однако, когда в тканях животных продолжают накапливаться кислые или щелочные продукты обмена веществ, степень повышения или понижения в них CO2 становится такой, что компенсация этих изменений становится невозможной. Тогда в организме животных развивается субкомпенсирований ацидоз (рН крови при этом составляет 7,34-7,25) или алкалоз (pН находится в пределах 7,46-7,55), т.е. изменение величины рН еще является незначительным (табл.2). Углубление патологии вызывает необратимые изменения показателей кислотно-щелочного баланса. Развивается некомпенсированный ацидоз (рН крови ниже 7,25) или алкалоз (рН больше 7,55). Таблица 2 - Ориентировочные показатели разных степеней ацидоза и алкалоза
Метаболический ацидоз относится к наиболее частым и тяжелым нарушениям кислотно-щелочного баланса, в основе которого лежит первичное повышение содержания в организме нелетучих кислот или потеря щелочей. Он развивается вследствие нарушений промежуточного обмена веществ в тканях и накопления в них органических кислот (молочной, пировиноградной, ацетоуксусной и др.)., фосфатов, сульфатов; при недостаточном выделении или распаде этих метаболитов пораженными органами - печенью, легкими, почками, кишечником, при скармливании животным некачественных кормов (кислый жом, барда, силос, сенаж), содержащие избыток органических кислот (масляной, уксусной, молочной). При этом гидрокарбонаты используются для нейтрализации их изомеров, в тканях животных не метаболизируются и выделяются в виде натриевих и калиевых солей. Респираторный ацидоз развивается при избытке в организме CO2 и повышении рСО2 (гиперкапнии) вследствие снижения легочной вентиляции. Гиповентиляция легких и гиперкапния наблюдаются при бронхитах и пневмониях, альвеолярной эмфиземе, ателектазе и отеке легких, злокачественных опухолях, экссудативном плеврите, пневмотораксе, сердечно-сосудистой недостаточности, повышении внутрибрюшного давления (тимпания рубца, острое расширение желудка, метеоризм кишечника), снижении возбудимости дыхательного центра при травмах мозга, кровоизлиянии в мозг, увеличении внутричерепного давления, передозировке анальгетических, седативных препаратов и анестетиков; вдыхании воздуха с высокой концентрацией CO2 и при длительной нехватке O2. Гиперкапния приводит развитие гипоксии, что вызывает недостаточное окисление продуктов промежуточного обмена в тканях и накопление кислых метаболитов, то есть к респираторному ацидозу присоединяется метаболический и развивается смешанный ацидоз. Респираторный ацидоз приводит прежде всего к нарушениям функций нервной системы и кровообращения. Повышение концентрации CO2 обуславливает развитие ацидоза в мозговой ткани, расширение сосудов и увеличение тока крови. Поставка крови к мозгу увеличивается лишь до определенного предела, а дальнейший рост рС02 и расширение сосудов вызывает просачивание плазмы через стенку сосудов и увеличение жидкости, которая отделяет клетки мозга от сосудистого русла. При этом нарушается диффузия кислорода из крови в клетки, вследствие чего развивается гипоксия нервной ткани. Гипоксемия стимулирует гликолиз, поэтому увеличивается образование молочной кислоты, что осложняет ацидоз мозговой ткани и еще больше расширяет сосуды мозга. Диффузия плазмы возрастает, усиливает гипоксию, и таким образом образуется замкнутый круг. Заключение Кислотно-щелочной баланс – это наш индикатор здоровья. Чем мы «кислее», тем скорее стареем и больше болеем. Для нормальной работы всех внутренних органов уровень рН в организме должен быть щелочным, в интервале от 7 до 9. Тело человека – это 70% воды. Поэтому качество воды, ее свойства являются основным условием хорошего здоровья и долговечности. Жизнь – это ни что иное, как движение жидкостей в клетках и между ними, при нарушении которого, человек заболевает. Поэтому необходимо кушать больше свежих фруктов и овощей для того, чтобы защитить свои клетки от стресса, старения и гибели, а организм от окисления. Щелочная вода и свежая растительная пища помогают нам сохранить молодость и красоту. А злоупотребление мясными, молочными продуктами и алкогольными/безалкогольными напитками, кофе, газированные напитки и прочее приводит к закислению организма и является причиной многих заболеваний. Список использованной литературы В.П. Комов, В.Н.Шведова "Биохимия: Учеб. для вузов" - М.: Дрофа, 2004 Евстратова К.И., Купина Н.А., Малахова Е.Е. "Физическая и коллоидная химия" - М.: Высш. шк., 1990 Большая медицинская энциклопедия (том 6); | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
