Полушин Ю.С Руководство. Руководство по анестезиологии и реаниматологии под редакцией профессора Ю. С. Полушина
 Скачать 4.32 Mb. Скачать 4.32 Mb.
|
4.3. Анатомо-физиологические основы учения о болиНесмотря на пристальное внимание к проблеме аналгезии, до сих пор нет общепризнанного определения, что же такое боль. В отличие от сенсорных ощущений (осязание, слух и т.п.) она не является мономодальным чувством и возникает не только при раздражении сенсорных рецепторов. Боль – это не просто симптом многих острых и хронических заболеваний, но и сложный психофизиологический феномен, вовлекающий механизмы формирования эмоций, моторные, гуморальные и гемодинамические проявления, в целом идентичные комплексу стресс-реакции на неблагоприятные воздействия. Установлено, что возникающая при повреждении тканей боль носит фазовый характер: сначала она острая и хорошо локализованная, а затем через несколько секунд сменяется разлитой, менее острой и более эмоционально окрашенной. Такую динамику болевых ощущений связывают с участием различных афферентных систем в проведении ноцицептивных импульсов. П.К. Анохин (1958) рассматривал боль как своеобразное психическое состояние человека, определяющееся совокупностью физиологических процессов в центральной нервной системе, вызванных к жизни каким-либо сверхсильным или разрушительным раздражителем. Крупный английский физиолог Ч. Шерингтон определил ее как психическое дополнение защитного рефлекса. Однако собственно ощущение боли (ее перцептуальный компонент) далеко не исчерпывает всей полноты реакций, которые развиваются в ответ на повреждение. В совокупности болевая реакция является системной, а это свидетельствует о чрезвычайной сложности ее механизмов. 4.3.1. Нейрофизиологические механизмы болиВедущая роль в формировании реакции организма на повреждение принадлежит нервной и эндокринной системам. При этом нейро-физиологические процессы в ЦНС развертываются в основном под влиянием потока ноцицептивных импульсов, берущих начало в соответствующих рецепторах поврежденных тканей. Но это нередко, особенно при тяжелой травме, не единственный источник импульсации, возбуждающей структуры ЦНС. Например, при сопутствующей травме кровопотере, гипоксемии, ацидозе возбуждающая импульсация исходит также от баро- и хеморецепторов. Раздражающее влияние на структуры мозга, контролирующие через афферентные пути системы жизнеобеспечения организма, часто усугубляются влиянием со стороны психической сферы. Имеет значение и прямое возбуждающее влияние на ЦНС некоторых биологически активных веществ, попадающих в кровоток из разрушенных тканей. Рецепторы, воспринимающие повреждение тканей и формирующие афферентный поток импульсов, являются специфическими. Они получили название болевых. В современной литературе широко используется термин «ноцицептор» в качестве аналога «болевого рецептора», так как разные по своей модальности стимулы, способные вызвать боль, являются следствием повреждения тканей – ноцицепции (по Ч. Шерингтону, 1900). Гипотезу о существовании специфических болевых рецепторов первым выдвинул M. Frey (1894). В настоящее время считается, что они представляют собой свободные нервные окончания немиелинизированных волокон и имеют множество концевых разветвлений с мелкими аксоплазматическими отростками, образующими плексиморфные сплетения в различных тканях и органах. В зависимости от возбуждающих факторов выделяют две их разновидности: механорецепторы (реагирующие на само повреждение) и хеморецепторы (реагирующие на результат этого повреждения). Раздражение первых происходит в результате деформации структур клеток в поврежденных тканях. Вторые возбуждаются веществами, которые в физиологических условиях в тканях отсутствуют или содержатся в незначительных количествах. Выделяют 3 типа таких веществ - тканевые (серотонин, гистамин, ацетилхолин, некоторые простагландины, ионы К+ и Н+), плазменные (брадикинин, каллидин) и выделяющиеся из нервных окончаний (субстанция Р и др.). Допускается, что одни субстанции, содержащиеся в основном в тканях, непосредственно активируют концевые разветвления немиелинизированных волокон и приводят к импульсной активности высокопороговых кожных, висцеральных и мышечных афферентов. Они вызывают ощущение боли у человека и псевдоаффективную ноцицептивную реакцию у животных при аппликации на ткани. Другие (кинины и пр.), сами не вызывающие боль, усиливают эффект ноцицептивного воздействия иной модальности. Cубстанция Р выделяется непосредственно из терминалей и взаимодействует с рецепторами, локализованными на их мембране. Деполяризуя ее, она вызывает генерацию импульсного ноцицептивного потока. Предполагается, что субстанция Р, содержащаяся в сенсорных нейронах спинномозговых ганглиев, действует и как синаптический передатчик в нейронах заднего рога спинного мозга. В качестве химических агентов, активирующих свободные нервные окончания, рассматриваются в том числе и не идентифицированные до конца вещества или продукты разрушения тканей, образующиеся при сильных повреждающих воздействиях, при воспалении, при локальной гипоксии. Например, арахидоновая кислота в нормальных условиях эстерифицируется и входит в состав фосфолипидов клеточных мембран. После повреждения клетки под действием активированного фермента фосфолипазы А она высвобождается из клеточных мембран. Под действием фермента циклооксигеназы на арахидоновую кислоту образуются простагландины (в частности простогландин Е2). Последние усиливают трансдукцию, сенсибилизируя ноцицепторы к влиянию других алгогенных соединений. Процесс перевозбуждения периферических рецепторов (ноцицепторов) под воздействием алгогенов носит название первичной гипералгезии (сенситизации). Он имеет первостепенное значение в развитии боли вообще, а при воспалении в особенности. Рассматриваемые виды ноцицептивных рецепторов распределены в тканях неравномерно. Механорецепторов больше в поверхностных слоях кожи, в фасциях, суставных сумках; хеморецепторы имеют более высокую концентрацию в глубоких слоях кожи, стенках сосудов, в висцеральных оболочках. Процесс, при котором повреждающее воздействие трансформируется в виде электрической активности на окончаниях чувствительных нервов носит название трансдукции. Истинные механизмы этого процесса пока неясны. Предполагают, что трансформация разномодальных раздражителей в электрический импульс осуществляется независимыми механизмами. Наряду с трансдукцией ноцицепцию составляют еще 3 физиологических процесса: трансмиссия, модуляция, перцепция (рис. 4.2). 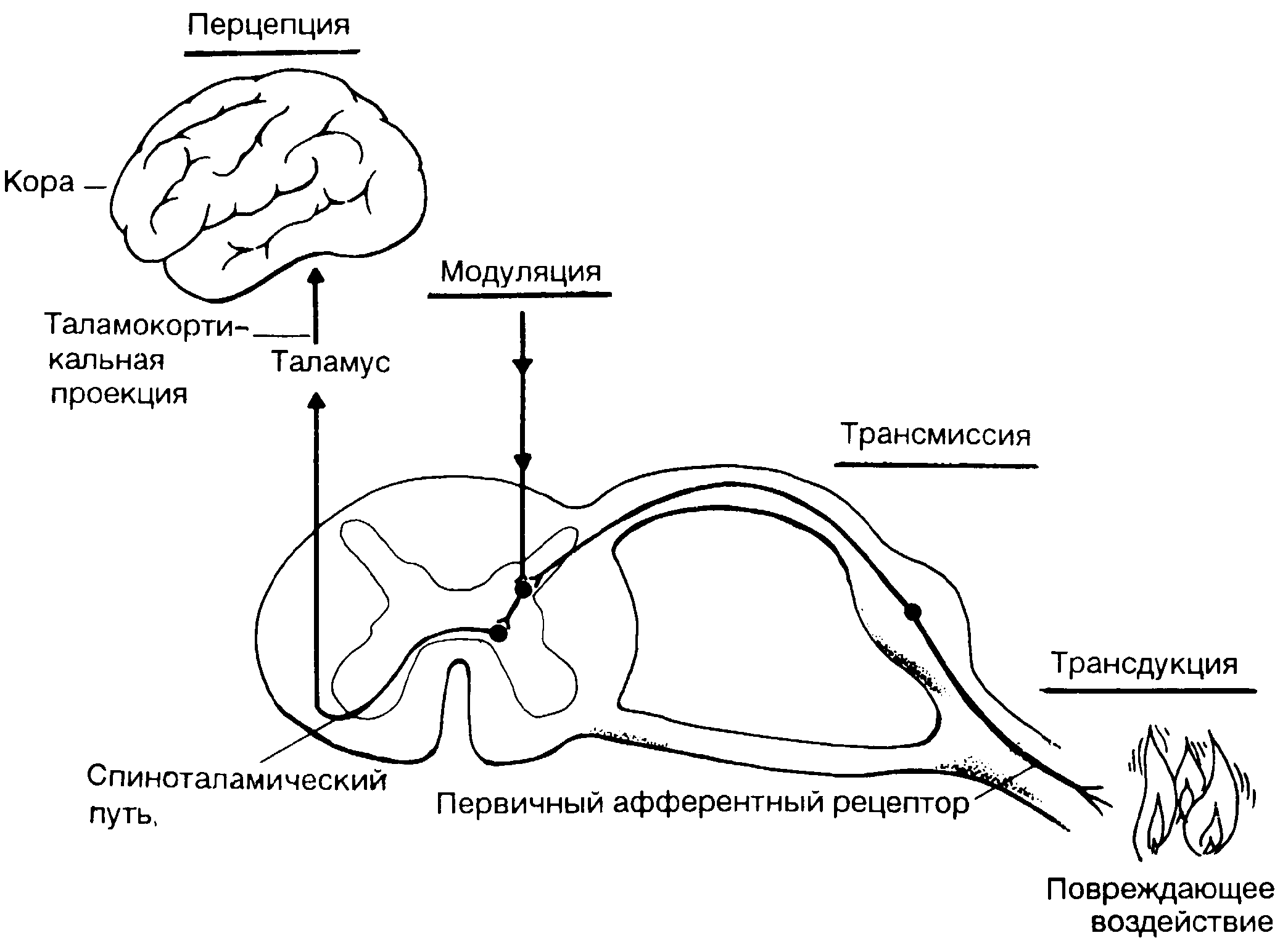 Рис. 4.2. Схема механизма ноцицептивных реакций (по N. Katz, F.M. Ferrante) Трансмиссия - проведение возникших импульсов по системе чувствительных нервов. Проводящие пути, ее обеспечивающие, сформированы из трех компонентов: - первичного чувствительного афферентного нейрона, доходящего до спинного мозга, - восходящего промежуточного нейрона, простирающегося от спинного мозга до стволовой части головного мозга и таламуса, - таламокортикальных проекций. Модуляция - это процесс, при котором ноцицептивная трансмиссия модифицируется под влиянием нейрональных воздействий. Перцепция является финальным процессом, при котором трансдукция, трансмиссия и модуляция, взаимодействуя с индивидуальными физиологическими особенностями личности, создают конечное субъективное эмоциональное ощущение, воспринимаемое как боль. От рецепторов возбуждение передается по нервным волокнам, которые являются аксонами нейронов межпозвонковых ганглиев. Структура и проводимость их неодинаковы. Применительно к импульсам, имеющим отношение к повреждению, выделяют волокна, обозначаемые латинскими буквами "А" и "С". Первые имеют хорошо выраженную миелиновую оболочку, связаны в основном с механорецепторами и обладают высокой скоростью проведения возбуждения (более 3 м/с). Среди них выделяют: а) Aβ (Аα) – толстые волокна, передающие импульсы с высокой скоростью (35 – 100 м/с) и ответственные за низкопороговую механочувствительность, например при прикосновении; б) А-волокна – более тонкие, передающие импульсы со скоростью 3-30 м/с. Они отвечают за передачу быстрой острой боли и с ноцицепторов, и с терморецепторов. Волокна же "С" еще тоньше, имеют скудную миелиновую оболочку и низкую проводимость (0,2-2 м/с) и связаны с тупой, длительной, истощающей болью, они особенно чувствительны к химическим воздействиям. Основными проводниками кожной и висцеральной болевой чувствительности считают А- и С-волокна. Афферентные миелинизированные волокна большого диаметра не повышают свою активность в ответ на повреждающую стимуляцию и поэтому не могут участвовать в ноцицепции. При сопоставлении ощущения боли у человека со спектром вовлеченных в возбуждение афферентных волокон при раздражении кожных нервов было убедительно показано, что «первичная» боль связана с афферентной импульсацией в А-волокнах, а «вторичная» - с С-волокнами. Нарушение проведения возбуждения в миелиновых волокнах (сдавление, ишемия) приводит к ослаблению «первичной» боли, но «вторичная» боль может даже усиливаться. Афферентные волокна различного калибра по-разному распределяются уже в задних корешках перед их входом в спинной мозг – толстые миелинизированные проводники занимают их медиальную часть, а тонкие миелинизированные и С-волокна располагаются более латерально. Перерезка этих латеральных пучков сопровождается уменьшением боли. Клетки чувствительных нейронов расположены в межпозвоночном ганглии (ганглии заднего корешка). Их центральный отросток проникает в задний рог спинного мозга в составе заднего корешка, а передний отросток входит в состав спинномозгового нерва. После входа в спинной мозг Аδ и С- волокна в составе тракта Лиссауэра идут в каудальном и ростральном направлениях в пределах 1-2 сегментов и оканчиваются в дорсальной части заднего рога (рис. 4.3). Нейрональная система заднего рога спинного мозга является первым центральным звеном, воспринимающим разномодальную афферентную информацию. Задние рога спинного мозга служат первой "релейной станцией" на пути импульсации к вышележащим отделам ЦНС. Именно здесь происходит взаимодействие между каналами болевой и неболевой чувствительности, на основании которого формируется поток восходящей испульсации нового качества и происходит переключение нервных волокон на нейроны второго порядка, а также на двигательные и симпатические нейроны с образованием сегментарной эфферентации к исполнительным структурам. А  Б 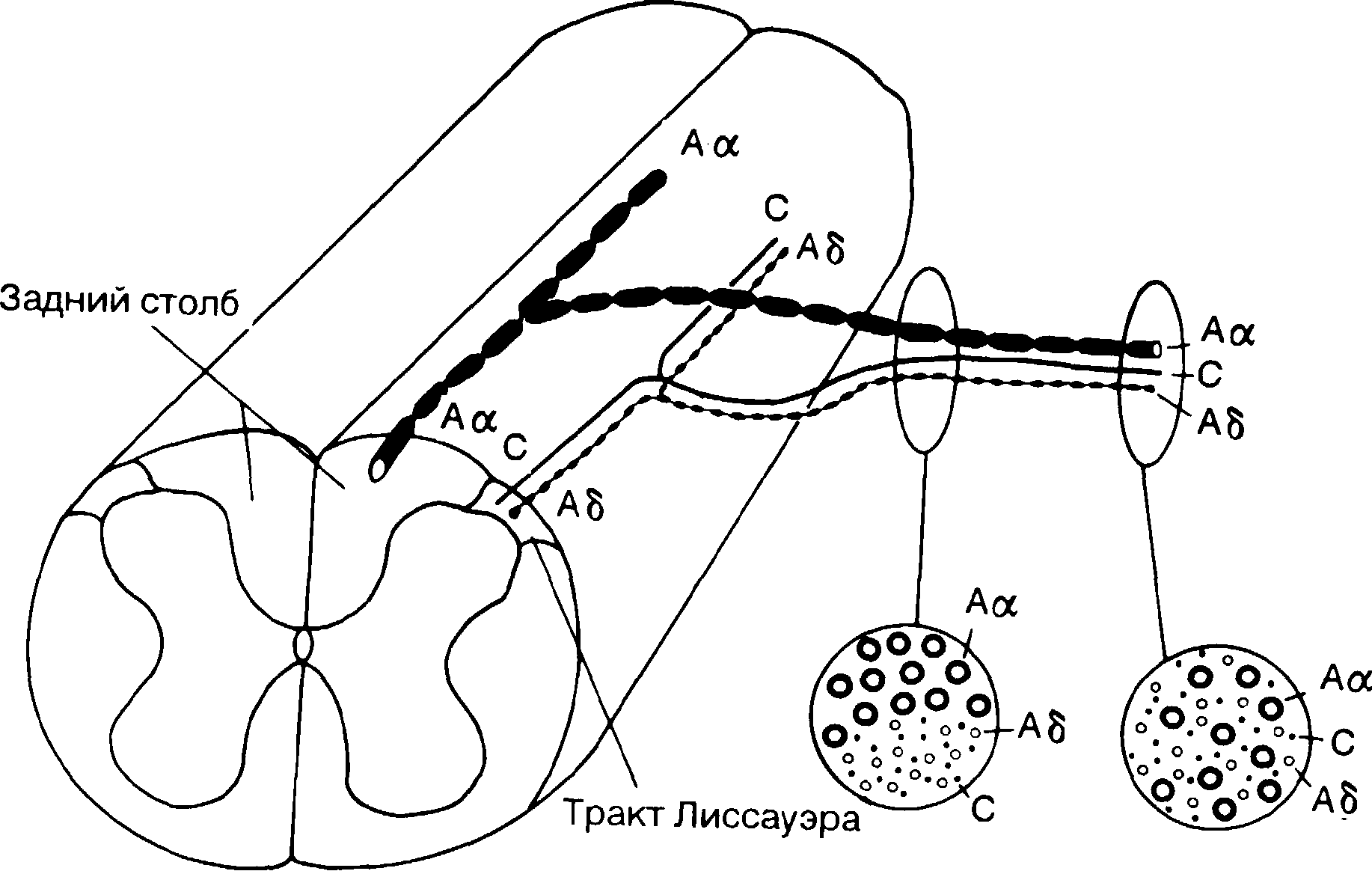 Рис. 4.3. Схема сегментарных анатомических структур, участвующих в формировании болевой реакции (А), и расположения волокон по отношению друг к другу В настоящее время считают, что формирование восходящего ноцицептивного потока в спинном мозге происходит не только на основании взаимодействия разномодальных афферентных входов на релейных (конвергентных) нейронах, но и в результате возбуждения «специфических болевых» нейронов, имеющих восходящие проекции. Предполагают, что активация этих нейронов происходит под воздействием различных биологически активных соединений (некоторых нейропептидов, в частности серотонина, активирующих аминокислот и пр.), которые являются нейротрансмиттерами при передаче ноцицептивного импульса. Интересно, что они могут опосредовать повторную стимуляцию ноцицептивных нейронов и повышать их чувствительность к привходящим импульсам. Данный эффект называют вторичной гипералгезией (сенситизацией). К числу модуляторов сенситизации (вторичной или центральной) относят субстанцию Р, вазоинтестинальный пептид, холецистокинин, ангиотензин, аланин, возбуждающие аминокислоты L-глутамат и L-аспартат. На мембране нейронов находятся рецепторы, связанные с L-белком. Нейромедиаторы взаимодействуют с этими рецепторами, изменяя возбудимость мембраны нейрона и вызывая выход ионов кальция из внутриклеточных депо. Активация NMDA (N-methyl-D-aspartate) – рецепторов увеличивает концентрацию внутриклеточного кальция в спинномозговых нейронах и активизирует фосфолипазу, что в конечном счете приводит к простагландиногенезу. Наряду с этим ноцицептивные импульсы распространяются по восходящим путям спинного мозга. Различают две классические восходящие афферентные системы. Одна из них (лемнисковая) в пределах спинного мозга располагается в дорсальной и дорсолатеральной зоне белого вещества, другая (экстралемнисковая) – в его вентролатеральной (антеролатеральной) части. Лемнисковая система включает задние столбы спинного мозга, спиноцервикальный и неоспиноталамический тракты. Последний имеет прямое отношение к интеграции болевой перцепции и к проявлению первичной, т.е. хорошо локализованной боли. Экстралемнисковые пути расположены в боковых столбах спинного мозга. В зависимости от места окончания восходящая антеролатеральная система разделяется на 3 основных тракта – спиноталамический, спиноретикулярный и спиномезенцефалический. Первый из них обозначается как неоспиноталамический, а два других объединяются в палеоспино-таламический тракт. Спиноталамический тракт обеспечивает проведение болевых и температурных импульсов. В стволе головного мозга спиноталамический тракт располагается дорсолатеральнее пирамид и не прерываясь достигает вентральных постериолатеральных и частично интраламинарных ядер таламуса. Он состоит из быстропроводящих волокон, несет чувствительную распознающую информацию в зрительный бугор, в конкретные зоны сенсорной коры и реализует информацию о локализации, идентификации и интенсивности боли. Спиноретикулярный тракт оканчивается в каудальной части ствола мозга. Он состоит из медленно проводящих волокон, отдает диффузные проекции в ретикулярную формацию ствола, околоводопроводное вещество, ядра шва, гипоталамус, лимбическую систему, лобные доли и таламус и играет главную роль в формировании аффективных, мотивационных и поведенческих реакций. Спиномезенцефалический тракт иногда рассматривается как компонент спиноретикулоталамической системы, поскольку он формируется аксонами нейронов тех же пластин, где локализованы спиноретикулярные клетки. Оканчивается спиномезенцефалический тракт в ретикулярной формации среднего мозга, в центральном сером веществе и в таламусе. Лемнисковая и экстралемнисковая системы функционируют в тесном взаимодействии, и феномен боли обусловлен интегративным взаимовлиянием этих систем (А.В. Вальдман, Ю.Д. Игнатов, 1976). Одной из главных супрасегментарных зон восприятия афферентного притока и его переработки является ретикулярная формация среднего мозга. Она не только является важной релейной (второй) станцией передачи ноцицептивной информации, но и осуществляет ее анализ и интеграцию. Здесь оканчиваются пути и (или) коллатерали восходящих систем и начинается диффузная проприоретикулярная система, а также восходящие проекции к вентробазальным и интраламинарным ядрам таламуса и далее - в соматосенсорную зону коры головного мозга. Через связи ретикулярной формации с гипоталамусом, базальными ядрами и лимбическим мозгом реализуются нейроэндокринные и эмоционально-аффективные компоненты боли, сопровождающие реакции защиты, бегства или нападения в ответ на повреждающие воздействия. Прямые и опосредованные многочисленные проекции ретикулярной формации в кору определяют ее участие в реакциях пробуждения, настораживания на повреждающие стимулы, в формировании ощущения боли и ее психофизиологической оценки. Конечной собирательной станцией ноцицептивной импульсации является таламус. Из его структур участие в ноцицепции принимают вентробазальный комплекс, задняя группа ядер, медиальные и интраламинарные ядра (рис.4.4). Вентробазальный комплекс состоит из двух ядер: вентрального заднебокового и вентрального заднемедиального. Два последних ядра наиболее тесно связаны с передачей боли и с нейроэндокринными реакциями на хирургический стресс. Сигналы, поступающие в вентробазальный комплекс, подвергаются обработке и уже в организованном виде проецируются в соматосенсорную зону коры. Мультисенсорная конвергенция на нейронах вентробазального комплекса обеспечивает точную соматотопическую информацию о локализации боли, ее пространственную соотнесенность и сенсорно-дискриминантный анализ. Задняя группа ядер. Ноцицептивные сигналы для этой системы ядер поступают по спино-таламическому пути и по задним столбам, передаваясь затем без соматотопической организации в ретроинсулярную зону коры и в дополнительную соматосенсорную область. Считается, что эти таламические ядра, наряду с вентробазальным комплексом, участвуют в передаче и оценке информации о локализации болевого воздействия и частично - в формировании мотивационно-аффективных компонентов боли. А 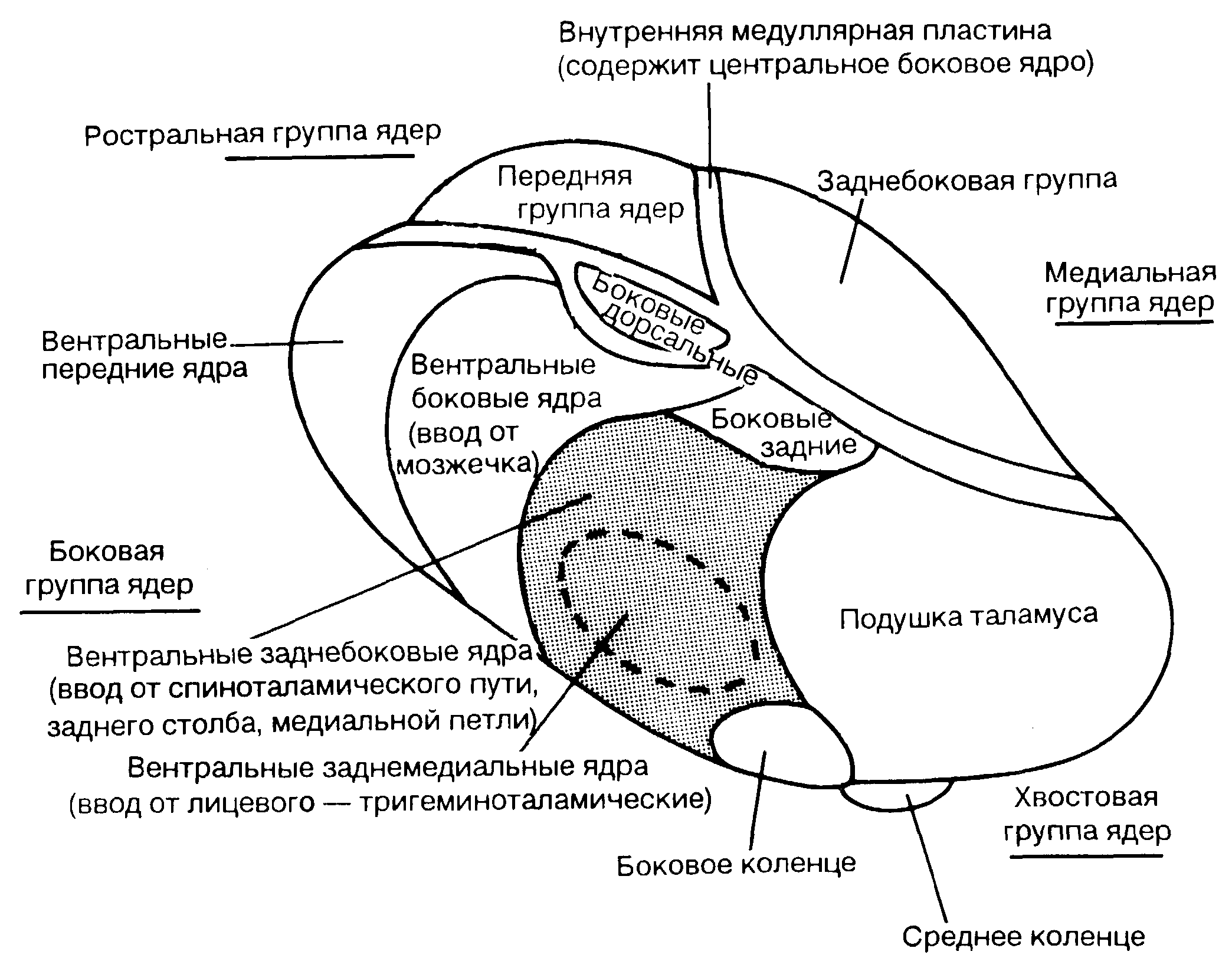 Б 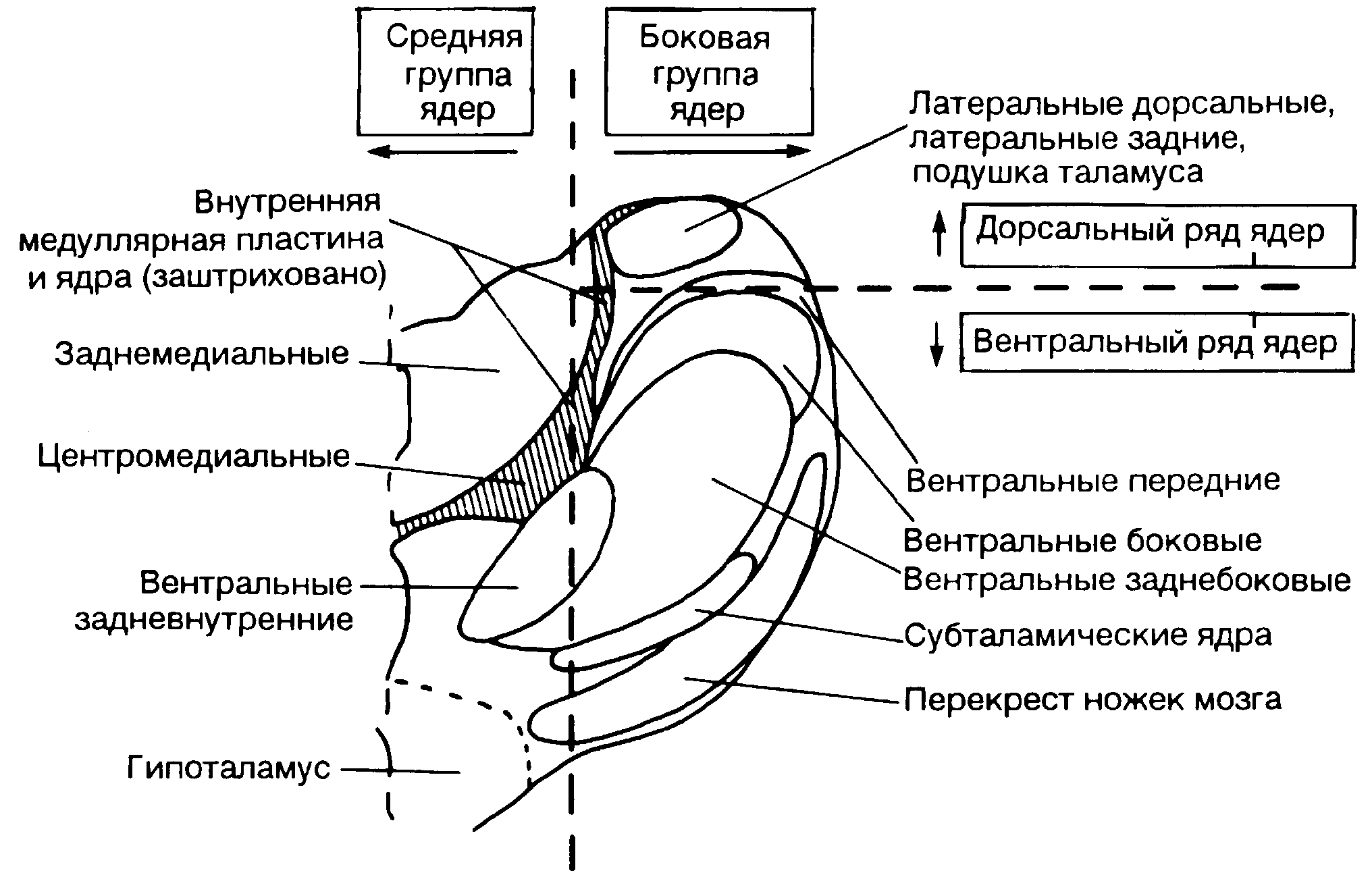 Рис. 4.4. Таламус: А - вид сверху, Б – продольный разрез Медиальные и интраламинарные ядра. К ним относятся ассоциативное медиодорсальное ядро и неспецифические интраламинарные ядра - центральное медиальное, центральное латеральное, парацентральное, парафасцикулярное и срединный центр. В них оканчиваются волокна спино-таламического тракта, а также обширные проекции из всех восходящих трактов, связанных с ноцицепцией. Клетки этих ядер отвечают на соматические, висцеральные, слуховые, зрительные и болевые стимулы. Деструкция интраламинарных и медиальных ядер у людей сопровождается аналгезией, особенно отчетливо выраженной, когда боль обусловлена преимущественной активацией высокопороговых висцеральных афферентов. Разрушение медиодорсального ядра снижает ответные реакции на боль, создает эмоциональную индифферентность (равнодушие) к боли. Медиальные и интраламинарные ядра таламуса играют основополагающую роль в интеграции «вторичной», протопатической, плохо локализованной боли. Эти ядра формируют также сложные вегетомоторные высокоинтегрированные защитные реакции на ноцицепцию, а также мотивационно-поведенческие проявления боли и ее аффективное, дискомфортное восприятие. Большое значение в формировании ноцицепции имеет и гипоталамус, как эмоциогенный и высший вегетативный центр. Особенно важно его паравентрикулярное ядро (ПВЯ), являющееся главным интегрирующим центром гуморальных и автономных реакций. Именно в этом ядре локализуются нейроны, содержащие вазопрессин (антидиуретический гормон - АДГ) и кортикотропин-рилизинг-гормон (КРГ). Нейроны этого ядра синтезируют КРГ и выделяют его в область средней возвышенности стебля гипофиза, откуда он секретируется непосредственно в кровь. Проходя по системе кровеносных сосудов к передней доле гипофиза, КРГ стимулирует высвобождение адренокортикотропного гормона (АКТГ), β-эндорфина и их поступление в общую гемоциркуляцию. Вазопрессин транспортируется из паравентрикулярного ядра и накапливается в задней доле гипофиза, откуда он секретируется в кровь. Таламус имеет двустороннюю связь с лимбической системой, полосатым телом и сенсомоторной (соматосенсорной) зоной (S1) коры больших полушарий. Именно с этой зоной связывают факт осознания человеком болевого ощущения, формирования перцептуального компонента боли. Вторая сенсомоторная зона (S2) играет ведущую роль в механизмах формирования адекватных защитных реакций организма в ответ на болевое раздражение. В формировании системной болевой реакции организма участвует не только сенсомоторные зоны коры. Происходит генерализованное возбуждение всех областей коры больших полушарий вследствие восходящих активирующих влияний ретикулярной формации. В частности, очень важное значение имеет возбуждение лобных отделов коры через связи с таламусом, гипоталамусом, лимбическими структурами, сенсомоторной зоной. Активацию данной области связывают с формированием мотивации избавления от болевых ощущений. В реализации нейроэндокринных реакций на ноцицептивные раздражители выделяют ось гипоталамус-гипофиз-надпочечники (ГГН) и симпато-адреналовую систему. Последняя накапливает и высвобождает катехоламины (норадреналин из периферических нервов и адреналин из мозгового вещества надпочечников). Система ГГН вносит свой вклад продукцией трофических гормонов гипоталамусом и стимуляцией гипофиза, выделяющего АКТГ, β-эндорфин, гормон роста и пролактин. Циркулирующий в крови АКТГ стимулирует надпочечники, которые в свою очередь усиливают секрецию кортизола и альдостерона. Нейрофизиологическим субстратом сегментарных гемодинамических реакций являются преганглионарные симпатические нейроны, локализованные в боковом роге спинного мозга. Аксоны этих нейронов не только выходят через передние корешки и достигают ганглиев, но и распространяются внутри спинного мозга, образуя проприоспинальный симпатический тракт. Посредством проприоспинальной системы преганглионарные нейроны активируются и участвуют в генерализации симпатических рефлексов. Именно вовлечение через систему проприоспинальных связей преганглионарных нейронов различных сегментов определяет сдвиги системной гемодинамики, сопряженные с изменениями регионарного кровообращения. Структура гемодинамической реакции при этом направлена на реализацию поведенческих реакций избегания или устранения вредоносного стимула и включает повышение артериального давления, увеличение сердечного выброса, сужение сосудов почек и желудочно-кишечного тракта с одновременным расширением сосудов скелетных мышц и т.д. Таким образом, болевая реакция есть интегративная реакция практически всех структур головного мозга и многих функциональных процессов, происходящих в организме и обеспечивающих активацию его защитно-приспособительных механизмов. В отличие от ноцицепции, боль – это не только сенсорная модальность, но и ощущение, эмоция и своеобразное психическое состояние. Как психофизиологический феномен она формируется на основе интеграции ноцицептивных и антиноцицептивных систем и механизмов головного мозга (Игнатов Ю.Д. и соавт.,1994). |
