КНИГА Советы молодому хирургу. Ратнер Г.Л.. Самара 1991 Аннотация
 Скачать 1.86 Mb. Скачать 1.86 Mb.
|
Как предупредить и бороться с послеоперационным парезом желудочно-кишечного трактаВ своей книге я не ставил целью рассматривать осложнения после хирургических операций, однако вынужден сделать исключение для такого осложнения, как послеоперационный парез желудочно-кишечного тракта и развивающаяся при этом клиническая картина острой динамической непроходимости кишечника. Причина этого заключается в том, что подобное осложнение встречается довольно часто, но почему-то подробно не рассматривается в учебниках и руководствах по хирургии. К тому же в большинстве случаев парез разрешается самостоятельно довольно быстро. Вместе с тем не так уж редко осложнение приводит к самым тяжелым последствиям. Во-первых, могут быть диагностические ошибки, когда за послеоперационный парез принимают острую кишечную непроходимость, развившуюся в результате наличия механического препятствия, образовавшегося вследствие самой операции. В результате необходимую повторную операцию своевременно не производят. Причинами ранней послеоперационной механической кишечной непроходимости могут быть следующие: ущемление кишки во вновь образованных и недостаточно тщательно ушитых отверстиях или в карманах брюшины после наложения анастомозов, например, в окне брыжейки поперечно-ободочной кишки; спайки; сдавления кишечной трубки воспалительным инфильтратом; заворот и узлообразование кишечника; технические ошибки хирурга: захватывание в шов стенки кишечника при зашивании брюшной раны; забытые инородные тела, а также оставление без соответствующей коррекции имеющихся спаек, инфильтрата или опухоли, вызвавших непроходимость. Больной М. с облитерирующим атеросклерозом бифуркации аорты и подвздошных артерий, которому 3 года назад было сделано бифуркационное аортобедренное шунтирование, поступил по поводу острого тромбоза шунта. Внебрюшинным доступом была обнажена аорта. Тромбированный протез удален. Поставлен новый аортобедренный бифуркационный шунт. Магистральный кровоток в конечностях был восстановлен, однако у больного после операции появился тяжелый парез кишечника, который несмотря на все лечебные мероприятия прогрессировал. Во время лапаротомии обнаружено ущемление петли тонкой кишки в отверстии брюшины на месте правой бранши удаленной тромбированного протеза. Во-вторых, имевшийся в начале парез кишечника в дальнейшем сам может оказаться причиной развития острой механической непроходимости кишечника. Больной У. был оперирован по поводу травматической диафрагмальной грыжи. Разрыв левого купола диафрагмы произошел 2 года назад в результате сдавления больного между кирпичной стенкой и бортом грузовой автомашины. Во время операции был обнаружен дефект в медиальной части купола диафрагмы размером 6-14 см. Содержимым грыжи являлись часть левой доли печени и поперечно-ободочная кишка, грыжевого мешка как такового не было. После вправления внутренностей в брюшную полость и освобождения диафрагмы из сращений была выполнена пластика грыжевых ворот с созданием дупликатуры из переднего и заднего лоскутов диафрагмы. По-видимому, в результате частичного повреждения левого блуждающего нерва у больного на следующий день после операции развился тяжелый парез желудочно-кишечного тракта. Метеоризм был сильно выражен и серьезно беспокоил больного. Дыхание была частым и поверхностным из-за того, что диафрагма оказалась высоко поднятой раздутым кишечником и желудком. Больному был поставлен постоянный зонд для разгрузки желудка и 12-перстной кишки, а также использован весь арсенал средств, направленных на стимуляцию тонуса и моторики желудочно-кишечного тракта, но эффект оказался минимальным. На третьи сутки у больного боли в животе приняли схваткообразный характер, резко усилились и начали иррадиировать в левую половину грудной клетки. При рентгенологическом исследовании были обнаружены раздутые петли кишечника, расположенные выше левого купола диафрагмы. Во время реторакотомии было установлено, что несколько швов, наложенных на диафрагму в медиальном углу раны, оказались несостоятельными, петля тощей кишки вышла в плевральную полость и ущемилась в образовавшемся в диафрагме отверстии. Кишка оказалась жизнеспособной. Она была погружена в брюшную полость. Дефект в диафрагме тщательно ушили. Парез с трудом разрешили через несколько дней. Больной поправился. Несомненно, что парез кишечника в данном случае сыграл далеко не последнюю роль в развитии недостаточности швов, наложенных на диафрагму. В-третьих, длительно существующий парез кишечника может перейти в уже необратимое состояние - паралич кишечника. В-четвертых, парез кишечника способствует появлению таких осложнений, как воспаление легких, полная или неполная эвентерация, образование дефектов по линии шва апоневроза с последующим формированием вентральных грыж, а также некоторых других осложнений. Наконец, парез кишечника иногда может быть единственным признаком вяло текущего гнойного перитонита, а несвоевременное распознавание причин пареза может привести к самым гяжелым последствиям. Одним из моих аспирантов, А.Ю. Сапожковым, было проделано большое исследование, специально посвященное вопросу ранней послеоперационной непроходимости. Прежде всего он изучил течение послеоперационного периода у 21976 больных. Вопреки общепринятому мнению, что такие явления, как вздутие живота, рвота, боли в животе, задержка стула и газов обычны для лапаротомированных больных, он нашел развитие подобной симпо-матики лишь у 425 больных, т.е. меньше, чем у 2% оперированных. У остальных же подобных явлений после операции вообще не наблюдалось. Отсюда он сделал справедливый вывод о том, что появление симптомов непроходимости желудочно-кишечного тракта, далеко не банальная реакция организма на оперативное вмешательство, а поэтому такие больные, у которых эти симптомы проявляются, должны находиться под постоянным пристальным вниманием со стороны врача. Второй вывод, к которому пришел А.Ю. Сапожков, вообще обескураживающий. Он убедительно доказал, что дифференциальный диагноз между послеоперационным парезом кишечника и ранней механической кишечной непроходимостью крайне труден, поскольку симптоматология их в первые дни после операции практически одинакова. Единственно полезными для этого оказываются лишь такие симптомы, как боль в животе схваткообразного характера, усиленная перистальтика и асимметрия живота. Причем только последний симптом отличается стабильностью, в то время как схваткообразный характер болей сменяется довольно скоро болями постоянного характера, а перистальтика быстро истощается. Исходя из этого, он предлагает вообще отказаться от попытки проведения дифференциального диагноза, а сразу приступить к энергичному лечению больного. Дифференциальный диагноз же вида послеоперационной кишечной непроходимости практически становится возможным лишь после оценки динамики изменения каждого симптома в процессе проведения лечебно-диагностических мероприятий. Лечение следует начинать с проведения консервативных мероприятий. В результате только консервативного лечения мы получили стойкий эффект у 77% больных. Вместе с тем чрезмерное увлечение консервативным лечением опасно, поскольку в ситуациях, когда необходимо оперативное вмешательство, это может привести к задержке релапаротомии. Хочу обратить ваше внимание на то, что имеется всего лишь три достоверных признака нарастания кишечной непроходимости:
Эти признаки выявляются обычно уже в первые 6-12 часов наблюдения за больным в условиях правильного и энергичного консервативного лечения и показывают, что больной подлежит неотложной операции. За десять лет проведения нами активной тактики, которая заключалась в более ранней релапаротомии при отсутствии эффекта от проводимой консервативной терапии летальность больных после релапаротомии снизилась с 52,2 до 21,7%. Исходя из этих стратегических предпосылок, я считаю возможным рекомендовать хирургам при ранней послеоперационной кишечной непроходимости четко придерживаться следующей тактики, разработанной А.Ю. Сапожковым. 1-й этап (продолжительность 4-6 часов). Обзорная рентгеноскопия или рентгенография брюшной полости, прием больным внутрь 100-150 мл взвеси сернокислого бария, проведение внутривенной инфузионной терапии с медикаментозной стимуляцией деятельности кишечника и одного сеанса гипербарической оксигенации (если есть возможность). По окончании комплекса названных лечебно-диагностических мероприятий проводится осмотр больного и контрольная рентгеноскопия (-графия) брюшной полости. Варианты:
2-й этап (продолжительность 4-6 часов). Блокада эпидурального пространства в сочетании с медикаментозной стимуляцией кишечника и сеанс ГБО. По окончании проводится осмотр больного и контрольная рентгеноскопия (-графия) брюшной полости. Варианты:
3-й этап (продолжительность 4-6 часов). Внутривенная инфузионная терапия в полном объеме, сеанс гипербарической оксигенации, медикаментозная стимуляция деятельности кишечника в комплексе с продленной эпидуральной блокадой. По окончании лечебных мероприятий проводится осмотр и контрольная рентгеноскопия (-графия) брюшной полости. Варианты:
Во время повторной операции перед хирургом стоит несколько задач. Прежде всего необходимо установить и устранить причину непроходимости желудочно-кишечного тракта. Во-вторых, следует определить жизнеспособность кишечника, принять решение о необходимости его резекции и выбрать метод восстановления про-кодимости. В-третьих, обеспечить адекватное дренирование желудочно-кишечного тракта. В-четвертых, надлежит произвести санацию брюшной полости. В-пятых, надежно закрыть операционную рану передней брюшной стенки. В случае высокой непроходимости причину ее установить бывает несложно, поскольку большая часть кишечника находится в спавшемся состоянии. При низкой же непроходимости раздутые петли кишечника являются серьезной помехой в поисках места и причины непроходимости. Иногда все-таки удается найти неизмененную петлю кишки. Тогда, идя по ней в оральном направлении, вы обязательно дойдете до места препятствия. Если такую петлю отыскать невозможно, а раздутые кишки не позволяют произвести надлежащую ревизию, то их предварительно приходится опорожнять путем пункции иглой с широким просветом, введения в просвет кишки наконечника электроотсоса или широкой трубки, а в некоторых случаях даже путем полного поперечного пересечения кишки. Последний способ используют обычно в тех случаях, когда необходимость последующей резекции кишки сомнения не вызывает. Оценивать жизнеспособность ущемленной петли кишки мы имеем право, только устранив причину непроходимости и разгрузив ее раздутый оральный отдел от содержимого либо путем опорожнения наружу, либо перераспределив содержимое в дистальные отделы кишечника. К сожалению, известная триада признаков "живой" кишки: нормализация цвета, сохранение пульсации брыжейки по ее кишечному краю и наличие перистальтики, не являются абсолютно достоверным доказательством ее жизнеспособности. Стенка кишки начинает некротизироваться прежде всего со стороны слизистой оболочки, состояние которой мы не видим. Поэтому известны случаи, когда петля кишки, оцененная на основании триады, как вполне жизнеспособная, в дальнейшем некротизируется на всю толщину стенки и происходит ее перфорация. Известны попытки определить жизнеспособность кишки более объективными методами: путем измерения импеданса, электровозбудимости, диафаноскопии, однако, к сожалению, ничего конкретного я рекомендовать не могу. Так что, пока приходится ориентироваться лишь на триаду и на собственный опыт. Другое дело, если при острой странгуляционной кишечной непроходимости мы сразу, не ликвидируя странгуляции, пойдем на резекцию ущемленной кишки, даже и не пытаясь установить, жизнеспособна ли она. Смысл подобного подхода заключается в том, чтобы надежно устранить отрицательный эффект реперфузии, возникающий после устранения странгуляции в результате включения в общий кровоток ранее выключенной части сосудистой системы брыжейки. Я лично убежден, что тяжелая интоксикация организма, наступающая после ликвидации странгуляционной непроходимости вследствие реперфузии, является основной причиной гибели больных с оставленной живой кишкой. Мое сообщение на эту тему, сделаннное на 4 Всероссийском съезде хирургов в Перми в 1973 году, вызвало бурную дискуссию, но, насколько мне известно, до сих пор последователей у меня не нашлось. В самом деле, хирургу кажется, по крайней мере, странным предложение удалять жизнеспособный кишечник, хотя это нередко позволяет спасти жизнь больного. Сегодня, когда появились такие мощные средства экстракорпоральной детоксикации, как лимфо- и гемосорбция, плазмаферез и другие, мое предложение, казалось бы, теряет смысл. Однако для тех учреждений, где этих методов детоксикации нет, оно по-прежнему остается в силе. К сожалению, настойчиво пропагандировать его я не имею права, поскольку в решениях съезда о нем ничего не было сказано, а ссылка на мой авторитет перед лицом комиссии по, разбору смертей, боюсь, хирургу не поможет. Существует известное правило: при резекции некротизированной кишки вместе с ней должно быть удалено около 30-40 см неизмененной кишки с оральной стороны и 10-15 см от ее дистальной границы. Однако, если дистальную границу резекции установить бывает просто, то определение оральной границы встречает серьезные трудности. Дело в том, что при странгуляционной непроходимости почти всегда имеет место и обтурационная непроходимость. Поэтому приводящая кишка, начиная с места странгуляции, будет резко вздута, нередко на значительном протяжении. В стенке этой кишки нарушается микроциркуляция, мускулатура кишки перерастягивается, нервные окончания и сплетения в стенке кишки страдают не только от ишемии, но и от действия на них токсического содержимого кишечника, т.е. имеются все условия для развития паралича кишки. Чем дольше длится непроходимость, тем на большем расстоянии от границы странгуляции будет паретически изменена приводящая петля кишки. Поэтому хирург должен ориентироваться при выборе орального уровня резекции не на рекомендуемые 30-40 см, а на внешний вид кишки и кровоточивость ее стенки на месте пересечения. При этом, если после определения вами предполагаемого размера резекции, кишечника остается еще достаточно много, лучше не экономьте. Еще три технических соображения. Первое. Даже при обширной резекции разница в диаметре сшиваемых орального и каудального концов кишки все равно может оказаться значительной. В этом случае будет предпочтительнее наложение анастомоза по типу «бок-в-бок». Если же желательно наложить анастомоз по типу «конец-в-конец», то каудальный конец кишки следует срезать косо с расчетом, чтобы срез кишки шел в сторону края, противоположного брыжейке (рис. 18). Второе. Перед пересечением кишки, ее брыжейку следует обязательно посмотреть на свет, чтобы убедиться, что вблизи места пересечения ее сосуды обеспечат хорошее кровоснабжение будущего анастомоза. Третье. Анастомоз получается очень красивым, если концы кишки на значительном протяжении освобождены от брыжейки, да и сшивать их тогда просто. Однако гнаться за такой красотой крайне опасно, поскольку при этом вследствие нарушения кровоснабжения сшиваемых концов кишки очень часто наступает недостаточность анастомоза. Поэтому без брыжейки может быть ставлен конец кишки лишь на расстоянии не более 0,5 см. Этого вполне достаточно, чтобы наложить первый ряд швов. При накладывании ряда серо-серозных швов у брыжеечного края анастомоза они могут быть наложены на серозу брыжейки (рис. 19-22). В немалой степени успех хирургического лечения непроходимости кишечника зависит от адекватности внутреннего дренирования кишечника и в первую очередь, места анастомоза. Многочисленными экспериментальными работами и клиническими наблюдениями совершенно определенно доказано, что если внутрикишечное давление в области анастомоза хоть немного повышено - следует ждать его несостоятельности. Поэтому еще перед наложением анастомоза должен быть выбран оптимальный метод и осуществлено соответствующее дренирование. В зависимости от локализации анастомоза дренирование осуществляют, выводя зонд наружу через нос, желудок, слепую кишку или задний проход. 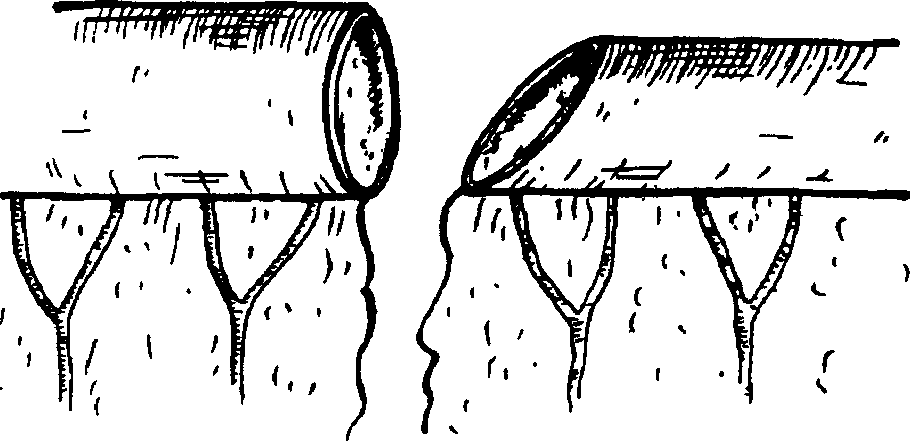 Рис. 18. Направление косого среза кишки при несоответствии просвета соединяемых концов.  Рис. 19. Методика наложения П-образного шва у брыжеечного края соединяемых концов кишки. 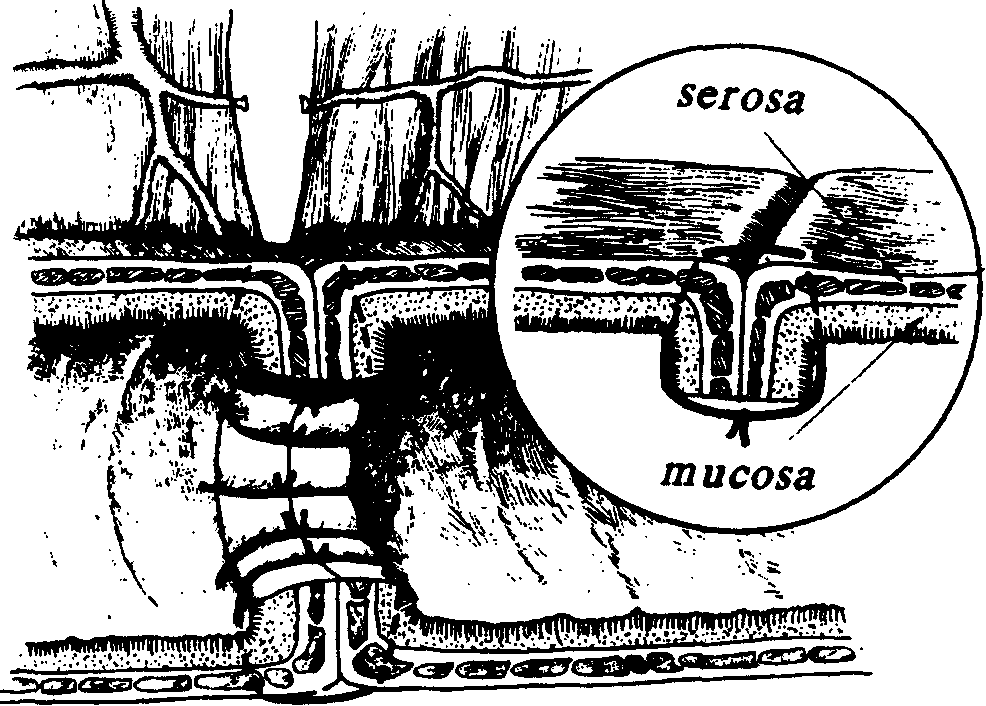 Рис. 20. Однорядный узловой шов с узелками в просвете кишки. 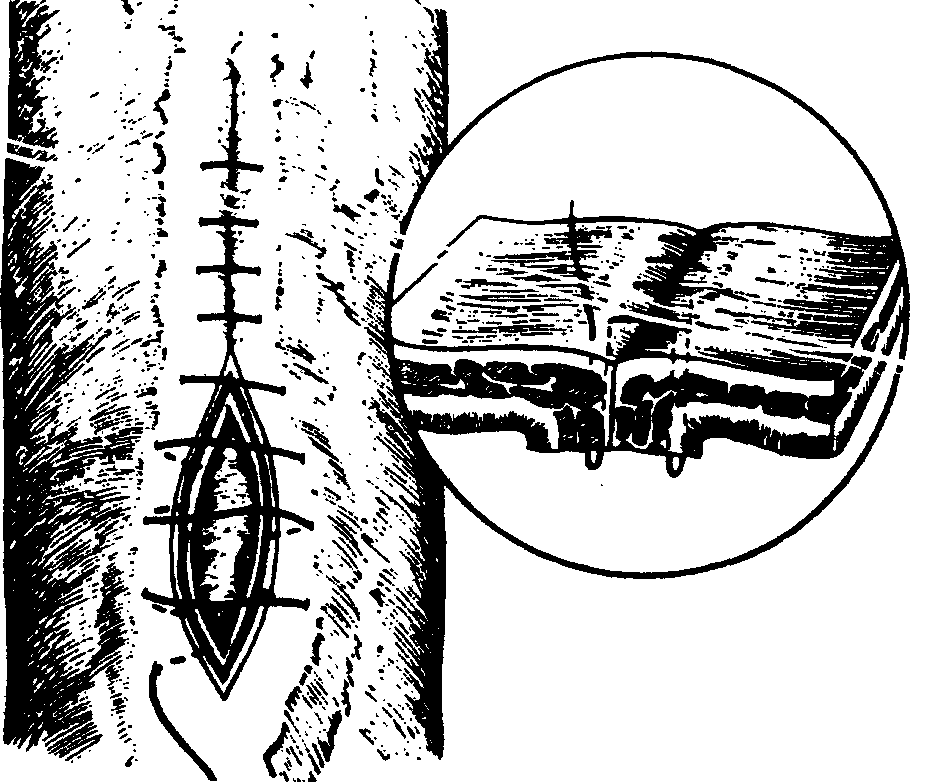 Рис. 21. Сквозной шов Коннеля-Апполито.  Рис. 22. Серозно-мышечный прямоугольный шов Кушинга. При этом дренажная трубка должна заходить за анастомоз не более чем на 10-15 см с тем, чтобы хорошо дренировать, главным образом, область анастомоза, а при удалении трубки не травмировать анастомоз. Полагаю, что то, как поставлена дренажная трубка в ортоградном или ретроградном направлении, особого значения не имеет, так как к тому времени, когда кишка начинает нормально перистальтировать и может сместить трубку, дренаж может быть уже удален. Я являюсь категорическим противником длинных трубок с множественными отверстиями, сделанными по всему длиннику. Дело в том, что основная наша задача - осуществить декомпрессию прежде всего в области анастомоза. Если в трубке имеется множество отверстий, то никогда нельзя быть уверенным, что она остается проходимой на всем протяжении до области анастомоза. В том случае, если конец трубки забивается кишечным содержимым, дренаж части кишки будет продолжать осуществляться, но дренаж наиболее необходимого нам участка, т.е. области анастомоза осуществляться при нем не будет. Даже вводя в дренаж рентгеноконтрастное вещество, вы не сможете установить, работает дренаж или нет, поскольку оно будет вытекать из многочисленных отверстий и не дойдет до конца. По этой же причине дренажную трубку не удастся полностью промыть, чтобы восстановить ее проходимость. Совсем другое дело. если поставленный дренаж, кроме торцового отверстия, будет иметь еще только два боковых отверстия по каждую сторону анастомоза. В этом случае можно будет абсолютно точно установить, работает ли дренаж. А если он забился - восстановить его проходимость, подавая по нему жидкость под напором. Если есть основание ожидать появления у больного после операции сильного метеоризма, то ему лучше поставить второй дренаж с множеством отверстий по длиннику, но главным всегда остается дренаж, расположенный вблизи анастомоза! Санация брюшной полости при релапаротомии имеет немаловажное значение для успешного лечения больного. При ранней релапаротомии в брюшной полости всегда можно обнаружить выпот. Характер его определяется рядом обстоятельств. В частности, при странгуляционной непроходимости скапливается в значительном количестве геморрагическая жидкость, которая часто оказывается инфицированной. Чтобы не намокло белье, ограничивающее операционное поле, большую часть жидкости следует удалить сразу как только будет чуть-чуть приоткрыта брюшина. С этой целью заранее включают электроотсос, анестезиолог делает больному "выдох", хирург приподнимает зажимами брюшину, снимает пару швов с брюшины или делает в ней небольшое отверстие, вводит через него наконечник аспиратора и удаляет возможно большее количество жидкости. Только после пого можно окончательно открывать брюшную полость. По ходу операции время от времени приходится дополнительно удалять жидкость, и тем не менее к концу операции она все еще будет скапливаться в отлогих местах. Поэтому, закончив все основные этапы операции, необходимо окончательно осушить брюшную полость. Затем нужно тщательно промыть ее растворами антисептиков или антибиотиков, и при необходимости поставить микроирригаторы для последующего введения лекарств или дренажные трубки. Последний этап релапаротомии - закрытие раны брюшной полости. При тяжелой перитонеальной инфекции рану вообще лучше не закрывать или вшить в нее "молнию", использовать другие приспособления, позволяющие многократно производить ревизию и повторные санации брюшной полости. Если же рану решено закрыть наглухо, то следует подумать о предупреждении эвентрации, которая после релапаротомии нередко катастрофически осложняет послеоперационный период. Кроме распространенных в нашей стране швов на пуговицах, на резиновых трубках и т.п. еще более прочно удерживают края раны 8-образные или блоковидные проволочные швы, наложенные через все слои брюшной стенки. Больному разрешается вставать с постели только с хорошо затянутым бандажом, носить который ему следует рекомендовать не менее 3-х месяцев после операции. Если же у больного наблюдается метеоризм, он сильно кашляет или имеются другие причины, в результате которых происходит повышение внутрибрюшного давления, то, во-первых, необходимо бороться с этими причинами; во-вторых, больной должен находиться с затянутым бандажом постоянно, даже в горизонтальном положении; в-третьих, снятие швов с раны (особенно наложенных через все слои брюшной стенки) следует задержать на 4-6 дней. Что касается профилактики развития острой послеоперационной непроходимости желудочно-кишечного тракта, то здесь следует выделить две стороны проблемы: предупреждение развитие послеоперационного пареза и предупреждение развития механической непроходимости. Причиной развития послеоперационного пареза может быть травматизация и раздражение рефлексогенных участков, повреждение нервных стволов, ответственных за моторику желудка и кишечника, инфицирование брюшной полости. Как известно, грубое оперирование с сильной тракцией брюшных органов является одной из причин развития после операции пареза желудочно-кишечного тракта. Однако следует помнить об особой опасности травматизации таких участков, как корень брыжейки тонкой кишки, ретроцекальное пространство и брыжейка терминального отдела подвздошной кишки. Отсюда следует не только требование нежного обращения с этими отделами, но и по-возможности введения 1/4% раствора новокаина в забрюшинное пространство этих областей или в брыжейку в количестве 100-200 мл. По крайней мере такая новокаиновая блокада желательна в случаях длительного поиска червеобразного отростка, ревизии подвздошной кишки при поисках меккелева дивертикула, ревизии тонкой кишки. |
