тесты физика. Физика тесты. Сборник тестов по курсу общей физики иваново 2006 удк 53 Кудин Л. С. Сборник тестов по курсу общей физики
 Скачать 1.31 Mb. Скачать 1.31 Mb.
|
МОЛЕКУЛЯРНАЯ ФИЗИКА И ТЕРМОДИНАМИКАПРИНЯТЫЕ ОБОЗНАЧЕНИЯ A - работа, константа P - давление a - константа Q - количество теплоты cp, cv- удельная теплоемкость при постоянном давле- нии и объеме СP, СV- молярная теплоемкость при постоянном давле- нии и объеме R - универсальная газовая по- стоянная S - энтропия, площадь D - коэффициент диффузии Т - термодинамическая темпе- ратура d - эффективный диаметр t - время F - сила U - внутренняя энергия H - энтальпия u - скорость направленного h - высота V - объем движения g- ускорение свободного падения vвер - наиболее вероятная скорость i - число степеней свободы <v>- vср. ар K- импульс <v2>- vср. кв средняя арифметическая скорость средняя квадратичная ско- рость k - постоянная Больцмана x, y, z - координата, смещение - коэффициент теплопро- - отношение темплоемкостей водности Сp/СV М - молярная масса - коэффициент внутреннего трения вязкость m- масса - средняя длина свободного пробега N - число частиц - плотность NА- постоянная Авогадро - эффективное сечение n - концентрация, константа ТЕСТОВЫЕ ЗАДАНИЯКакие графики, изображенные на рисунках представляют изобарный процесс? 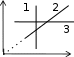 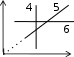 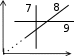 Р Р V Р Р VV T T а) 1, 5, 8; б) 3, 6, 8; в) 2, 5, 7; г) 3, 6, 7; д) 2, 6, 9. Какие процессы изображены на графиках? Как изменяется объем газа в процессе I (рис. 1) и давление газа в процессе II (рис. 2)?  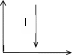 P V P VT Рис. 1. T Рис. 2. а) изобарический, V - увеличивается, P - уменьшается; б) изотермический, V – увеличивается, P - уменьшается; в) изохорический, V–уменьшается, P – увеличивается; д) изотермический, V – увеличивается, P –увеличивается. Как изменяется с ростом температуры давление в газовом процессе, для которого T–1? а) увеличивается; б) уменьшается; в) не изменяется. В газовом процессе, для которого T 2V = Const, P Tn. Найти значение n. Масса газа постоянна. а) ½; б) 2; в) 3; г) – ½; д) – 2. Чему равно общее число степеней свободы для молекулы идеального двухатомного газа? а) 2; б) 3; в) 4; г) 5; д) 6. Сколько степеней свободы колебательного движения имеет молекула NH3? а) 3; б) 5; в) 6; г) 7; д) 9. Объем некоторой массы идеального газа изобарически уменьшился в 2 раза. Как изменилась средняя энергия поступательного движения одной молекулы газа? а) увеличилась в 4 раза; б) уменьшилась в 4 раза;в) не изменилась; г) уменьшилась в 2 раза;д) увеличилась в 2 раза. На рис. 1 в координатах P и V изображен процесс, проведенный с иде- альным газом (m = сonst). Укажите номер графика, соответствующий этому процессу в координатах Р и Т на рис 2. 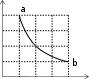 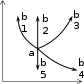 P P P P4 3 2 1 0 1 2 3 4 V T Рис. 1 Рис. 2 а) 1; б) 2; в) 3; г) 4; д) 5. Привести в соответствие графики, изображенные на рисунке, изопроцес- сам с идеальным газом? 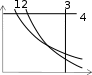 P P
На рис.а в координатах P – V изображен круговой процесс с некоторым количеством идеального газа. Выберите из графиков, рассмотренных ниже, (рис. 1-4) график этого процесса в координатах P – Т. 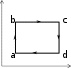 P PРис. а  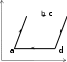 P P P PT T Рис. 1 Рис. 2   P P P Pb T T Рис. 3 Рис. 4 а) 1; б) 2; в) 3; г) 4. Установите соответствие между изопроцессом и выражением для работы расширения. Изопроцесс Математическое выражение а) изотермический 1) А =0 б) изобарический 2) А =m iRT М 2 в) изохорический 3) А = P(V2 -V1) г) адиабатический m А = МRTln P1 P2 а) ; б) ; в) ; г) . Чему равно отношение C P/СVдля идеального двухатомного газа при умеренных температурах? а) 1,01; б) 1,33; в) 1,40; г) 1,67; д) 1,80. Установить правильную последовательность между отношениями = С P/CVдля идеальных газов: 1) одноатомный, 2) двухатомный, 3) трехатомный. а) 1<2<3; б) 1<2>3; в) 1>2<3; г) 1>2>3. Давление некоторой массы идеального газа изохорически уменьшилось в 2 раза. Как изменилась средняя энергия поступательного движения одной молекулы газа? а) увеличилась в 4 раза;б) уменьшилась в 4 раза; в) увеличилась в 2 раза;г) уменьшилась в 2 раза; д) не изменилась. На рисунке изображен цикл из двух изобар и двух изохор. Пользуясь рисунком, выберите номера ответов, для которых приведены непра- вильные соотношения между температурами в состояниях 1, 2, 3, 4.  P PV а) T4 г) T1>T4; T2>T3; д) T 4>T1>T2. Изопроцессам поставьте в соответствие выражения первого начала тер- модинамики. Изопроцесс Первое начало термодинамики а) изотермический 1) Q =dH б) изобарический 2) Q =A в) изохорический 3) А = – dU г) адиабатический 4) Q = dU а) ; б) ; в) ; г) . Два различных идеальных газа – одноатомный и двухатомный - нахо- дятся при одинаковой температуре и занимают одинаковый объем. Га- зы сжимаются адиабатически до уменьшения объема в 2 раза. Какой газ нагрелся больше? а) газы нагрелись одинаково; б) одноатомный нагрелся больше; в) двухатомный нагрелся больше. Укажите среди нижеприведенных выражений то, которое соответствует энергии одной молекулы газа. а) i+2kT; б) ikT; в) mi+2 kT; г) iRT; д) miRT. 2 2 М 2 2 М2 Найдите число степеней свободы молекул идеального газа, если 3/5 энергии его теплового движения приходится на поступательное движе- ние молекул. а) 7; б) 3; в) 4; г) 5; д) 6. Молярные теплоемкости гелия при процессах 1-2 и 2-3 (см. рис.) обо- значены соответственно через С1 и С2. Найдите разность С1 и С2. 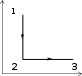 P PV а) 2,5R; б) 2R; в) 1,5R; г) R; д) 0,5R. Какое из приведенных выражений первого начала термодинамики при- менимо только к изотермическому процессу? а) Q = U + PV; б) U + A = 0; в) Q = U; m г) C mT+PV; д) Q = mRT ln V2 . М p T = МCV M V1 Установите соответствие между законом (определением) и его матема- тическим выражением. T Закон (определение) Математическое выражение а) первый закон термодинамики 1) S = Q б) второй закон термодинамики 2) S0 = 0 в) третий закон термодинамики 3) TdS = dU +PdV г) определение энтропии 4) dS =0 д) объединенный закон 5) Q = dU +PdV а); б) ; в) ; г) ; д) . Поставьте в соответствие определениям их математические выражения. Определение Математическое выражение а) уравнение состояния идеальных газов б) работа расширения в изотерми- mRT ln V2 М V 1 mCT ческом процессе M V в) первый закон термодинамики 3) TV -1 = const г) внутренняя энергия идеального газа PV =mRT М д) уравнение Пуассона 5) Q = dU +PdV а); б) ; в) ; г) ; д) . На каких стадиях процесса, график которого дан на рисунке, газ погло- щает теплоту? 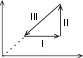 V VT а) I, II; б) II, III; в) I, III; г) I; д) II. На графике изображены изотермы идеального газа (m = const). Как из- меняются приращение внутренней энергии U и теплота Q при перехо- де от графика МА к графику МD? 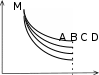 P PV1 V2 V а) U < 0, Q - уменьшается; б) U < 0, Q - возрастает; в) U > 0, Q - уменьшается; г) U > 0, Q - возрастает; д) U = 0, Q - уменьшается; е) U = 0, Q - возрастает. Установить правильную последовательность в изменении температуры для схематически представленных на рисунке кривых распределения Максвелла по скоростям.  dNТ1 dNТ1Ndv Т2 Т3 O а) T1 < T2 < T3; б) T 1 < T2 > T3; в) T 1 > T2 < T3; г) T 1 > T2 > T3. В каком соотношении находятся наиболее вероятная, средняя арифме- тическая и средняя квадратичная скорости: vвер : vср. ар : vср. кв? а) 1,22 : 1,13 : 1; б) 1,22 : 1 : 1,13; в) 1 : 1,13 : 1,22; г) 1 : 1,22 : 1,13; д) 1,13 : 1,22 : 1. Сравнить средние квадратичные скорости молекул двух идеальных га- зов с параметрамиР 1, 1 иР 2, 2, еслиР 1/Р2=2, a 2/1=1/2. а) v1 > v2; б) v 1 < v2; в) v 1 = v2. Чему равно среднее значение <х 2> некоторой величиных, функция распределения вероятностей значений которой изображена на рисунке. а) 1 2a; б) -a O 2  a; в) a; в) a 2a2 a2   3 ; г) 3 ; 3 ; г) 3 ;Функции распределения частиц по квантовым состояниям поставьте в со- ответствие математическое выражение. Определение Математическое выражение  e–Ei/kT а) распределение Гиббса 1) Ni =N n e–Ei/kT i  б) распределение Больцмана 2) Ni = Nn б) распределение Больцмана 2) Ni = Nne–Ei/kT e–Ei/kT + 1 i в) распределение Ферми - Дирака 3) n = n0 e–mgh/kT  e–Ei/kT г) распределение Бозе – Эйнштейна 4) w= n e–Ei/kT i e–Ei/kT д) распределение Больцмана в грави- тационном поле N  n e–Ei/kT – 1 i а) ; б) ; в) ; г) ; д) . Поставьте в соответствие закону (определению) его математическое вы- ражение. Закон Математическое выражение а) сила внутреннего трения 1) mi = – D diS t dz б) закон Фика (уравнение диффузии в газах) в) закон Фурье (уравнение теплопро- водности в газах) K= – duSt dz dz F = ⎢du⎢S dz г) уравнение вязкости в газах 4) Q = – dTSt а) ; б) ; в) ; г) . Установите соответствие между параметром и математическим выраже- нием, вытекающим из молекулярно-кинетических представлений. Параметр Математическое выражение а) коэффициент теплопроводности 1 1) 3 <v> 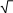 б) коэффициент вязкости 2) 1 б) коэффициент вязкости 2) 1 2 n в) коэффициент диффузии 1 3) 3 <v> СV 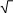 г) средняя длина свободного пробега 4) 2d2<v>n г) средняя длина свободного пробега 4) 2d2<v>nд) среднее число столкновений 1 5) 3 <v> а) ; б) ; в) ; г) ; д) . На рисунке приведены нормированные зависимости давления молекул воздуха: а) H2, б) N2, в) O2, г), H2О, д) CO2 от высоты h над уровнем мо- ря. Каждому из газов поставьте в соответствие кривую, описывающую зависимость давления от высоты.  Р Рh а) ; б) ; в) ; г) ; д) . |
