Рыков РГР 1. Технологический расчет ректификационной колонны для разде
 Скачать 231.53 Kb. Скачать 231.53 Kb.
|
|
РГУ НЕФТИ И ГАЗА (НИУ) ИМЕНИ И.М. ГУБКИНА
РАСЧЕТНАЯ РАБОТА
Оренбург, 2020 РГУ НЕФТИ И ГАЗА (НИУ) ИМЕНИ И.М. ГУБКИНА
ЗАДАНИЕ НА РАСЧЕТНУЮ РАБОТУ
Содержание работы:
Рекомендуемая литература: Прокофьева Т.В., Щелкунов В.А., Андриканис В.В., Фёдорова Е.Б. Технологиче- ский расчёт ректификационной колонны для разделения бинарной смеси. – М.: РГУ нефти и газа, 2005. – 37 с. 2. Скобло А.И., Молоканов Ю.К., Владимиров А.И., Щелкунов В.А. Процессы и ап- параты нефтепереработки и нефтехимии. - М: ООО «НедраБизнесцентр», 2000. - 677 с. 3. Кузнецов О.А. Технологический расчёт ректификационной колонны для разделе- ния бинарной смеси с использованием табличного процессора EXCEL. - Оренбург: филиал РГУ нефти и газа им. И.М. Губкина, 2009. – 39 с. 4. Кузнецов О.А. Основы работы в программе AspenHYSYS. - М.- Берлин: Директ- Медиа, 2015. – 153 с. 5. Кузнецов О.А. Начало работы в Aspen HYSYS V8. - М.-Берлин: Директ-Медиа, 2015. – 68 с. 6. Кузнецов О.А. Моделирование схемы переработки природного газа в Aspen HYSYS V8. - М.-Берлин: Директ-Медиа, 2015. – 116 с. Кузнецов О.А. Моделирование установки переработки нефти в Aspen HYSYS V8. - М.-Берлин: Директ-Медиа, 2015. – 133 с. Данные:
Руководитель: к.т.н. доцент Кузнецов О.А.
Содержание Расчет зависимости давлений насыщенных паров компонентов от температуры, равновесных концентраций, энтальпий 4 Материальный баланс колонны 11 Расчет флегмового числа 12 Графический метод МакКейб-Тиле расчета числа теоретических тарелок в колонне 14 Аналитический метод расчета числа теоретических тарелок в колонне 18 Определение основных размеров колонны 27 ЛИТЕРАТУРА 33 Приложение 1 34 Приложение 2 35 Приложение 3 36 1 Расчет зависимости давлений насыщенных паров компонентов от температуры, равновесных концентраций, энтальпий Методику выполнения расчёта ректификационной колонны для разделения бинарной смеси поясним на примере. Возьмём следующие исходные данные: сырье состоит из смеси гептана и октана; содержание пропилена в сырье хF= 0,45; содержание пропилена в ректификате yD= 0,95, в остатке xВ= 0,04; массовая доля отгона сырья e= 0,5; массовый расход сырья F = 12 000 кг/ч. Сначала определим давление в аппарате. Преимущественно, при более низких температурах экономически выгоднее вести процесс ректификации. В этом случае значение коэффициента относительной летучести имеет более высокие значения. Но основными определяющими параметрами являются условия отвода тепла вверху колонны и подвода тепла в низу колонны. Наименее затратным теплоотводом является воздушное охлаждение, при котором можно обеспечить температуру верха колонны равной 45 °С. Возможно применение водяного охлаждения, которое позволяет поддерживать 35 °С. Для создания более низких температур наиболее широко применяется пропановый холодильный цикл создающий -25 °С. Другие способы отвода тепла применяются значительно реже. Выберем для нашего процесса воздушное охлаждение и определим давление в аппарате по верху колонны, по условию конденсации низкокипя- щего компонента – бензола. Для расчёта давления насыщенных паров гептана и октана от темпера- туры можно воспользоваться уравнением Антуана ln Р a b T c d ln T eTf или Р e ab dln T eT f T c , (1) где Р – давление насыщенных паров, кПа; T – температура, ОК; a, b, c, d, e, f – константы уравнения Антуана. Из Приложения 1 определяем константы уравнения Антуана для гептана (a=78,3285, b=-6947, c=0, d=-9,44866, e=6,47481∙10-6, f=2) и октана (a=86,997, b=-7890,6, c=0, d=-10,6255, e=6,47441∙10-6, f=2). Обратите внимание на интервал температур, расчётные значения температуры никогда не должны выходить за пределы указанного интервала. При 45 градусах низкокипящий компонент создаёт давление около 15 кПа, что существенно ниже атмосферного давления. Надо помнить, что расчёты ведутся при абсолютном давлении, а не при манометрическом. Для разделения заданных компонентов организовывать работу вакуумной ко- лонны, скорее всего, будет экономически нецелесообразным. Поэтому примем давление на вверху колонны незначительно выше атмосферного, 120 кПа. Получим значение температуры кипения НКК tа=-189,46 °С. Продолжаем температурный ряд. Получаем значение температуры кипения ВКК tw=87,75 °С. Для расчета состава равновесных фаз и построения кривой равновесия фаз, изобарных температурных кривых и энтальпийной диаграммы построим кривые зависимости давления насыщенных паров (ДНП) компонентов от температуры. 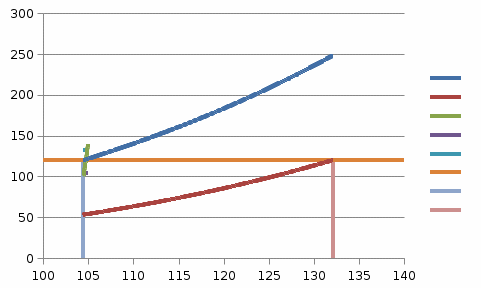 Рисунок 1 - Зависимости давления насыщенных паров компонентов от темпе- ратуры в Exсel Вычислим составы равновесных жидкой х' и паровой у' фаз по уравнениям (2) и (3): x' P2 P1 P2 y' P1 x' , (2) . (3) Пересчёт мольных концентраций х' и у' в массовые х и у производят по следу- ющим формулам x М1х' М1х'M2 1 х' , (4) y М1 y' М1 y'M2 1 y' , (5) где М1 и М2 – соответственно молекулярные массы НКК и ВКК. 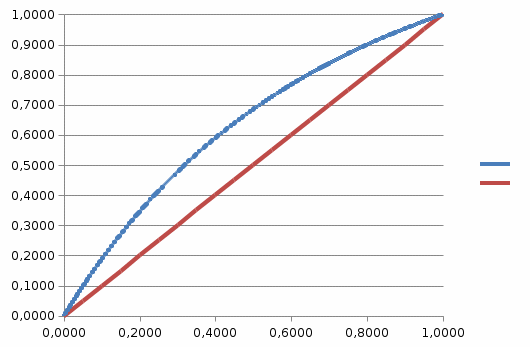 Рисунок 2 – Кривая равновесия фаз построенная в Exсel. Для построения изобарных температурных кривых t=f(x) и t=f(y) выделив любую пустую ячейку, вставляем точечную диаграмму с гладкими кривыми 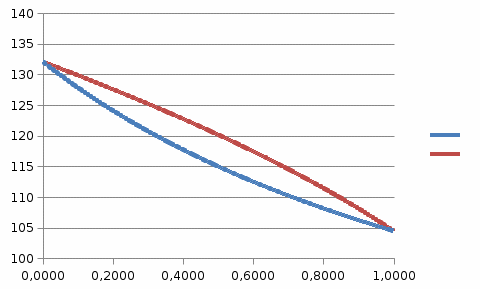 Рисунок 3 – Изобарные температурные кривые, построенные в Exсel. Для дальнейших расчетов необходимо знать энтальпию жидкости и паров в различных сечениях колонны. Энтальпии могут быть определен прибли- жённо по формулам Крэга: для жидкости ht 0,403t 0,000405t2  , ккал/кг, (6) , ккал/кг, (6)для паров 15 Нt 50,2 0,109t 0,00014t2 4,0 15 73,8 , ккал/кг. (7) Значение плотностей углеводородов приведены в приложении 1 (пропилен – 521; винилацетилен – 688,4). Для пересчёта величин плотностей можно воспользоваться приближённой формулой: 4 15 20 15 6 , (8) где α – температурная поправка (приложение 2), у гептана – 0,923 октана – 0,897). Найдём значения 15 для гептана – 692,338, а для винилацетилена – 710,782. Зна- 15 чения, получаемые в формулах 6 и 7 имеют размерность ккал/кг. Для перевода в кДж/кг полученные значения необходимо умножить на 4,187. Энтальпия жидкости состава х при температуре t определяется уравнением ℎ𝑡 = ℎ1𝑥 + ℎ2(1 − 𝑥). (9) Аналогично энтальпия паров состава у равна 𝐻𝑡 = 𝐻1𝑦 + 𝐻2(1 − 𝑦). (10) Построим энтальпийную диаграмму, связывающую составы жидкой и паро- вой фаз с их энтальпией. 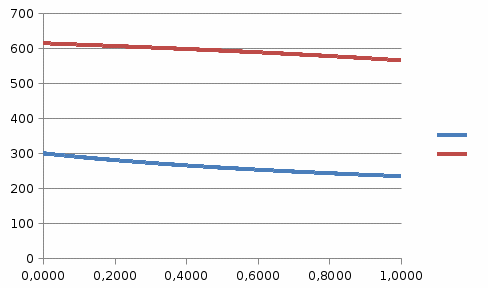 Рисунок 4 – Энтальпийная диаграмма, построенная в Excel. Результаты вычислений приведены в таблице 1. Таблица 1 - Результаты вычислений
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
