Тема Липиды I. Цель
 Скачать 73.38 Kb. Скачать 73.38 Kb.
|
|
Тема: Липиды I. Цель: Сформировать знания строения и химических свойств омыляемых липидов и их структурных компонентов для изучения структуры биологических мембран и процессов липидного обмена. II. Исходный уровень Трехатомный спирт глицерин. Сложные эфиры. Конформация открытой углеродной цепи. Учебно-целевые вопросы 1. Нейтральные липиды. Естественные жиры как смесь триацилглицеринов. 2. Основные природные высшие жирные кислоты, входящие в состав липидов: пальмитиновая, стеариновая, олеиновая, линолевая, линоленовая, арахидоновая. 3. Пероксидное окисление фрагментов жирных кислот в клеточных мембранах. -окисление насыщенных кислот. 4. Фосфолипиды. Фосфатидные кислоты. Фосфатидилколамины (кефалины), фосфотидилсерины, фосфатидилхолины (лецитины) – структурные компоненты клеточных мембран. Общей характеристикой липидов является их отношение к растворителям: они не растворяются _____________________________, растворимы в _________________________. По отношению к гидролизу липиды делятся на две группы: омыляемые - _______________________________________________________ и неомыляемые - _____________________________________________________ Омыляемые липиды Омыляемые липиды делятся на простые _______________________________ _________________________________ и сложные _______________________ ________________________________________________. Простые липиды 1. Воска – это сложные эфиры ВЖК и высших одноатомных спиртов. Представители: А) спермацет, цетилпальмитат ________________________________________ Б) пчелиный воск (мерицилпальмитат) _________________________________ __________________________________________________________________. Приведите формулы восков. 2. Жиры и масла. Это сложные эфиры _____________________________ и _________________________________, т.е. триацилглицерины (ТАГ). Конформационное строение ВЖК, входящих в состав жиров. Напишите формулы и кнормационное строение: Насыщенные кислоты: пальмитиновая С15Н31СООН __________________________________________________________________ стеариновая С17Н35СООН Ненасыщенные кислоты: олеиновая С17Н33СООН линолевая С17Н31СООН линоленовая С17Н29СООН арахидоновая С19Н31СООН __________________________________________________________________ __________________________________________________________________ Ненасыщенные кислоты существуют только в цис-форме. Самая распространенная кислота в природных липидах – олеиновая. В некоторых жирах она составляет 50% от общей массы ВЖК. Организм человека способен синтезировать насыщенные жирные кислоты и олеиновую (с одной двойной связью). Остальные ненасыщенные кислоты организм должен получать с пищей, в основном, с растительными маслами. Эти кислоты называются ____________________________________________. ВЖК не растворимы в воде, так как их молекулы содержат большой углеводородный радикал (гидрофобный «хвост»). Их натриевые, калиевые, аммонийные соли (мыла) гидролизуются в воде, обладают хорошей растворимостью, так как содержат высокополярный гидрофильный анион (полярная «головка»). Укажите эти части в молекулах мыла 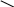 СН3 …… (СН2)n ……С = О СН3 …… (СН2)n ……С = О О – Na+ Химические свойства жиров 1) Гидролиз в кислой среде протекает с образованием глицерина и ВЖК. Допишите уравнение реакции Назовите жир и получающиеся жирные кислоты.  СН2 – О – СО – С15Н31 + 3 Н2О, Н+ СН2 – О – СО – С15Н31 + 3 Н2О, Н+  СН – О – СО – С17Н33 СН – О – СО – С17Н33СН2 – О – СО – С17Н35 В щелочной среде жиры омыляются с образованием глицерина и солей ВЖК, которые называются ________________________________________________. Допишите уравнение реакции, назовите соли ВЖК.  СН2 – О – СО – С15Н31 + 3 NaOH СН2 – О – СО – С15Н31 + 3 NaOH  СН – О – СО – С17Н33 СН – О – СО – С17Н33СН2 – О – СО – С17Н35 2) Гидрирование. В каталитических условиях жидкие масла превращаются в твердые жиры. Допишите реакцию, назовите исходный и конечный продукты реакции.  СН2 – О – СО – С17Н33 + 12 Н/Рt СН2 – О – СО – С17Н33 + 12 Н/Рt СН – О – СО – С17Н31 СН – О – СО – С17Н31СН2 – О – СО – С17Н29 3) Мерой ненасыщенности природных жиров и масел является йодное число. Оно соответствует количеству г I2, которое может быть присоединено к 100 г жира. Допишите реакцию. Назовите исходный и конечный продукты реакции.  СН2 – О – СО – (СН2)7 – СН = СН – (СН2)7 – СН3 + 3 I2 СН2 – О – СО – (СН2)7 – СН = СН – (СН2)7 – СН3 + 3 I2   СН2 – О – СО – (СН2)7 – СН = СН – (СН2)7 – СН3 СН2 – О – СО – (СН2)7 – СН = СН – (СН2)7 – СН3 СН2 – О – СО – (СН2)7 – СН = СН – (СН2)7 – СН3  СН2 – О – СО – СН2 – О – СО – СН – О – СО –  СН2 – О – СО – СН2 – О – СО – 4) Реакции окисления А) Окисление кислородом воздуха, сопровождаемое гидролизом. Допишите реакцию, назовите все продукты.  СН2 – О – СО – (СН2)7 – СН = СН – (СН2)7 – СН3 +6 О2 + 3Н2О СН2 – О – СО – (СН2)7 – СН = СН – (СН2)7 – СН3 +6 О2 + 3Н2О   СН2 – О – СО – (СН2)7 – СН = СН – (СН2)7 – СН3 СН2 – О – СО – (СН2)7 – СН = СН – (СН2)7 – СН3 СН2 – О – СО – (СН2)7 – СН = СН – (СН2)7 – СН3 Б) Пероксидное окисление липидов Напишите схему процесса В) -окисление насыщенных кислот Напишите уравнения реакций. Сложные липиды Ткани головного и спинного мозга содержат сложные структурные единицы, построенные из белков и фосфолипидов – фосфатидов. Фосфатиды – это ____________________________, дающие при гидролизе, кроме глицерина и ВЖК, _____________________________ и аминоспирты или другие сложные спирты. Они являются сложно-эфирными производными L- фосфатидных кислот. L- фосфатидные кислоты – это этерифицированные ВЖК L –глицеро-3-фосфата. R   СН2 – ОН СН2 – О – С = О СН2 – ОН СН2 – О – С = О   СН – ОН СН – О – С = О СН – ОН СН – О – С = О  СН2 – О – Р = О R СН2 – О – Р = О R НО ОН CН2 – О – Р = О НО ОН CН2 – О – Р = ОL –глицеро-3-фосфат НО ОН L – фосфатидные кислоты В природных фосфатидах в 1-м положении находится остаток __________ _______________________ кислоты, во 2-м положении __________________. 1) Фосфатидилэтаноламины (кефалины) Допишите уравнеия: Образование:   СН2 – ОН С17Н35СООН СН2 – СН2 – ОН С17Н35СООН СН2 –   СН – ОН + СН – СН – ОН + СН –    СН2 – О – Р = О С17Н35СООН - 3 H2O СН2 – СН2 – О – Р = О С17Н35СООН - 3 H2O СН2 – НО ОН +   СН2 – СН2 СН2 – СН2 ОН NH2 Строение внутренней соли:  СН2 – СН2 –  СН – СН – СН2 – Омыление:  СН2 – О – СО – С17Н35 СН2 – О – СО – С17Н35 СН – О – СО – С17Н33 + 5 NaOH СН – О – СО – С17Н33 + 5 NaOH СН2 – О – Р = О СН2 – О – Р = ОДопишите уравнение реакции. 2) Фосфатидилхолины (лецитины) Допишите уравнения реакции: Образование:  СН2 – ОН С15Н31СООН СН2 – ОН С15Н31СООНСН – ОН + С17Н31СООН  СН2 – О – Р = О + + СН2 – О – Р = О + +  НО ОН (СН2 – СН2 – N(CH3)3) OH - 3 Н2О НО ОН (СН2 – СН2 – N(CH3)3) OH - 3 Н2ОOH  СН2 – О – СН2 – О – СН – О – СН2 – О – Р = О Приведите строение внутренней соли данного фосфатида Напишите уравнение реакции омыления фосфатида, образованного пальмитиновой и линолевой кислотами. 3) Фосфатидилсерины содержат в качестве азотистого основания аминокислоту серин. Допишите все формулы и уравнения. Образование:  СН2 – ОН С17Н35СООН СН2 – ОН С17Н35СООН   СН – ОН + С17Н29СООН СН – ОН + С17Н29СООН     СН2 – О – Р = О СН2 – СН – СООН - 3Н2О СН2 – О – Р = О СН2 – СН – СООН - 3Н2О НО ОН ОН NH2 Приведите строение внутренней соли фосфатидилсерина. Напишите уравнение реакции омыления этого фосфатида. Все фосфатиды имеют консистенцию ___________________, окрашены в ___________ цвет. Они являются ПАВ, так как обладают способностью накапливаться на поверхности раздела между водой и другими жидкостями и ____________________________ поверхностное натяжение. 3. Упражнения 1. Напишите структурные формулы (с учетом конформационного строения) ВЖК: Пальмитиновой Стеариновой Олеиновой Линолевой Линоленовой Арахидоновой 2. Напишите уравнение реакций гидролитического расщепления в кислой и щелочной средах: Триацилглицерина дипальмитоилстеароил глицерина Линоленоил-линооил-пальмитоил глицерина 3. Напишите уравнения реакций образования: Фосфатидилэтаноламина Фосфатидилсерина Фосфатидилхолина Приведите строение их внутренних солей. 4. Напишите уравнения реакций омыления: Фосфатидилэтаноламина Фосфатидилсерина Фосфатидилхолина 5. Напишите уравнение реакции пероксидного окисления олеиновой кислоты. 6. Приведите уравнение реакции -окисления насыщенных кислот 5. Лабораторная работа Опыт 1. Гидролиз спиртового раствора мыла. Материалы и реактивы: хозяйственное мыло, этанол, фенолфталеин, пробирки, пипетки, стеклянные палочки. Ход работы. Внесите в пробирку небольшой кусочек мыла, добавьте 5 капель этанола и 1 каплю фенолфтолеина. При этом __________________________смеси __________________, что указывает на то, что мыло не содержит свободной ______________________ и имеет _____________________ реакцию. При добавлении 10 капель дист. воды содержимое пробирки _____________ в _____________ цвет, интенсивность которого _________________________ при добавлении большего количества воды. Следовательно, при добавлении воды происходит ___________________ с образованием свободной ______________________, благодаря чему происходит изменение окраски _________________________. Реакция гидролиза протекает по уравнению С17Н35СООNa + НОН Допишите уравнение реакции. Реакция водных растворов натриевого мыла ___________________________. Опыт 2. Проба на ненасыщенные жирные кислоты. Материалы и реактивы. Растительное масло, спиртовой раствор йода, крахмальный клейстер, бромная вода, штатив с пробирками, пипетки. Ход работы. К смеси 1 мл растительного масла и 1 мл воды добавить 2 капли спиртового раствора йода. После непродолжительного встряхивания содержимое пробирки проверить на реакцию с крахмалом. Раствор крахмала не дает синего окрашивания, т.е. не обнаруживается присутствие свободного йода. Уравнение реакции:  СН2 – О – СО – (СН2)7 – СН = СН – (СН2)7 – СН3 СН2 – О – СО – (СН2)7 – СН = СН – (СН2)7 – СН3 СН – О – СО – С15Н31 + I2 СН – О – СО – С15Н31 + I2 СН2 – О – СО – (СН2)7 – СН = СН – (СН2)7 – СН3 Допишите уравнение реакции. Данную работу оформить в тетради и сделать выводы. V. Литература Н.А. Тюкавкина, Ю.И. Бауков. Биоорганическая химия.М.: Медицина, 1985, с. 427-442; 1991 г., с. 457-472. Руководство к лабораторным занятиям по биоорганической химии. Под ред. Н.А. Тюкавкиной, М.: 1985, с. 118-127. Конспект лекций. |
