Тэла. Учебнометодическое пособие для обучающихся Контрольные вопросы Эпидемиология. Факторы риска тэла
 Скачать 2.16 Mb. Скачать 2.16 Mb.
|
|
ДИАГНОСТИКА ТЭЛА В ОСОБЫХ КЛИНИЧЕСКИХ СИТУАЦИЯХ Особыми клиническими ситуациями можно считать случаи, когда использование изложенных выше алгоритмов диагностики ТЭЛА оказывается невозможным. К их числу относится внезапная смерть и недоступность рекомендуемых для диагностики ТЭЛА исследований. Внезапная смерть, чаще всего, является следствием фибрилляции желудочков, спровоцированной нарушением кровоснабжения миокарда. Подозрение на ТЭЛА, как причину внезапной смерти можно считать оправданным, если смерть: наступила у больного со значительными или умеренными факторами риска венозного тромбоэмболизма развилась после изменения положения тела, натуживания или восстановления синусового ритма (у лиц с фибрилляцией предсердий) дебютировала остановкой дыхания и сопровождалась резко выраженным цианозом верхней половины туловища сопровождалась в первые минуты гемодинамически эффективным сердечным ритмом. В отличие от ТЭЛА при фибрилляции желудочков дыхание угасает постепенно и полностью прекращается примерно через минуту после остановки кровообращения. В случае успешной реанимации диагноз верифицируется так же, как при ТЭЛА высокого риска, в случае смерти больного - по результатам вскрытия. Невозможность выполнения КТ из-за гемодинамической нестабильности пациента не затрудняет диагностику ТЭЛА высокого риска, поскольку в этом случае для подтверждения или исключения предполагаемого диагноза достаточно результатов эхокардиографического исследования. В случае выявления признаков перегрузки правого желудочка диагноз ТЭЛА у больного с шоком можно считать доказанным, при отсутствии таковых - исключенным. Диагностические проблемы резко возрастают, если недоступно не только эхокардиографическое исследование, но и КТ. В такой ситуации вопрос о наличии или отсутствии ТЭЛА приходится решать, исходя из наличия или отсутствия признаков перегрузки правого желудочка на ЭКГ и результатов рентгенографии легких. Нужно отметить, что оба метода не обладают достаточной чувствительностью и специфичностью для постановки диагноза ТЭЛА ЭКГ признаки перегрузки правого желудочка симптом QIIISI, то есть появление патологического зубца Q в III отведении глубокого зубца S в I отведении; увеличение амплитуды зубца R в правых грудных отведенияхRV1 > SV1; увеличение глубины зубца S в левых грудных отведениях SV5 > RV5; появление отрицательных зубцов T в отведениях V1–V3; появление высоких (более 2 мм) заостренных зубцов Р в III и aVF отведениях (p-pulmonale); появление блокады правой ножки пучка Гиса. ЭКГ-признаки перегрузки правого желудочка выявляются при ТЭЛА высокого риска примерно в 70–80 % случаев, поэтому их отсутствие не позволяет отклонить этот диагноз. Кроме того, ЭКГ-признаки перегрузки правого желудочка малоспецифичны, что не позволяет считать их выявление убедительным доказательством ТЭЛА. Исключение составляют случаи, когда появления признаков перегрузки правого желудочка четко связано с ухудшением состояния больного. Наиболее специфичным рентгенологическим признаком ТЭЛА является симптом Вастермарка — обеднение легочного рисунка в бассейне обтурированной артерии. Косвенными признаками ТЭЛА служат высокое стояние купола диафрагмы на стороне поражения, выбухание конуса легочной артерии, связанное с повышением давления в ней, увеличение правых отделов сердца и расширение верхней полой вены, отражающие дилатацию и декомпенсацию правого желудочка. К сожалению, перечисленные симптомы выявляются достаточно редко, особенно, при проведении исследования у лежащего пациента. Перечисленные рентгенологические симптомы наиболее ярко выражены в первые часы после ТЭЛА, то есть в период максимальной выраженности гемодинамических нарушений, обусловленных прекращением кровотока по обтурированным ветвям легочной артерии. Позже, примерно через сутки после ТЭЛА, рентгенологическое исследование позволяет выявить инфильтративные изменения, связанные с формированием инфаркта легкого. Классическим рентгенологическим симптомом инфаркта легкого служит треугольная тень, обращенная основанием к плевре. К сожалению, такая рентгенологическая картина выявляется лишь в 5% случаев. ЛЕЧЕНИЕ ТЭЛА ВЫСОКОГО РИСКА Шок или стойкая артериальная гипотензия создают непосредственную угрозу жизни больного, что делает их устранение первоочередной задачей лечения ТЭЛА высокого риска. Для устранения гемодинамических нарушений необходимо восстановление или, как минимум, улучшение кровотока в легочной артерии, что может быть достигнуто с помощью тромболизиса или эмболэктомии. Вторая, не менее важная задача — предотвращение повторной ТЭЛА, которая в условиях нестабильной гемодинамики практически всегда ведет к летальному исходу. Решение этой задачи может обеспечить интенсивная антикоагулянтная терапия. Кардиореспираторная поддержка при ТЭЛА высокого риска необходима для сохранения жизни пациента во время подготовки и проведения тромболизиса или эмболэктомии. При систолическом АД выше75 мм рт. ст. может оказаться эффективным внутривенное введение 250 мг добутамина в 250 мл 0,9% раствора физиологического раствора хлориданатрия, а в случае более выраженного снижения АД — 200 мг допамина в400 мл 5 % раствора глюкозы. Скорость введения указанных препаратов увеличивают с 5 мкг/кг/мин до стабилизации систолического АД на уровне90 мм рт. ст. Для коррекции гемодинамических нарушений могут использоваться также норадреналин или адреналин. Целесообразность инфузионной терапии при ТЭЛА высокого риска вызывает сомнения, поскольку показано, что агрессивная объемная нагрузка может усугубить дисфункцию правого желудочка. Для устранения гипоксемии показано назальное введение кислорода, при чрезмерной работе дыхательной мускулатуры может потребоваться искусственная вентиляция легких. Однако следует учитывать, что индуцированное искусственной вентиляцией положительное внутригрудное давление может уменьшить венозный возврат и усугубить недостаточность правого желудочка. Тромболитическая терапия (ТЛТ) может сыграть решающую роль в стабилизации гемодинамики при ТЭЛА высокого риска. Отказ от ТЛТ при ТЭЛА, приведшей к развитию шока или стойкой гипотонии, можно оправдать только наличием абсолютных противопоказаний к ее проведению. Следует учитывать, что противопоказания к ТЛТ, такие, например, как хирургическая операция в течение предшествующих 3 недель или желудочно-кишечное кровотечение в течение последнего месяца, будучи абсолютными при остром коронарном синдроме, при ТЭЛА высокого риска могут стать относительными. Абсолютные противопоказания к ТЛТ когда-либо перенесенный геморрагический инсульт или инсульт неизвестного характера ишемический инсульт в течение последних 6 месяцев заболевание или опухоль ЦНС недавно перенесенная травма или операция (в течение 3 недель) желудочно-кишечное кровотечение в течение последнего месяца кровотечение неясного генеза Относительные противопоказания к ТЛТ транзиторная ишемическая атака в течение последних 6 месяцев прием оральных антикоагулянтов беременность или первый месяц после родов пункция сосудов с невозможностью компрессии травма вследствие реанимационных мероприятий рефрактерная гипертензия (САД выше 180 мм рт. ст.) прогрессирующее заболевание печени инфекционный эндокардит активная пептическая язва Все тромболитические препараты активируют плазминоген, превращая его в плазмин — протеолитический фермент, разрушающий фибрин и способствующий тем самым растворению тромба. В настоящее время можно говорить о трех поколениях тромболитиков, типичными представителями которых служат стрептокиназа, альтеплаза (Актилизе) и тенектеплаза (Метализе). Тромболитические средства разных поколений различаются по своей тромболитической активности, селективности действия, антигенным свойствам и способам введения. Важной характеристикой тромболитических препаратов является селективность их действия по отношению к фибрину. Фибрин-неселективные тромболитики вызывают лизис не только образующего тромбфибрина, но и содержащегося в крови фибриногена, что ведет к массивному образованию продуктов их деградации, обладающих антикоагулянтной активностью. Кроме того, фибрин-неселективные препараты истощают V иVIII факторы свертывания, что также ведет к гипокоагуляции. В такойс итуации назначение гепарина может существенно повысить риск развития кровотечений, в связи с чем после ТЛТ фибрин-неселективными тромболитиками гепаринотерапию начинают после снижения АЧТВ до 80 с. Фибрин-селективные тромболитики практически не вызывают системногофибринолиза и не снижают способность крови к свертыванию. Поэтомупроведение ТЛТ фибрин-селективными тромболитиками требует проведения гепаринотерапии. Стрептокиназа применяется в медицинской практике с 1958 года и является классическим представителем тромболитических средств первого поколения. Стрептокиназу получают из ß-гемолитического стрептококка группы С, что делает ее высокоантигенной. Вследствие этого в течение 5дней после введения стрептокиназы образуется большое количество антител, которые циркулируют в крови не менее 2 лет. В случае повторного введения стрептокиназы она инактивируется антителами и не оказывает тромболитического действия. Кроме того, высокая антигенность стрептокиназы создает опасность развития аллергических реакций при ее повторном введении. Более того, примерно 10–25 % больных имеют исходный повышенный титр антител к стрептокиназе из-за перенесенных ранее стрептококковых инфекций. Поэтому уже при первом введении могут развиваться перекрестные реакции, что проявляется артериальной гипотензией и неэффективностью тромболизиса. По своей тромболитической активности стрептокиназа уступает тромболитикам второго и третьего поколения (табл. 3) и, в то же время, не обладая селективным действием на фибрин, ведет к неконтролируемой гипокоагуляции, повышая тем самым риск развития кровотечений. Единственным преимуществом ТЛТ стрептокиназой является ее относительно невысокая стоимость, однако, следует учитывать, что неэффективность тромболизиса, развитие аллергических реакций и кровотечений может свести это преимущество к нулю из-за увеличения общей стоимости лечения. Альтеплаза – генноинженерный тромболитик второго поколения. Альтеплаза - точная копия тканевого активатора плазминогена (ТАП) человека, получаемая рекомбинантым путем на культуре клеток млекопитающих. Альтеплаза не обладает антигенными свойствами, практически не действует на фибриноген (фибрин-селективный тромболитик) и по своей тромболитической активности существенно превосходит стрептокиназу. Сочетание высокой эффективности, щадящее действие на системные факторы гемостаза и отсутствие антигенности позволяет считать альтеплазу одним из лучших тромболитических препаратов. Тенектеплаза - рекомбинантный тканевой активатор плазминогена, генетически модифицированный в трех участках, что придает ему ряд преимуществ перед естественным ТАП и его рекомбинантным аналогом - альтеплазой. Во-первых, тенектеплаза обладает более высоким сродством к фибрину и, как следствие, менее выраженным системным фибринолитическим действием. Во-вторых, генетическая модификация обеспечивает устойчивость препарата к инактивирующему действию эндогенного ингибитора ТАП. В-третьих, длительный период полувыведения позволяет вводить тенектеплазу в виде однократного болюса, что особенноудобно при проведении ТЛТ на догоспитальном этапе. Схемы введения, описанных выше тромболитических препаратов при ТЭЛА высокого риска: Стрептокиназа- 250 000 ЕД за 30 мин (нагрузочная доза), далее по 100 000 ЕД/час в течение 12–24 часов или ускоренный режим: 1,5 млн ЕД за 2 часа. Альтеплаза – внутривенная инфузия 100 мг в течение 2 часов или ускоренный режим: 0,6 мг/кг в течение 15 минут (но не более 50 мг) Тенектеплаза - болюс в дозе зависящей от веса: до 60 кг - 30 мг; 60-69 кг - 35 мг; 70–79 кг - 40 мг; 80–89 кг- 45 мг; 90 кг и более - 50 мг. Хирургическая эмболэктомия может применяться для лечения ТЭЛА высокого риска при наличии абсолютных противопоказаний к ТЛТ или ее неэффективности. Альтернативой хирургическому лечению служат методы катетерной эмболэктомии или фрагментации тромбов в проксимальных легочных артериях. Гепаринотерапия при ТЭЛА высокого риска не может служить альтернативой тромболизису или эмболэктомии, поскольку риск смерти в этом случае возрастает примерно в 2 раза. Правда, преимущества ТЛТ перед гепаринотерапией в виде быстрого улучшения гемодинамики сохраняются только в первые дни лечения. Спустя неделю различия между группами ТЛТ и лечения гепарином в тяжести легочной обструкции и правожелудочковой недостаточности нивелируются. Поэтому в исключительных случаях, при недоступности ТЛТ и эмболэктомии, гепаринотерапия может стать основой лечения ТЭЛА высокого риска. При этом до ликвидации шока требуется внутривенное введение нефракционированного гепарина (НФГ), поскольку подкожное введение лекарств на фоне выраженных гемодинамических нарушений является неэффективным. Как отмечалось выше, гепаринотерапия не показана при проведении ТЛТ стрептокиназой или другими фибрин-неселективными тромболитиками, поскольку при этом возрастает опасность неконтролируемой гипокоагуляциии риск развития кровотечений. Если ТЛТ не проводилась, то при отсутствии противопоказаний, НФГ назначается в виде болюса 80 Ед/кг с последующей инфузией 18 Ед/кг/час. После завершения ТЛТ фибрин-селективными препаратами инфузию гепарина начинают без его болюсного введения. В случае использования фибрин-неселективных тромболитиков гепаринотерапию начинают лишь в том случае, если АЧТВ менее 80 с. В дальнейшем дозу НФГ подбирают в зависимости от величины активированного частичного тромбопластинового времени (АЧТВ), которое должно быстро увеличиться в 1,5–2,5 раза по сравнению с контролем и поддерживаться на этом уровне. АЧТВ определяется ежесуточно. ЛЕЧЕНИЕ ТЭЛА НЕВЫСОКОГО РИСКА Антикоагулянтная терапия является основным компонентом лечения ТЭЛА невысокого риска. В случае низкой клинической вероятности ТЭЛА антикоагулянтная терапия начинается сразу после подтверждения диагноза, а при высокой и средней вероятности диагноза может быть назначена даже до его окончательного подтверждения. Внутривенное введение НФГ является предпочтительным у лиц с тяжелой почечной недостаточностью (клиренс креатинина менее 30 мл/мин), поскольку он не выводится почками, и у больных с высоким риском кровотечения, так как его антикоагулянтное действие быстро нейтрализуется. Во всех остальных случаях могут использоваться низкомолекулярные гепарины (НМГ) или фондапарин — селективный ингибитор фактора Xa, которые назначаются, как минимум, на 5 дней. Альтернативой НМГ и фондапарину при лечении ТЭЛА невысокого риска являются прямые оральные антикоагулянты (ПОАК) - ривароксабан (Ксарелто), дабигатран (Прадакса), апиксабан (Эликвис). Ривароксабан в первые 3 недели лечения назначают по15 мг 2 раза в сутки во время еды, далее - по 20 мг 1 раз в сутки во время еды. Ривароксабан, как и другие ПОАК следует использовать с осторожностью у пациентов с тяжелым нарушением функции почек. Препараты противопоказаны пациентам с клиренсом креатинина менее 15мл/мин. Кардиореспираторная поддержка может потребоваться при ТЭЛА промежуточного риска, то есть при наличии признаков перегрузки правого желудочка и/или миокардиального повреждения. Увеличение сердечного выброса при ТЭЛА с нормальным уровнем АД может быть достигнуто после инфузии 500 мл декстрана, а также на фоне введения добутамина. Безусловно оправданным является назальное введение кислорода, Потребность в искусственной вентиляции легких обычно не возникает. ВТОРИЧНАЯ ПРОФИЛАКТИКА ТЭЛА Для профилактики рецидивов ТЭЛА используют оральные антикоагулянты, прием которых продолжают в течение 3 месяцев. У больных с неустранимыми факторами риска, при неизвестной причине ТЭЛА и в случае ее рецидива антикоагулянтная терапия может назначаться на неопределенно длительный срок. У больных с онкологическими заболеваниями для длительной антикоагулянтной терапии вместо оральных антикоагулянтов рекомендуется использовать НМГ. Варфарин – производное монокумарина, подавляющее синтез в печени витамин К-зависимых факторов свертывания, а именно — II, VII, IX иX. Противосвертывающий эффект в полной мере проявляется на 3–5 день от начала применения препарата, а прекращается через 3–5 дней после приема последней дозы. Выраженность антикоагулянтного эффекта оценивают по величине международного нормализованного отношения (МНО). При лечении ТЭЛА показано достижение среднего уровня гипокоагуляции с целевым МНО приблизительно равным 2,5 (2,0–3,0). Для достижения целевого МНО требуется несколько дней, поэтому прием варфарина при ТЭЛА следует начинать с первых дней болезни еще на фоне гепаринотерапии. До начала лечения следует оценить риск развития кровотечений по шкале HAS-BLED. При сумме баллов 3 и более риск кровотечения является высоким. Высокий риск кровотечения по шкале HAS-BLED не является основанием для отказа от антитромботической терапии, поскольку риск кровотечений, связанных с приемом варфарина, возрастает только при увеличении МНО свыше 3,5–4,0, а терапевтический диапазон у больных ТЭЛА равен 2,0–3,0. Таким образом, высокий индекс по шкале HAS-BLED(3 и более) указывает на необходимость тщательного контроля уровня МНО и устранения потенциально обратимых факторов риска кровотечения, таких как АГ, прием а 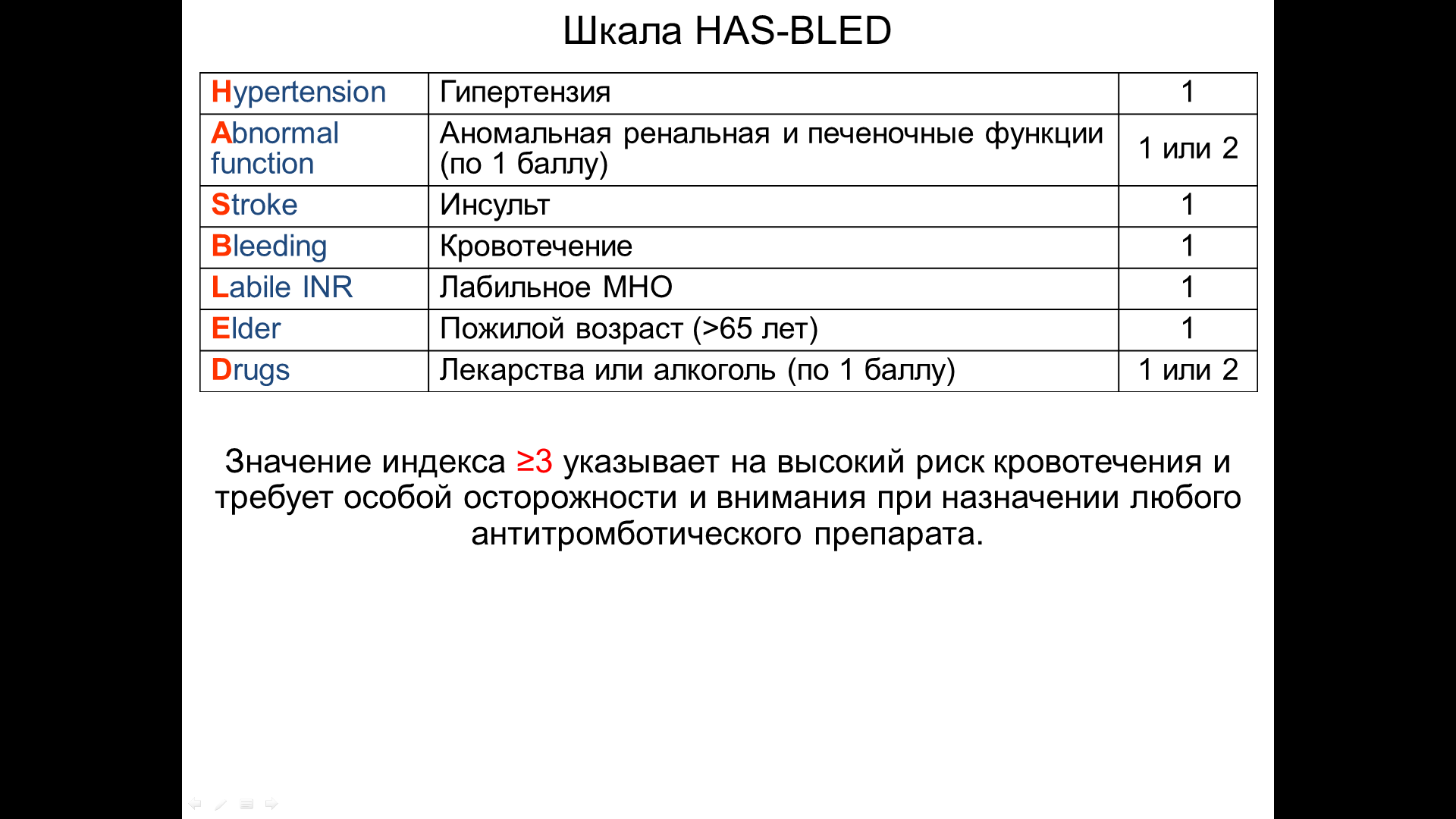 нтитромбоцитарных средств и нестероидных противовоспалительных препаратов. К абсолютным противопоказаниям для назначения варфарина относятся активное кровотечение, аллергия на препарат, геморрагический инсульт в анамнезе и тромбоцитопения (количество тромбоцитов менее 100×109/л). В остальных случаях вопрос о возможности назначения варфарина решается на основе индивидуальной оценки потенциального риска тромбоэмболических и геморрагических осложнений. Варфарин принимают 1 раз в день, после еды, вечером, а МНО определяют утром. Подбор дозы проводится в соответствии с алгоритмом, |
