Методичка. Методичка по биоорганической химии 2 семестр СТОМ 20-21 (1). Учебнометодическое пособие для подготовки и проведения лабораторнопрактических занятий для студентов, обучающихся по специальности Стоматология (31. 05. 03)
 Скачать 0.74 Mb. Скачать 0.74 Mb.
|
МоносахаридыРибоза, 2-дезоксирибоза, ксилоза, рибулоза, ксилулоза, глюкоза, манноза, галактоза, фруктоза – цепные (незамкнутые) формулы.-Д-глюкопираноза, -Д-глюкопираноза, -Д-галактопираноза, -Д-галактопираноза, -Д-фруктофураноза, -Д-рибофураноза, -Д-рибофураноза, 2-дезокси-Д-рибофураноза, -Д-2-дезоксирибофура-ноза – циклические формулы Хеуорса.ТЕМА Моносахариды. Химические свойства План занятия Устный опрос и коррекция знаний Подведение итогов занятия УЧЕБНЫЕ ЭЛЕМЕНТЫ ТЕМЫ Окислительно-восстановительные свойства моносахаридов При восстановлении моносахаридов (их альдегидной или кетонной группы) образуются многоатомные спирты – сахарные спирты. Их часто используют как заменители сахара при сахарном диабете. Восстановление проводится водородом в присутствии металлических катализаторов: 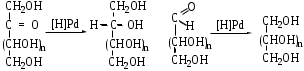 При восстановлении Д–ксилозы получают спирт ксилит; Д–глюкозы – сорбит; Д–маннозы– маннит. При окислении моносахаридов в зависимости от условий образуются различные продукты: а) окисление в щелочной среде сопровождается разрушением углеродной цепи моносахаридов. В этом случае применяются различные реактивы, содержащие ионы Ag+ или Cu+2 , способные восстанавливаться: 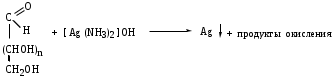 Аналогично окисляются и кетозы, т.к. в щелочной среде они изомеризуются в альдозы. б) окисление альдоз в кислой или нейтральной средах осуществляется без разрушения углеродного скелета моносахарида. При этом получаются различные кислоты. При использовании сильного окислителя – разбавленной азотной кислоты – концевые группы альдоз одновременно окисляются в карбоксильные. При этом образуются двухосновные гликаровые кислоты: 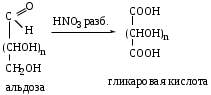 При окислении мягким окислителем (бромной водой) в карбоксильную группу превращается только альдегидная группировка. При этом получаются альдоновые или гликоновые кислоты: 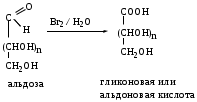 При окислении Д–глюкозы в этих условиях образуется глюконовая кислота, соль которой – глюконат кальция используется в медицине. При окислении концевой первичноспиртовой группы без затрагивания альдегидной группировки образуются гликуроновые или уроновые кислоты. Для этого окислению подвергается моносахарид с защищенной альдегидной группой, например, в виде гликозида: 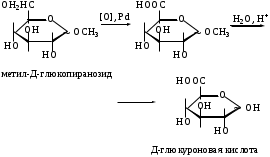 Уроновые кислоты имеют большое значение. Их представители входят в состав гепарина, пектиновых веществ плодов и ягод. Они также выполняют важную биологическую функцию – выводят из организма с мочой токсичные и посторонние вещества (детоксикация). Контрольные вопросы по теме 1. Как образуются О- и N- гликозиды? 2. Как образуются простые и сложные эфиры, фосфаты моносахаридов? 3.До каких соединений происходит восстановление моносахаридов? Напишите формулы сахарных спиртов: ксилит, сорбит, маннит. 4. В каких условиях протекает окисление моносахаридов? Напишите реакции получения гликоновых, гликаровых, гликуроновых кислоты. ЗАДАНИЯ для II ЭТАПА экзамена Производные моносахаридовЭфиры фосфорной кислоты: 1-фосфат--Д-глюкопиранозы, 6-фосфат-Д-глюкопиранозы, 1,6-дифосфат--Д-фруктофуранозы.Сахарные спирты: рибит, ксилит, сорбит, маннит.Кислоты: гликоновая, глюконовая, галактоновая, гликаровая, глюкаровая, галактаровая, маннаровая, глюкуроновая.Напишите уравнение следующих реакций с указанием механизма Восстановление фруктозы. К какому классу органических соединений относится продукт реакции? Образование кислот: глюкаровой, галактаровой, глюкуроновой. Указать условия. Образование О- и N-гликозидов моносахаридов. Образование простого и сложного эфиров моносахаридов ТЕМА Сложные углеводы План занятия Устный опрос и коррекция знаний Лабораторная работа №6 Подведение итогов занятия УЧЕБНЫЕ ЭЛЕМЕНТЫ ТЕМЫ Сложные углеводы в отличие от моносахаридов подвергаются гидролизу с образованием более простых углеводов. Сложные углеводы подразделяются на: олигосахариды, при гидролизе которых образуются от двух до десяти молекул моносахаридов, и полисахариды, при гидролизе которых образуются сотни и тысячи молекул; гомополисахариды, гидролизующиеся с образованием моносахаридов одного вида, и гетерополисахариды, гидролизующиеся с образованием различных моносахаридов. Мальтоза – солодовый сахар – основной продукт расщепления крахмала ферментом, выделяемым слюнной железой. Мальтоза в 3 раза менее сладкая, чем сахароза; она полностью усваивается человеческим организмом. Мальтоза состоит из остатков α–Д–глюкопиранозы и α–(или β)–Д–глюкопиранозы, связанных α–1,4–гликозидной связью. Целлобиоза в чистом виде встречается в природе редко. Она является фрагментом целлюлозы и образуется при неполном гидролизе этого полисахарида. Целлобиоза состоит из остатков β–Д–глюкопиранозы и α–(или β–)–Д–глюкопиранозы, связанных β–1,4–гликозидной связью. Лактоза – молочный сахар. Содержится в молоке млекопитающих (4–6%), в женском молоке – до 8%. Промышленно ее получают из сыворотки после отделения творога. Лактоза в 4–5 раз менее сладкая, чем сахароза, поэтому ее применяют в фармацевтической промышленности при изготовлении таблеток, порошков и как питательное средство для грудных детей. Однако, лактоза не усваивается некоторыми людьми из–за недостаточности у них фермента лактазы. Это следует учитывать в педиатрии, так как детей с лактазной недостаточностью нельзя вскармливать искусственными молочными смесями. Лактоза состоит из остатков β–Д–галактопиранозы и α–(или β)–Д–глюкопиранозы, связанных β–1,4–гликозидной связью: Сахароза относится к невосстанавливающим дисахаридам. Она наиболее значима из приведенных дисахаридов. Содержится сахароза в сахарном тростнике, сахарной свекле, соках плодов и ягод. Образуется она из остатков α–Д–глюкопиранозы и β–Д–фруктофуранозы, связанных α–1,2–гликозидной связью. Целлюлоза или клетчатка – это наиболее распространенный растительный полисахарид. Она является гомополисахаридом, так как состоит из остатков только β–Д–глюкопиранозы, связанных β–1,4–гликозидными связями. Биозный фрагмент целлюлозы – целлобиоза Целлюлоза имеет неразветвленное строение. Ее цепь содержит до 12 тысяч глюкозидных звеньев. Линейное сочленение β–Д–глюкопиранозных циклов в макромолекуле целлюлозы способствует образованию водородных связей внутри цепи и между соседними цепями. Этим объясняется высокая механическая прочность и волокнистость целлюлозы, что делает ее исключительным материалом для построения клеточных стенок растений. Древесина содержит 50–70% целлюлозы; хлопок, волокна льна и конопли – почти чистая целлюлоза. Большое значение имеют эфирные производные целлюлозы. Они являются основой ацетатных волокон, искусственного шелка, целлофана, вискозы, а также взрывчатых веществ. Крахмал – это ассоциат двух гомополисахаридов: амилозы (10–20%) и амилопектина (90–80%), связанных между собой водородными связями и построенных из остатков α–Д–глюкопиранозы. Крахмал образуется в процессе фотосинтеза в растениях и запасается в клубнях, корнях, семенах. Он содержится в хлебе, картофеле, овощах и является важным источником питания. В медицине его используют для изготовления присыпок, паст, таблеток. Амилоза состоит из остатков α–Д–глюкопиранозы, связанных α–1,4–гликозидными связями. Следовательно, биозный фрагмент амилозы – мальтоза. Неразветвленная цепь амилозы включает 200–3000 глюкозидных звеньев: Амилоза обладает вторичной структурой. Пространственная форма ее макромолекулы – спираль. На каждый виток спирали приходится 6 остатков глюкозы. При неполном гидролизе амилозы образуется мальтоза, при полном гидролизе – α-Д-глюкопираноза. Амилопектин в отличие от амилозы имеет разветвленное строение. Его макромолекула содержит от 6 тыс. до 9 млн. Д–глюкозных остатков. В основной цепи α–Д–глюкопиранозные остатки связаны α-1,4-гликозидными связями; в точках разветвления – α-1,6-гликозидными связями: Гепарин – естественный антикоагулянт, препятствует свертыванию крови. Содержится в малых количествах в печени, крови, легких, селезенке. Построен гепарин из повторяющихся дисахаридных фрагментов, связанных между собой α–1,4 или β–1,4–гликозидными связями. Каждый дисахаридный фрагмент содержит остатки Д–глюкозамина и двух уроновых кислот – Д-глюкуроновой или L-идуроновой, связанных α-1,4-гликозидной связью. Хондроитинсульфаты содержатся в соединительной ткани кожи, хрящей, сухожилий. Они являются эфирами серной кислоты. Построены эти соединения из повторяющихся дисахаридных фрагментов, связанных между собой β–1,4–гликозидными связями. Каждый дисахаридный фрагмент состоит из остатков β–Д–глюкуроновой кислоты и N–ацетил–Д–галактозамина, связанных β–1,3–гликозидной связью. Гиалуроновая кислота содержится в пуповине, суставной жидкости, стекловидном теле глаз. Она выполняет роль межклеточной смазки, поэтому присутствует в сухожилиях, коже, хрящах. Обладая высокой вязкостью и липкостью, обеспечивает непроницаемость соединительной ткани для болезнетворных бактерий. В то же время в присутствии гиалуроновой кислоты возрастает упругость тканей.Неразветвленные цепи гиалуроновой кислоты состоят из повторяющихся дисахаридных фрагментов, соединенных β–1,4–гликозидными связями. Дисахаридный фрагмент включает остатки β–Д–глюкуроновой кислоты и N–ацетил–Д–глюкозамина, связанных β-1,3-гликозидной связью. Контрольные вопросы по теме 1. Что называют сложным углеводами? Как классифицируют сложные углеводы? 2. Каков состав и строение дисахаридов (мальтоза, целлобиоза, лактоза, сахароза) В чем заключается их биологическое значение? 3. Каковы свойства дисахаридов (цикло-оксо-таутомерия; восстановительная способность; мутаротация; гидролиз)? Как записать уравнения реакций? 4. Какие полисахариды относят к гомополисахаридам? Как записать биозный фрагмент гомополисахаридов? 5. Какие полисахариды относят к гетерополисахаридам? Как записать фрагмент гиалуроновой кислоты? 7. Как записать реакции гидролиза полисахаридов? ЗАДАНИЯ для II ЭТАПА ЭКЗАМЕНА (Напишите структурные формулы следующих соединений) Дисахариды Мальтоза, целлобиоза, лактоза, сахароза. Полисахариды Биозный фрагмент крахмала (амилозы), биозный фрагмент целлюлозы, амилоза, крахмал, целлюлоза, фрагмент гиалуроновой кислоты. Напишите уравнение следующих реакций с указанием механизма Гидролиз мальтозы, целлобиозы, лактозы, сахарозы Цикло-оксо-таутомерия на примере мальтоз ТЕМА α-Аминокислоты. Пептиды. Белки План занятия 1. Устный опрос и коррекция знаний 2. Лабораторная работа № 7 3. Решение ситуационных задач 4 .Подведение итогов занятия УЧЕБНЫЕ ЭЛЕМЕНТЫ ТЕМЫ α 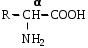 –Аминокислоты – это гетерофункциональные соединения. Они содержат одновременно карбоксильную и аминогруппу, которые находятся у одного и того же α–углеродного атома: –Аминокислоты – это гетерофункциональные соединения. Они содержат одновременно карбоксильную и аминогруппу, которые находятся у одного и того же α–углеродного атома:Классифицируют α–аминокислоты различным образом: По химической природе радикала: Ациклические (алифатические): 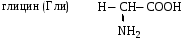 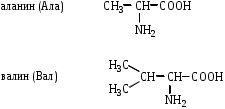 Циклические: 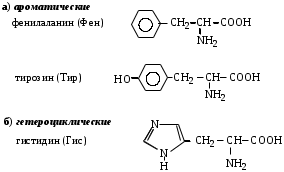 По наличию функциональных групп или по кислотно–основным свойствам: Моноаминомонокарбоновые, или нейтральные – все кислоты, указанные выше. Моноаминодикарбоновые, или кислые: 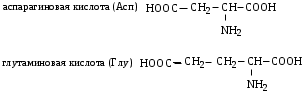 Диаминомонокарбоновые, или оснóвные:  По полярности радикалов: Неполярные. В радикалах не содержатся дополнительные функциональные группы. Это алифатические аминокислоты. Полярные. В радикалах содержатся дополнительные функциональные группы – ОН, SH, S и др.  Приведенные классификации достаточно условны, так как одна и та же кислота может быть отнесена к различным группам. Медико–биологическое значение α–аминокислот обусловлено тем, что они занимают ключевое положение в азотистом обмене. Реакции комплексообразования аминокислот играют чрезвычайно важную роль в поддержании металло–лигандного гомеостаза, а также в хелатотерапии. Многие из α–аминокислот используются как лекарственные средства, влияющие на тканевой обмен. Так, глутаминовая кислота применяется для лечения заболеваний центральной нервной системы; метионин и гистидин – для лечения и предупреждения заболеваний печени; цистеин – глазных болезней. Кроме того, цистеин является эффективным антиоксидантом, выполняя защитные функции при воздействии на организм сильных окислителей, благодаря восстановительным свойствам тиольной группы –SH. В то же время цистеин был первым препаратом, проявившим противолучевое действие. Он уменьшал степень лучевого поражения и повышал выживаемость больных. Ряд заболеваний, чаще всего врожденных, связаны с неспособностью данного организма синтезировать некоторые α–аминокислоты. Например, при фенилкетонурии человеческий организм не синтезирует тирозин, который у здоровых людей образуется из фенилаланина. Но главная биологическая роль α–аминокислот состоит в том, что они являются структурными единицами (мономерами) белков. Пептиды и белки – это природные или синтетические полимеры. Они построены из остатков α–аминокислот, соединенных пептидными или амидными связями. Пептиды имеют меньшую молекулярную массу, чем белки. Условно считают, что пептиды содержат в молекуле до 100, а белки – свыше 100 аминокислотных остатков. Молекулярная масса пептидов – до 10 тысяч; белков – от 10 тысяч до нескольких миллионов. В свою очередь пептиды подразделяют на олигопептиды и полипептиды. Олигопептиды включают до 10, а полипептиды – от 10 до 100 остатков аминокислот. Ввиду многообразия пептидов и белков их классифицируют различным образом: по составу, пространственному строению, биологическим функциям. По составу белки подразделяют на простые и сложные. Простые белки гидролизуются с образованием только α–аминокислот. Сложные белки кроме белковой части, состоящей из α–аминокислот, содержат также органическую или неорганическую часть небелковой природы. Эта небелковая часть молекулы называется "простетическая группа". По типу простетической группы различают: гемопротеины, в которых белковая часть глобин соединена с простетической группой гемом (гемоглобин, миоглобин); фосфопротеины, которые в качестве простетической группы содержат остаток фосфорной кислоты; металлопротеины – ионы металла. К сложным белкам также относят смешанные биополимеры. Их молекулы кроме белковой части могут содержать простетическую группу липидного характера (липопротеины), углеводного характера (гликопротеины) и т.д. По пространственной структуре белки делят на глобулярные и фибриллярные. Глобулярные белки растворяются в воде и солевых растворах с образованием коллоидных систем. Для них более характерна α–спиральная структура. Их макромолекула имеет форму сферы. Это яичный белок, миоглобин, почти все ферменты. Фибриллярные белки часто имеют волокнистое строение, не растворяются в воде. Для них более характерна β–структура. К ним относят: кератин волос и роговой ткани; миоинозин мускульной ткани; коллаген соединительной ткани. Контрольные вопросы по теме 1. Что называют аминокислотами? Каков состав и строение аминокислот, образующих природные белки? Как классифицируют аминокислоты? 2. Что называют изоэлектрической точкой и изоэлектрическом состоянием аминокислот (нейтральные, кислые, основные)? 3. В чем заключается амфотерность аминокислот (взаимодействие с сильными кислотами и щелочами)? Напишите уравнения химических реакций. 4. Каковы специфические реакции аминокислот (декарбоксилирование, трансаминирование, дезаминирование, взаимодействие с формалином, взаимодействие с гидроксидом меди (II) с образованием хелатного комплекса)? Каковы особенности химических свойств -, -, -аминокислот? Что называют пептидами, белками? Приведите их классификацию и биологическое значение. Как образуются пептиды и белке? Охарактеризуйте их состав, дайте названия. Опишите строение полипептидной цепи. Какие белки называют нейтральными, кислыми, основными? Изоэлектрическая точка белков. Строение пептидной (амидной) группы. Какие виды гидролиза белков выделяют? Что называется денатурацией белков? Виды денатурации. ЭТАЛОНЫ РЕШЕНИЯ СИТУАЦИОННЫХ ЗАДАЧ Диаминомонокарбоновую кислоту поместили в раствор, содержащий избыток щелочи (рН>>7). Вопрос: Будет ли эта аминокислота перемещаться в данном растворе при электрофорезе? Если да, то к (+) или (-) заряженному электроду? Ответ обоснуйте. Напишите форму аминокислоты, в которой она будет существовать в этом растворе. Решение: В водном растворе диаминомонокарбоновая кислота находиться в катионной форме, но при добавлении избытка щелочи к раствору кислоты, ее молекулы будут заряжаться отрицательно и при электрофорезе, перемещаться к положительно заряженному электроду.  изб. 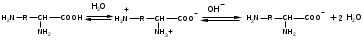 В какой раствор, содержащий избыток щелочи или избыток сильной кислоты, надо поместить моноаминомонокарбоновую кислоту, чтобы при электрофорезе она перемещалась к (-) заряженному электроду? Ответ обоснуйте. Напишите форму аминокислоты, в которой она будет существовать в выбранном растворе. Решение: Для того, что моноаминомонокарбоновая кислота перемещалась к отрицательно заряженному электроду, она должна находиться в катионной форме. Для этого кислоту необходимо поместить в кислую среду. 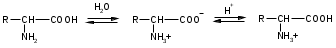 Ситуационные задачи 1. Моноаминомонокарбоновую кислоту поместили в раствор, содержащий избыток щелочи (рН>>7). Вопрос: Будет ли эта аминокислота перемещаться в данном растворе при электрофорезе? Если да, то к (+) или (-) заряженному электроду? Ответ обоснуйте. Напишите форму аминокислоты, в которой она будет существовать в этом растворе. 2. Моноаминодикарбоновую кислоту поместили в раствор, содержащий избыток щелочи (рН>>7). Вопрос: Будет ли эта аминокислота перемещаться в данном растворе при электрофорезе? Если да, то к (+) или (-) заряженному электроду? Ответ обоснуйте. Напишите форму аминокислоты, в которой она будет существовать в этом растворе. 3. Диаминомонокарбоновую кислоту поместили в раствор, содержащий избыток щелочи (рН>>7). Вопрос: Будет ли эта аминокислота перемещаться в данном растворе при электрофорезе? Если да, то к (+) или (-) заряженному электроду? Ответ обоснуйте. Напишите форму аминокислоты, в которой она будет существовать в этом растворе. 4. Моноаминомонокарбоновую кислоту поместили в раствор, содержащий избыток сильной кислоты (рН<<7). Вопрос: Будет ли эта аминокислота перемещаться в данном растворе при электрофорезе? Если да, то к (+) или (-) заряженному электроду? Ответ обоснуйте. Напишите форму аминокислоты, в которой она будет существовать в этом растворе. 5. Моноаминодикарбоновую кислоту поместили в раствор, содержащий избыток сильной кислоты (рН<<7). Вопрос: Будет ли эта аминокислота перемещаться в данном растворе при электрофорезе? Если да, то к (+) или (-) заряженному электроду? Ответ обоснуйте. Напишите форму аминокислоты, в которой она будет существовать в этом растворе. 6. Диаминомонокарбоновую кислоту поместили в раствор, содержащий избыток сильной кислоты (рН<<7). Вопрос: Будет ли эта аминокислота перемещаться в данном растворе при электрофорезе? Если да, то к (+) или (-) заряженному электроду? Ответ обоснуйте. Напишите форму аминокислоты, в которой она будет существовать в этом растворе. 7. Моноаминомонокарбоновую кислоту поместили в нейтральный раствор (рН=7). Вопрос: Будет ли эта аминокислота перемещаться в данном растворе при электрофорезе? Если да, то к (+) или (-) заряженному электроду? Ответ обоснуйте. Напишите форму аминокислоты, в которой она будет существовать в этом растворе. 8. Моноаминодикарбоновую кислоту поместили в нейтральный раствор (рН=7). Вопрос: Будет ли эта аминокислота перемещаться в данном растворе при электрофорезе? Если да, то к (+) или (-) заряженному электроду? Ответ обоснуйте. Напишите форму аминокислоты, в которой она будет существовать в этом растворе. 9. Диаминомонокарбоновую кислоту поместили в нейтральный раствор (рН=7). Вопрос: Будет ли эта аминокислота перемещаться в данном растворе при электрофорезе? Если да, то к (+) или (-) заряженному электроду? Ответ обоснуйте. Напишите форму аминокислоты, в которой она будет существовать в этом растворе. 10. В какой раствор, содержащий избыток щелочи или избыток сильной кислоты, надо поместить моноаминомонокарбоновую кислоту, чтобы при электрофорезе она перемещалась к (+) заряженному электроду? Ответ обоснуйте. Напишите форму аминокислоты, в которой она будет существовать в выбранном растворе. 11. В какой раствор, содержащий избыток щелочи или избыток сильной кислоты, надо поместить моноаминодикарбоновую кислоту, чтобы при электрофорезе она перемещалась к (+) заряженному электроду? Ответ обоснуйте. Напишите форму аминокислоты, в которой она будет существовать в выбранном растворе. 12. В какой раствор, содержащий избыток щелочи или избыток сильной кислоты, надо поместить диаминомонокарбоновую кислоту, чтобы при электрофорезе она перемещалась к (+) заряженному электроду? Ответ обоснуйте. Напишите форму аминокислоты, в которой она будет существовать в выбранном растворе. 13. В какой раствор, содержащий избыток щелочи или избыток сильной кислоты, надо поместить моноаминомонокарбоновую кислоту, чтобы при электрофорезе она перемещалась к (-) заряженному электроду? Ответ обоснуйте. Напишите форму аминокислоты, в которой она будет существовать в выбранном растворе. 14. В какой раствор, содержащий избыток щелочи или избыток сильной кислоты, надо поместить моноаминодикарбоновую кислоту, чтобы при электрофорезе она перемещалась к (-) заряженному электроду? Ответ обоснуйте. Напишите форму аминокислоты, в которой она будет существовать в выбранном растворе. 15. В какой раствор, содержащий избыток щелочи или избыток сильной кислоты, надо поместить диаминомонокарбоновую кислоту, чтобы при электрофорезе она перемещалась к (-) заряженному электроду? Ответ обоснуйте. Напишите форму аминокислоты, в которой она будет существовать в выбранном растворе. 16. В раствор с каким значением рН надо поместить моноаминомонокарбоновую кислоту, чтобы она не перемещалась при электрофорезе? Ответ обоснуйте. Напишите форму аминокислоты, в которой она будет существовать в выбранном растворе. 17. В раствор с каким значением рН надо поместить моноаминодикарбоновую кислоту, чтобы она не перемещалась при электрофорезе? Ответ обоснуйте. Напишите форму аминокислоты, в которой она будет существовать в выбранном растворе. 18. В раствор с каким значением рН надо поместить диаминомонокарбоновую кислоту, чтобы она не перемещалась при электрофорезе? Ответ обоснуйте. Напишите форму аминокислоты, в которой она будет существовать в выбранном растворе. 20. В раствор с каким значением рН надо поместить моноаминомонокарбоновую кислоту, чтобы она находилась в изоэлектрическом состоянии? Ответ обоснуйте. Напишите форму аминокислоты, в которой она будет существовать в выбранном растворе. 21. В раствор с каким значением рН надо поместить моноаминодикарбоновую кислоту, чтобы она находилась в изоэлектрическом состоянии? Ответ обоснуйте. Напишите форму аминокислоты, в которой она будет существовать в выбранном растворе. 22. В раствор с каким значением рН надо поместить диаминомонокарбоновую кислоту, чтобы она находилась в изоэлектрическом состоянии? Ответ обоснуйте. Напишите форму аминокислоты, в которой она будет существовать в выбранном растворе. ЗАДАНИЯ для II ЭТАПА экзамена (Напишите структурные формулы следующих соединений) |
