Методичка. Методичка по биоорганической химии 2 семестр СТОМ 20-21 (1). Учебнометодическое пособие для подготовки и проведения лабораторнопрактических занятий для студентов, обучающихся по специальности Стоматология (31. 05. 03)
 Скачать 0.74 Mb. Скачать 0.74 Mb.
|
ФенолыФенол (карболовая кислота), ортодигидроксибензол (пирокатехин), метадигидроксибензол (резорцин), парадигидроксибензол (гидрохинон), хинон. Задания для самостоятельного решения Окисление первичных и вторичных спиртов. Назвать продукты реакций по М.Н. Качественная реакция на многоатомные спирты на примере пропантриола-1,2,3. Уравнение реакции, подтверждающей наличие кислотных свойств у спиртов. Уравнения реакций, подтверждающих наличие кислотных свойств у фенолов. Образование простых и сложных эфиров. Элиминирование (внутримолекулярная дегидратация) спиртов. Реакция, конкурирующая с реакцией элиминирования спиртов. Назвать механизм, по которому она протекает. ТЕМА Альдегиды. Кетоны План занятия Устный опрос и коррекция знаний Лабораторная работа №3 Подведение итогов занятия УЧЕБНЫЕ ЭЛЕМЕНТЫ ТЕМЫ Альдегиды и кетоны — это производные углеводородов, содержащие карбонильную группу >С=О, называемую также оксогруппой или карбонилом. Общая формула альдегидов 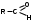 и кетонов и кетонов  Биологически активные представители альдегидов и кетонов: Альдегидная группа обуславливает наркотические и дезинфицирующие свойства соединений. 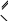 О ОН−С Н - муравьиный альдегид или формальдегид свертывает белки. Используется в виде формалина для дезинфекции и консервирования анатомических препаратов. Производные формальдегида, например, уротропин, также обладают дезинфицирующими свойствами.  О ОСН3−С Н - уксусный альдегид – естественный метаболит в организме человека.   Cl OH Cl OHCl− C − C − OH Cl H - хлоральгидрат – успокаивающее и снотворное средство. Наличие галогена усиливает специфическое действие альдегидной группы на организм, а гидратация карбонильной группы снижает токсичность вещества в целом.   СН3−С − СН3 СН3−С − СН3O - ацетон – недоокисленный продукт обмена. Образуется в организме при некоторых заболеваниях, например, диабете. Используется в синтезах рзличных лекарственных препаратов. α-галогензамещенные альдегиды и кетоны сильно раздражают слизистые оболочки носа и глаз. Они являются лакриматорами, входят в состав слезоточивых газов. КОНТРОЛЬНЫЕ ВОПРОСЫ ПО ТЕМЕ 1 Что называют альдегидами и кетонами? Каково электронное строение оксогруппы? 2. Какой тип реакции характерен для альдегидов и кетонов? Приведите примеры и запишите механизм реакции в ряду альдегидов и кетонов. 4. Как образуются открытые полуацетали и ацетали? Напишите уравнения химических реакций. 5. Как протекают реакции восстановления и окисления альдегидов? 6. Какая реакция у альдегидов и кетонов идет одновременно по механизму присоединение-отщепления? 7. Что называется кето-енольной таутомерией? Приведите примеры. 8. Какой механизм реакции альдольной и кротоновой конденсации? 9. Как протекают галоформные реакции? ЗАДАНИЯ для II ЭТАПА ЭКЗАМЕНА (Напишите структурные формулы следующих соединений) АльдегидыМетаналь (муравьиный альдегид, формальдегид), этаналь (уксусный альдегид, ацетальдегид), пропаналь, бутаналь, 3-метил-бутаналь, 2,2-диметилбутаналь, 2-метилпентаналь. КетоныПропанон-2 (ацетон), бутанон-2, пентанон-3. Задания для самостоятельного решения Взаимодействие альдегидов и кетонов с водой. Назвать механизм реакции. Взаимодействие альдегидов и кетонов с цианводородной кислотой. Назвать механизм реакции. Взаимодействие альдегидов и кетонов с первичными аминами (метиламином). Назвать механизм реакции. Образование полуацеталей и ацеталей. Альдольная конденсация. Кето-енольная таутомерия на примере альдегида. Галоформная реакция на примере этаналя. Окисление альдегидов. Назвать продукт реакции по М.Н. Восстановление альдегидов и кетонов. Назвать продукт реакции по Международной номенклатуре. ТЕМА Карбоновые кислоты. Функциональные производные карбоновых кислот План занятия Устный опрос и коррекция знаний Лабораторная работа № 4 Подведение итогов занятия УЧЕБНЫЕ ЭЛЕМЕНТЫ ТЕМЫ Карбоновые кислоты - это производные углеводородов, в которых один или более атомов замещены карбоксильной группой  : :Общая формула карбоновых кислот:  Представители монокарбоновых кислот: насыщенные:  O H−C OH - метановая /муравьиная/ кислота. Содержится в крапиве и выделениях муравьёв. При попадании на кожу вызывает ожоги. 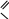 O H3C−C OH - этановая /уксусная/ кислота - естественный метаболит, продукт уксуснокислого брожения сахаров. В медицине используется в виде солей.  O H3C−CH2−CH2−C OH -бутановая /масляная/ кислота. Имеет неприятный запах, содержится в поте. ненасыщенные: -простейшим представителем ненасыщенных монокарбоновых кислот является пропеновая /акриловая/ кислота. Её эфиры используются в производстве пластмасс для медицинского приборостроения. Оксокислоты- это соединения, содержащие одновременно карбоксильную и карбонильную группы. Различают: альдегидокислоты: 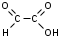 - глиоксиловая кислота, содержится в недозрелых фруктах - глиоксиловая кислота, содержится в недозрелых фруктахкетонокислоты: 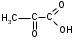 - пировиногдадная кислота - пировиногдадная кислота 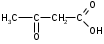 - ацетоуксуснаая кислота - ацетоуксуснаая кислота  - щавелевоуксусная кислота - щавелевоуксусная кислота  - α-кетоглутаровая кислота - α-кетоглутаровая кислота Кетонокислоты играют важную роль в биохимических процессах. Пировиноградная, щавелевоуксусная, α-кетоглутаровая кислоты участвуют в цикле трикарбоновых кислот. При их переаминировании образуются соответствующие α- аминокислоты. Пировиноградная кислота– промежуточный продукт молочнокислого и спиртового брожения углеводов. Ацетоуксусная кислота образуется в организме в процессе метаболизма высших жирных кислот и при окислении β- гидроксимасляной кислоты. Вместе с продуктами превращений она накапливается в организме у больных сахарным диабетом / ацетоновые или кетоновые тела/. Гидроксикислоты – соединения, содержащие одновременно карбоксильную и гидроксильную группы. 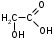 -2-гидроксиэтановая /гликолевая/ кислота. Содержится во многих растениях, свекле, винограде. -2-гидроксиэтановая /гликолевая/ кислота. Содержится во многих растениях, свекле, винограде.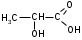 -2-гидроксипропановая кислота /молочная/. Продукт молочнокислого брожения в организме. При интенсивной работе накапливается мышцах, вызывая характерную боль. -2-гидроксипропановая кислота /молочная/. Продукт молочнокислого брожения в организме. При интенсивной работе накапливается мышцах, вызывая характерную боль.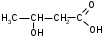 -β-гидроксимасляная кислота или 3-гидроксибутановая. Промежуточный продукт окисления жирных кислот; предшественник ацетоуксусной кислоты. Накапливается в организме у больных сахарным диабетом. -β-гидроксимасляная кислота или 3-гидроксибутановая. Промежуточный продукт окисления жирных кислот; предшественник ацетоуксусной кислоты. Накапливается в организме у больных сахарным диабетом.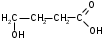 -γ-гидроксимасляная кислота /ГОМК/ или 4-гидроксибутановая. Оказываетнаркотическое действие. Применяется в виде натриевой соли как снотворное, а также в качестве неингаляционного наркотического средства в анестезиологии. -γ-гидроксимасляная кислота /ГОМК/ или 4-гидроксибутановая. Оказываетнаркотическое действие. Применяется в виде натриевой соли как снотворное, а также в качестве неингаляционного наркотического средства в анестезиологии.Контрольные вопросы по теме 1.Что называют карбоновыми кислотами? Каково электронное строение карбоксильной группы? 2. По какому механизму протекают реакции в карбоновых кислотах (образование хлорангидридов, ангидридов, амидов, сложных эфиров, ацилглицеринов (глицеридов))? 3. Какие специфические реакций характерны для дикарбоновых кислот: декарбоксилирование и образование циклических ангидридов? 4. Что называют оксокислотами? Приведите примеры. 5. Что называют гидроксикислотами? Приведите примеры. Каково их медикобиологическое значение? Какие специфические реакции характерны для гидроксикислот? 6. Каковы основные понятия стереоизомерии (асимметрический атом углерода, энантиомеры, диастереомеры, рацемат)? Проекционные формулы Фишера; относительная и абсолютная конфигурации. Нарисуйте энантиомеры молочной кислоты, изомеры L и Д-ряда. ЗАДАНИЯ для II ЭТАПА ЭКЗАМЕНА (Напишите структурные формулы следующих соединений) Карбоновые кислоты Монокарбоновые: метановая (муравьиная), этановая (уксусная), пропеновая, бутановая (масляная), пальмитиновая, стеариновая, олеиновая, линолевая, линоленовая, арахидоновая. Дикарбоновые: этандиовая (щавелевая), пропандиовая (мало-новая), бутандиовая (янтарная), пентандиовая (глутаровая), бутендиовая (фумаровая, малеиновая). Трикарбоновые: лимонная. Оксокислоты Альдегидокислоты: глиоксиловая. Кетонокислоты: 2-оксопропановая (пировиноградная), 3-оксо-бутановая (ацетоуксусная), 2-оксобутандиовая (щавелевоуксусная), 2-оксопентандиовая (-кетоглутаровая). Гидроксикислоты 2-гидроксиэтановая (гликолевая), 2-гидроксипропановая (молочная), 3-гидроксибутановая (-гидроксимасляная), 4-гидроксибутано-вая (-гидроксимасляная, ГОМК). ЗАДАНИЯ В ТЕСТОВОЙ ФОРМЕ Инструкция Выберите один или несколько правильных ответов 1.Соединения, при взаимодействии которых можно получить калийную соль метановой кислоты 1) К 2) КОН 3) Н3СОН 4) Н – СООН 2. Соединения, при взаимодействии которых получают амид пропановой кислоты 1) Н3С –СООН 2) Н3С – СН2 – СОН 3) NН3 4)  3. При двухстадийном восстановлении пропановой кислоты образуется 1) пропаналь 2) пропанол-1 3) пропен 4) пропанол-2 4. При одностадийном восстановлении уксусной кислоты образуется 1) этановая кислота 2) этаналь 3) этен 4) этанол 5. Для карбоновых кислот характерны реакции 1) электрофильного замещения 2) электрофильного присоединения 3) нуклеофильного замещения 4) нуклеофильного присоединения 6.При восстановлении карбоновых кислот на первой стадии получают 1) кислоту с меньшим числом атомов углерода 2) альдегид 3) спирт 4) кетон 7.Ацилом называют 1) продукт реакции этерификации 2) остаток карбоновой кислоты после отщепления гидроксильной группы 3) нуклеофил 4) ангидрид 8. При декарбоксилировании янтарной кислоты получают 1) уксусную кислоту 2) муравьиную кислоту 3) пальмитиновую кислоту 4) пропионовую кислоту 9. Для карбоновых кислот не характерно 1) окисление 2) восстановление 3) декарбоксилирование 4) ацилирование 10.Для ненасыщенных карбоновых кислот нехарактерна изомерия 1) геометрическая 2) оптическая 3) положения кратной связи 4) углеродного скелета 11. Линоленовая кислота содержит атомы углерода в количестве 1) 7 2) 3 3) 18 4) 17 12.Кетокислота, являющаяся естественным метаболитом и участником обменных процессов в организме 1) ацетоуксусная 2) пальмитинова 3) фумаровая 4) молочная 13. Метиловый эфир пропионовой кислоты содержит атомы углерода в количестве 1) 7 2) 3 3) 4 4) 17 14.Реакция галогенирования карбоновых кислот идет по способу 1) Фриделя-Крафтца 2) Геля-Фольгарда-Зелинского 3) Зинина-Геля 4) Фольгард-Эрдман 15.Продукт реакции межмолекулярной дегидратации α-гидроксикислот 1) лактид 2) лактон 3) лактам 4) дикетопиперазин Задания для самостоятельного решения Образование хлорангидрида карбоновой кислоты. Назвать механизм реакции. Образование амида карбоновой кислоты. Образование ангидрида карбоновой кислоты. Взаимодействие карбоновой кислоты со спиртом. К какому классу органических соединений относится продукт реакции? Декарбоксилирование дикарбоновых кислот. Образование циклического ангидрида пентадиовой кислоты. ТЕМЫ РЕФЕРАТОВ Физиологическое действие и применение в медицине арахидоновой кислоты. Применение в медицинском приборостроении акриловой кислоты. МОДУЛЬ III. УГЛЕВОДЫ. α- АМИНОКИСЛОТЫ ПЕПТИДЫ, БЕЛКИ ТЕМА Углеводы. Моносахариды План занятия Устный опрос и коррекция знаний Лабораторная работа № 5 Подведение итогов занятия УЧЕБНЫЕ ЭЛЕМЕНТЫ ТЕМЫ Моносахариды – это полигетерофункциональные соединения. В их молекулах одновременно содержатся одна оксо-группа (альдегидная или кетонная) и несколько гидроксильных групп Моносахариды классифицируют: I. По характеру карбонильной группы: 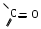  с группой – альдозы с группой – кетозы 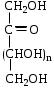 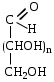 II. По числу атомов углерода в цепи: 1. Триозы: альдотриозы кетотриозы 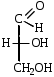  глицериновый альдегид дигидроксиацетон – простейшие представители моносахаридов. 2. Тетрозы: альдотетрозы и кетотетрозы – в природе встречаются редко. 3. Пентозы: альдопентозы:  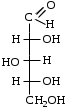  рибоза 2–дезоксирибоза ксилоза кетопентозы:   рибулоза ксилулоза 4. Гексозы: альдогексозы: кетогексозы:    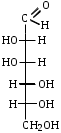 манноза глюкоза галактоза фруктоза Приведенные формулы являются проекционными формулами Фишера. С их помощью изображают моносахариды с открытой, незамкнутой цепью. Кроме того, эти формулы используют для определения относительной конфигурации моносахаридов (принадлежности к L- или Д-ряду), т.е. для изображения их стереоизомеров. Циклические формы моносахаридов Являясь гидроксиальдегидами или гидроксикетонами, открытые (незамкнутые) формы моносахаридов могут самопроизвольно превращаться в полуацетали с циклическим строением. Это обусловлено тем, что пяти– и шестиуглеродные цепи моносахаридов способны находиться в выгодной клешневидной конформации. При этом карбонильная (альдегидная или кетонная) группа сближается в пространстве со спиртовой ОН–группой у С4 или С5 . Нуклеофильный атом кислорода ОН–группы атакует элеткрофильный атом углерода карбонильной группы. В результате их внутримолекулярного взаимодействия по механизму нуклеофильного присоединения происходит замыкание цикла и образуется циклический полуацеталь. При этом группы атомов, находящиеся в цепной, незамкнутой формуле слева от линии углеродной цепи, располагаются над циклом, а находящиеся справа – под циклом. Исключение составляет ОН–группа, которая образуется при циклизации и называется полуацетальной или гликозидной. Она может располагаться как над, так и под плоскостью цикла. Этим обусловлено наличие у каждого моносахарида двух стереоизомеров (аномеров): α–аномера, если гликозидный гидроксил у моносахарида Д–ряда располагается под циклом; и β–аномера, если – над циклом: 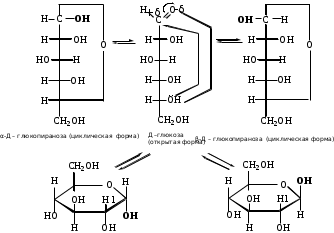 Шестичленный цикл с кислородом называется пиранозным. Вследствие этого Д–глюкозу в циклической форме называют α-Д-глюкопираноза или β-Д-глюкопираноза. Причем, у моносахаридов Д–ряда группировка СН2ОН шестого атома углерода всегда располагается над циклом. П  ятичленный цикл с кислородом называется фуранозным. Рибоза в циклической форме существует в виде двух изомеров – α-Д-рибофуранозы или β-Д-рибофуранозы. ятичленный цикл с кислородом называется фуранозным. Рибоза в циклической форме существует в виде двух изомеров – α-Д-рибофуранозы или β-Д-рибофуранозы.Несмотря на то, что фруктоза – это кетогексоза (шестиуглеродный моносахарид), в циклической форме она существует, преимущественно, в виде фуранозного цикла: 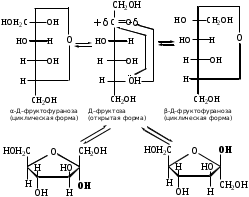 Приведенные циклические формулы моносахаридов называются формулами Хеуорса. Они не отражают реальной пространственной формы молекул, поскольку пиранозы в пространстве принимают наиболее выгодную кресловидную конформацию, а фуранозные циклы – конформацию конверта. КОНТРОЛЬНЫЕ ВОПРОСЫ ПО ТЕМЕ 1. Что называют углеводами? Какова их биологическую роль? Как классифицируют углеводы? 2. Как классифицируют моносахариды? Приведите примеры. 3 Каковы основные понятия стереоизомерии? Что называют L и Д-стереохимическими рядами? Что называют эпимерами и диастереомерами? 4. Как образуются циклические формы моносахаридов? Перечислите правила записи формул Хеуорса. Фуранозные и пиранозные циклы; и -аномеры. Что называют цикло-оксо-таутомерией? ЗАДАНИЯ для II ЭТАПА Экзамена (Напишите структурные формулы следующих соединений) |
