ГОРМОНЫ. Учебнометодическое пособие по курсу нормальной физиологии Общие закономерности гормональной регуляции
 Скачать 1.75 Mb. Скачать 1.75 Mb.
|
Основные эффекты тестостерона
Регуляция секреции тестостерона осуществляется лютеинизирующим гормоном передней доли гипофиза, этот гормон иногда называют «гормон стимулирующий интерстициальные клетки» (ГСИК). Концентрация ЛГ в свою учередь увеличивается под влиянием гонадолиберина гипоталамуса. Высокие концентрации тестостерона подавляют и секрецию ЛГ, и секрецию гонадолиберина, а низкие, наоборот, стимулируют (рисунок 9). ГОНАДОЛИБЕРИН - гипоталамический декапептид, который регулирует секрецию и фолликулостимулирующего (ФСГ) и лютеинизирующего (ЛГ) гормонов. Механизм высвобождения ФСГ и ЛГ опосредуется ц-АМФ и ионами кальция. Через 10 минут после выделения (или экзогенного введения) гонадолиберина, ФСГ и ЛГ гормоны уже обнаруживаются в эндоплазматической сети гипофизарных клеток, а через 30 минут в секреторных гранулах. ГОНАДОТРОПИНЫ - гормоны аденогипофиза - фолликулостимулирующий (ФСГ) и лютеинизирующий (ЛГ), которые мы рассматриваем вместе потому, что они секретируются одними клетками, и активируются единым гонадолиберином гипоталамуса. Основные эффекты оказывают на половые железы, причем регулируют и функции яичников и семенников, и синтез и секрецию половых гормонов. Реализация эффектов осуществляется через систему аденилатциклаза – цАМФ. Основные эффекты гонадотропинов в мужском организме
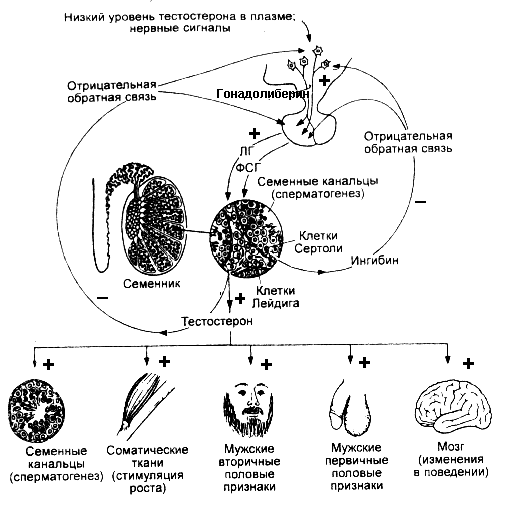 Рисунок 9. Регуляция секреции и эффекты тестостерона Женские половые гормоныК женским половым гормонам относятся эстрогены и прогестерон. В фолликулах яичников осуществляется синтез эстрогенов, желтое тело яичника продуцирует прогестерон. Основная функция по регуляции роста организма, его развития ы соответствии с полом, репродуктивной функции принадлежит эстрогенам. К эстрогенам относятся: Е1 –эстрон, Е2 – эстрадиол, Е3 – эстриол, Е4 – эстетрон, основной эстроген - Е2. Для формирования женской половой системы в эмбриогенезе не нужно специальной программы, поэтому если нет фактора регрессии мюллеровых каналов, развитие организма идет по женскому типу, при этом вырабатываются почти одинаковые количества эстрогенов и андрогенов. В пубертатном периоде эстрогены, прежде всего, завершают формирование органов женской половой сферы: влагалища, матки, фаллопиевых труб. Эстрогены стимулируют развитие и рост молочных желез. Одним из важнейших эффектов эстрогенов является их сенсибилизирующий эффект по отношению ко многим гормонам: прогестерону, пролактину, андрогенам, катехоламинам. Под влиянием эстрогенов усиливается синтез белка в печени, синтезируются транспортные альбумины для переноса витаминов и гормонов, анитигены, липопротеины, ферменты, метаболизирующие глюкокортикоиды. В гипоталамусе эстрогены стимулируют циклические центры, оказывают непосредственное действие на систему гипоталамус – гипофиз – гонады, активируют синтез окситоцина и вазопрессина. Кроме этого эстрогены влияют на развитие костного скелета, ускоряя его созревание. За счет действия на эпифизарные хрящи они тормозят рост костей в длину. Эстрогены оказывают выраженный анаболический эффект, усиливают образование жира и его распределение, типичное для женской фигуры, а также способствуют оволосению по женскому типу. Эстрогены задерживают азот, воду, соли. Под влиянием этих гормонов изменяется эмоциональное и психическое состояние женщин. Во время беременности эстрогены способствуют росту мышечной ткани матки, эффективному маточно-плацентарному кровообращению, вместе с прогестероном и пролактином - развитию молочных желез. Женский половой (овариально-менструальный) цикл Секреция женских половых стероидных гормонов (эстрогены и прогестерон), а так же овогенез и овуляция, происходят в яичниках циклически — в рамках овариального цикла средней продолжительностью 28 дней. Возможны колебания от 21 до 32 дней. Менструальный цикл обеспечивает интеграцию во времени различных процессов, необходимых для репродуктивной функции: созревание яйцеклетки и овуляцию, периодическую подготовку эндометрия к имплантации оплодотворенной яйцеклетки, изменения в организме женщины, включая поведение. Яичниковый цикл состоит из трех фаз: фолликулярной (с 1-го по 14-й день цикла), овуляторной (13-й день цикла) и лютеиновой (с 15-го по 28-й день цикла). После завершения предыдущего цикла новый фолликул включается в новый цикл. Рост фолликула происходит под влиянием фолликулостимулирующего гормона гипофиза (ФСГ) – фолликулярная фаза. В это время происходит формирование наружной и внутренней оболочек фолликула, растет и дозревает яйцеклетка. Клетки оболочки по мере роста увеличивают синтез эстрогенов, концентрация эстрогенов зависит не только от ФСГ, но и ЛГ и увеличивается к середине цикла. Именно эстрогены определяют те изменения, которые происходят в организме женщины в первую половину цикла. Рассмотрим их эффекты по отношению к различным органам. В первую очередь эстрогены усиливают рост и развитие яйцеклетки и самого фолликула. В матке под влиянием гормонов начинается пролиферативная фаза, во время которой происходит утолщение слизистой оболочки эндометрия и развитие его желез. В гипоталамусе в первой четверти цикла под действием небольших концентраций гормонов усиливается секреция ФСГ и ЛГ, на пике концентрации эстрогенов – середина цикла – подавляется секреция ФСГ. Таблица 1 Эффекты эстрогенов
Фолликулиновая фаза цикла завершается овуляцией, которая происходит на пике секреции ЛГ, обратим внимание на то, что без лютеинизирующего гормона овуляции не происходит, в этом случае цикл становится ановуляторным. После овуляции в желтом теле яичника, которое развивается на месте лопнувшего фолликула, начинает вырабатываться гормон - прогестерон. Регуляция секреции прогестерона обеспечивается ЛГ. Главная функция прогестерона - подготовка эндометрия к имплантации оплодотворенной яйцеклетки и обеспечение нормального протекания беременности. Если оплодотворение не наступает, желтое тело дегенерирует. Прогестерон вместе с эстрогенами регулирует морфологические перестройки в матке и молочных железах, усиливая процессы пролиферации и секреторной активности. В результате этого в секрете желез эндометрия возрастают концентрации липидов и гликогена, необходимых для развития эмбриона. Прогестерон усиливает гиперплазию и гипертрофию миометрия во время беременности и снижает возбудимость матки. У небеременных женщин прогестерон участвует в регуляции менструального цикла. Гормон способствует росту альвеол в молочных железах. В гипоталамусе высокие концентрации прогестерона подавляют секрецию всех тропных гормонов: ФСГ, ЛГ, ПРл. Именно поэтому и происходит кровотечение – отторжение нового слизистого слоя с сосудами. В головном мозге под влиянием прогестерона наблюдается снижение возбудимости. Прогестерон усиливает основной обмен и повышает базальную температуру тела, что используется в практике для определения времени наступления овуляции. Регуляция менструального цикла осуществляется гонадолиберином и гонадотропинами. ГОНАДОЛИБЕРИН - гипоталамический декапептид, который регулирует секрецию и фолликулостимулирующего (ФСГ) и лютеинизирующего (ЛГ) гормонов. Способность ГЛ в одних случаях стимулировать синтез и высвобождение ФСГ, а в других ЛГ объясняется модулирующим влиянием половых гормонов (различный уровень во время полового цикла) и участием простагландинов. ГОНАДОТРОПИНЫ - гормоны аденогипофиза - фолликулостимулирующий (ФСГ) и лютеинизирующий (ЛГ). Основные эффекты гонадотропинов в женском организме
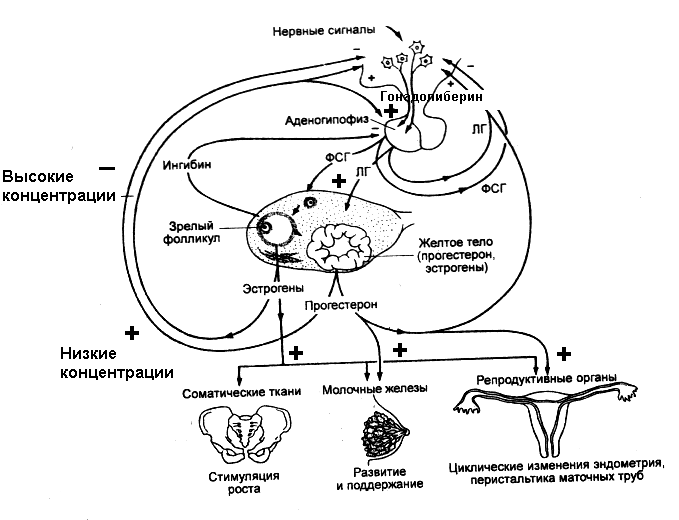 Рисунок 10. Регуляция секреции и основные эффекты женских половых гормонов 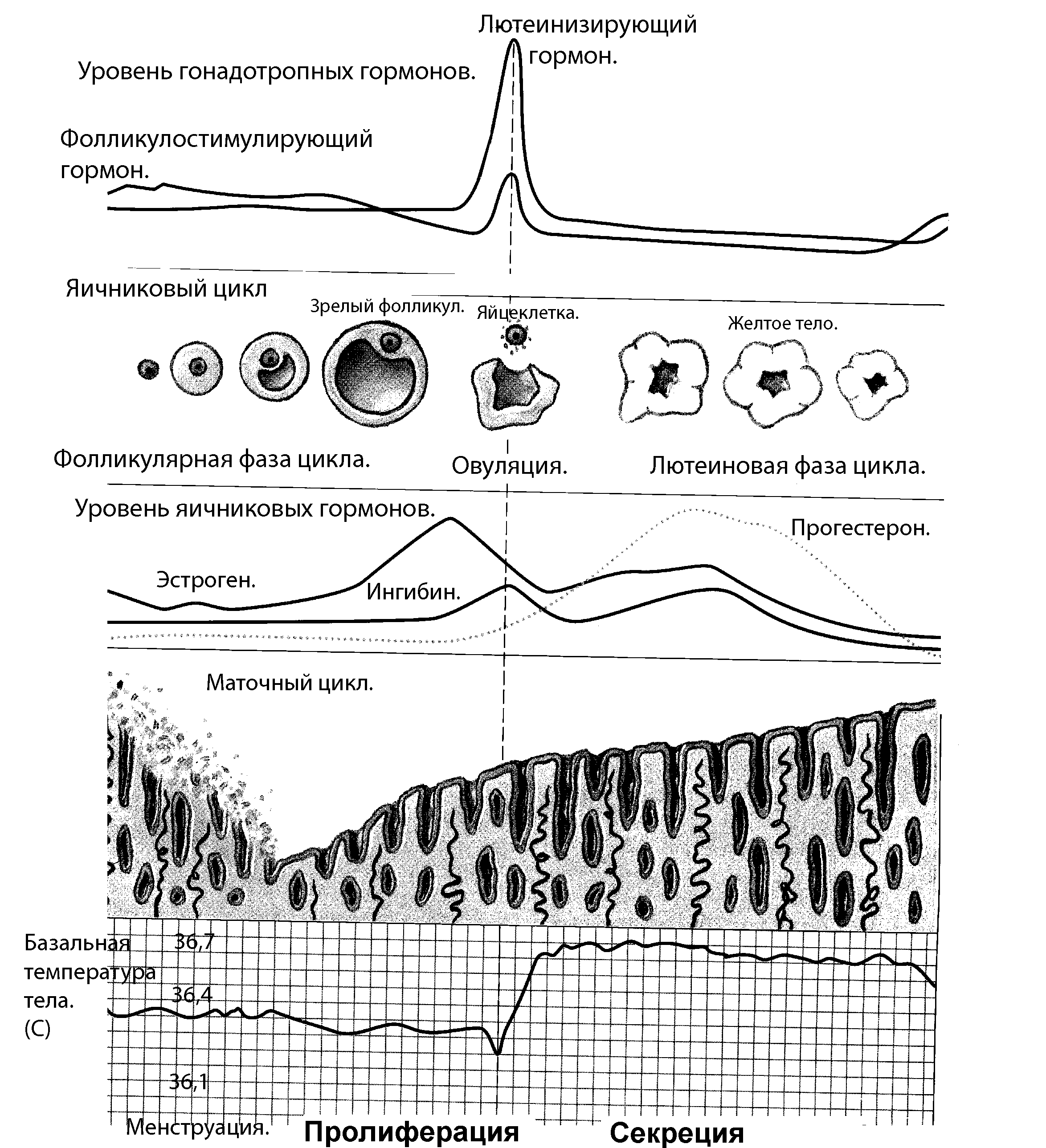 Рисунок 11. Овариально-менструальный цикл Овариальный и менструальный циклы (овариально–менструальный цикл) продолжаются в течение репродуктивного периода женщины (около 30 лет). После возрастного прекращения овариально–менструальных циклов (менопауза, климакс) в яичниках прерываются как герминативная (образование яйцеклеток), так и эндокринная (синтез эстрогенов) функции. Поскольку половые стероиды необходимы для поддержания вторичных половых признаков, в постклимактерическом периоде в некоторых случаях показан приём экзогенных эстрогенов. Плацента Плацента человека вырабатывает прогестерон, предшественники эстрогенов, хорионический гонадотропин, соматомамотропин, хориональный тиреотропин, АКТГ, окситоцин, релаксин. Гормоны плаценты обеспечивают нормальное протекание беременности. Наиболее изучен хорионический гонадотропин. По своим физиологическим свойствам он близок к гонадотропинам гипофиза. Гормон оказывает эффект на процессы дифференцировки и развитие плода, а также на метаболизм матери: задерживает воду и соли, стимулирует секрецию антидиуретического гормона и сам обладает антидиуретическим действием, стимулирует механизмы иммунитета. Из-за тесной функциональной связи плаценты с плодом принято говорить о "фетоплацентарном комплексе" или фетоплацентарной системе". Например, синтез эстриола в плаценте идет из предшественника дегидроэпиандростерона, который образуется в надпочечниках плода. Итак, половые гормоны и в женском, и в мужском организме реализуют генетическую программу пола, обеспечивают рост и развитие органов репродуктивной системы и осуществляют их регуляцию, оказывают влияние на рост и форму тела. Понятно, что только половые гормоны не могут обеспечить нормального роста всего организма, эту функцию выполняет гормон, который поэтому и получил название гормона роста. Соматотропный гормонСоматотропный гормон (СТГ), или гормон роста секретируется эндокринными клетками аденогипофиза. Одна из главных функций гормона - стимулирующее влияние на линейный рост, общие размеры тела, его массу, размеры отдельных органов. СТГ у человека начинает секретироваться уже в первой трети эмбрионального развития, однако основные эффекты проявляются значительно позднее. Соматотропный гормон принимает участие в регуляции процессов роста и физического развития. Стимуляция процессов роста обусловлена способностью соматотропина усиливать образование белка в организме, повышать синтез РНК, усиливать транспорт аминокислот из крови в клетки. Наиболее ярко влияние гормона выражено на костную и хрящевую ткани. В растущем организме к действию соматотропина наиболее чувствительна хрящевая ткань и, прежде всего, хрящи, расположенные в эпифизарной области трубчатых костей. В этой ткани СТГ усиливает пролиферацию и синтез структурных белков. Действие соматотропина происходит посредством "соматомединов", которые образуются под влиянием соматотропина. СОМАТОМЕДИНЫ - гуморальные факторы, которые синтезируются и секретируются печенью и костной тканью под влиянием соматотропина. Эффекты в хрящевой ткани: стимуляция включения сульфата в протеогликаны, стимуляция включения тимидина в ДНК, синтеза РНК и синтеза белка. Кроме того, соматомедины стимулируют митогенную активностью, причем не только в хрящевой ткани. Этим свойством они похожи на многие другие пептидные ростовые факторы, которые называются инсулиноподобными (фактор роста фибробластов, тромбоцитарный фактор роста, эпидермальный фактор роста, фактор роста нервов, эритропоэтин, тимозин), большинство этих факторов не только обладают определенной инсулиноподобной активностью, но и имеют с инсулином некоторые общие аминокислотные последовательности. Предполагается, что все эффекты этих факторов, и соматомединов в том числе, опосредованы в первую очередь стимуляцией транспорта аминокислот в клетки, хотя не понятно как это может затронуть митотическую активность. Обнаружено, что у пигмеев на фоне нормального содержания соматотропина не образуется соматомедин С, что, по мнению исследователей, служит причиной их маленького роста. Соматотропин влияет на углеводный обмен, оказывая инсулиноподобное действие. Гормон усиливает мобилизацию жира из депо и использование его в энергетическом обмене. 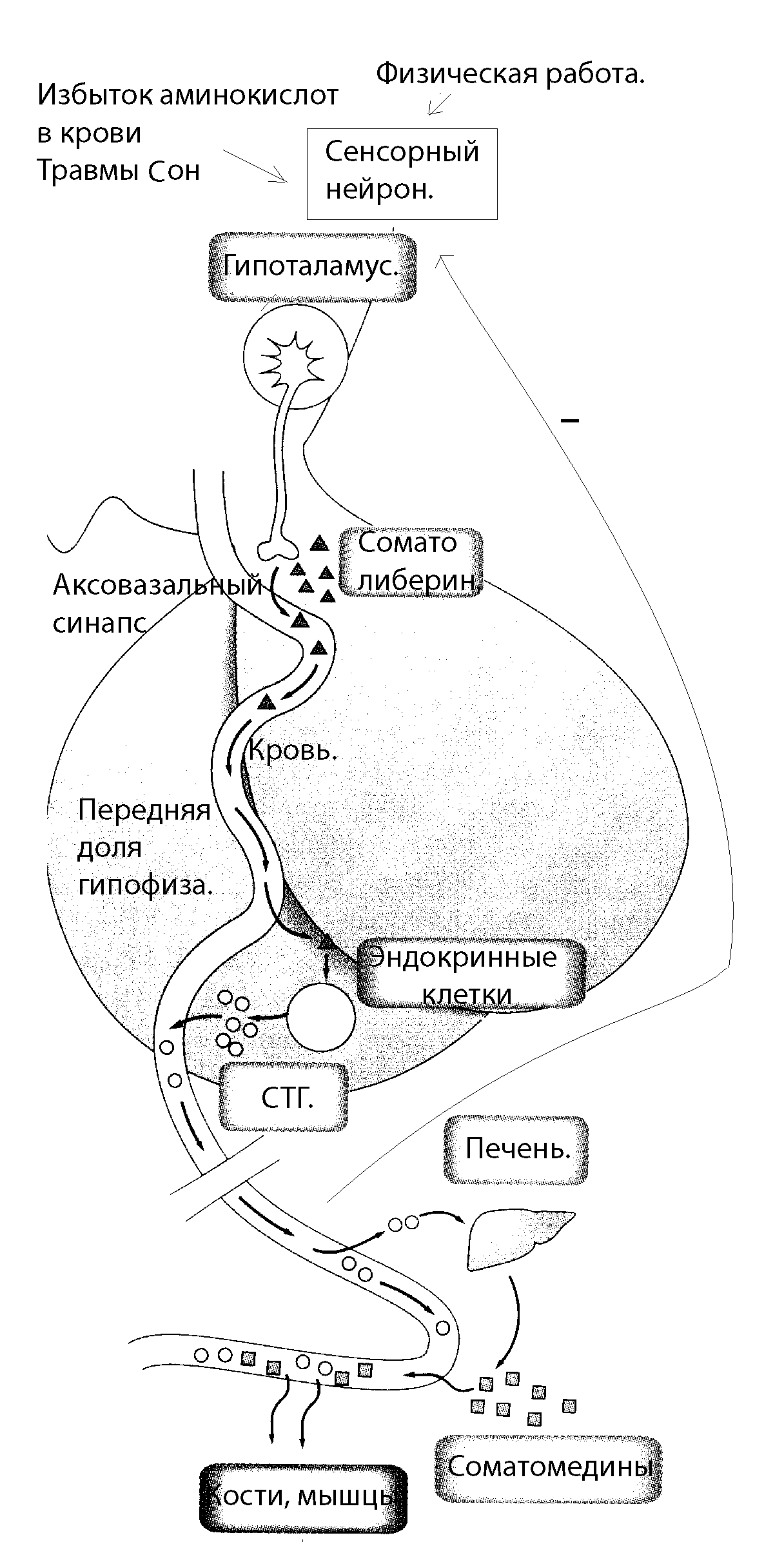 Продукция соматотропина регулируется соматолиберином и соматостатином гипоталамуса (рисунок 12). СОМАТОЛИБЕРИН - пептид, состоящий из 44 аминокислот, синтезируется преимущественно в вентромедиальном и дугообразном ядрах гипоталамуса. Селективно стимулирует секрецию соматотропного гормона. Стимулы - сон, физическая нагрузка, стрессирующие воздействия такие, как боль, физическая работа, повреждение тканей, снижение содержания глюкозы и жирных кислот, избыток аминокислот в плазме крови также приводят к увеличению секреции соматолиберина. Вазопрессин, эндорфин стимулируют продукцию соматотропина. Продукция соматотропина регулируется соматолиберином и соматостатином гипоталамуса (рисунок 12). СОМАТОЛИБЕРИН - пептид, состоящий из 44 аминокислот, синтезируется преимущественно в вентромедиальном и дугообразном ядрах гипоталамуса. Селективно стимулирует секрецию соматотропного гормона. Стимулы - сон, физическая нагрузка, стрессирующие воздействия такие, как боль, физическая работа, повреждение тканей, снижение содержания глюкозы и жирных кислот, избыток аминокислот в плазме крови также приводят к увеличению секреции соматолиберина. Вазопрессин, эндорфин стимулируют продукцию соматотропина. Рисунок 12. Регуляция секреции СТГ Если гиперфункция передней доли гипофиза проявляется в детском возрасте, то это приводит к усиленному пропорциональному росту в длину - гигантизму. Если гиперфункция возникает у взрослого человека, когда рост тела в целом уже завершен, наблюдается увеличение лишь тех частей тела, которые еще способны расти. Это пальцы рук и ног, кисти и стопы, нос и нижняя челюсть, язык, органы грудной и брюшной полостей. Это заболевание называется акромегалией. Причиной являются доброкачественные опухоли гипофиза. Гипофункция передней доли гипофиза в детстве выражается в задержке роста - карликовости ("гипофизарный нанизм"). Умственное развитие не нарушено. Эффекты соматотропина во многом сходны с эффектами кортизола, но во многих отношениях этот гормон является его антагонистом. СТГ, как и кортизол, стимулирует липолиз в жировой ткани, глюконеогенез в печени и повышает уровни глюкозы и липидов в крови - это катаболические эффекты гормона. Гипергликемия под действием СТГ поддерживается и его способностью стимулировать секрецию глюкагона, и активировать инсулиназу печени. Катаболические эффекты СТГ проявляются в случае секреции больших доз гормона, или длительной стимуляции секреции. Основные эффекты СТГ являются анаболическими и связаны со стимуляцией синтеза белка. СТГ, в отличие от кортизола, стимулирует синтез белка не только в печени, но и в других органах. Увеличение синтеза белка под действием СТГ происходит в два этапа: первый (30 минут) обусловлен активацией транспорта амминокислот и глюкозы через клеточную мембрану, второй (10 - 18 часов) - увеличением синтеза рибосомальной РНК и формированием ансамблей полисом, активацией процессов трансляции в рибосомах. СТГ стимулирует синтез белка в мышцах, мягких соединительных тканях, паренхиматозных органах не только в растущем оганизме, но и у взрослых. Однако, если у детей анаболический эффект гормона сочетается с выраженным митогенным эффектом - гормон усиливает пролиферацию клеток, способствуя их переходу из периода G1в период S (синтез ДНК), то у взрослых анаболический эффект преобладает над митогенным и приводит к гипертрофии клеток. Известно, что транспорт аминокислот в клетки печени происходит преимущественно по градиенту концентрации и не лимитирован специальными мембранными факторами. Поэтому эффекты СТГ на клетки печени не связаны с транспортом аминокислот. Усиление синтеза белка в печени под действием СТГ имеет свои принципиальные особенности - это стимуляция синтеза особых гормональных соединений - соматомединов, опосредующих многие эффекты гормона. Главным соматомедином является соматомедин С, который называется еще инсулиноподобным ростовым фактором 1 (ИРФ-1). Кроме того, под действием СТГ в тканях стимулируется выработка специальных факторов роста - факторы роста нервов, эпидермиса, тромбоцитов. Важно отметить, что все эти факторы не только опосредуют эффекты СТГ, но и существенно усиливают их, именно поэтому действие СТГ продолжается очень длительно. Одним из важных свойств СТГ является его действие на тимус. В тот период, когда эта железа еще не начала подвергаться инволюции, гормон вызывает гиперплазию и гипертрофию лимфоидной ткани железы и стимулирует иммуногенез. Однако усиливающее действие СТГ на процессы иммуногенеза сохраняются и у взрослых, гормон способен усиливать рост лимфатических желез, процессы лимфопоэза и антителообразования. Установлено, что СТГ не только стимулятор иммуногенеза, но и провоспалительный гормон. Таким образом, и в отношении иммуногенеза и процессов воспаления СТГ является антагонистом кортизола. Основные эффекты соматотропина:
Гормоны щитовидной железы Для нормального развития организма, особенно в раннем возрасте, совершенно необходимы гормоны щитовидной железы. Ткань железы состоит из фолликулов, заполненных коллоидом, в котором имеются йодсодержащие гормоны тироксин (тетрайодтиронин) и трийодтиронин в связанном состоянии с белком тиреоглобулином. В межфолликулярном пространстве расположены парафолликулярные клетки, которые вырабатывают гормон тиреокальцитонин. Содержание тироксина (Т4) в крови больше, чем трийодтиронина (Т3). Однако активность трийодтиронина выше, чем тироксина. Эти гормоны образуются из аминокислоты тирозина путем ее йодирования. Инактивация происходит в печени посредством образования парных соединений с глюкуроновой кислотой. 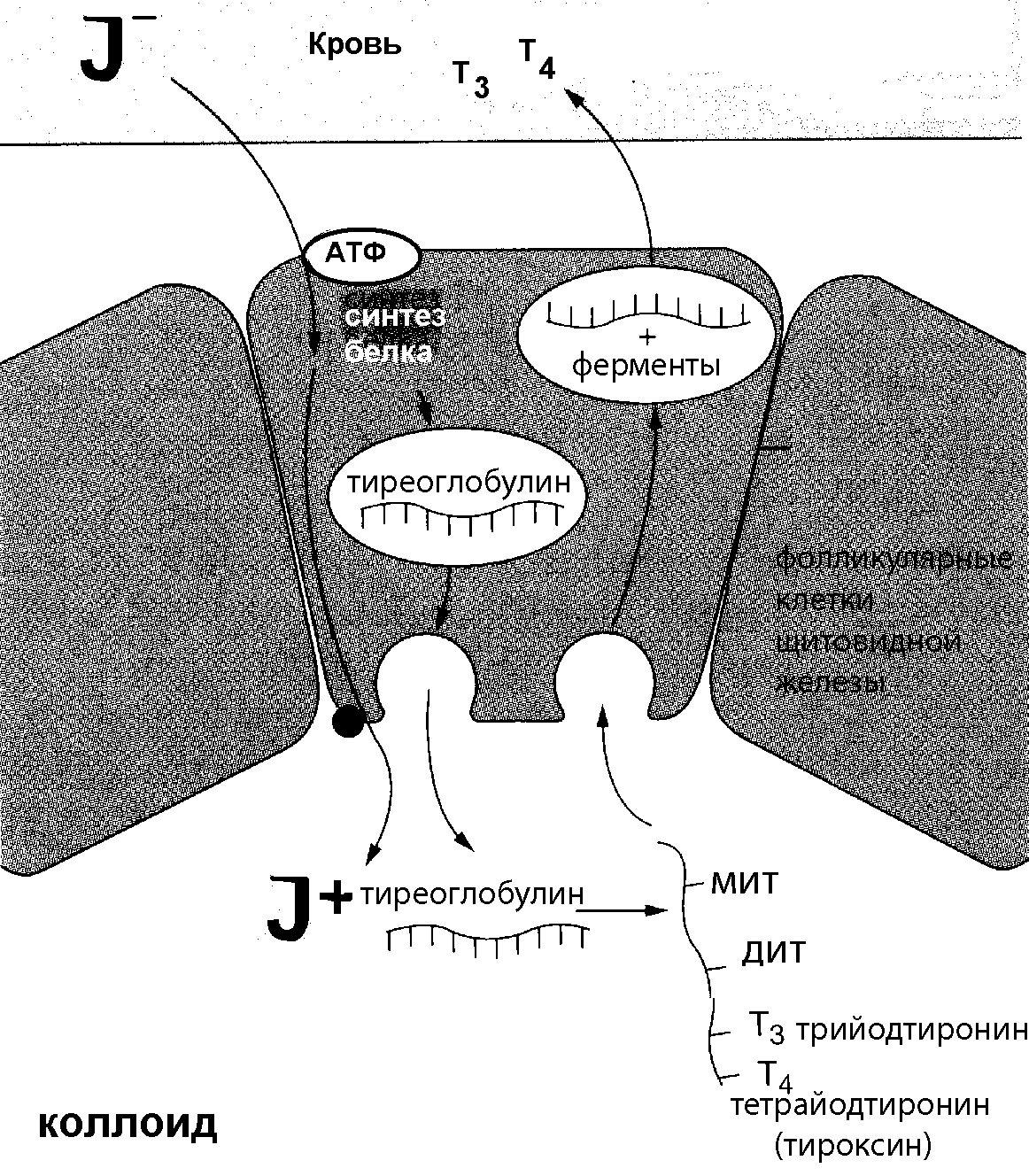 Рисунок 13. Синтез тиреоидных гормонов Регуляция синтеза и секреции тиреоидных гормонов осуществляется в соответствии с работой гипоталамо-гипофизарно-тиреоидной системы: гипоталамическим тиреолиберином и тиреотропным гормоном аденогипофиза. При недостатке йода в крови, а также йодсодержащих гормонов по механизму положительной обратной связи усиливается выработка тиреолиберина, который стимулирует синтез тиреотропного гормона, что, в свою очередь, приводит к увеличению продукции гормонов щитовидной железы. При избыточном количестве йода в крови и гормонов щитовидной железы работает механизм отрицательной обратной связи. Возбуждение симпатического отдела вегетативной нервной системы стимулирует гормонообразовательную функцию щитовидной железы, возбуждение парасимпатического отдела - тормозит ее. ТИРЕОЛИБЕРИН - трипептид гипоталамуса, который стимулирует синтез и высвобождение тиреотропина клетками аденогипофиза. Уровень тиреотропина и последующее повышение уровней тиреоидных гормонов увеличиваются уже через 5 минут после выделения тиреолиберина. Кроме того, тиреолиберин увеличивает выделение пролактина. На секрецию гормона роста у здоровых людей этот фактор не оказывает влияния, но вызывает повышение уровня СТГ в крови у больных акромегалией. Такое изменение чувствительности гипофиза настолько специфично, что используется для диагностики акромегалии. ТИРЕОТРОПИН (ТТГ) В щитовидной железе стимулирует ее рост и продукцию тиреоидных гормонов. Гормон связывается со специфическим рецептором фолликулярных клеток, в клетках активируется захват йода, синтез тиреоглобулина. Под действием ТТГ усиливается распад тиреоглобулина и секреция тиреоидных гормонов в кровь. Вне щитовидной железы гормон активирует синтез гликозаминогликанов в коже, подкожной и заорбитальной клетчатке. ТИРОКСИН (Т4) и ТРИИОДТИРОНИН (Т3) Гормоны щитовидной железы. Тетраиодтиронин (Т4) взаимодействует с клеточной мембраной, диффундирует в клетку, при этом теряет один атом йода, таким образом, основным действующим гормоном является трийодтиронин (Т3). В клетках повышается активность натрий/калиевой АТФ-азы, поглощение кислорода митохондриями, следовательно, темп окислительных процессов. Увеличивается синтез м-РНК и соответственно синтез специфических клеточных белков и ферментов. Основные эффекты можно разделить на метаболические и физиологические. Метаболические эффекты:
Основные физиологические эффекты
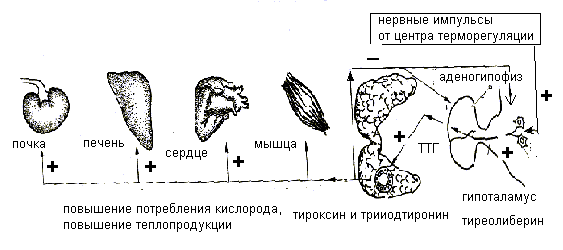 Рисунок 14. Регуляция секреции и эффекты тиреоидных гормонов Тиреоидные гормоны способствуют экспрессии гена соматотропина, и поэтому их недостаток может привести к карликовости. Врожденная недостаточность тиреоидных гормонов - гипотиреоз (наследственные дефекты, дефицит иода в организме матери) приводит к нарушению развития, особенно структур ЦНС и кретинизму. В соответствии со своими эффектами йодсодержащие гормоны выполняют в организме следующие функции:
Нарушения функции щитовидной железы проявляются ее гипофункцией и гиперфункцией. Если недостаточность функции развивается в детском возрасте, то это приводит к задержке роста, нарушению пропорций тела, полового и умственного развития. Такое патологическое состояние называется кретинизмом. У взрослых гипофункция щитовидной железы приводит к развитию патологического состояния - микседемы. При этом заболевании наблюдается торможение нервно-психической активности, что проявляется в вялости, сонливости, апатии, снижении интеллекта, уменьшении возбудимости симпатического отдела вегетативной нервной системы, нарушении половых функций, угнетении всех видов обмена веществ и снижении основного обмена. У таких больных увеличена масса тела за счет повышения количества тканевой жидкости и отмечается одутловатость лица. Отсюда и название этого заболевания: микседема - слизистый отек Гипофункция щитовидной железы может развиться у людей проживающих в местностях, где в воде и почве отмечается недостаток йода. Это так называемый эндемический зоб. Щитовидная железа при этом заболевании увеличена (зоб), возрастает количество фолликулов, однако из-за недостатка йода гормонов o6разуется мало, что приводит к соответствующим нарушениям в организме, проявляющимся в виде гипотиреоза. При гиперфункции щитовидной железы развивается заболевание тиреотоксикоз (диффузный токсический зоб, Базедова болезнь, болезнь Грейвса). Характерными признаками этого заболевания являются увеличение щитовидной железы (зоб) экзофтальм, тахикардия, повышение обмена веществ, особенно основного, потеря массы тела, увеличение аппетита, нарушение теплового баланса организма, повышение возбудимости и раздражительности. Таблица 2
Тимус Тимус, или вилочковая железа - парный орган, расположенный в верхнем средостении. После 30 лет подвергается возрастной инволюции. В вилочковой железе наряду с образованием из стволовых клеток костного мозга Т-лимфоцитов продуцируются гормональные факторы - тимозин и тимопоэтин. Гормоны обеспечивают дифференцировку Т-лимфоцитов и играют определенную роль в клеточных иммунных реакциях. Имеются также сведения, что гормоны обеспечивают синтез клеточных рецепторов к медиаторам и гормонам, например, рецепторов ацетилхолина на постсинаптических мембранах нервно-мышечных синапсов. Вопросы и задания
Роль гормонов в адаптации Адаптация Освоение не только экстремальных регионов нашей планеты, но и окружающего ближнего и дальнего космического пространства определяет особую фундаментальную и практическую значимость адаптации, которая становится одной из центральных проблем в современной биологии и медицине, проявляясь как на индивидуальном, так и на популяционном уровне. Вместе с тем, для медика не менее важно иметь представление о механизмах адаптации и к изменениям во внутренней среде: человек адаптируется и живет с удаленным желчным пузырем, долей легкого или печени, с одной почкой, адаптируется к высокому артериальному давлению, виду пищи, условиям и виду деятельности. Постоянство внутренней среды организма, которое обеспечивает и целостность клеток, и возможность выполнения ими своих функций, следовательно, и функционирование организма, является необходимым условием существования организма в постоянно меняющихся условиях внешней, окружающей нас, среды. Естественно, что в процессе эволюции все организмы приобрели способность к адаптации приспособлению к конкретным условиям обитания, проявляющейся в устойчивость к действию определенных факторов окружающей среды. Для человека проблема адаптации приобретает особое значение, во-первых, потому, что смена условий жизни, как правило, включает не только изменение основных параметров окружающей среды, но и социальные изменения, во-вторых, человек должен не просто выжить при перемене условий, но и активно работать. Индивидуальную адаптацию можно рассматривать, как процесс, в результате которого организм приобретает устойчивость к определенному фактору (факторам) окружающей среды, и, таким образом, получает возможность жить в условиях ранее не совместимых с жизнью и решать задачи, прежде не разрешимые. Адаптация включает в себя два параллельно протекающих процесса специфические изменения в системе органов, на которую ложится основная нагрузка в адаптации к конкретному повреждающему фактору и неспецифическая реакция всего организма, которая создает необходимые для специфической адаптации условия. Эту реакцию называют общим адаптационным синдромом, или стрессом. Именно этой реакции организма мы уделим особое внимание, и сделаем это по двум причинам: 1) эта реакция сопровождает любое напряжение организма, 2) эта реакция обеспечивается гормональной регуляцией, 3) в том случае, если реакция слишком выражена, или протекает долго, способна из средства адаптации перейти в основу патогенеза большого класса заболеваний. Начальный этап адаптации возникает непосредственно после начала действия раздражителя, и реализуется на основе напряжения определенной функциональной системы например, системы кровообращения, дыхательной, выделительной. Этот начальный этап называется срочной адаптацией, или аварийной фазой. Срочная адаптация это быстрое повышение активности системы, ответственной за адаптацию до пределов ее функционального резерва. Повышение активности системы происходит на основе готовых, генетически детерминированных программ. Долговременный этап адаптации возникает постепенно, в том случае, если повреждающий факторы действуют длительно или многократно. Долговременная адаптация развивается на основе многократной реализации срочной адаптации. В результате количественного накопления изменений организм приобретает новое качество, при адаптации, например к гипоксии, характеризующееся тем, что происходит увеличение числа альвеол в легких, концентрации миоглобина в миокарде, эритроцитов и гемоглобина в крови, увеличивается количество митохондрий в ткани миокарда, происходит умеренная гипертрофия миокарда. Организм становится адаптированным, приспособленным к новым условиям существования. Если сравнить срочный и долговременный этапы адаптации, то становится ясно, что переход от срочного к долговременному этапу является узловым моментом потому, что делает возможной постоянную жизнь организма в новых условиях. Из приведенного примера становится ясно, что долговременная адаптация не возможна без изменения структуры клеток, органа, или системы органов. Итак, долговременная адаптация - это повышение активности системы, ответственной за адаптацию на основании изменения ее структуры - появления системного структурного следа адаптации. Уже давно установлено и постоянно подтверждается в новых экспериментах, что темп синтеза ДНК и РНК прямо пропорционален интенсивности функционирования структуры. Выяснилось, что ключевым звеном, активирующим синтез РНК, является снижение концентрации АТФ в интенсивно работающей клетке. Оказалось, что гипертрофию клеток можно вызвать любыми воздействиями, которые снижают в ней концентрацию макроэргических фосфатных соединений. Чрезвычайно важно то, что ни повышение транспорта аминокислот, ни доставка глюкозы в клетку не приводят к активации генетического аппарата. Следовательно доставка пластического материала является необходимым, но не достаточным условием повышения синтетических процессов в клетках. Только повышение интенсивности функции клетки является тем обязательным процессом, который открывает доступ к генетическому аппарату. Энергетический баланс клетки и концентрация фосфорных макроэргических соединений - не единственный регулятор генетического аппарата клеток. Мощным индуктором процессов транскрипции является ц-АМФ, вторичный, внутриклеточный посредник большого числа гормонов и биологически активных соединений. Следовательно, активация нервной и гуморальной регуляции, стимуляция клетки тоже приводит к увеличению синтеза РНК и белка Формирование системного структурного следа в легких (при адаптации к гипоксии), скелетных мышцах (при адаптации к физической нагрузке), печени (при действии ядов и токсинов) приведет к тому, что организм приобретет устойчивость или резистентность к конкретному повреждающему агенту. Такая резистентность называется специфической. Совершенно ясно, что только одна легочная ткань, или клетки печени не в состоянии обеспечить выживание организма и его активность в новых условиях. Доставка кислорода тканям при увеличении только жизненной емкости легких не изменится, если параллельно не произойдет увеличения минутного объема крови, увеличения числа открытых капилляров в легких, увеличения концентрации гемоглобина и числа эритроцитов. Таким образом, изменяется функционирование всего организма в целом, он приобретает резистентность к гипоксии за счет подключения новых звеньев к системе, ответственной за адаптацию и общая мощность этой системы становится намного выше. Вместе с тем изменяется и деятельность других органов и систем организма. Возникают перекрестные эффекты, которые могут быть двух видов: 1). При адаптации к одному фактору среды повышается и адаптация к другим факторам (адаптация к гипоксии увеличивает адаптацию к физической нагрузке). 2) При адаптации к одному фактору среды адаптация к другим факторам снижается (адаптция к гипоксии снижает устойчивость к холоду). Такие перекрестные эффекты называются кросс-адаптациями. Кросс-адаптации могут быть и положительными, и отрицательными, могут повышать общую резистентность организма к различным повреждающим факторам и снижать ее. Формирование системного структурного следа адаптации имеет свои особенности: формирование системного структурного следа обеспечивает увеличение физиологических возможностей доминирующей системы не за счет глобального роста массы ее клеток, а за счет роста именно тех клеточных структур, которые лимитируют функцию данной системы. Системный структурный след образуется при адаптации к самым различным факторам, и конкретные морфологические изменения специфичны для каждого из повреждающих факторов. Системный структурный след почти всегда содержит некоторые избыточные компоненты. Попытаемся схематично представить основные этапы адаптации.
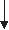
Стресс как неспецифическая реакция организма Итак, адаптация – это специфическое для каждого варианта изменение структуры системы, ответственной за эту адаптацию. Однако уже давно было отмечено, что организм реагирует на любое повреждение или сильное раздражение еще и неспецифическим ответом. Позднее были описаны характерные черты этой неспецифической реакции, и такая реакция получила название стресс. Этот термин ввел канадский исследователь Ганс Селье. После того, как были изучены и описаны гормональные, биохимические, клеточные механизмы стресса, стало ясно, что эта неспецифическая реакция, протекающая параллельно с изменениями в деятельности системы, отвечающей на конкретный раздражитель, лежит в основе морфологической перестройки и долговременной адаптации. Поэтому стресс называют еще общим адаптационным синдромом, чтобы отличить от специфической адаптации. Таким образом, понятия стресс и адаптация стали неразделимы, потому, что стало ясно: без стресса неспецифической реакции организма на любой повреждающий фактор долговременная адаптация невозможна. Если механизмы специфических адаптаций разнообразны, зависят от конкретного агента, от реактивности организма, включают в себя несколько структурных и функциональных изменений, то неспецифическая реакция довольно стандартна, протекает в соответствии с общими закономерностями, которые, правда, пока изучены далеко не все. Итак, стресс это неспецифическая реакция организма, которая возникает при воздействии различных сильных раздражителей. Эта реакция представляет собой комплекс изменений, который включает в себя реакции на всех регуляторных уровнях поведенческом, вегетативном, гуморальном, биохимическом, а так же на психическом, включая субъективные эмоциональные переживания. Воздействия, вызывающие стресс называются стрессорами. Различают физиологические и психологические стрессоры. Физиологические стрессоры оказывают непосредственное действие на клетки организма, к ним относятся боль, гипоксия, изменение осмотического давления внутренней среды, температуры, чрезмерная физическая нагрузка, давление, длительное голодание, словом все изменения, которые нарушают постоянство параметров внутренней среды организма. Понятно, что все эти стрессоры могут воздействовать как на интеро-, так и на экстерорецепторы. Психологические стрессоры это стимулы, которые сигнализируют и биологической или социальной значимости событий. Это сигналы угрозы, опасности, переживания, обиды, необходимость решения сложной задачи. Для того чтобы стать стрессирующим воздействие должно быть достаточно сильным, чтобы включить механизмы центральной регуляции, и продолжительным, чтобы поддерживать их потоком импульсов от рецепторов. Организм должен использовать все готовые, генетически определенные программы реагирования, именно в такой ситуации в организме появляется необходимость активации какой-то дополнительной, неспецифической, реакции, которая способна вывести организм из сложившегося состояния принципиально другим путем стресс. В существовании единого механизма реакции на неблагоприятное воздействие заложен глубокий биологический смысл. Угрожающие воздействия настолько разнообразны, что не может быть готовых программ для выживания и приспособления к любым условиям, поэтому в процессе эволюции выработался единый механизм, который не адаптирует сам, но создает метаболическую и структурную основу для самых разнообразных адаптаций. Физиологические механизмы стресса Центральное место в реализации стресс-реакции принадлежит эндокринной системе потому, что эта система, благодаря разнообразию гормонов и многочисленности их эффектов способна: 1) мобилизовать энергетические ресурсы (вместе с нервной системой) 2) перераспределить их в зоны, работающие с максимальной нагрузкой в данной ситуации (вместе с системой кровообращения) и 3) способствовать изменению функциональной мощности и структуры системы органов, работающих с нагрузкой (совершенно самостоятельно, потому, что способна воздействовать на активность уже имеющихся ферментных систем и имеет доступ к генетическому аппарату, следовательно, способствует синтезу новых ферментов и изменению структуры тканей). Гормональные системы, принимающие участие в реализации стресса получили название стресс-реализующих систем. В развитии стресса принято выделять несколько стадий в соответствии с уровнем резистентности организма. Неспецифическая резистентность организма, т.е. способность его сопротивляться любым повреждающим факторам, понятие весьма не конкретное, поскольку его невозможно оценить, как, например специфическую резистентность к определенному фактору, и в определенной степени условное. Однако поскольку литература пока не предлагает нам ничего другого, будем пользоваться этим традиционным, введенным еще Г. Селье термином, понимая под ним способность организма выжить, жить и активно функционировать. 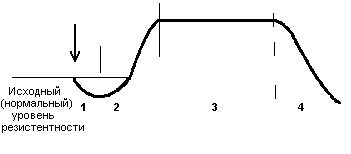 Рисунок 15. Изменение резистентности организма в соответствии с фазами стресса На рисунке стрелкой обозначено начало действия стрессора, цифрами стадии стресса, а толстой линией изменение резистентности организма:
Стадия тревоги характеризуется активной мобилизацией энергетических и структурных резервов организма. В это время резистентность организма быстро возрастает. Мобилизация энергетических ресурсов организма обусловлена совместным взаимодополняющим и взаимопотенциирующим действием симпато-адреналовой и гипоталамо-гипофизарно-надпочечниковой систем. Повышение активности симпато-адреналовой системы в ответ на стрессирующее воздействие происходит в первые же минуты, вместе с повышением активности симпатического отдела вегетативной нервной системы начинается выделение гормонов мозгового вещества надпочечников - адреналина и норадреналина. На долю адреналина приходится около 80%, на долю норадреналина - около 20% гормональной секреции. Секреция адреналина и норадреналина осуществляется хромаффинными клетками из аминокислоты тирозина. Физиологические эффекты адреналина и норадреналина аналогичны активации симпатической нервной системы, но гормональный эффект является более длительным. 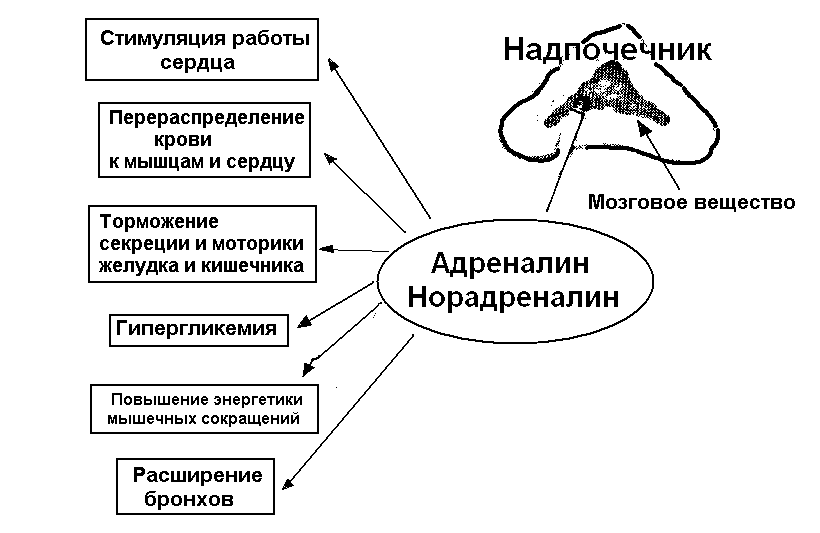 Рисунок 16. Основные эффекты катехоламинов Адреналин стимулирует деятельность сердца, суживает сосуды внутренних органов, а коронарные, сосуды легких, головного мозга, работающих мышц, наоборот, расширяет, т.к. на гладких мышцах сосудов в этих органах расположены преимущественно β-адренорецепторы. Следовательно, адреналин приводит к перераспределению крови в пользу сердца, мозга и мышц. Адреналин расслабляет мышцы бронхов, тормозит перистальтику и секрецию кишечника и повышает тонус сфинктеров, расширяет зрачок, уменьшает потоотделение, усиливает процессы катаболизма и образования энергии. Адреналин выражение влияет на углеводный обмен, усиливая расщепление гликогена в печени и мышцах, в результате чего повышается содержание глюкозы в плазме крови. Адреналин активирует липолиз. Эффекты адреналина и норадреналина опосредованы их взаимодействием с α и β адренорецепторами. Адреналин имеет большее сродство к β-адренорецепторам, норадреналин - к α-адренорецепторам. Взаимодействие катехоламинов с 1 адренорецепторами приводит к деполяризации клеточной мембраны, формированию ВПСП и образованию вторичных посредников - инозитол -3-фосфат и ионизированный Са++ Взаимодействие катехоламинов с адренорецепторами приводит в действие другую систему вторичных, внутриклеточных посредников - аденилатциклаза - ц-АМФ и гиперполяризации постсинаптической мембраны. Таблица 3Распределение адренорецепторов
Таблица 4 Основные эффекты стимуляции адренорецепторов:
Эффекты адреналина настолько разнообразны, что удобнее рассмотреть их в таблице в соответствии с действием, оказываемым на определенные системы. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
