ГОРМОНЫ. Учебнометодическое пособие по курсу нормальной физиологии Общие закономерности гормональной регуляции
 Скачать 1.75 Mb. Скачать 1.75 Mb.
|
Таблица 5Эффекты адреналина
Вторая стресс-реализующая система гипоталамо-гипофизарно-надпочечниковая система (ГГНС). Основным эффекторным гормоном ГГНС является кортизол – гормон пучковой зоны коры надпочечников, синтез и секреция которого стимулируется АКТГ гипофиза. АДРЕНОКОРТИКОТРОПНЫЙ ГОРМОН - пептидный гормон, вырабатываемый базофильными клетками аденогипофиза. У человека и животных в норме секреция адренокортикотропного гормона регулируется гипоталамусом, в нейронах которого вырабатывается кортиколиберин (АКТГ- рилизинг-фактор), стимулирующий выделение адренокортикотропного гормона в кровь. Вызванное адренокортикотропным гормоном увеличение секреции кортикостероидов по механизму отрицательной обратной связи оказывает тормозящее влияние на гипоталамус и подавляет секрецию АКТГ-рилизинг-фактора. Биологические свойства аденокортикотропного гормона целиком обусловлены структурой N-концевого участка (1-24) пептидной цепи, одинакового у разных видов животных и человека. АКТГ взаимодействует с высокоспециализированными мембранными рецепторами клеток пучковой зоны коры надпочечников. Для связывания гормона с рецепторами необходим Са++. Основной физиологический эффект АКТГ в организме - стимулирование синтеза и секреции глюкокортикоидов. Эффекты АКТГ на клетки пучковой зоны коры надпочечников реализуются через систему аденилатциклаза - ц-АМФ, их можно разделить на три основные группы в зависимости от времени ответа. 1. Срочный эффект в течение нескольких минут: облегчение под действием АКТГ связывания имеющихся в клетках запасов свободного холестерола с цитохромом Р-450. 2. Промежуточный эффект наблюдается в течение нескольких часов и заключается в индукции синтеза цитохромов и других ферментов стероидогенеза. Происходит не просто повышение активности ферментов, а именно увеличение их синтеза, потому, что в клетках резко повышается концентрация новых м-РНК. 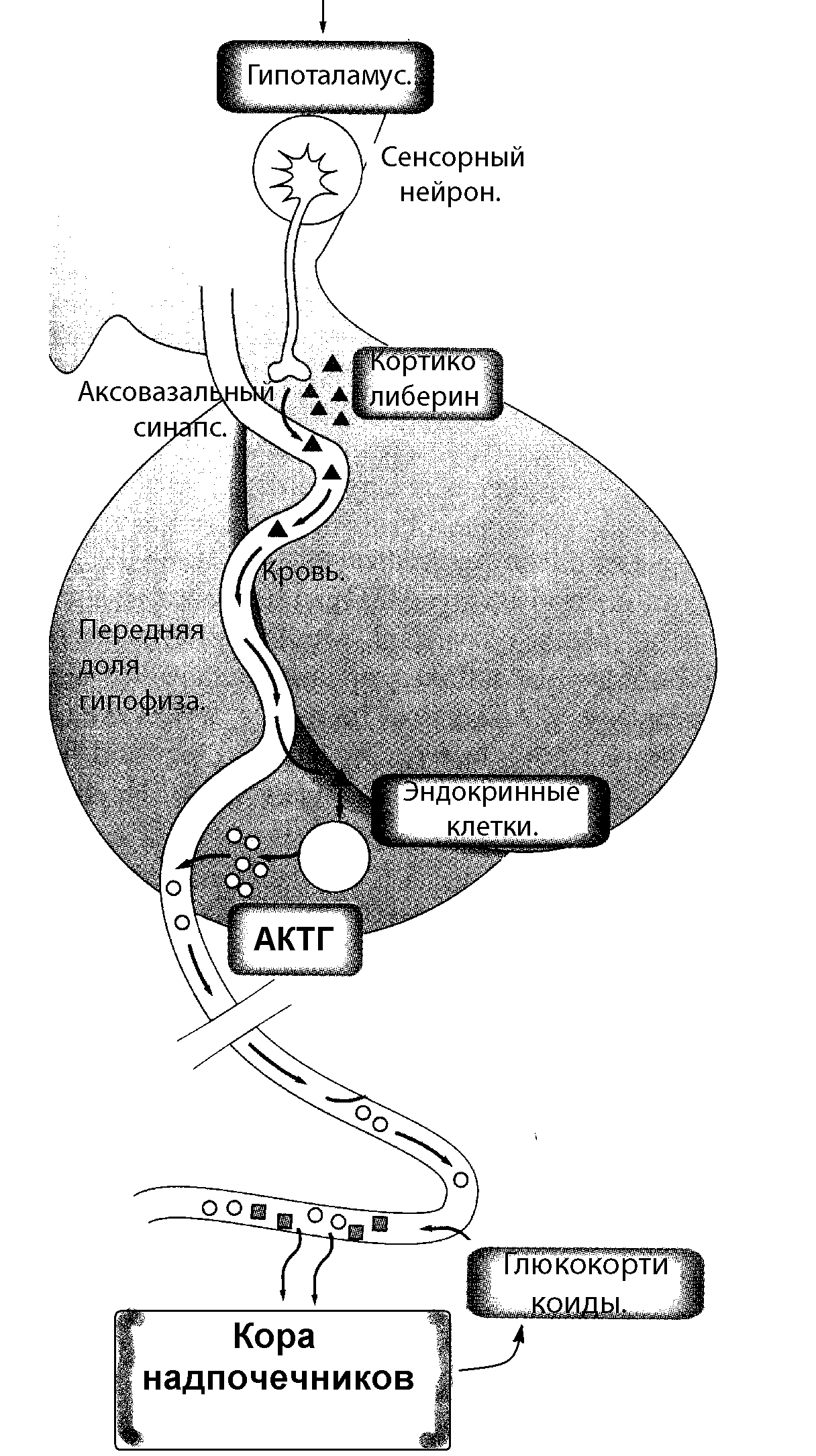 3. Хронический эффект - от часов до суток - гипертрофия и гиперплазия клеток железы. АКТГ в данном случае не только увеличивает общее содержание белка и ДНК и число митозов в клетках, но и повышает проницаемость клеток для аминокислот, глюкозы и ЛПНП. В случае длительного воздействия гормона на клетки коры надпочечников основным источником холестерола служат практически неограниченные его запасы в крови, где он находится в составе ЛПНП. 3. Хронический эффект - от часов до суток - гипертрофия и гиперплазия клеток железы. АКТГ в данном случае не только увеличивает общее содержание белка и ДНК и число митозов в клетках, но и повышает проницаемость клеток для аминокислот, глюкозы и ЛПНП. В случае длительного воздействия гормона на клетки коры надпочечников основным источником холестерола служат практически неограниченные его запасы в крови, где он находится в составе ЛПНП. Рисунок 16. Функциональная организация гипоталамо-гипофизарно-надпочечниковой системы. Гипоталамический кортиколиберин стимулирует секрецию АКТГ гипофизом. АКТГ стимулирует секрецию глюкокортикоидов в коре надпочечников. Эти гормоны, поступая в кровь и оказывая свои эффекты на клетки и ткани организма, одновременно тормозят выработку и АКТГ, и кортиколиберина. Кроме непосредственно го влияния на надпочечники, аденокортикотропный гормон обладает рядом вненадпочечниковых эффектов. Он проявляет меланоцитостимулирующую активность, которая обусловлена присутствием в молекуле 13 аминокислотных остатков N -концевого участка, повторяющих последовательность аминокислот в -меланоцитостимулирующем гормоне (-МСГ). АКТГ обладает также липотропным действием, выражающемся в активации липазы жировой ткани и повышении выхода свободных жирных кислот из жировых депо в кровь. Этот эффект гормона невелик и непродолжителен, однако наступает быстро. Минимальным фрагментом молекулы адренокортикотропного гормона, еще обладающим заметной меланоцитостимулирующей и липотропной активностью, является пентапептид NH2-Гис- Фен- Арг- Три- Гли- OH. АКТГ повышает секрецию инсулина и соматотропина. В ЦНС при увеличении секреции АКТГ повышается скорость образования и прочность условных рефлексов. Основные эффекты АКТГ
Обсуждая вненадпочечниковые эффекты АКТГ, необходимо учитывать то, что АКТГ выделяется в качестве фрагмента очень большой молекулы – проопиомеланокортина, поэтому одновременно с АКТГ в крови и структурах ЦНС появляются вещества с высокой биологической активностью: липотропин, эндорфин. ПРООПИОМЕЛАНОКОРТИН - предшественник ряда гормонов аденогипофиза, состоящий из 239 аминокислот. В таблице представлены пептиды, которые получаются из проопиомеланокортина (цифрами отмечено число аминокислот). МСГ - меланоцитстимулирующий гормон.
Собственные эффекты кортизола, основного глюкокортикоида пучковой зоны коры надпочечников, чрезвычайно разнообразны и осуществляются несколькими путями: это влияние на тимико-лимфоидную ткань, метаболизм, ЦНС и сердечно-сосудистую систему. Кортизол вызывает лизис тимико-лимфоидной ткани и быстрый выброс в кровь антител из разрушающихся лимфоидных клеток. Этот эффект обеспечивает срочную защиту от проникающих бактерий и чужеродных белков, однако образование иммунных антител тормозится. Эффекты кортизола в ЦНС и сердечно- сосудистой системе в большой степени являются косвенными кортизол повышает возбудимость нейронов, гладких и сердечной мышцы, потому что способствует накоплению ионов кальция в клетках. Следовательно, эти структуры становятся более возбудимыми и легче отвечают на воздействие, например адреналина. Такие эффекты глюкокортикоидов называются пермиссивными. Кортизол, обладая незначительным минералокортикоидным эффектом, вызывает задержку натрия и повышение объема циркулирующей крови. Чрезвычайно важны для адаптации метаболические эффекты кортизола: увеличение концентрации глюкозы жирных кислот в крови. Эти метаболиты обеспечивают энергией интенсивно работающие ткани. Таблица 6 Влияние глюкокортикоидов на обмен белков, жиров и углеводов
Еще одна важная система, которая обеспечивает рост тканей и органов, ответственных за адаптацию – система соматотропин – соматомедины. Эффекты этого гормона уже рассмотрены, поэтому понятно, что под действием этого гормона происходит включение аминокислот в клетки, синтез в них белков, пролиферация клеток и увеличение мощности системы, ответственной за адаптацию. Обратим внимание лишь на то, что при высоких концентрациях СТГ одновременно с ростовыми реализуются и контринсулярные эффекты гормона (рисунок 17). 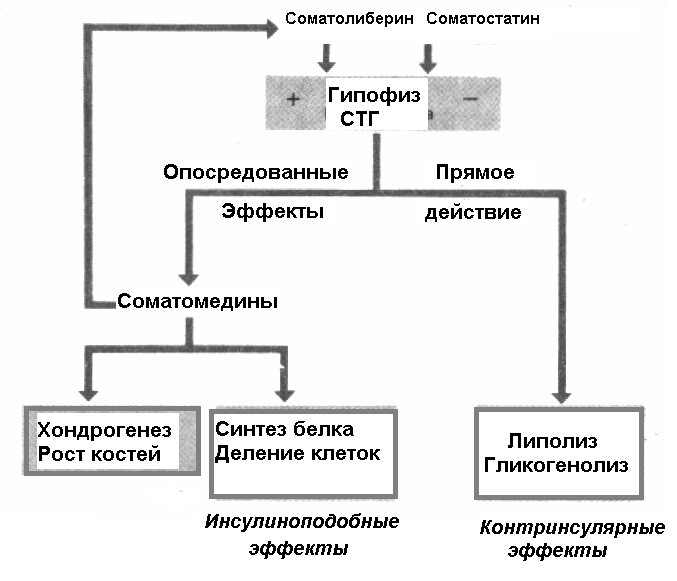 Рисунок 17. Ростовые и метаболические эффекты СТГ Таким образом, в реализации стресса параллельно протекают две цепи событий: первая это мобилизация системы, которая доминирует при адаптации к конкретному повреждающему фактору, и вторая, совершенно не специфическая, которая активируется при действии любого сильного или нового раздражителя. Эта вторая цепь событий выполняет три важнейшие и необходимые для адаптации функции: 1. Мобилизация энергетических и структурных ресурсов организма, которая проявляется в повышении уровней глюкозы, аминокислот и жирных кислот в крови и их доступности для тканей. 2. Перераспределение ресурсов и направление их в доминирующую систему. Перераспределение происходит в результате избирательного расширения сосудов работающих мышц, активно работающих органов. Такое расширение сосудов обеспечивается не только гормональными влияниями, но и местными механизмами, прежде всего расширением капиллярных сфинктеров под влиянием углекислоты, накапливающейся в интенсивно работающих клетках. Кроме того, такие метаболиты как молочная кислота, АДФ, оксид азота тоже обладают вазодилататорными эффектами. 3. Активация совместно с метаболитами-регуляторами процессов синтеза нуклеиновых кислот и белка в системе, ответственной за адаптацию приводит к формированию системного структурного следа и повышению мощности и эффективности в доминирующей системе. Все эти три приводящие к адаптации функции возможны при активации симпато-адреналовой, гипоталамо-гипофизарно-надпочечниковой систем и системы соматолиберин-соматотропин-соматомедины. Необходимо остановиться еще на одной системе, которая не является классической стресс-реализующей, но принимает обязательное участие в реакции – система ТТГ-тиреоидные гормоны. Эффекты гормонов описаны выше, значение их заключается в повышении темпа метаболизма (поглощение кислорода, окисление и фосфориллирование, накопление АТФ) и увеличении синтеза специфических белков в тканях. Повреждающее действие стресса Начиная обсуждение повреждающих эффектов сильного или длительного стресса, вспомним триаду Г. Селье, в которую входят: гипертрофия коры надпочечников, атрофия тимико - лимфоидной системы и язвы желудка и кишечника, и попытаемся найти возможные причины этих повреждений. Возможные, потому что окончательно механизмы этих повреждений пока не установлены. Повреждающее действие стресса можно рассматривать с нескольких позиций: 1) напряжение и поломка системы, ответственной за адаптацию, 2) прямые повреждающие эффекты избытка гормонов стресс-реализующих систем и 3) нарушение деятельности органов и систем, в которых длительно обедняется кровообращение в результате перераспределения крови к системе, ответственной за адаптацию. Первый вариант не рассматриваем – он зависит от конкретной ситуации, к которой происходит адаптация, это касается и третьего пункта. Остановимся на неспецифических механизмах повреждения. Одной из стресс- реализующих систем является симпато-адреналовая система со своими эффектами, направленными, в частности, на деятельность сердечно-сосудистой системы. Высокие концентрации адреналина и интенсивное выделение норадреналина симпатическими волокнами увеличивают и частоту, и силу сердечных сокращений, оказывают сосудосуживающий эффект, что приводит к повышению артериального давления. Наряду с этим происходит перераспределение крови с обеднением кровоснабжения внутренних органов в пользу сердца, мозга, скелетных мышц. Это обеднение кровью внутренних органов является общим, далеко не единственным механизмом образования язв кишечника. Накопление в кардиомиоцитах и сосудистых гладких мышцах ионов кальция в результате деполяризующего эффекта норадреналина повышает реактивность этих структур и по отношению к адреналину, и по отношению к другим биологически активным веществам. Повышение возбудимости миокарда может лежать в основе возникновения экстрасистол и аритмий. Адреналин оказывает возбуждающее влияние на структуры головного мозга, в частности на эрготрофные зоны гипоталамуса и приводит к стойкому возбуждению сосудодвигательного центра, повышению выработки АКТГ и тиреотропина гипоталамусом, а так же, у ряда лиц, повышает аппетит, что сопровождается увеличением веса. Все это свидетельствует о том, что чрезмерное повышение активности САС может быть пусковым механизмом развития артериальной гипертензии, ИБС и являться фактором риска в развитии вторичных иммунодефицитов и заболеваний связанными с эти состоянием. Повышение активности гипоталамо-гипофизарно надпочечниковой системы проявляется в значительном и длительном увеличении концентрации в крови глюкокортикоидов. Эти эффекты очень разнообразны, поэтому представим их в таблице. Таблица 6 Эффекты избытка глюкокортикоидов
Выделены комплексы признаков, характерные для длительного стресса. Эти признаки оказались столь важными в клинике, что объединены в триады: кальциевая и липидная. Понятно, что основные эффекты кальциевой триады реализуются в мышечной ткани, например в миокарде эта триада проявляется в: контрактуре миофибрилл, повреждении митохондрий, активации миофибриллярных протеаз. В своем максимальном проявлении кальциевая триада приводит к некробиозу миокарда, при умеренном проявлении - к повышению возбудимости и сократимости миокарда, нарушению процесса расслабления. Чрезмерное напряжение процессов мобилизации жира при длительном стрессе оказалось настолько важным фактором повреждения клеток, что получило у клиницистов название «липидной триады», которая включает активацию липаз и фосфолипаз, детергентное действие высоких концентраций СЖК и активацию ПОЛ. Перечислим повреждающие эффекты липидной триады. Активация ПОЛ приводит к появлению продуктов свободно радикального окисления, которые вызывают хромосомные аберрации, следовательно, нарушают и процессы деления клеток, и регенерации тканей. Повышение активности липаз приводит к накоплению в клетках капель жира и повреждению мембран. Повреждение мембран, в свою очередь, приводит к набуханию митохондрий, их слипанию, разобщению процессов окисления и фосфориллирования, а затем и к нарушению их при разрушении митохондрий. Повреждение клеточной мембраны и мембран лизосом приводит к тому, что лизосомальные ферменты выходят из клеток и процесс клеточного разрушения многократно ускоряется. В последнее время все более укрепляется мнение о том, что устойчивость к стрессирующему воздействию является в конечном итоге устойчивостью клеточных мембран к повреждению. | ||||||||||||||||||||||||||||||||||||||||||||||||||
