Л_Р Физика атомов и молекул_43_44_46_52. Учебное пособие по выполнению лабораторных работ по физике (модуль 6 Атомная физика) для студентов инженернотехнических направлений подготовки
 Скачать 2.11 Mb. Скачать 2.11 Mb.
|
|
МИНИСТЕРСТВО НАУКИ И ВЫСШЕГО ОБРАЗОВАНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ федеральное государственное бюджетное образовательное учреждение высшего образования «Сибирский государственный университет науки и технологий имени академика М. Ф. Решетнева» Кафедра технической физики Рекомендовано для использования в учебном процессе методической комиссией института НОЦ ИКИВТ____ протокол № __ от «__» _______ 2020_ г. Ф И З И К А АТОМНАЯ ФИЗИКА Учебное пособие по выполнению лабораторных работ по физике (модуль 6 «Атомная физика») для студентов инженерно-технических направлений подготовки очной и очно-заочной форм обучения Красноярск, 2020 Маркова, О.Ю. ФИЗИКА. АТОМНАЯ ФИЗИКА. Учебное пособие по выполнению лабораторных работ по физике (модуль 6 «Атомная физика») для студентов инженерно-технических направлений подготовки очной и очно-заочной форм обучения / О.Ю. Маркова, Т.С. Розанова: М-во науки и высш. образования Рос. Федерации, Сиб. гос. ун-т науки и технологий им. акад. М. Ф. Решетнева. - Красноярск: СибГУ им. М.Ф. Решетнева, 2020. – 70 с. Рецензент: канд. физ.-мат. наук, доцент, доцент кафедры Вопилова Л.В. © О.Ю. Маркова, Т.С. Розанова, 2020 © ФГБОУ ВО «Сибирский государственный университет науки и технологий имени академика М.Ф. Решетнева», 2020 ВВЕДЕНИЕ Методические указания к выполнению лабораторных работ по физике (модуль 6 «Атомная физика») предназначены для самостоятельной подготовки студентов I и II курсов инженерно-технических специальностей всех форм обучения. Методические указания содержат лабораторные работы № 43 «Исследование оптического спектра атомарного водорода и определение постоянной Ридберга», № 44 «Оптические спектры атомов ртути и неона», № 46 «Изучение принципа действия лазера и оценка параметров лазерного излучения», № 52 «Изучение бета-распада». Данные лабораторные работы способствуют усвоению и закреплению пройденного материала, а также проверке знаний студентов. Методические указания содержат: теоретическую часть, в которой даны основные законы и формулы, а также их следствия; задания и методические указания по выполнению лабораторной работы; контрольные вопросы для самоподготовки и список рекомендуемой литературы. К лабораторной работе студенты готовятся самостоятельно. Подготовка к выполнению лабораторной работы предусматривает изучение теоретического материала и содержания лабораторной работы по методическому указанию, а также по рекомендуемой литературе. В рабочей тетради необходимо сделать письменную подготовку, которая должна включать: наименование работы, цель работы, приборы и принадлежности, теоретическое введение, схему установки, таблицы для записи результатов измерений и вычислений и необходимые расчётные формулы. В отчёте должно быть предусмотрено место для графиков экспериментально полученных зависимостей, графики можно сделать на миллиметровке, и приложить к отчёту. Студенты, не имеющие подготовки и не сдавшие отчёт по предыдущей лабораторной работе, к выполнению очередной лабораторной работы не допускаются. Перед выполнением работы необходимо внимательно ознакомиться с измерительными приборами и схемой установки. После окончания выполнения опытов, не отключая её, предъявляют результаты работы преподавателю, который, убедившись в том, что данные эксперимента записаны правильно, разрешает выключить схему. Рекомендуется обработку экспериментальных данных и построение графиков проводить в лаборатории в целях полного использования времени, отведённого для лабораторных занятий. На защиту лабораторной работы студенты должны представить полностью оформленный отчёт. После сдачи отчёта преподавателю работа должна быть защищена. Защита осуществляется в виде устных ответов на вопросы к данной лабораторной работе или в какой-либо другой форме по усмотрению ведущего преподавателя. Требования правил техники безопасности: Лабораторную работу можно выполнять только на исправной установке. Запрещается включение приборов без преподавателя или лаборанта. При обнаружении неисправности или нарушения изоляции проводов лабораторную установку нужно немедленно обесточить, и сообщить об этом преподавателю или лаборанту. Сборка и разборка схемы, а также любые изменения соединений элементов схемы, производятся только при отключении от сети напряжения. ЛАБОРАТОРНАЯ РАБОТА № 43 Исследование оптического спектра атомарного водорода и определение постоянной Ридберга ЦЕЛЬ РАБОТЫ: Изучение сериальной закономерности в спектре атомарного водорода. Определение постоянной Ридберга, путем измерения длин волн видимой части спектра излучения атомарного водорода. ПРИБОРЫ И ПРИНАДЛЕЖНОСТИ: универсальный спектрометр – монохроматор МУМ, водородная лампа с источником питания, оптическая скамья с рейтерами. Теоретические сведения Оптические спектры атомов Все нагретые тела являются источниками электромагнитного излучения. Совокупность длин волн электромагнитного излучения, испускаемых источниками, называется спектром его излучения. Характер спектра излучения определяется температурой и природой источника. Оптическое излучение– это электромагнитные волны, длина которых заключена в диапазоне (10-3÷10-9) м. Помимо воспринимаемого человеческим глазом видимого излучения, к оптическому диапазону относится инфракрасное и ультрафиолетовое излучение. Именно в оптическом диапазоне отчетливо проявляются одновременно и волновые и корпускулярные свойства электромагнитного излучения. Спектр – совокупность всех значений какой-либо физической величины, характеризующей систему или процесс. В данном случае это – совокупность частот или длин волн, на которые может быть разложено оптическое излучение. Спектр можно наблюдать визуально, можно также регистрировать каким-либо прибором. Излучение, испускаемое нагретыми твердыми телами и жидкостями, обладает непрерывным (сплошным) спектром, т.е. содержит все длины волн видимого диапазона без исключения. Линейчатый спектр. Спектр излучения атомарных газов и паров представляет собой набор отдельных линий с характерными значениями длин волн, обусловленными структурой электронных оболочек атомов данного элемента. Полосатые спектры возникают при свечении молекулярных газов и паров, представляют собой сгруппированные по определенному закону совокупности спектральных линий. Количество и расположение линий в спектре излучения газа или пара зависят от структуры химического элемента или соединения. По спектру излучения с помощью спектрального анализа можно выявлять наличие отдельных элементов в соединении и определять химический состав вещества. В отличие от спектра испускания, который получается при разложении излученного телом света, спектр поглощения возникает, когда вещество поглощает из белого света отдельные спектральные линии. При этом получается непрерывный (сплошной) спектр, в котором отсутствуют отдельные спектральные линии. Твердые тела и жидкости имеют широкие области поглощения. Газы и пары поглощают только излучения с теми длинами волн, которые они сами излучают. Это так называемые линии поглощения. Как и спектр испускания, спектр поглощения используется при спектральном анализе для обнаружения и идентификации веществ. Наиболее изученным спектром поглощения, является солнечный спектр. При прохождении света через газовую оболочку Солнца возникают многочисленные линии поглощения, которые называются фраунгоферовыми линиями. Разряженные газы и пары (возбужденные атомы) дают излучение, состоящее из отдельных линий (линейчатый спектр). Распределение этих линий для большинства атомов представляет собой сложную картину, но для атома водорода и водородоподобных ионов она достаточно проста. Спектры таких атомов представляют собой группы (серии) линий, причем эти серии четко разделены, и находятся в инфракрасной, видимой и ультрафиолетовой частях спектра. Наиболее простой линейчатый спектр – спектр атомарного водорода – состоит из нескольких серий: серии Лаймана, серии Бальмера, Пашена, Брэкета и Пфунда. Закономерность расположения линий в спектре водорода выражается эмпирической формулой Бальмера где - длина волны спектральных линий, R- постоянная Ридберга (R = 1,09737107 м-1) ,niи nk –целые числа от 1 до , причем nk= ni+1. Серии в спектре испускания атомарного водорода расположены в различных областях спектра а) серия Лаймана — крайняя ультрафиолетовая область, ni= 1, nk= 2, 3,…,; б) серия Бальмера — видимая и близкая ультрафиолетовая области, ni= 2, nk= 3, 4,…,; в) серия Пашена — инфракрасная область спектра, ni= 3, nk= 4, 5,…,; г) серия Брэккета — инфракрасная область спектра, ni= 4, nk= 5, 6,…,; д) серия Пфунда — инфракрасная область спектра, ni= 5, nk= 6, 7,…,. Схема энергетических уровней атома водорода и соответствующих переходов показана на рисунке 43.1. Заштрихованные переходы соответствуют границе серии и определяются формулой (43.1). 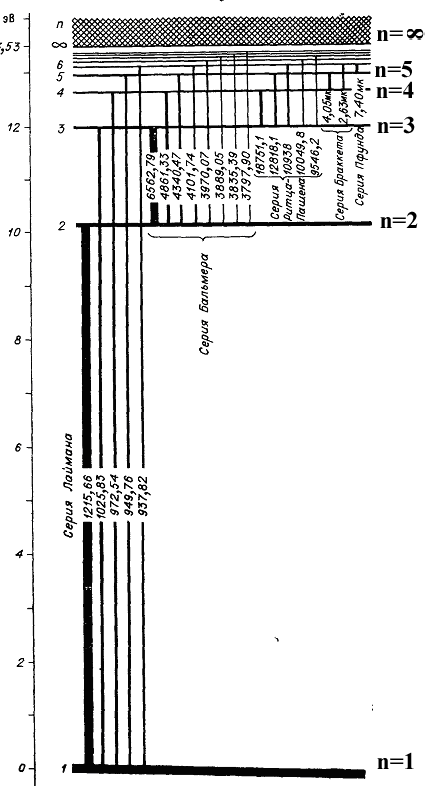 Рисунок 43.1. Энергетические уровни атома водорода. В спектрах атомарного водорода визуально наблюдается лишь серия Бальмера, четыре линии которой находятся в видимой области спектра и соответственно обозначаются следующим образом: Красная линия Н (nk= 3) Сине-голубая Н (nk= 4) Голубая Н (nk= 5) Фиолетовая Н (nk= 6) Разработка теоретического обоснования формулы Бальмера способствовала созданию квантовой теории атома (Н.Бор, 1913 г.). Формула (43.1) получается из решения квантовомеханического уравнения Шредингера для атома Водорода. Сериальная структура — одна из важнейших закономерностей строения атомных спектров. Сериальные закономерности представляют собой яркое проявление квантовых свойств излучающих атомных систем. Линии линейчатого спектра атомов газа, находящегося при низком давлении, могут быть объединены в определенные, закономерно построенные группы — так называемые серии. Длины волн всех линий, принадлежащих к одной и той же серии, связаны между собой. |
