Реферат Отбор и подготовка пробы. реферат. В ходе почти любого анализа можно выделить следующие основные этапы
 Скачать 36.91 Kb. Скачать 36.91 Kb.
|
СодержаниеВведениеПриступая к анализу данного вещества, необходимо сначала подготовить его соответствующим образом к анализу, и лишь потом приступить к исследованию. Подготовка исследуемого вещества к анализу представляет собой очень важную часть всего исследования. В ходе почти любого анализа можно выделить следующие основные этапы: 1) Отбор и усреднение пробы, и взятие навески; 2) Разложение (вскрытие) пробы, растворение; 3) Разделение (выделение определяемого компонента) и концентрирование; 4) Химический анализ; 5) Расчет результатов анализа. В большинстве случаев стадия отбора пробы и подготовка ее к анализу определяет надежность и качество получаемых результатов. Погрешность при отборе и подготовке пробы к анализу часто определяет общую ошибку анализа и, в случае неправильно выполненных операций, делает бессмысленным использование высокоточных методов. Приемы и порядок отбора пробы и ее подготовка к анализу настолько важны, что обычно предписываются Государственным стандартом. Отбор пробПроба - маленькая часть всего анализируемого объекта. По маленькой части судят о качестве всего объекта, поэтому любая проба должна быть, в первую очередь, представительной. Пробу называют представительной (средней), если ее состав и свойства идентичны среднему составу и свойствам всего анализируемого объекта. Генеральная проба - первичная, отбирается от объекта анализа, она может быть большой (от 1 кг до 5 т), поэтому ее сокращают до лабораторной (от 25 г до I кг), которую делят на три части: 1) для предварительных исследований; 2) для непосредственного анализа (анализируемая проба); 3) для арбитражного анализа (для повторного анализа другой аналитической лабораторией в случае несогласия заказчика с результатами анализа). Для анализируемой пробы проводят несколько определений компонента: из отдельных навесок (10–1000 мг) - если анализируемый объект - твердое вещество, или аликвот - если анализируют жидкость или газ. Анализируемая проба должна быть представительной. Чем больше материала отобрано для пробы, тем она представительнее. Но с очень большой пробой трудно работать, увеличивается время анализа и расходы на него. Таким образом, отбирать пробу нужно так, чтобы она была представительной и не очень большой. Способы отбора пробы.Способы отбора пробы и размер пробы определяются прежде всего физическими и химическими свойствами анализируемого объекта. При отборе пробы следует учитывать: 1) агрегатное состояние анализируемого объекта (способы отбора пробы различны для газов, жидкостей и твердых веществ); 2) неоднородность анализируемого материала и размер частиц, с которых начинается неоднородность (чем однороднее вещество, тем проще отобрать пробу); 3) требуемую точность оценки содержания компонента во всей массе анализируемого объекта в зависимости от задачи анализа и природы исследуемого объекта (так, при определении физиологически активного компонента в лекарстве требуется большая точность, чем при определении содержания металла в руде для оценки рентабельности месторождения). Обязательно при отборе пробы необходимо учитывать возможность изменения состава объекта и содержания определяемого компонента во времени (состав воды в реке, состав дымовых выбросов и т. п.) 1.1.1 Отбор газообразных проб. Газообразные пробы состоят из газов, паров летучих жидкостей, аэрозолей. Степень однородности газов и их смесей велика, поэтому генеральная проба может быть небольшой. Для отбора пробы газа из производственных аппаратов и трубопроводов применяются стеклянные аспираторы, газовые пипетки, газометры с гидравлическим затвором, сухие газометры, сосуды шарообразной формы и реже резиновые баллоны. Выбор емкости зависит от количества и состава газа и от давления в системе. Из емкостей и газопроводов пробу газа отбирают в большинстве случаев в аспираторы и газовые пипетки. Аспиратор — это прибор, состоящий из двух склянок с боковыми тубусами. Тубусы соединены между собой резиновым шлангом, на середине которого имеется винтовой зажим. Одна из склянок снабжена стеклянным краном и служит для забора газа, другая является напорной уравнительной склянкой. Так как многие газы растворимы в воде, то в качестве напорной жидкости применяют насыщенный раствор поваренной соли, подкисленный соляной кислотой, или 10%-ный раствор серной кислоты, который подкрашивают метиловым оранжевым. Перед отбором пробы склянку с краном заполняют напорной жидкостью доверху, а склянку без крана - до тубуса. Для насыщения напорной жидкости исследуемым газом его набирают через кран в заборную склянку и встряхивают аппарат в течение 3–5 мин. Эту операцию повторяют 2–3 раза, беря каждый раз свежую порцию газа. Для уменьшения выделения газа из напорной жидкости уравнительную склянку аспиратора следует закрывать пробкой с капиллярной трубкой. Для проверки аспиратора на герметичность заборную склянку заполняют напорной жидкостью до крана и при закрытом кране опускают уравнительную склянку вниз, наблюдая при этом за изменением уровня жидкости в заборной склянке. Если после некоторого снижения уровень жидкости станет постоянным, аспиратор герметичен. Такой же порядок соблюдают и при подготовке газовых пипеток. В зависимости or вместимости бутылки в аспиратор можно набрать до 15 л газа. В газовые пипетки набирают 100–500 мл газа. Часто газ конденсируют в ловушках разного типа при низких температурах. Различаются правила отбора пробы газа из замкнутой емкости и из потока. В замкнутой емкости (цех предприятия, помещение лаборатории и т. п.) пробу отбирают в разных точках, в зависимости от задачи объемы газа смешивают или анализируют по отдельности. При отборе пробы газа из потока используют метод продольных струй или метод поперечных сечений. Метод продольных струй применяют, когда состав газа вдоль потока не меняется. В этом случае поток делят на несколько струй вдоль потока и пробы газа отбирают в струях через одну. Чтобы учесть изменение состава газовой смеси во времени, пробы отбирают в разное время и, в зависимости от поставленной задачи, пробы усредняют, или анализируют отдельно. Для сбора взвешенных частиц и аэрозолей можно использовать фильтры. В качестве материалов фильтров обычно используют тефлон или стекло. При этом собираются все частицы независимо от их размера. Для фракционированного пробоотбора используют каскадные фильтры (ипмакторы). Ток воздуха проходит через каскадный фильтр, содержащий систему насадок с разным диаметром отверстий. Таким образом, частицы сортируются по их размеру. Для снятия частиц с фильтра используют кислотное разложение, вымывание или экстракцию, например, в аппарате Сокслета. 1.1.2 Отбор проб жидкостейСпособы отбора гомогенных и гетерогенных жидкостей различны. Гомогенные жидкости отличаются высокой степенью однородности, поэтому отбор проб таких жидкостей достаточно прост. Пробу отбирают с помощью пипеток, бюреток и мерных колб. Отбор пробы из большой емкости проводят после тщательного перемешивания. Если по какой-то причине пробу нельзя хорошо перемешать (например, воду в реке), то отбор проводят на разной глубине и в разных местах, затем анализируют, в зависимости от поставленной задачи, отдельно или после смешивания. Отбор гомогенной жидкости из потока проводят через определенные интервалы времени и в разных местах. Для этого используют специальные приспособления - батометры, представляющие собой цилиндрический сосуд вместимостью 1–3 л, закрывающийся сверху и снизу крышками. После погружения сосуда на требуемую глубину крышки сосуда закрывают, сосуд поднимают на поверхность. Место и время отбора пробы согласовывают, исходя из поставленных задач. Например, чтобы оценить степень загрязнения водоема сточными водами предприятия, необходимо отбирать пробу не только самих стоков, но и воду водоема выше и ниже места сброса стоков. Пробы гетерогенных жидкостей отбирают не только по объему, но и по массе. В одних случаях пробу гомогенизируют, в других – дожидаются полного расслоения жидкостей. Гомогенизируют пробу путем интенсивного перемешивания, вибрацией, ультразвуком и т. п. Если гомогенизировать жидкость невозможно, то после расслоения жидкости пробу отбирают из каждой фазы, на различной глубине. Размер генеральной пробы жидкости не превышает нескольких литров или килограммов. 1.1.3 Отбор проб твердых веществ.При отборе генеральной, лабораторной и анализируемой проб твердых веществ прежде всего возникает вопрос о размере пробы, который должен обеспечивать ее представительность. Оптимальная масса пробы обусловлена неоднородностью анализируемого объекта, размером частиц, с которого начинается неоднородность, и требованиями к точности анализа. Зависимость массы Q представительной пробы от размера (диаметра d) неоднородных частиц показана в Таблице 1. Таблица 1- Зависимость массы генеральной пробы от размера частиц.
Для расчета оптимальной массы представительной пробы чаще всего используют формулу Ричердса - Чеччота: 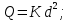 где Q - масса пробы, обеспечивающая ее представительность, кг; К -эмпирический коэффициент пропорциональности, характеризующий степень неоднородности распределения определяемого компонента в материале, он меняется в пределах 0,02 -1,0; d — наибольший диаметр неоднородных частиц, мм При отборе твердых проб различают объекты анализа, которые представляют собой монолиты, кусковые, сыпучие системы. Для отбора представительной пробы монолитного объекта (слиток, стержень и т. д.) производят сверление в разных местах объекта, стружки, опилки собирают и перемешивают. Кусковые отбирают каждую двадцатую, пятидесятую, сотую тачку, вагонетку, упаковку из партии образца, подлежащего анализу, перемешивают, измельчают, усредняют, сокращают. Сыпучие материалы тщательно перемешивают и отбирают в разных местах емкости и на разной глубине специальными щупами пробоотборниками. 1.2Хранение и консервация проб.Допустимый промежуток времени между отбором и анализом зависит от состава пробы, природы определяемых компонентов и условий хранения. Чем больше вероятность изменения состава и содержания определяемых компонентов в пробе, тем скорее должен быть проведен анализ. Если невозможно провести анализ сразу после отбора, пробу консервируют в соответствии с рекомендациями утвержденных инструкций. Причины погрешностей при отборе, транспортировке, хранении проб: - потери в виде пыли при измельчении (до 3 %); - потери летучих продуктов (изменение температуры при измельчении, транспортировке или хранении); -потери вследствие адсорбции компонентов на стенках пробоотборников; - потери вследствие внесения загрязнений со стенок пробоотборников или ступок и пестиков при измельчении пробы; - изменение состава анализируемого образца за счет химических реакций (взаимодействие с компонентами атмосферы, ОВР и др.). 2. Подготовка пробы к анализуПодготовка пробы — важный этап проведения химического анализа. Выделяют три основные стадии подготовки пробы к анализу: 1) высушивание; 2) разложение (с переведением пробы в раствор); 3) разделение и концентрация. 2.1 Высушивание образцов.Для правильного установления состава объекта анализа и получения достоверных результатов необходимо удалить влагу из анализируемого образца: высушить пробу до постоянной массы или определить содержание воды в анализируемой пробе. Вода в твердых пробах: - адсорбированная (на поверхности пробы твердого вещества); - сорбированная (щелями и капиллярами аморфных веществ); - окклюдированная (полостями при формировании вещества); - кристаллизационная (неотъемлемая часть структуры вещества, ВаСl2·Н2О, CaSO4-2H2O, Na2B4O7·10H20); - конституционная (неотъемлемая часть структуры вещества, выделяющаяся при нагревании, Са(ОН)2 → СаО + Н2О). Высушивание производят в сушильных шкафах, (105-120°С), в установках с инфракрасными источниками тепла, в вакуумных печах, в эксикаторах (над влагопоглощающими веществами: СаСl2, Mg(ClO4)2, Р4О10, плавленый КОН, силикагель и др.). Жидкости, содержащие относительно большое количество воды, высушивают в два этапа: сначала проводят экстракцию, или фракционную перегонку, или дистилляцию и т. д., а затем досушивают с помощью химических осушающих реагентов и сорбентов. Газы осушают химическими реагентами и вымораживанием. Известно большое число методов определения воды. Так, воду определяют гравиметрически косвенным или прямым методом. В косвенном методе о содержании воды судят по потере массы анализируемой пробы при ее высушивании или прокаливании. Этот метод часто не дает правильных результатов, что связано с трудностью определения температуры, необходимой для полного выделения воды, и потерей с водой летучих компонентов образца. Прямой гравиметрический метод основан на поглощении выделившейся из образца воды подходящим поглотителем, чаще всего безводным перхлоратом магния. О содержании воды судят по увеличению массы предварительно взвешенного поглотителя. Для определения воды часто используют газожидкостную хроматографию и ИК-спектроскопию. 2.2 Разложение пробы. Перевод пробы в растворВ современных методах можно проводить анализ и без разложения пробы (спектроскопические и т. п.), но все же большинство методов анализа требуют предварительное переведение компонента в раствор. Выбор способа переведения пробы в раствор зависит как от природы определяемого компонента, так и от природы матрицы, то есть основы, в которой содержится определяемый компонент. На способ разложения пробы влияют и цели анализа, и выбранная аналитическая методика. Способы разложения делятся на сухие и мокрые. Мокрые: Растворение в воде. Многие неорганические соли (особенно соли щелочных металлов, аммония и магния) и некоторые органические соединения (низшие и многоатомные спирты, аминокислоты, гидрохлориды аминов, соли щелочных металлов органических кислот, мочевина и т. п.) легко растворяются в воде. Растворение в воде с небольшими добавками кислот для предотвращения гидролиза и частичного осаждения некоторых катионов металлов. Растворение в органических растворителях или их смесях для для растворения органических веществ. 4) Разложение в сильных кислотах и их смесях. Сухие (термическое разложение): Пиролиз – это разложение органических веществ при высоких температурах в отсутствии веществ, реагирующих с разлагаемым соединением. Пиролиз проводят в атмосфере инертного газа (азота, гелия) или в вакууме. Cухое озоление – это разложение пробы при нагревании с окислением, чаще всего в качестве окислителя берут кислород. Сожжение в кислороде применяют в основном при анализе органических соединений, а также некоторых неорганических веществ, например металлов и сульфидов. Выбор условий проведения окисления (в открытых или закрытых сосудах, в потоке кислорода или воздуха и т. д.) зависит от химической природы анализируемого вещества и применяемых в дальнейшем методов определения. Cплавление. Как метод разложения пробы сухим способом сплавление чаще используют при анализе неорганических веществ. При сплавлении тонко измельченный образец перемешивают с 8-10 кратным количеством реагента (плавня) и нагревают (300 - 1 000 °С) до получения прозрачного плава. Время плавления определяют опытным путем. Спекание. Нагревание пробы при высоких температурах с подходящим твердым реагентом не всегда сопровождается образованием расплава; в отдельных случаях смесь не расплавляется, а только спекается. Спекание - сложный, до конца не изученный процесс. Предполагается, что спекание основано на высоком химическом сродстве компонентов пробы к введенным реагентам, диффузии и реакциях обмена. В отдельных случаях спекание позволяет провести разложение пробы быстрее и проще, способствует уменьшению загрязнений, поскольку при этом часто используют меньшие (двух или четырехкратный избыток) количества реагентов и менее высокие температуры. Сухой способ используют тогда, когда мокрый способ не дает удовлетворительных результатов. Сухой способ менее предпочтителен, чем растворение в кислотах, поскольку возрастает вероятность и величина погрешностей, особенно при сплавлении. 2.3 Разделение и концентрированиеКак для отделения определяемого компонента от матрицы, так и для его концентрирования можно применять одни и те же способы. Концентрированием называется процесс, в результате которого возрастает концентрация компонента в растворе либо его доля по отношению к матрице по сравнению с исходной пробой. Важнейшими методами разделения и концентрирования являются: 1)отгонка летучих компонентов; 2)осаждение или соосаждение компонента на коллекторе; 3)экстракция и ионный обмен; 4)электролитическое выделение; 5)колоночная хроматография и сорбция. Разделение и концентрирование газовых проб можно осуществить непосредственно в ходе пробоотбора, используя абсорбцию жидкостью или адсорбцию твердой фазой. Так, на тенаксе — разновидности активированного угля — хорошо адсорбируются пары спиртов, сложных эфиров, кетонов и ароматических соединений. Выделение легколетучих органических веществ из водных растворов можно осуществить с помощью следующего приема. Раствор пробы кипятят на водяной бане и продувают потоком газа-носителя (гелий), поступающим на адсорбционную колонку. После термической десорбции адсорбированные компоненты определяют методом газовой хроматографии. Можно определять легколетучие вещества и непосредственно в паровой фазе. Сосуд с анализируемым раствором плотно закрывают. Через некоторое время между определяемым компонентом, находящимся в растворе, и его парами устанавливается равновесие. С помощью соответствующей градуировки можно установить зависимость между содержанием паров в газовой фазе и концентрацией вещества в растворе. В этом методе определяемый компонент и матрица разделяются сами собой. Такой способ пробоподготовки используют, например, при определении летучих углеводородов в водах или содержания алкоголя в крови. ВыводыРоль отбора пробы и пробоподготовки значительно важна в химическом анализе. Погрешность при отборе и подготовке пробы часто определяет общую ошибку анализа, поэтому эти этапы определяют надежность и качество получаемых результатов анализа. Методы отбора пробы и пробоподготовки зависят от химических и физических свойств исследуемого вещества, поэтому не существует методов, подходящих сразу для всех случаев. Библиографический списокКарпов Ю.А., Савостин А.П. Методы пробоотбора и пробоподготовки. Ю.А. Золотов "Основы аналитической химии". Книга 2 С.В. Дорожке, Н.Ф. Макаревич. АНАЛИТИЧЕСКАЯ ХИМИЯ. Учебно-методическое пособие |
