химия. V2 Введение в курс общей и неорганической химии
 Скачать 230 Kb. Скачать 230 Kb.
|
V2: d-Элементы.*I: S: Для d-элементов характерным является является  -: сопряженным окислителем -: сопряженным окислителем-: сопряженным восстановителем +: способность к образованию комплексных соединений -: образование бесцветных соединений -: постоянные степени окисления -: низкая каталитическая активность I: S: Все d-элементы являются +: металлами с характерным металлическим блеском -: типичными неметаллами I: S: Хром так же, как алюминий и железо -: эффективными полупроводниками -: хорошими изоляторами +: пассивируется холодными концентрированными H2SO4 и HNO3 -: способен образовывать соединения со степенью окисления +6 -: образует оксид со степенью окисления +3 зеленого цвета -: образует типичный кислотный оксид I: S: Серебро, так же, как и медь, не может +: реагировать с разбавленными соляной и серной кислотами -: растворяться в разбавленной азотной кислоте -: растворяться в концентрированной серной кислоте -: образовывать соединения со степенью окисления +1 I: S: Самый распространенный на земле d-металл - +: железо -: алюминий -: титан -: медь I: S: Тяжелые металлы (ртуть, свинец, кадмий, хром, никель) попадая в организм человека, приводят к отравлениям, токсикозам. Это объясняется тем, что катионы металлов +: взаимодействуют с биоорганическими комплексами, образуя более прочные комплексы -: являются антагонистами биогенных элементов -: образуют хелаты, выпадающие в осадок -: взаимодействуют с ферментами, образуя непрочные комплексы *I: S: Для определения ионов железа (II) в аналитической практике применяют реакцию с солью +: K3[Fe(CN)6] -: K4[Fe(CN)6] -: KSCN -: KNO3 I: S: По своим свойствам молибден во многом похож на +: вольфрам -: ванадий -: хром -: марганец *I: S: Соответствие между d-металлом и его ролью в организме L1: кобальт L2: цинк L3: кадмий L4: железо L5: R1: входит в состав витамина В12 R2: входит в состав металлоферментов R3: ингибирует ферментативные реакции, разрушает ферменты R4: входит в состав гемоглобина R5: входит в состав хлорофилла S: Продуктом реакции Sc + H2SO4 ? является соль ### (укажите название по М.Н.). S: Продуктами реакции разложения нитрата La(NO3)3 ? являются +: оксид лантана, оксид азота (IV), кислород -: гидроксид лантана, оксид азота (II), кислород -: оксид лантана, оксид азота (II) -: гидроксид лантана, оксид азота (IV) *I: Q: Правильная последовательность оксидов хрома по возрастанию кислотных свойств 1: CrO 2: Cr2O3 3: CrO2 4: Cr2O5 5: CrO3 *I: +: Сr2O3 -: Cr(OH)3 -: H2CrO4 -: СrO3 S: Нерастворимым продуктом реакции MnCl2 + NaOH ? является ### марганца (II) (укажите название по М.Н.). +: гидроксид *I: S: Белый Fe(OH)2 окисляется кислородом воздуха до … красно-бурого цвета. +: Fe(OH)3 -: Fe2O3 -: HFeO2 -: FeOOH  *I: *I:S: Продуктом реакции NiO + HCl +: хлорид никеля (II) I: является зеленый ### (укажите название по М.Н.). +: желтая кровяная соль -: красная кровяная соль -: турнбулева синь -: берлинская лазурь *I: S: Продуктом реакции разложения сине-голубого осадка Cu(OH)2 при нагревании является черный ### (укажите формулу). +: CuO *I: S: Гидроксид Au(OH)3 +: является амфотерным, взаимодействует с кислотами и щелочами -: проявляется свойства оснований -: проявляет свойства кислот -: химически инертен V2: р-Элементы.*I: S: Йод относится к числу незаменимых биогенных элементов. Он необходим для +: функционирования щитовидной железы, которая секретирует гормон тирозин -: функционирования организма, т.к. входит в состав витаминов группы В -: переваривания пищи, т.к. входит в состав желудочного сока -: синтеза металлозависимых ферментов *I: S: Газовые выбросы высокотоксичных диоксидов серы и азота в атмосферу могут привести к +: образованию кислотных дождей -: формированию смога I: S: Бактерицидное действие озона основано на том, что -: парниковому эффекту -: развитию сидероза +: озон инициирует радикальные реакции в молекулах микробов -: это яд для микробов -: озон – сильнейший восстановитель, приводит к повреждению и гибели микробов -: озон блокирует выработку АТФ *I: S: Как антисептик в медицине широко применяется соединение бора, которое хорошо растворимо в воде, легко проникает в клетку через липидную мембрану. Это +: H3BO3 -: B2O3 I: S: Активированный уголь применяют в качестве +: адсорбента -: топлива I: S: Только неметаллы содержатся в главной подгруппе +: 7-ой группы -: 6-ой группы I: -: NaBO2 -: ВН3 -: карандаша -: косметического средства -: 5-ой группы -: 4-ой группы S: Соответствие между галогеном и его физическими свойствами L1: фтор L2: хлор L3: бром L4: йод L5: *I: R1: бледно-желтый газ R2: легко сжижаемый газ желто-зеленого цвета R3: красно-коричневая густая жидкость с тяжелыми коричневыми парами R4: серовато-черные блестящие кристаллы R5: легкокипящая бесцветная жидкость Q: Правильная последовательность кислот по возрастанию их силы 1: HF 2: HCl 3: HBr 4: HI I: S: Соли всех галогеноводородных кислот представляют собой +: твердые кристаллические вещества -: летучие жидкости I: S: Кислород и сера - +: имеют аллотропные модификации -: хорошие проводники электричества *I: S: Раствор SO3 в 100%-ной серной кислоте называют +: олеумом -: царской водкой *I: -: газообразные вещества -: жидкости и газы -: хорошо растворимы в воде -: типичные восстановители -: плавиковой кислотой -: олеиновой кислотой S: Соответствие между неметаллом и его физическими свойствами (н.у.) L1: кислород L2: сера L3: красный фосфор L4: углерод L5: I: S: Графит и кремний – типичные +: восстановители -: окислители *I: R1: газ без цвета и запаха R2: твердое вещество желтого цвета R3: полимерное вещество, нерастворимо в сероуглероде R4: черно-серое кристаллическое вещество со слабым металлическим блеском R5: жидкость зеленого цвета -: металлы -: полудрагоценные камни S: Угольная кислота, так же как и кремниевая, относится к +: слабым кислотам -: сильным кислотам I: S: При сплавлении Al2O3 с KOH образуется +: метаалюминат калия -: ортоалюминат калия *I: -: восстановителям -:твердым веществам -: гидроксид алюминия -: гексагидроксоалюминат (III) калия +: фосгеном -: карбонилом -: бораном -: хлорной известью S: Углекислый газ под давлением взаимодействует с аммиаком (CO2 + NH3 ?) образуя +: мочевину СО(NH2)2 -: дициан C2N2 I: -: цианистоводородную кислоту HCN -: карбонат аммония (NH4)2CO3 +: карбид S: По реакции K2SiO3 + H2SO4 ? получают +: метакремниевую кислоту H2SiO3 -: оксид кремния (IV) SiO2 I: S: Аммиак в струе кислорода горит (NH3 + O2 -: силан SiH4 -: оксид кремния (II) SiO 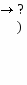 с образованием с образованиемS: Продуктом реакции S + F2 ? является ### (укажите формулу самого устойчивого продукта) +: SF6 I: S: Плавиковая кислота (HF) разрушает стекло (SiO2) с образованием S: Йодоводород в реакции HI + O2 ? является +: восстановителем S: В реакции Pb + NaOH + H2O ? образуется +: тетрагидроксоплюмбат (II) натрия -: гидроксид свинца (II) -: сопряженным восстановителем -: сопряженным окислителем -: оксид свинца (IV) -: метасвинцовая кислота |
