Вещества кислотного характера
 Скачать 0.5 Mb. Скачать 0.5 Mb.
|
|
Часть исследуемого хлороформного раствора помещают в пробирку, хлороформ испаряют при нагревании на теплой водяной бане. К сухому остатку добавляют 1 мл воды очищенной и 1 мл разведённой серной кислоты. При наличии хинина появляется голубая флуоресценция, особенно хорошо наблюдаемая в УФ–свете. От прибавления к этой жидкости нескольких капель 0,1 моль/л раствора едкого натра интенсивность голубой флуоресценции ослабевает, а затем (при рН = 9) появляется фиолетовая флуоресценция. Если к раствору хинина, подкисленному серной кислотой, прибавить несколько капель бромной воды, разбавленной десятикратным объёмом воды (до полного тушения флуоресценции), а затем прибавить несколько капель 25 % раствора аммония гидроксида до щелочной реакции, то появляется жёлто–зелёная флуоресценция. 3. Таллейохинная реакция Сухой остаток в фарфоровой чашке (после удаления хлороформа при нагревании на теплой водяной бане) смешивают с 1 мл воды очищенной. К раствору добавляют 2 – 3 капли (избегая избытка) насыщенной бромной воды, 2 – 3 капли 25 % раствора аммония гидроксида и 0,5 мл хлороформа. При наличии хинина наблюдают ярко–зелёное окрашивание хлороформного слоя; при подкислении окрашивание меняется, становится сначала синим (нейтральная реакция среды), а затем фиолетовым или красным (кислая среда). 4. Эритрохинная реакция Несколько капель исследуемого раствора выпаривают досуха. К сухому остатку прибавляют 1 мл воды, затем 1 – 2 капли 1% раствора серной кислоты, каплю бромной воды и каплю 10 % раствора калия гексациано- (III) феррата. Полученную жидкость хорошо взбалтывают, а затем к ней по каплям прибавляют аммиак до щелочной реакции. При наличии хинина появляется розовая или красно–фиолетовая окраска, которая при взбалтывании с хлороформом переходит в хлороформный слой. Открываемый минимум 10 мкг. 5. Реакция с раствором аммония роданида К сухому остатку на предметном стекле добавляют каплю 0,1 моль/л раствора хлороводородной кислоты и каплю 10% раствора аммония роданида. Через 10 – 15 мин под микроскопом наблюдают игольчатые бесцветные кристаллы, собранные в сростки в виде характерных пучков. 19. Химико-токсикологический анализ производных фенотиазина. Метаболизм производных фенотиазина, способы идентификации метаболитов. АМИНАЗИН Аминазин (хлорпромазин, плегома Зин, хлоразин, ларгактил и др.) представляет собой белый или бе- лыи с кремоватым оттенком мелко- кристаллический порошок. Ами- назин гигроскопичен, темнеет под влиянием света, хорошо растворяется в воде, этиловом спирте и хлороформе. Он практически не растворяется в диэтиловом эфире. Растворы аминазина имеют кислую реакцию. Аминазин экстрагируется органическими растворителями из щелочных растворов. Применение. Действие на организм. Аминазин принадлежит к числу основных нейролептиков. Он оказывает сильное седативное действие. При больших дозах аминазин вызывает сон. Он усиливает действие снотворных, наркотических и местноанестезирующих веществ. Аминазин имеет противорвотное действие и успокаивает икоту. Он уменьшает проницаемость сосудов, снимает страх, тревогу, напряжение у больных психозами и неврозами. Аминазин применяется для лечения бессонницы, зудящих дерматозов. Он назначается при ряде психических заболеваний и т. д. Метаболизм. Метаболизм аминазина довольно сложный. При метаболизме происходит гидроксилирование, сульфоокисление, N-деметилирование, разрыв боковой цепи и другие изменения Обнаружение аминазина Реакция с концентрированной серной кислотой. Аминазин с концентрированной серной кислотой дает пурпурно-красную окраску. Реакция с концентрированной азотной кислотой. При взаимодействии аминазина с концентрированной азотной кислотой возникает пурпурно-фиолетовая окраска. Реакция с концентрированной соляной кислотой. Аминазин с концентрированной соляной кислотой дает розовато-фиолетовую, переходящую в красно-фиолетовую окраску. Реакция с реактивом Марки. Аминазин под влиянием реактива Марки приобретает пурпурную окраску. Реакция с реактивом Манделина. Аминазин с этим реактивом дает зеленую окраску, переходящую в пурпурную. Обнаружение аминазина методом хроматографии. На хроматографическую пластинку наносят исследуемый раствор и раствор «свидетель» (спиртовой раствор аминазина). Пластинку подсушивают на воздухе, а затем вносят в камеру для хромато-графирования, насыщенную парами системы растворителей (смесь бензола, диоксана и аммиака 75 : 20:5). После того как жидкость поднимется на 13 см выше линии старта, пластинку вынимают из камеры высушивают на воздухе и опрыскивают реактивом Марки или свежеприготовленной смесью концентрированной азотной кислоты и этилового спирта (1:9). При наличии аминазина пятна на пластинке приобретают розово-фиолетовую окраску. Обнаружение аминазина по УФ- и ИК-спектрам. Аминазин в 0,1 н. растворе серной кислоты имеет максимумы поглощения при 255 и 307 нм. Сульфоксид аминазина, являющийся метаболитом этого препарата, в 0,1 н. растворе серной кислоты имеет максимумы поглощения при 239, 274, 300 и 341 нм. В ИК-области спектра основание аминазина (диск с бромидом калия) имеет основные пики при 1561, 1455, 1402, 1240, 747 см-1. ДИПРАЗИН Дипразин экстрагируется органическими растворителями из щелочной среды. Применение. Действие на организм. Дипразин имеет выраженную противогистаминную активность. Он обладает седативным действием, усиливает действие наркотических, снотворных и анальгезирующих средств. Дипразин применяется для лечения аллергических заболеваний, зудящих дерматозов, хореи, энцефалита и др. Метаболизм. Главным метаболитом дипразина является сульфоксид этого препарата. Часть дипразина в неизмененном виде выделяется е мочой. Кроме этого, с мочой выделяется и сульфоксид дипразина, который можно обнаружить в моче даже через 14 сут после приема указанного препарата. Выделение дипразина из биологического материала. Дипразин выделяют из биологического материала так, как и аминазин. Обнаружение дипразина Реакция с концентрированной серной кислотой. Дипразин с концентрированной серной кислотой дает пурпурно-красную окраску. Реакция с концентрированной азотной кислотой. При взаимодействии дипразина с концентрированной азотной кислотой по является бледная пурпурно-красная окраска, переходящая в желтую. Реакция с концентрированной соляной кислотой. Дипразин с концентрированной соляной кислотой дает розовато-фиолетовую окраску, переходящую в пурпурно-фиолетовую. Реакция Витали — Морена. Дипразин дает реакцию Витали — Морена. Реакция с реактивом Марки. Дипразин с реактивом Марки дает пурпурную окраску. ТИЗЕРЦИН Тизерцин (левомепромазин. левопромазин, метотримепразин и др.)—белый кристаллический порошок, слаборастворимый в воде, 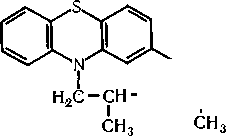 хорошо растворяется в этиловом спирте, диэтиловом эфире и хлороформе. Тизерцин экстрагируется органическими растворителями из щелочных растворов. Применение. Действие на организм. Тизерцин обладает адренолитической и противогистаминной активностью, проявляет анальгезирующее действие. Под влиянием тизерцина быстро наступает седативный эффект. Поэтому он применяется при острых психозах. Этот препарат применяется при психомоторном воз буждении различной этиологии (в том числе и при алкогольных психозах), бессоннице, зудящих дерматозах и ряде других заболеваний. Метаболизм. Часть принятой дозы тизерцина выделяется из организма с мочой в неизмененном виде. Около 10 % тизерцина выделяется с мочой в виде сульфоксида или глюкуронида. Некоторое количество тизерцина выделяется с калом в неизмененном виде. Выделение тизерцина из биологического материала. Тизерцин выделяется из биологического материала так, как и аминазин. Обнаружение тизерцина Реакции с реактивами Марки и Фреде. Тизерцин с реактивами Марки и Фреде дает синевато-красную окраску. Реакция с реактивом Манделина. К 1 мл исследуемого раствора прибавляют 0,1 мл реактива Манделина. Жидкость взбалтывают и охлаждают в ледяной воде. К жидкости прибавляют 5 мл концентрированной серной кислоты. При наличии тизерцина раствор приобретает красно-фиолетовую окраску. Обнаружение тизерцина методом хроматографии. На хроматографическую пластинку наносят каплю исследуемого раствора. Нанесенное пятно подсушивают на воздухе. Затем пластинку вносят в камеру для хроматографирования, насыщенную парами системы растворителей (смесь раствора аммиака и этилового спирта (1 : 1), этилацетата и ацетона (4:90:45). После хроматографирования пятна тизерцина на пластинках проявляют 50 %-м раствором серной кислоты в этиловом спирте. Затем пла стинку на 3—5 мин помещают в сушильный шкаф, нагретый до 100°С. Обнаружение тизерцина по УФ- и ИК-спектрам. Раствор тизерцина в этиловом спирте имеет максимумы поглощения при 255 и 310 нм; тизерцин в 0,1 н. растворе соляной кислоты имеет максимумы поглощения при 251 и 302 нм. В ИК-области спектра основание тизерцина (диск с бромидом калия) имеет основные пики при 1587, 1460, 1269 и 1446 см"1. 20. Химико-токсикологический анализ производных 1,4-бензодиазепина по нативным соединениям. ХЛОРДИАЗЕПОКСИД Хлордиазепоксид (элениум, декадил, либриум и др.) представляет собой белый или светло-желтый кристаллический порошок, хорошо растворяется в воде. Он экстрагируется органическими растворителями из щелочной среды. Пактам, являющийся метаболитом хлордиазепоксида, экстрагируется диэтиловым эфиром из нейтральной и кислой среды. Выделение хлордиазепоксида из биологического материала. 25 г измельченного биологического материала 3 раза по одному часу настаивают со 100 мл воды, подкисленной соляной кислотой до рН = 1. Вытяжки центрифугируют, полученный центрифугат подщелачивают до рН = 10 и 3 раза взбалтывают с хлороформом (по 25, 15 и 15 мл). Хлороформные вытяжки соединяют и используют для обнаружения и количественного определения хлордиазепоксида. Один из методов определения хлордиазепоксида состоит в том, что этот препарат выделяют из биологического материала, а затем при нагревании гидролизуют соляной кислотой. Образовавшийся при этом 2-амино-5-хлорбензофенон переводят в диазосоединение. Предварительная проба на наличие хлордиазепоксида в крови и моче. От 5 до 10 мл плазмы крови или мочи подщелачивают аммиаком и дважды взбалтывают с хлороформом по 10 мл. Соединенные хлороформные вытяжки взбалтывают с 2 мл воды. Водную фазу отделяют, а хлороформный слой взбалтывают с 5 мл 6 н. раствора соляной кислоты в течение 5 мин. Водные солянокислые вытяжки отделяют от хлороформа, нагревают на водяной бане, а затем эти вытяжки нагревают при 125 °С на парафиновой бане в течение 30 мин (при этом образуется 2-амино-5-хлорбензофенон). К охлажденной жидкости прибавляют 0,5 мл 10 %-го раствора нитрита натрия и оставляют на 3 мин. По истечении указанного времени прибавляют 0,5 мл 0,5 %-го раствора сульфамината аммония и оставляют на 3 мин. Затем прибавляют 0,5 мл 0,1 %-го раствора N-1-нафтилэтилендиамина дигидрохлорида. При наличии хлордиазепоксида в крови или в моче появляется вишнево-красная окраска. Эту реакцию можно использовать для фотоколориметриче ского определения хлордиазепоксида. Обнаружение хлордиазепоксида Реакция с нингидрином. Эту реакцию выполняют так, как указано при обнаружении диазепама. При этой реакции хлордиазепоксид дает коричневую окраску. Реакция с реактивом Марки. Хлордиазепоксид с реактивом Марки дает желтую окраску. Реакция с реактивом Фреде. С этим реактивом хлордиазепоксид дает оранжевую окраску. Реакция Витали — Морена. Хлордиазепоксид при реакции Витали — Морена дает желтую окраску. Обнаружение хлордиазепоксида методом хроматографии в тонком слое сорбента. Обнаружение хлордиазепоксида с помощью этого метода производится так, как и обнаружение диазепама. Обнаружение хлордиазепоксида по УФ- и ИК-спектрам. Хлор диазепоксид в 0,1 н. растворе гидроксида натрия имеет максимумы поглощения при 243 и 260 нм; в 0,1 н. растворе серной кислоты хлордиазепоксид имеет максимумы поглощения при 245 и 306 нм. Хлордиазепоксид в 0,1 н. растворе соляной кислоты имеет максимумы поглощения при 246 и 308 нм. В ИК-области спектра основание хлордиазепоксида (диск с бромидом калия) имеет основные пики при 1625, 1458 и 760 см-1. ДИАЗЕПАМ Диазепам (седуксен, эридан,реланиум и др.) представляет собой белый или белый с желтоватым оттенком кристаллический порошок, не растворяется в воде, трудно растворяется в этиловом спирте, растворяется в хлороформе. Этот препарат экстрагируется органическими растворителями как из кислой, так и из щелочной среды. Выделение диазепама из крови и мочи. К 10 мл мочи или 5 мл крови прибавляют равный объем фосфатного буферного раствора (рН = 7,0). Полученную жидкость 2 раза по 5 мин взбалтывают с новыми порциями диэтилового эфира. Объем диэтилового эфира, применяемого для взбалтывания, должен быть равным объему водной фазы. Соединенные эфирные вытяжки дважды взбалтывают с 0,1 н. раствором гидроксида натрия (по 2 мл), а затем с 2 мл воды. После отделения водной фазы эфирную вытяжку взбалтывают с 3 мл 2 н. раствора соляной кислоты в течение 10 мин, а затем от эфирного слоя отделяют солянокислую вытяжку. Оптическую плотность этой вытяжки измеряют в диапазоне длин волн от 200 до 300 нм. Параллельно измеряют оптическую плотность диазепама, обработанного указанным выше способом. Наличие максимумов поглощения при 242 и 287 нм указывает на наличие диазепама в крови или моче Обнаружение диазепама Реакция с нингидрином. К 2—3 мл раствора диазепама в этиловом спирте прибавляют около 10 мг нингидрина и 2 мин нагревают на водяной бане. После прибавления 5 мл этилового спирта раствор приобретает синюю окраску, которая от прибавления двух капель 1 %-го раствора сульфата меди (II) переходит в красную или в оранжево-красную. В указанных выше условиях нитразепам дает желто-коричневую, а хлордиазепоксид — коричневую окраску. Обнаружение диазепама методом хроматографии в тонком слое сорбента. Для обнаружения диазепама и других производных бензодиазепина с помощью этого метода применяют пластинки, покрытые тонким закрепленным слоем силикагеля КСК или пластинки «силуфол». В качестве системы растворителей применяют смесь этилацетата, 25 %-го раствора аммиака и метилового спирта (26 : 1,6 : 3,3) или смесь хлороформа и ацетона (9: 1). Пятна на пластинках проявляют с помощью реактива Драгендорфа. Обнаружение диазепама по УФ- и ИК-спектрам. Диазепам в 2 н. растворе соляной кислоты имеет максимумы поглощения при 242 и 287 нм, в 0,1 н. растворе серной кислоты имеет максимумы поглощения при 241, 284 и 359 нм; в ИК-области спектра дназепам (диск с бромидом калия) имеет основные пики при 1681, 1484 и 1313 см-1. НИТРАЗЕПАМ Нитразепам (радедорм, эуноктин, могадон, неозепам и др.) — светло-желтый или светло-желтый с зеленым оттенком кристаллический порошок. Практически нерастворим в воде. Выделение нитразепама из биологического материала. Биологический материал трижды настаивают с новыми порциями насыщенного водного раствора щавелевой кислоты (рН=1). Че рез 1 ч после каждого настаивания вытяжки отделяют от биологического материала центрифугированием. Объединенный кислый центрифугат трижды взбалтывают со смесью (1:1) хлороформа и этилацетата (по 20, 15 и 15 мл). Затем кислый центрифугат подщелачивают до рН = 10 и трижды взбалтывают с новыми порциями (20, 15 и 15 мл) смеси хлороформа и этилацетата (1 : 1). Полученные при этом вытяжки подвергают исследованию на наличие нитразепама. Предварительные пробы на наличие нитразепама в моче. Нитразепам можно обнаружить в моче в неизмененном виде и в виде 7-амино- и 7-ацетиламино-производных, являющихся метаболитами этого препарата, как указано ниже. Обнаружение нитразепама в неизмененном виде в моче. 5 мл мочи подщелачивают аммиаком до рН=10 и прибавляют 250 г дитионита натрия (Na2S204). Смесь взбалтывают в течение 10 мин, затем нагревают при 50 °С в течение часа и охлаждают. Охлажденную жидкость 10 мин взбалтывают с 10 мл смеси, состоящей из равных объемов метиленхлорида и этилацетата. После этого от водной фазы отделяют слой смеси органическихрастворителей. Слой взбалтывают с 10 мл 5 %-го раствора буры. Водную фазу отделяют от фазы органических растворителей. К фазе органических растворителей прибавляют 5 мл 0,2 н. раствора соляной кислоты и взбалтывают. После этого отделяют фазу органических растворителей. 4 мл кислой водной фазы охлаждают в ледяной воде и прибавляют 0,2 мл 0,4 н. раствора нитрита натрия. Через 5 мин к кислому раствору прибавляют 0,2 мл 2%-го раствора сульфамината аммония. Жидкость хорошо перемешивают и оставляют на 5 мин, а затем прибавляют 0,2 мл 0,4 %-го раствора N-1-нафтилэтилендиамина дигидрохлорида. При наличии нитразепама в моче появляется вишнево-красная окраска (А = 555 нм). Выделение метаболитов нитразепама из мочи. Выделение этих соединений из мочи проводят так же, как и при обнаружении нитразепама, находящегося в моче в неизмененном виде. Однако при исследовании метаболитов в процессе их выделения из мочи к ней не прибавляют дитионит натрия. Выделенные из мочи метаболиты нитразепама обнаруживают методом хроматографии. Обнаружение нитразепама и его метаболитов методом хроматографии. Исследуемый раствор наносят на хроматографическую пластинку, покрытую тонким закрепленным слоем силикагеля, или на пластинку «силуфол». Для развития хроматограммы на пластинке применяют систему растворителей, являющуюся смесью этилацетата, метилового спирта и 25 %-го аммиака(85: 10:5). Пятна нитразепама и его метаболитов на пластинках проявляются реактивом Драгендорфа. |
