Аттестационная работа Жданкин РП-183. Виды химических связей
 Скачать 310.42 Kb. Скачать 310.42 Kb.
|
|
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ ФЕДЕРАЦИИ ФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ «ВОРОНЕЖСКИЙ ГОСУДАРСТВЕННЫЙ ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ» (ФГБОУ ВПО «ВГТУ», ВГТУ) Факультет радиотехники и электроники Кафедра РЭУС АТТЕСТАЦИОННАЯ РАБОТА по дисциплине: Радиоматериалы и радиокомпоненты. Тема: «Виды химических связей» Выполнил студент гр. РП-183 Жданкин А.А Руководитель: Бадаев А.С. Оценка______________Дата_____________ Воронеж 2021 Замечания руководителя Содержание Введение…………………………………………………………………………….4 Химическая связь………………………………………………………………6 Виды химической связи………………………………………………………..7 Металлическая связь…………………………………….………………...7 Ионная связь……………………………………………………………….9 Диполь-дипольная связь………………………………………………….13 Водородная связь…………………………………………………………18 Ковалентная связь………………………………………………………...20 Литература………………………………………………………………………...22 Введение Одним из центральных понятий химии служит понятие «химическая связь». Химическая связь - взаимное притяжение атомов, приводящее к образованию молекул и кристаллов. Принято говорить, что в молекуле или в кристалле между соседними атомами существуют химическая связь. Валентность атома показывает число связей, образуемых данным атомом с соседними атомами Э. Франкленд в 1852 году предложил концепцию, согласно которой каждый элемент образует соединения, связываясь с определённым числом эквивалентов др. элементов, при этом один эквивалент соответствует количеству, требуемому одной валентностью. Ф. А. Кекуле и А. В. Г. Кольбе в 1857году в соответствии с представлениями валентности выдвинули положение, что углерод обычно имеет валентность 4, образует 4 связи с другими атомами. А. С. Купер в 1858 году указал, что атомы углерода, связываясь между собой, могут образовывать цепочки. В его записи химические формулы имели очень большое сходство с современными, связи изображались чёрточками, соответствующими валентным связям между атомами. Термин "химическое строение" впервые ввёл А. М. Бутлеров в 1861году. Он подчёркивал, сколь существенно выражать строение единой формулой, показывающей, как в молекуле соединения каждый атом связан с другими атомами. Согласно Бутлерову, все свойства соединения предопределяются его молекулярным строением; он высказал уверенность, что точную структурную формулу можно установить по результатам изучения путей синтеза данного соединения. Следующий шаг, заключавшийся в приписывании молекулам пространственной трёхмерной структуры, был сделан в 1874 году Я. Х. Вант-Гоффом и Ж. А. Ле Белем. В 19 веке валентная связь изображалась чёрточкой между символами двух химических элементов. Природа этой связи была совершенно неизвестна. После открытия электрона делались многочисленные попытки развить электронную теорию химической связи. Наиболее успешными были работы Г. Н. Льюиса, который в 1916 году предложил рассматривать образование химической связи, называемой теперь ковалентной связью, как результат того, что пара электронов становится общей для двух атомов. Разработка квантовой механики (1925) и использование многих экспериментальных методов (молекулярной спектроскопии, рентгенографии кристаллов, газовой электронографии, методов изучения магнитных свойств) для определения длин связей (межатомных расстояний), углов между связями, числа неспаренных электронов и других структурных параметров молекул и кристаллов привели к более глубокому пониманию природы химических связей. Основными параметрами химической связи является её длина, прочность и валентные углы, характеризующие строение веществ, которые образованы из отдельных атомов. Длина связи - это межъядерное расстояние между химическими связанными атомами. Угол между воображаемыми прямыми, проходящими через ядра химически связанных атомов, называется валентным углом. Энергия связи - энергия, необходимая для разрыва такой связи. При образовании химической связи происходит перераспределение в пространстве электронных плотностей, первоначально принадлежавших разным атомам. Поскольку наименее прочно связаны с ядром электроны внешнего уровня, то этим электронам принадлежит главная роль в образовании химической связи. Количество химических связей, образованных данным атомом в соединении, называют валентностью. Электроны, принимающие участие в образовании химической связи, называются валентными: у s- и р элементов -- это внешние электроны, у d- элементов -- внешние (последние) s-электроны и предпоследние d-электроны. С энергетической точки зрения наиболее устойчивым является атом, на внешнем уровне которого содержится максимальное число электронов (2 и 8 электронов). Такой уровень называют завершенным. Завершенные уровни отличаются большой прочностью и характерны для атомов благородных газов, поэтому при обычных условиях они находятся в состоянии химически инертного одноатомного газа. У атомов других элементов внешние энергетические уровни незавершенные. В процессе химической реакции осуществляется завершение внешних уровней, что достигается либо присоединением, либо отдачей электронов, а также образованием общих электронных пар. Эти способы приводят к образованию двух основных типов связи: ковалентной и ионной. Таким образом, при образовании молекулы каждый атом стремится приобрести устойчивую внешнюю электронную оболочку: либо двухэлектронную (дублет), либо восьми-электромную (октет). Эта закономерность положена в основу теории образования химической связи. Образование химической связи за счет завершения внешних уровней в образующих связь атомах сопровождается выделением большого количества энергии, то есть возникновение химической связи всегда протекает экзотермически, поскольку оно приводит к появлению новых частиц (молекул), обладающих при обычных условиях большей устойчивостью, а, следовательно, они меньшей энергией, чем у исходных. Одним из существенных показателей, определяющих какая связь образуется между атомами, является электроотрицательность, то есть способность атомом притягивать к себе электроны от других атомов. Электроотрицательность атомов элементов изменяется постепенно: в периодах периодической системы слева направо ее значение возрастает, а в группах сверху вниз -- уменьшается. Химическая связь Химическая связь — это сила, удерживающая вместе два или несколько атомов, ионов, молекул или любую их комбинацию. Под химической связью в химии понимается взаимное сцепление атомов в молекуле и кристаллической решетке, в результате действия силы притяжения, существующей между атомами. Именно благодаря химическим связям происходит образование различных химических соединений, в этом заключается природа химической связи. Природа химической связи универсальна: это электростатическая сила притяжения между отрицательно заряженными электронами и положительно заряженными ядрами, определяемая конфигурацией электронов внешней оболочки атомов. Способность атома образовывать химические связи называется валентностью, или степенью окисления. С валентностью связано понятие о валентных электронах — электронах, образующих химические связи, то есть находящихся на наиболее высокоэнергетических орбиталях. Соответственно, внешнюю оболочку атома, содержащую эти орбитали, называют валентной оболочкой. В настоящее время недостаточно указать наличие химической связи, а необходимо уточнить ее тип: ионная, ковалентная, диполь-дипольная, металлическая, водородная. Виды химической связи Механизм образования химической связи сильно зависит от ее типа или вида, в целом различаются такие основные виды химической связи: Металлическая связь Металлическая связь, химическая связь, обусловленная взаимодействием электронного газа (валентные электроны) в металлах с остовом положительно заряженных ионов кристаллической решетки. Идеальная модель металлической связи отвечает образованию частично заполненных валентными электронами металла зон энергетических уровней, называемых зонами проводимости. При сближении атомов, образующих металл, атомные орбитали валентных электронов переходят в орбитали, делокализованные по кристаллической решетке аналогично делокализованным p-орбиталям сопряженных соединений. Количественно описать металлическую связь можно только в рамках квантовой механики, качественно образование металлической связи можно понять исходя из представлений о ковалентной связи. При сближении двух атомов металла, например, Li - образуется ковалентная связь, при этом происходит расщепление каждого энергетического уровня валентного электрона на два. Когда N атомов Li образуют кристаллическую решетку, перекрывание электронных облаков соседних атомов приводит к тому, что каждый энергетический уровень валентного электрона расщепляется на N уровней, расстояния между которыми из-за большой величины N настолько малы, что их совокупность может считаться практически непрерывной зоной энергетических уровней, имеющей конечную ширину. Поскольку каждый атом участвует в образовании большего числа связей, чем, например, в двухатомной молекуле при том же числе валентных электронов, то минимум энергии системы (или максимум энергии связи) достигается при расстояниях больших, чем в случае двуцентровой связи в молекуле. Межатомные расстояния в металлах заметно больше, чем в соединениях с ковалентной связью (металлический радиус атомов всегда больше ковалентного радиуса), а координационное число (число ближайших соседей) в кристаллических решетках металлов обычно 8 или больше 8. Для наиболее часто встречающихся кристаллических структур координационные числа равны 8 (объёмно-центрированная кубическая), 12 (гранецентрированная кубическая и гексагональная плотноупакованная). Расчеты параметров металлических решеток с использованием ковалентных радиусов дают заниженные результаты. Так, расстояние между атомами Li в молекуле Li2 (ковалентная связь) равно 0,267 нм, в металле Li-0,304 нм. Каждый атом Li в металле имеет 8 ближайших соседей, а на расстоянии, в 6 раз больше. Энергия связи в расчете на один атом Li в результате увеличения числа ближайших соседей увеличивается с 0,96.10-19 Дж для Li2 до 2,9.10-19 Дж для кристаллического Li. Во многих металлах металлическая связь между атомами включает вклады ионной или ковалентной составляющей. Особенности металлической связи у каждого металла могут быть связаны, например, с электростатическим отталкиванием ионов друг от друга с учетом распределения электрических зарядов в них, с вкладом в образование связи электронов внутренних незаполненных оболочек переходных металлов, с корреляцией движения электронов в электронном газе и некоторыми другими причинами. Ионная связь В соответствии с электронной теорией валентности Льюиса и Косселя, атомы могут достичь устойчивой электронной конфигурации двумя способами: во-первых, теряя электроны, превращаясь в катионы, во-вторых, приобретая их, превращаясь в анионы. В результате электронного переноса благодаря электростатической силе притяжения между ионами с зарядами противоположного знака образуется химическая связь, названная Косселем «электровалентной» (теперь ее называют ионной). В этом случае анионы и катионы образуют устойчивую электронную конфигурацию с заполненной внешней электронной оболочкой. Типичные ионные связи образуются из катионов Т и II групп периодической системы и анионов неметаллических элементов VI и VII групп (16 и 17 подгрупп — соответственно, халькогенов и галогенов). Связи у ионных соединений ненасыщенные и ненаправленные, поэтому возможность электростатического взаимодействия с другими ионами у них сохраняется. На рис. 2 и 3 показаны примеры ионных связей, соответствующих модели электронного переноса Косселя. 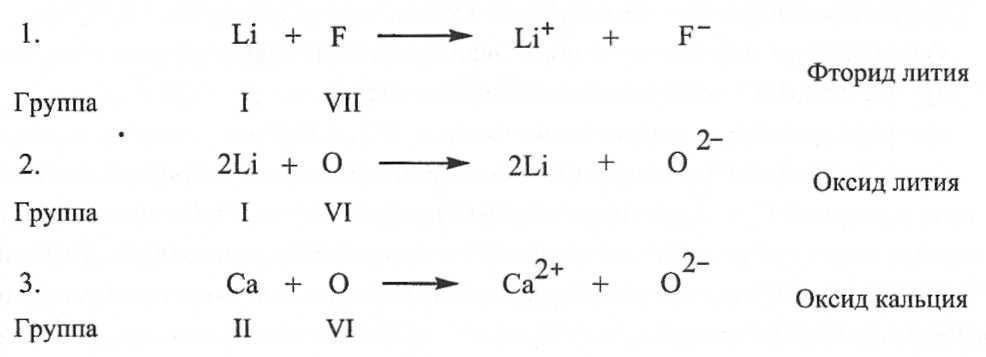 Рис. 1. Ионная связь 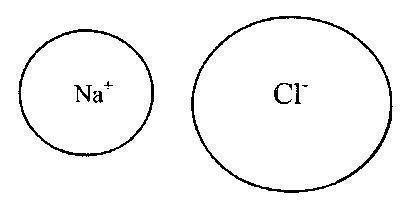 Рис. 2. Ионная связь в молекуле поваренной соли (NaCl) Здесь уместно напомнить о некоторых свойствах, объясняющих поведение веществ в природе, в частности, рассмотреть представление о кислотах и основаниях. Водные растворы всех этих веществ являются электролитами. Они по-разному изменяют окраску индикаторов. Механизм действия индикаторов был открыт Ф.В. Оствальдом. Он показал, что индикаторы представляют собой слабые кислоты или основания, окраска которых в недиссоциированном и диссоциированном состояниях различается. Основания способны нейтрализовать кислоты. Не все основания растворимы в воде (например, нерастворимы некоторые органические соединения, не содержащие ОН-групп, в частности, триэтиламин N (С 2 Н 5 ) 3 ); растворимые основания называют щелочами. Водные растворы кислот вступают в характерные реакции: а) с оксидами металлов — с образованием соли и воды; б) с металлами — с образованием соли и водорода; в) с карбонатами — с образованием соли, СO 2 и Н 2 O. Свойства кислот и оснований описывают несколько теорий. В соответствие с теорией С.А. Аррениуса, кислота представляет собой вещество, диссоциирующее с образованием ионов Н + , тогда как основание образует ионы ОН. Эта теория не учитывает существования органических оснований, не имеющих гидроксильных групп. В соответствие с протонной теорией Бренстеда и Лоури, кислота представляет собой вещество, содержащее молекулы или ионы, отдающие протоны (доноры протонов), а основание — вещество, состоящее из молекул или ионов, принимающие протоны (акцепторы протонов). Отметим, что в водных растворах ионы водорода существуют в гидратированной форме, то есть в виде ионов гидроксония H 3 O + . Эта теория описывает реакции не только с водой и гидроксидными ионами, но и осуществляющиеся в отсутствие растворителя или с неводным растворителем. Например, в реакции между аммиаком NH 3 (слабым основанием) и хлороводородом в газовой фазе образуется твердый хлорид аммония, причем в равновесной смеси двух веществ всегда присутствуют 4 частицы, две из которых - кислоты, а две другие - основания: 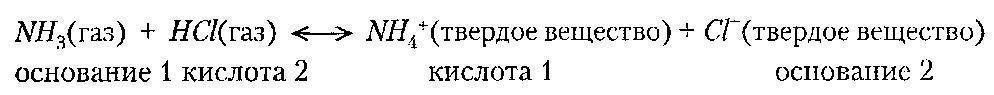 Эта равновесная смесь состоит из двух сопряженных пар кислот и оснований: 1) NH 4 + и NH 3 2) HCl и Сl Здесь в каждой сопряженной паре кислота и основание различаются на один протон. Каждая кислота имеет сопряженное с ней основание. Сильной кислоте соответствует слабое сопряженное основание, а слабой кислоте — сильное сопряженное основание. Теория Бренстеда-Лоури позволяет объяснить уникальность роли воды для жизнедеятельности биосферы. Вода, в зависимости от взаимодействующего с ней вещества, может проявлять свойства или кислоты, или основания. Например, в реакциях с водными растворами уксусной кислоты вода является основанием, а с водными растворами аммиака — кислотой. 1) СН 3 СООН + Н 2 O ↔ Н 3 O + + СН 3 СОО. Здесь молекула уксусной кислоты доминирует протон молекуле воды; 2) NH 3 + Н 2 O ↔ NH 4 + + ОН. Здесь молекула аммиака акцептирует протон от молекулы воды. Таким образом, вода может образовывать две сопряженные пары: 1) Н 2 O (кислота) и ОН (сопряженное основание) 2) Н 3 О + (кислота) и Н 2 O (сопряженное основание). В первом случае вода доминирует протон, а во втором — акцептирует его. Такое свойство называется амфипротонностью. Вещества, способные вступать в реакции в качестве и кислот, и оснований, называются амфотерными. В живой природе такие вещества встречаются часто. Например, аминокислоты способны образовывать соли и с кислотами, и с основаниями. Поэтому пептиды легко образуют координационные соединения с присутствующими ионами металлов. Таким образом, характерное свойство ионной связи — полное перемещение нары связывающих электронов к одному из ядер. Это означает, что между ионами существует область, где электронная плотность почти нулевая. Диполь-дипольная связь Кроме перечисленных типов связи, различают еще диполь-дипольные межмолекулярные взаимодействия, называемые также вандерваалъсовыми. Сила этих взаимодействий зависит от природы молекул. Выделяют взаимодействия трех типов: постоянный диполь — постоянный диполь (диполь-дипольное притяжение); постоянный диполь — индуцированный диполь (индукционное притяжение); мгновенный диполь — индуцированный диполь (дисперсионное притяжение, или лондонские силы) 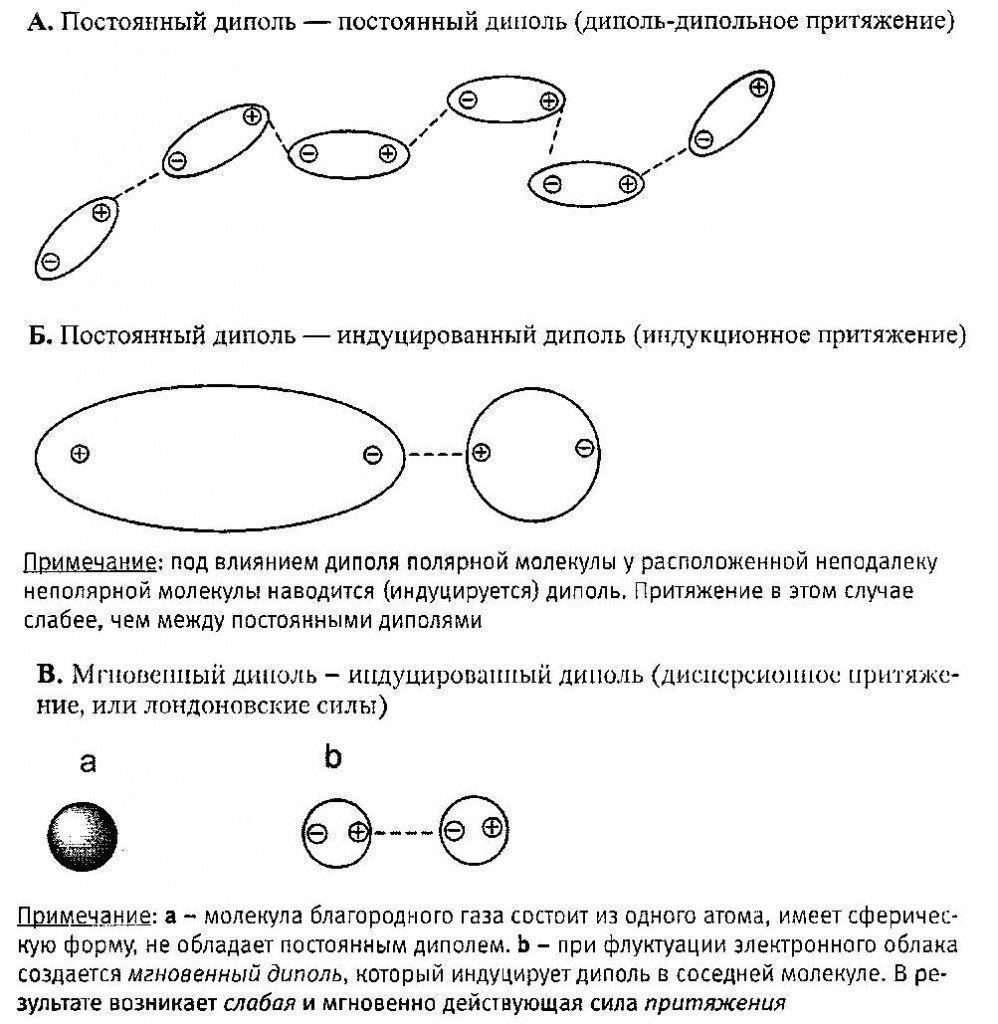 Рис. 3. Вандерваальсовая связь Диполь-дипольным моментом обладают только молекулы с полярными ковалентными связями (HCl, NH 3, SO 2, Н 2 O, C 6 H 5 Cl), причем сила связи составляет 1-2 Дебая (1Д = 3,338 × 10 30 кулон-метра — Кл × м). В биохимии выделяют еще один тип связи - водородную связь, являющуюся предельным случаем диполь-дипольного притяжения. Эта связь образована притяжением между атомом водорода и электроотрицательным атомом небольшого размера, чаще всего - кислородом, фтором и азотом. С крупными атомами, обладающими аналогичной электроотрицательностью (например, с хлором и серой), водородная связь оказывается значительно более слабой. Атом водорода отличается одной существенной особенностью: при оттягивании связывающих электронов его ядро — протон — оголяется и перестает экранироваться электронами. Поэтому атом превращается в крупный диполь. 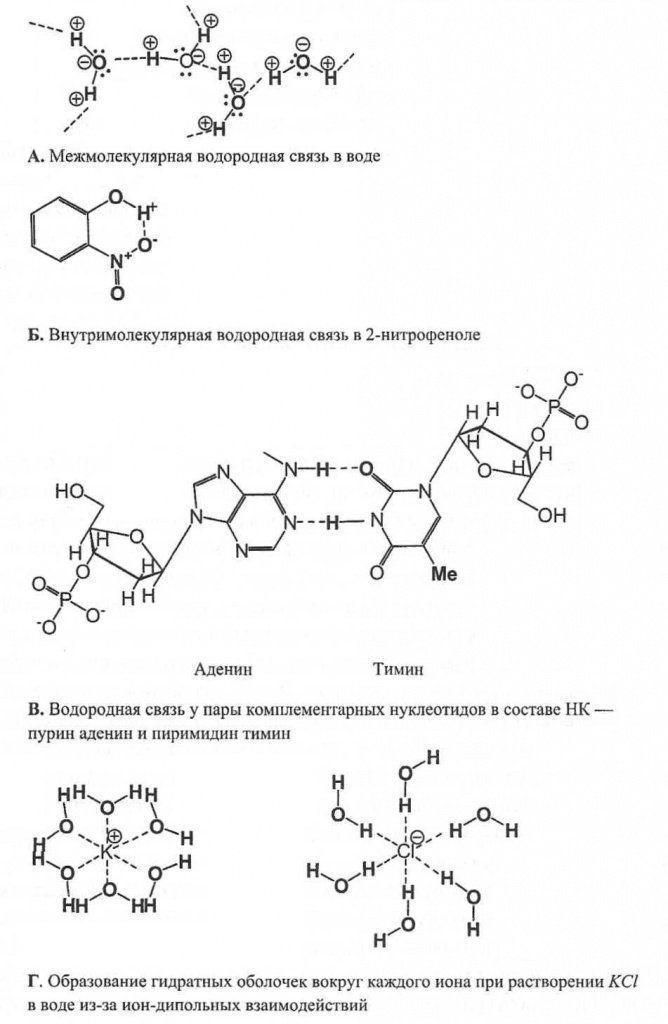  Рис.4. Водородная связь Водородная связь, в отличие от вандерваальсовой, образуется не только при межмолекулярных взаимодействиях, но и внутри одной молекулы — внутримолекулярная водородная связь. Водородные связи играют в биохимии важную роль, например, для стабилизации структуры белков в виде а-спирали, или для образования двойной спирали ДНК (рис. 4). Водородная и вандерваальсовая связи значительно слабее, чем ионная, ковалентная и координационная. Энергия межмолекулярных связей указана в табл. 1.
Таблица 1. Энергия межмолекулярных сил Примечание: Степень межмолекулярных взаимодействий отражают показатели энтальпии плавления и испарения (кипения). Ионным соединениям требуется для разделения ионов значительно больше энергии, чем для разделения молекул. Энтальпии плавления ионных соединений значительно выше, чем молекулярных соединений. Водородная связь Водородная связь, вид химического взаимодействия атомов в молекулах, отличающийся тем, что существенное участие в нём принимает атом водорода (Н), уже связанный ковалентной связью с другим атомом (А). Группа А — Н выступает донором протона (акцептором электрона), а другая группа (или атом) В — донором электрона (акцептором протона). Иначе говоря, группа А — Н проявляет функцию кислоты, а группа В — основания. Для обозначения В. с. употребляют, в отличие от обычной валентной чёрточки, пунктир, т. е. А — Н···В [в предельном случае симметричной В. с., например, в бифториде калия, K + (F···Н···F)-, различие двух связей исчезает]. К образованию В. с. способны группы А — Н, где А — атомы О, N, F, Cl, Вr и в меньшей мере С и S. В качестве второго, электродонорного центра В могут выступать те же атомы О, N, S разнообразных функциональных групп, анионы F-, С1- и др., в меньшей мере ароматические кольца и кратные связи. Если А — Н и В принадлежат отдельным (разнородным или идентичным) молекулам, то В. с. называют межмолекулярной, а если они находятся в разных частях одной молекулы, — внутримолекулярной. От общих для всех веществ ван-дер-ваальсовых сил взаимного притяжения молекул В. с. отличается направленностью и насыщаемостью, т. е. качествами обычных (валентных) химических связей. В. с. не сводится, как ранее считали, к электростатическому притяжению полярных групп А — Н и В, а рассматривается как донорно-акцепторная химическая связь. По своим энергиям, обычно 3—8 ккал/моль, В. с. занимает промежуточное положение между ван-дер-ваальсовыми взаимодействиями (доли ккал/моль) и типичными химическими связями (десятки ккал/моль) (1 ккал = 4,19·103·дж). Наиболее распространены межмолекулярные В. с. Они приводят к ассоциации одинаковых или разнородных молекул в разнообразные агрегаты-комплексы с В. с., или Н-комплексы, которые при обычных условиях находятся в быстро устанавливающемся равновесии. При этом возникают как бинарные комплексы (кислота — основание и циклические димеры), так и большие образования (цепи, кольца, спирали, плоские и пространственные сетки связанных молекул). Наличием таких В. с. обусловлены свойства различных растворов и жидкостей (в первую очередь, воды и водных растворов, ряда технических полимеров — капрона, нейлона и т.д.), а также кристаллическая структура многих молекулярных кристаллов и кристаллогидратов неорганических соединений, в том числе, разумеется, и льда. Точно так же В. с. существенно определяет структуру белков, нуклеиновых кислот и других биологически важных соединений и поэтому играет важнейшую роль в химии всех жизненных процессов. Вследствие всеобщей распространённости В. с. её роль существенна и во многих других областях химии и технологии (процессы перегонки, экстракции, адсорбции, хроматографии, кислотно-основные равновесия, катализ). Образование В. с., специфически изменяя свойства групп А — Н и В, отражается и на молекулярных свойствах; это обнаруживается, в частности, по колебательным спектрам и спектрам протонного магнитного резонанса. Поэтому спектроскопия, особенно инфракрасная, является важнейшим методом изучения В. с. и зависящих от неё процессов. Ковалентная связь Ковалентная связь – это химическая связь, образованная за счет образования общей электронной пары А: В. При этом у двух атомов перекрываются атомные орбитали. Ковалентная связь образуется при взаимодействии атомов с небольшой разницей электроотрицательностей (как правило, между двумя неметаллами) или атомов одного элемента. Свойства ковалентной связи Ковалентная связь образуется двумя электронами с противоположно направленными спинами, причем эта электронная пара принадлежит двум атомам. Ковалентная связь тем прочнее, чем в большей степени перекрываются электронные облака. Прочность ковалентной связи -- это свойства характер длинной связи (межъядерное пространство) и энергии энергией связи. Насыщаемость ковалентной связи -- это способность атома участвовать только в определенном числе ковалентной связи, насыщаемость характеризует валентностью атома. Количественные меры валентности являются число не спаренных электронов у атома в основном и в возбужденном состоянии. Гибридизация ковалентной связи -- при гибридизации происходит смещение атомных орбиталей, т.е. происходит выравнивание по энергии и по форме. Существует sp, sp2, sp3 --гибридизация. sp -- форма молекулы линейная (угол 1800), sp2 -- форма молекулы плоская треугольная (угол 1200), sp3 - форма тетраэдрическая (угол 109028). Кратность ковалентной связи или делоколизация связи -- Число связей, образующихся между атомами, называется кратностью (порядком) связи. С увеличением кратности (порядка) связи изменяется длина связи и ее энергия. Ковалентная связь делится на полярную и неполярную связь Ковалентная неполярная (симметричная) связь – это ковалентная связь, образованная атомами с равной элетроотрицательностью (как правило, одинаковыми неметаллами) и, следовательно, с равномерным распределением электронной плотности между ядрами атомов.  Ковалентная полярная связь – это ковалентная связь, которая возникает между атомами с разной электроотрицательностью (как правило, разными неметаллами) и характеризуется смещением общей электронной пары к более электроотрицательному атому (поляризацией). Электронная плотность смещена к более электроотрицательному атому – следовательно, на нем возникает частичный отрицательный заряд (δ-), а на менее электроотрицательном атоме возникает частичный положительный заряд (δ+, дельта +) (рис. 6) 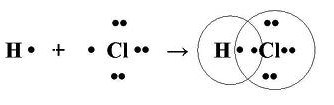 Рис. 6. Ковалентная полярная связь Литература Маррел Дж., Кеттл С., Теддер Дж. Химическая связь. М.: Мир, 1980. 384 с. Пиментел Г., Спратли Р. Как квантовая механика объясняет химическую связь. Пер. с англ. М.: Мир, 1973. 332 с. Рюденберг К. Физическая природа химической связи. М.: Мир, 1964. 164 c. Бердетт Дж. Химическая связь. М.: Бином. Лаборатория знаний, 2008. 248 с. ISBN 978-5-94774-760-7, ISBN 978-5-03-003847-6, ISBN 0-471-97129-4 Яцимирский К. Б., Яцимирский В. К. Химическая связь. Киев: Вища школа, 1975. 304 c. Краснов К. С. Молекулы и химическая связь. 2-ое изд. М: Высшая школа, 1984. 295 с. Татевский В. М. Строение молекул. М.: Химия, 1977. 512 с (Глава VIII. «Проблема химической связи в квантовой механике») Татевский В. М. Квантовая механика и теория строения молекул. М.: Изд-во МГУ, 1965. 162 с. (§§ 30-31) Бейдер Р. Атомы в молекулах. Квантовая теория. М.: Мир, 2001. 532 c. ISBN 5-03-003363-7 Глава 7. Модели химической связи. |
